鲁教版九年级化学下册第七单元第一节 酸及其性质
文档属性
| 名称 | 鲁教版九年级化学下册第七单元第一节 酸及其性质 |

|
|
| 格式 | zip | ||
| 文件大小 | 5.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-02-10 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
第七单元 常见的酸和碱
第一节 酸及其性质
在生活中你接触过或知道一些有酸味的物质吗?
-----酸
定义:溶于水后解离出的阳离子全为---氢离子(H+ ) 的化合物
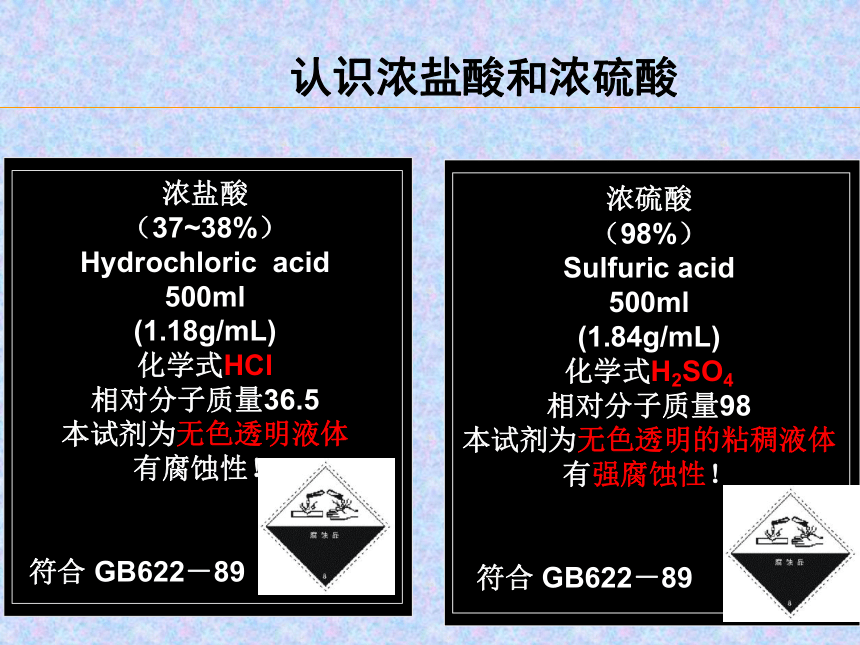
认识浓盐酸和浓硫酸
一、常见的酸
看看浓盐酸和浓硫酸试剂瓶标签上的内容,观察浓硫酸和浓盐酸的颜色和状态,打开瓶塞,你观察到什么现象?闻一闻浓硫酸和浓盐酸是否有气味?
认识浓盐酸和浓硫酸
因为浓盐酸挥发出来的氯化氢气体跟空气里的水蒸气接触,形成盐酸小液滴的缘故。
为什么打开盛浓盐酸的试剂瓶会看到有白雾出现?体现浓盐酸什么性质?
体现浓盐酸的挥发性。
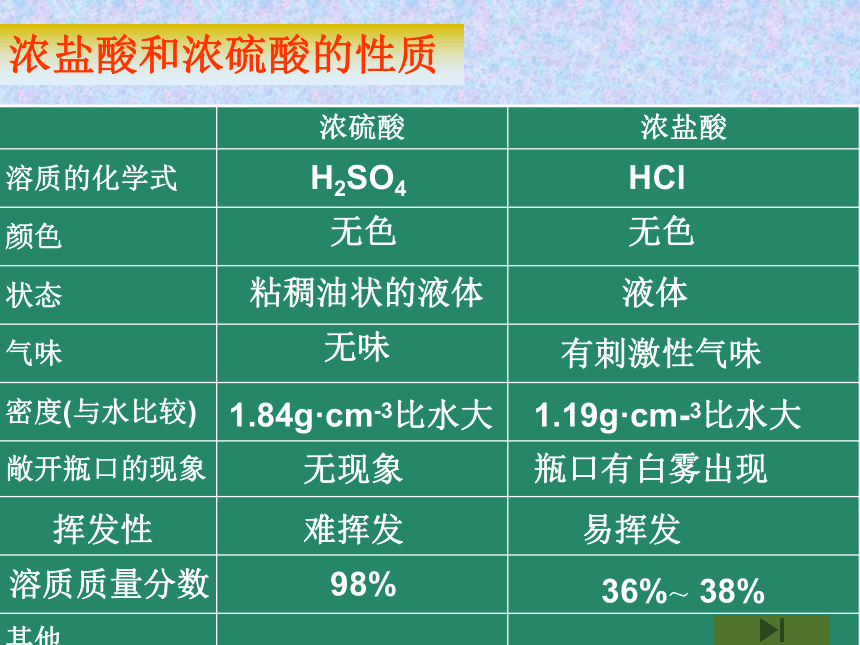
浓盐酸和浓硫酸的性质
H2SO4
HCl
无色
无色
液体
粘稠油状的液体
有刺激性气味
1.84g·cm-3比水大
瓶口有白雾出现
无现象
无味
易挥发
难挥发
1.19g·cm-3比水大
溶质质量分数
98%
36%~ 38%
挥发性
浓硫酸 浓盐酸
溶质的化学式
颜色
状态
气味
密度(与水比较)
敞开瓶口的现象
其他
代表水分子
代表氢分子
浓硫酸
氢气和水蒸气
的混合气体
氢气
浓硫酸可做某些气体的干燥剂
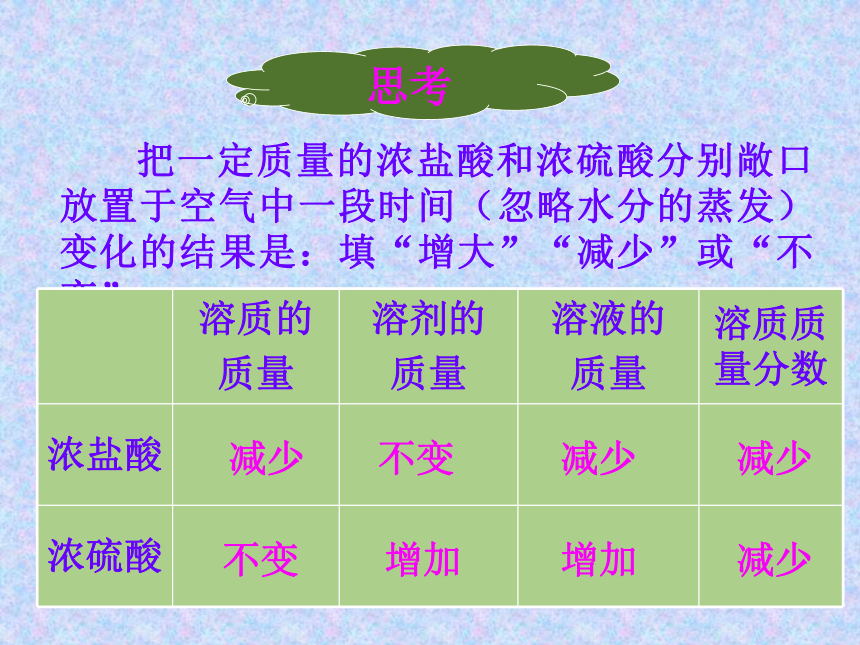
把一定质量的浓盐酸和浓硫酸分别敞口放置于空气中一段时间(忽略水分的蒸发)变化的结果是:填“增大”“减少”或“不变”
减少
不变
不变
增加
减少
增加
减少
减少
思考
溶质的
质量 溶剂的
质量 溶液的
质量 溶质质量分数
浓盐酸
浓硫酸
浓硫酸的稀释
浓硫酸沿着器壁慢慢注入水中,并不断搅拌。
稀释浓硫酸的方法:
切不可将水倒进浓硫酸里
当心
浓硫酸溅到皮肤上的处理方法:
应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液
紫色石蕊试液变红
无色酚酞试液不变色
镁条溶解,有大量
气泡生成。
Mg+2HCl=MgCl2+H2↑
铁锈溶解,溶液由无色变为黄色。
Fe2O3+6HCl=2FeCl3+3H2O
一会儿后,有气泡生成,溶液慢慢变为浅绿色。
Fe+2HCl=FeCl2+H2↑
Na2CO3+2HCl=2NaCl+CO2↑+H2O
AgNO3+HCl=AgCl↓+HNO3
无明显现象
二、酸的化学性质
实验探究
有气泡产生
产生白色沉淀
实验内容 反应现象 化学方程式
稀盐酸 紫色石蕊试液
无色酚酞试液
镁条
生锈
铁钉
碳酸钠
硝酸银溶液
氯化钡溶液
如果把上述实验中的稀盐酸换成稀硫酸,
你认为是否会产生类似的实验现象?
请试着写出这些反应的化学方程式。
Mg + H2SO4 =
Fe + H2SO4 =
Fe2O3 + H2SO4 =
CaCO3 + H2SO4 =
MgSO4 + H2↑
FeSO4 + H2 ↑
3 Fe2(SO4)3 + 3H2O
CaSO4 + H2O + CO2↑
HCl + AgNO3 = AgCl↓ + HNO3
观察下列化学方程式,你发现它们有何特点?
A + C
AB+CD
B
D
化合物
化合物
两种化合物互相交换成分,生成另外两种化合物,这样的反应就叫做复分解反应。
复分解反应
下列化学反应是复分解反应吗?
1.Fe+2HCl=FeCl2+H2↑
2.Fe2O3+6HCl=2FeCl3+3H2O
3.CaCO3+2HCl=CaCl2+CO2↑+H2O
4.Ca(OH)2+CO2 =CaCO3↓+H2O
H2CO3
像NaCl、FeCl3、KNO3、Na2CO3、CaCO3、Na2SO4等由金属离子和酸根离子组成的化合物称为盐。
HCl=H+ + Cl-
H2SO4=2H+ + SO42-
HNO3=H+ + NO3-
硫酸根
像NH4Cl﹑ (NH4)2SO4等由铵根离子(NH4+)和酸根离子组成的化合物 ,也是盐。
硝酸根
盐酸根
H2CO3=2H+ + CO32-
碳酸根
为什么酸具有相似的化学性质呢?
HCl = H+ + Cl-
H2SO4 = 2H+ + SO42-
注意:不同的酸溶于水时解离出的酸根阴离子不同,其性质也存在差异。
BaCl2+H2SO4=BaSO4↓+2HCl
分析上述有关酸的反应的化学方程式,从组成上看,酸可以与哪些类别的物质反应?
1、酸与指示剂作用
2、酸+金属=
Mg+2HCl=MgCl2+H2↑
Fe+2HCl=FeCl2+H2↑
3、酸+金属氧化物=
Fe2O3+6HCl=2FeCl3+3H2O
4、酸+盐=
CaCO3+2HCl=CaCl2+CO2↑+H2O
盐+氢气
盐+水
新盐+新酸
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
小结
酸溶液能使紫色石蕊试液变红
无色酚酞试液不变色
Zn+H2SO4=ZnSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
BaCl2+H2SO4=BaSO4↓+2HCl
AgNO3+HCl=AgCl↓+HNO3
Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
我的收获
浓盐酸和浓硫酸的性质
盐酸和稀硫酸的化学性质
酸的通性
1.(2012年四川自贡,5题,2分)实验室中下列物质因没有密封保存而使质量减少的是__
A.浓硫酸 B.生石灰
C.烧碱 D.浓盐酸
2.(2012年四川自贡,6题,2分)酸具有酸的通性的原因是____
A.酸都能电离出H+ B.酸都含有酸根
C.酸中都含有氢元素 D.酸中都含有氧元素
D
挑战自我
A
1.人的胃液里含有什么酸?
2.汽车电瓶里含有什么酸?
3.食醋里含有什么酸?
4.汽水里含有什么酸?
你 知 道 吗 ?
盐酸(HCl)
硫酸(H2SO4)
醋酸(CH3COOH)
碳酸(H2CO3)
1.不法分子常用金光闪闪的“假金元宝”(铜、锌合金)蒙骗人们,下列鉴别办法中错误的是( )
A.加盐酸 B.测密度 C.用火烧 D.看颜色
2.盛浓硫酸的铁槽,用水冲洗时遇明火爆炸,试用化学方程式解释原因。
(1)_____________________
(2)_____________________。
D
Fe+H2SO4=FeSO4+H2↑
下列说法不正确的是
A、不能用铁制容器盛放稀盐酸和稀硫酸
B、用稀盐酸可以除去热水瓶中的水垢 主要成分是
CaCO3和 Mg(OH)2
C、用含Al(OH)3的药物胃舒平可治疗胃酸过多
D、铁制零件在电镀前,放在盐酸池中浸泡时间越
长越好
D
1、下列说法错误的是( )
A、浓盐酸敞口放置一段时间后,溶液的质量会减少,溶质的质量分数增大
B、浓盐酸在空气中会冒白烟
C、浓硫酸敞口一段时间后,溶液的质量会增加,溶质的质量分数变小
D、浓硫酸溶于水时会放出大量的热
2 、下列说法不正确的是( ):
A 、盐酸溶液中含有氢离子和氯离子
B 、氢氧化钠溶液中含有钠离子和氢氧根离子
C 、两种溶液混合时,氢离子与氢氧根离子结合
生成了水分子
D 、两种溶液混合时,钠离子与氯离子结合生成
了氯化钠分子
3、浓硫酸可以用作干燥剂,是因为它具 性,所以敞口放置的浓硫酸质量会 ,溶质质量分数会 。稀释浓硫酸一定要把 沿器壁慢慢注入 里,并不断用玻璃棒搅拌,其目的是 。切不可将 。如果不慎将浓硫酸溅到手上,应 。
AB
D
吸水性
增加
减小
浓硫酸
水
让热量迅速扩散
水倒入浓硫酸中
立即用大量水冲洗
3、稀盐酸中有H2O、H+、Cl-三种微粒,是哪种微粒使紫色的石蕊试液变成红色的?你能设计一个实验进行证明吗?
1.取少量水于试管中,滴加几滴紫色的石蕊,溶液不变色,说明水分子不能使紫色石蕊变红。
2.取少量NaCl溶液于试管中,滴加几滴紫色石蕊,溶液不变色,说明Cl-不能使紫色石蕊变红。
3.取少量稀盐酸于试管中,滴加几滴紫色的石蕊,溶液变成红色,说明是H+使紫色石蕊变红。
第七单元 常见的酸和碱
第一节 酸及其性质
在生活中你接触过或知道一些有酸味的物质吗?
-----酸
定义:溶于水后解离出的阳离子全为---氢离子(H+ ) 的化合物
认识浓盐酸和浓硫酸
一、常见的酸
看看浓盐酸和浓硫酸试剂瓶标签上的内容,观察浓硫酸和浓盐酸的颜色和状态,打开瓶塞,你观察到什么现象?闻一闻浓硫酸和浓盐酸是否有气味?
认识浓盐酸和浓硫酸
因为浓盐酸挥发出来的氯化氢气体跟空气里的水蒸气接触,形成盐酸小液滴的缘故。
为什么打开盛浓盐酸的试剂瓶会看到有白雾出现?体现浓盐酸什么性质?
体现浓盐酸的挥发性。
浓盐酸和浓硫酸的性质
H2SO4
HCl
无色
无色
液体
粘稠油状的液体
有刺激性气味
1.84g·cm-3比水大
瓶口有白雾出现
无现象
无味
易挥发
难挥发
1.19g·cm-3比水大
溶质质量分数
98%
36%~ 38%
挥发性
浓硫酸 浓盐酸
溶质的化学式
颜色
状态
气味
密度(与水比较)
敞开瓶口的现象
其他
代表水分子
代表氢分子
浓硫酸
氢气和水蒸气
的混合气体
氢气
浓硫酸可做某些气体的干燥剂
把一定质量的浓盐酸和浓硫酸分别敞口放置于空气中一段时间(忽略水分的蒸发)变化的结果是:填“增大”“减少”或“不变”
减少
不变
不变
增加
减少
增加
减少
减少
思考
溶质的
质量 溶剂的
质量 溶液的
质量 溶质质量分数
浓盐酸
浓硫酸
浓硫酸的稀释
浓硫酸沿着器壁慢慢注入水中,并不断搅拌。
稀释浓硫酸的方法:
切不可将水倒进浓硫酸里
当心
浓硫酸溅到皮肤上的处理方法:
应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液
紫色石蕊试液变红
无色酚酞试液不变色
镁条溶解,有大量
气泡生成。
Mg+2HCl=MgCl2+H2↑
铁锈溶解,溶液由无色变为黄色。
Fe2O3+6HCl=2FeCl3+3H2O
一会儿后,有气泡生成,溶液慢慢变为浅绿色。
Fe+2HCl=FeCl2+H2↑
Na2CO3+2HCl=2NaCl+CO2↑+H2O
AgNO3+HCl=AgCl↓+HNO3
无明显现象
二、酸的化学性质
实验探究
有气泡产生
产生白色沉淀
实验内容 反应现象 化学方程式
稀盐酸 紫色石蕊试液
无色酚酞试液
镁条
生锈
铁钉
碳酸钠
硝酸银溶液
氯化钡溶液
如果把上述实验中的稀盐酸换成稀硫酸,
你认为是否会产生类似的实验现象?
请试着写出这些反应的化学方程式。
Mg + H2SO4 =
Fe + H2SO4 =
Fe2O3 + H2SO4 =
CaCO3 + H2SO4 =
MgSO4 + H2↑
FeSO4 + H2 ↑
3 Fe2(SO4)3 + 3H2O
CaSO4 + H2O + CO2↑
HCl + AgNO3 = AgCl↓ + HNO3
观察下列化学方程式,你发现它们有何特点?
A + C
AB+CD
B
D
化合物
化合物
两种化合物互相交换成分,生成另外两种化合物,这样的反应就叫做复分解反应。
复分解反应
下列化学反应是复分解反应吗?
1.Fe+2HCl=FeCl2+H2↑
2.Fe2O3+6HCl=2FeCl3+3H2O
3.CaCO3+2HCl=CaCl2+CO2↑+H2O
4.Ca(OH)2+CO2 =CaCO3↓+H2O
H2CO3
像NaCl、FeCl3、KNO3、Na2CO3、CaCO3、Na2SO4等由金属离子和酸根离子组成的化合物称为盐。
HCl=H+ + Cl-
H2SO4=2H+ + SO42-
HNO3=H+ + NO3-
硫酸根
像NH4Cl﹑ (NH4)2SO4等由铵根离子(NH4+)和酸根离子组成的化合物 ,也是盐。
硝酸根
盐酸根
H2CO3=2H+ + CO32-
碳酸根
为什么酸具有相似的化学性质呢?
HCl = H+ + Cl-
H2SO4 = 2H+ + SO42-
注意:不同的酸溶于水时解离出的酸根阴离子不同,其性质也存在差异。
BaCl2+H2SO4=BaSO4↓+2HCl
分析上述有关酸的反应的化学方程式,从组成上看,酸可以与哪些类别的物质反应?
1、酸与指示剂作用
2、酸+金属=
Mg+2HCl=MgCl2+H2↑
Fe+2HCl=FeCl2+H2↑
3、酸+金属氧化物=
Fe2O3+6HCl=2FeCl3+3H2O
4、酸+盐=
CaCO3+2HCl=CaCl2+CO2↑+H2O
盐+氢气
盐+水
新盐+新酸
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
小结
酸溶液能使紫色石蕊试液变红
无色酚酞试液不变色
Zn+H2SO4=ZnSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
BaCl2+H2SO4=BaSO4↓+2HCl
AgNO3+HCl=AgCl↓+HNO3
Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
我的收获
浓盐酸和浓硫酸的性质
盐酸和稀硫酸的化学性质
酸的通性
1.(2012年四川自贡,5题,2分)实验室中下列物质因没有密封保存而使质量减少的是__
A.浓硫酸 B.生石灰
C.烧碱 D.浓盐酸
2.(2012年四川自贡,6题,2分)酸具有酸的通性的原因是____
A.酸都能电离出H+ B.酸都含有酸根
C.酸中都含有氢元素 D.酸中都含有氧元素
D
挑战自我
A
1.人的胃液里含有什么酸?
2.汽车电瓶里含有什么酸?
3.食醋里含有什么酸?
4.汽水里含有什么酸?
你 知 道 吗 ?
盐酸(HCl)
硫酸(H2SO4)
醋酸(CH3COOH)
碳酸(H2CO3)
1.不法分子常用金光闪闪的“假金元宝”(铜、锌合金)蒙骗人们,下列鉴别办法中错误的是( )
A.加盐酸 B.测密度 C.用火烧 D.看颜色
2.盛浓硫酸的铁槽,用水冲洗时遇明火爆炸,试用化学方程式解释原因。
(1)_____________________
(2)_____________________。
D
Fe+H2SO4=FeSO4+H2↑
下列说法不正确的是
A、不能用铁制容器盛放稀盐酸和稀硫酸
B、用稀盐酸可以除去热水瓶中的水垢 主要成分是
CaCO3和 Mg(OH)2
C、用含Al(OH)3的药物胃舒平可治疗胃酸过多
D、铁制零件在电镀前,放在盐酸池中浸泡时间越
长越好
D
1、下列说法错误的是( )
A、浓盐酸敞口放置一段时间后,溶液的质量会减少,溶质的质量分数增大
B、浓盐酸在空气中会冒白烟
C、浓硫酸敞口一段时间后,溶液的质量会增加,溶质的质量分数变小
D、浓硫酸溶于水时会放出大量的热
2 、下列说法不正确的是( ):
A 、盐酸溶液中含有氢离子和氯离子
B 、氢氧化钠溶液中含有钠离子和氢氧根离子
C 、两种溶液混合时,氢离子与氢氧根离子结合
生成了水分子
D 、两种溶液混合时,钠离子与氯离子结合生成
了氯化钠分子
3、浓硫酸可以用作干燥剂,是因为它具 性,所以敞口放置的浓硫酸质量会 ,溶质质量分数会 。稀释浓硫酸一定要把 沿器壁慢慢注入 里,并不断用玻璃棒搅拌,其目的是 。切不可将 。如果不慎将浓硫酸溅到手上,应 。
AB
D
吸水性
增加
减小
浓硫酸
水
让热量迅速扩散
水倒入浓硫酸中
立即用大量水冲洗
3、稀盐酸中有H2O、H+、Cl-三种微粒,是哪种微粒使紫色的石蕊试液变成红色的?你能设计一个实验进行证明吗?
1.取少量水于试管中,滴加几滴紫色的石蕊,溶液不变色,说明水分子不能使紫色石蕊变红。
2.取少量NaCl溶液于试管中,滴加几滴紫色石蕊,溶液不变色,说明Cl-不能使紫色石蕊变红。
3.取少量稀盐酸于试管中,滴加几滴紫色的石蕊,溶液变成红色,说明是H+使紫色石蕊变红。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
