【全国百强校】甘肃省静宁县一中高中化学选修五课件:3.2醛(共28张PPT)
文档属性
| 名称 | 【全国百强校】甘肃省静宁县一中高中化学选修五课件:3.2醛(共28张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-02-14 00:00:00 | ||
图片预览




文档简介
(共29张PPT)
第二节 乙 醛 醛 类
学习目标:1.认识乙醛的结构
2.初步学会乙醛的化学性质
3.了解甲醛、掌握醛类同性
学习重点:乙醛的化学性质
学习难点:乙醛的银镜反应及反应的方程式
【问题探究】
1.你能写出乙醛的“五式”吗?通过乙醛的结构式你能推测它可能具有的性质吗?
2.请你设计实验来验证它可能具有的性质。
3.乙醛能发生加成、氧化反应,请通过实例判断其发生反应是的断键位置。
4.根据乙醛的结构和性质,你能完成甲醛的性质吗?
【自学探究】
选修5P56-58及《学业质量模块检测》完成上面四个问题
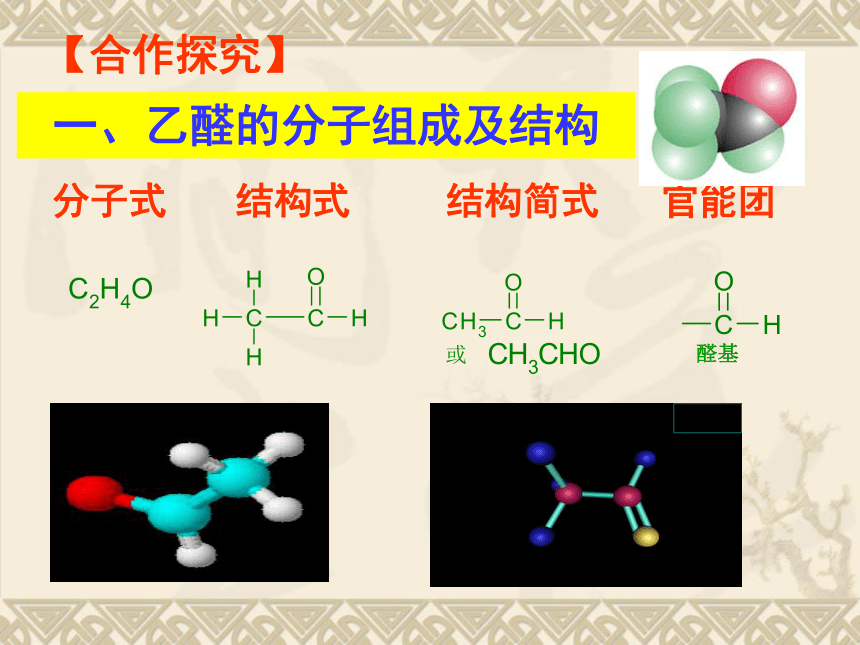
一、乙醛的分子组成及结构
分子式
结构式
结构简式
官能团
或
醛基
【合作探究】
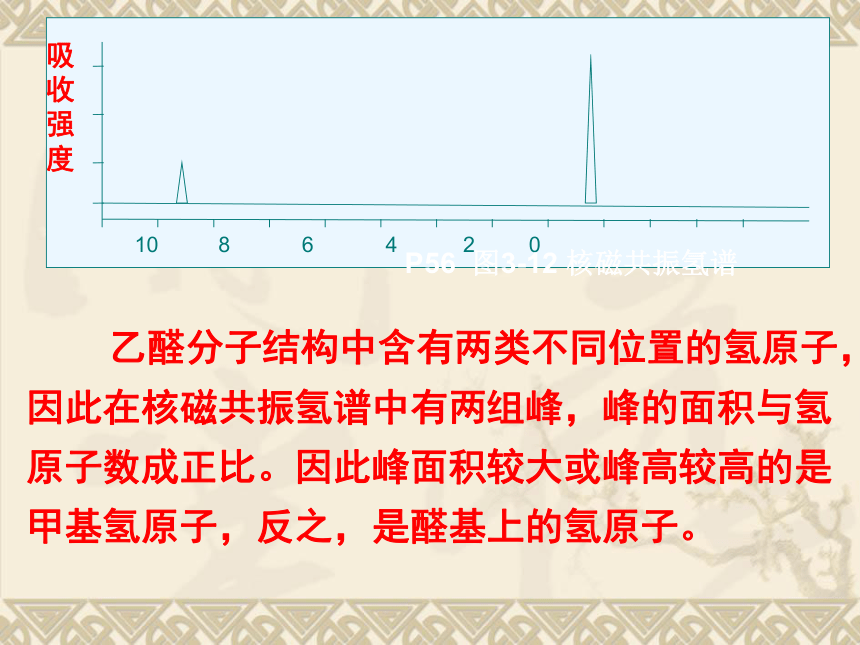
P56 图3-12 核磁共振氢谱
乙醛分子结构中含有两类不同位置的氢原子,因此在核磁共振氢谱中有两组峰,峰的面积与氢原子数成正比。因此峰面积较大或峰高较高的是甲基氢原子,反之,是醛基上的氢原子。
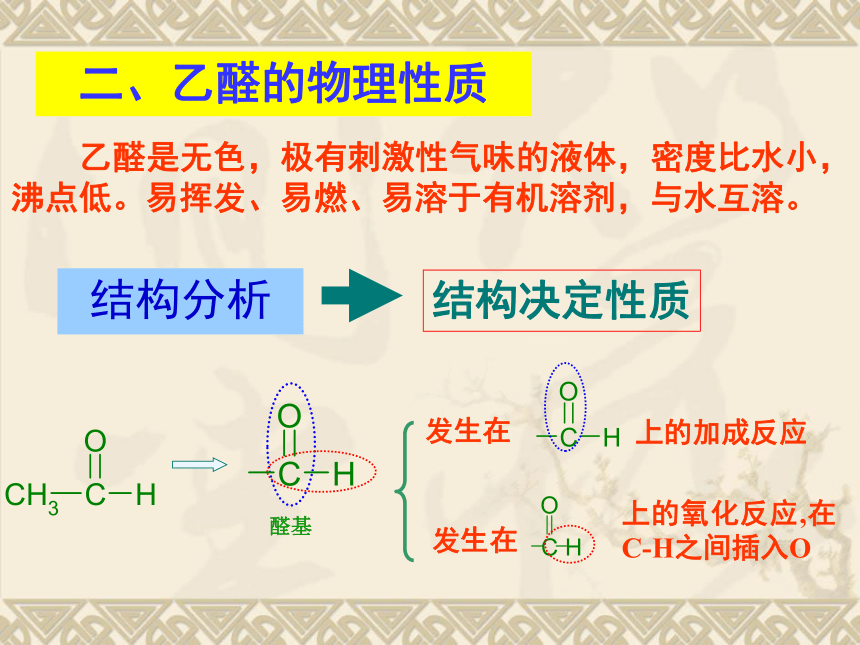
上的氧化反应,在C-H之间插入O
上的加成反应
结构分析
结构决定性质
二、乙醛的物理性质
乙醛是无色,极有刺激性气味的液体,密度比水小,
沸点低。易挥发、易燃、易溶于有机溶剂,与水互溶。
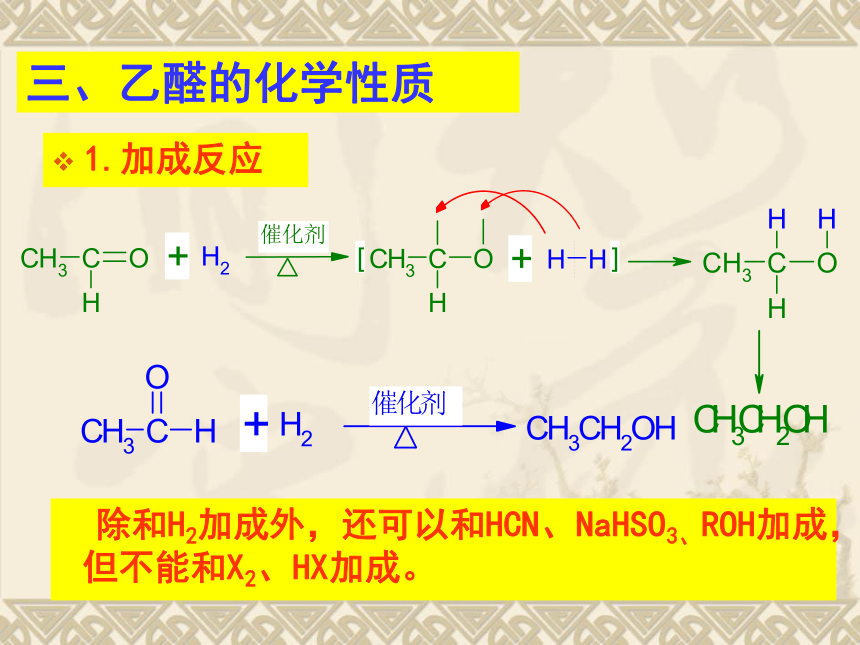
1.加成反应
三、乙醛的化学性质
除和H2加成外,还可以和HCN、NaHSO3、ROH加成,但不能和X2、HX加成。
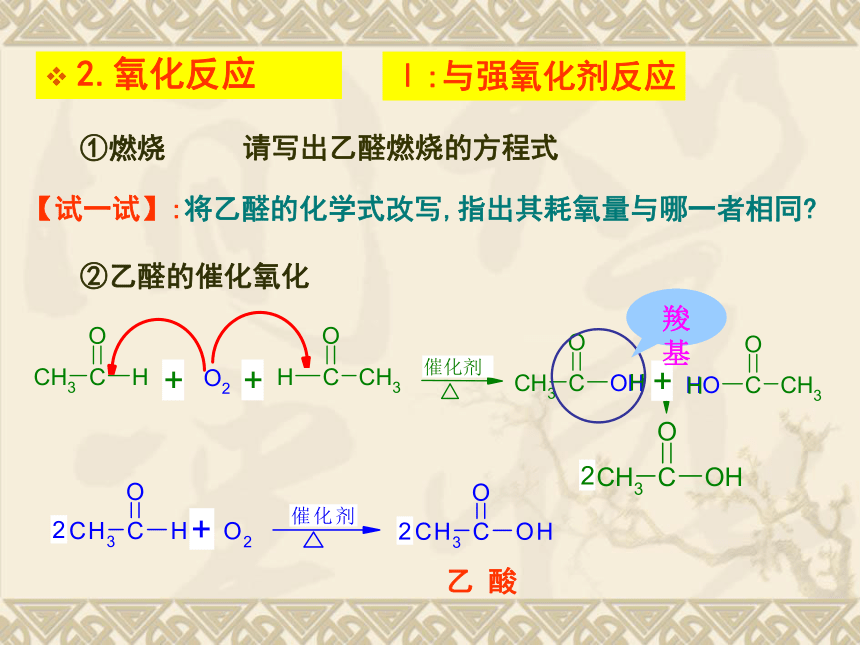
2.氧化反应
羧基
乙 酸
Ⅰ:与强氧化剂反应
①燃烧
请写出乙醛燃烧的方程式
【试一试】:将乙醛的化学式改写,指出其耗氧量与哪一者相同?
②乙醛的催化氧化
4、加热时不宜震荡试管
实验注意事项
1、试管内壁要洁净(如有油污,得不到光亮的银,而是黑色沉淀)
2、银氨溶液应随配随用。
3、必须用水浴加热,不能在酒精灯上加热
氧化反应
①银镜反应
【实验探究】
Ⅱ——与弱氧化剂反应
说明:
a、银镜反应方程式的书写 :
反应物:银氨:Ag(NH3)2OH 乙醛
生成物:一水、二银、三氨、乙酸铵
①银镜反应
②与新制Cu(OH)2反应
检验醛基的存在
应用:
四、甲醛和醛类
2、醛的定义:
由烃基和醛基相连而构成的化合物。
②饱和一元醛的通式:
1、甲醛
或
物理性质:甲醛又叫蚁醛,无色、具有强烈刺激性气味的气体,35%—40%的甲醛溶液,叫福尔马林,具有防腐能力。
①通式: 官能团为:
R—CHO
—CHO
CnH2n+1CHO 或CnH2nO
用途:制酚醛树脂,有杀菌防腐功能,可制生物标本
化学性质
化学性质
⑴银镜反应
1mol甲醛最多可以还原得到4molAg。
⑵与碱性的新制氢氧化铜(菲林试剂)反应
⑶还原反应
(4)缩聚反应
甲醛中有2个活泼氢可被氧化
酚醛树脂
单体
单体
★
为求延长保质期 不良奸商竟然给冰鲜鱼浸甲醛保鲜
甲醛有毒,如果用它来浸泡水产,可以固定海鲜、河鲜形态,保持鱼类色泽水发鱿鱼全部含甲醛 食用过量会休克和致癌
儿童房甲醛超标易诱发儿童白血病
给孩子买衣服既要注意款式也要注意安全
去甲醛十大植物高手
吊兰
龙舌兰
醛可看成醛基取代了烃中的氢原子,书写同分异构体时应把醛写成
3. 醛的同分异构体
R-CHO
再判断烃基-R有几种同分异构体
写出C5H10O属于醛类的所有同分异构体
4、醛酮的分类和命名
①按烃基类型不同:
(1)分类
②按烃基中是否含不饱和键分:
①习惯命名法
(2)醛酮的命名
酮根据羰基所连的两个烃基名来命名,把较简单的烃基名称放在前面,较复杂的烃基名称放在后面,最后加“酮”字。
②系统命名法
(1)脂肪族醛酮的命名
选择包含羰基的最长碳链为主链,从靠近羰基的一端开始编号,依次标明碳原子的位次。在名称中要注明羰基的位置。
3-甲基丁醛
2-苯基丙醛
3-戊酮
2,4-戊二酮
3-甲基环戊酮
醛、酮碳原子的位次,除用1,2,3,4,…表示外,也可用α,β,γ…希腊字母表示。α是指官能团羰基旁第一个位置,β是指第二个位置…。酮中一边用α,β,γ…,另一边用α’ β’ γ’…。
β—戊烯醛
(2)不饱和醛、酮的命名
从靠近羰基一端给主链编号。命名称为“某烯醛(酮)”或“某炔醛(酮)”。
2,3-二甲基-4-戊烯醛
3-甲基-4-己烯-2-酮
(3)含醛基、酮基的碳链上的氢被芳环或环烷基取代,就把芳环或环烷基当作主链上的取代基看待:
醛基与芳环、脂环或杂环上的碳原子直接相连时,它们的命名可在相应的环系名称之后加上“醛”字。
2-苯丙醛
1-环己基-1-丙酮
环己醛
1,2-萘二醛
(4)多元醛、酮命名
含有两个以上羰基的化合物,可用二醛、二酮等,醛作取代基时,可用词头“甲酰基”或“氧代”表示;酮作取代时,用词头“氧代”表示。
2,4—戊二酮
3—氧代丁醛
化学性质
(1)和H2加成被还原成醇
(2)氧化反应
a.燃烧
b.催化氧化成羧酸
c.被弱氧化剂氧化
Ⅰ.银镜反应
Ⅱ.与新制的氢氧化铜反应
d.使酸性KMnO4溶液和溴水褪色
小结:醛类的化学性质
还原反应:加氢或失氧
氧化反应:加氧或失氢
有机的氧化还原反应
>C=O称羰基,是酮的官能团,丙酮是最简单的酮。
科学视野
酮:羰基碳原子与两个烃基相连的化合物。
丙酮
丙酮不能被银氨溶液、新制的氢氧化铜等弱氧化剂氧化,但可催化加氢生成醇。
作业 P.59 1、2、3、4
第二节 乙 醛 醛 类
学习目标:1.认识乙醛的结构
2.初步学会乙醛的化学性质
3.了解甲醛、掌握醛类同性
学习重点:乙醛的化学性质
学习难点:乙醛的银镜反应及反应的方程式
【问题探究】
1.你能写出乙醛的“五式”吗?通过乙醛的结构式你能推测它可能具有的性质吗?
2.请你设计实验来验证它可能具有的性质。
3.乙醛能发生加成、氧化反应,请通过实例判断其发生反应是的断键位置。
4.根据乙醛的结构和性质,你能完成甲醛的性质吗?
【自学探究】
选修5P56-58及《学业质量模块检测》完成上面四个问题
一、乙醛的分子组成及结构
分子式
结构式
结构简式
官能团
或
醛基
【合作探究】
P56 图3-12 核磁共振氢谱
乙醛分子结构中含有两类不同位置的氢原子,因此在核磁共振氢谱中有两组峰,峰的面积与氢原子数成正比。因此峰面积较大或峰高较高的是甲基氢原子,反之,是醛基上的氢原子。
上的氧化反应,在C-H之间插入O
上的加成反应
结构分析
结构决定性质
二、乙醛的物理性质
乙醛是无色,极有刺激性气味的液体,密度比水小,
沸点低。易挥发、易燃、易溶于有机溶剂,与水互溶。
1.加成反应
三、乙醛的化学性质
除和H2加成外,还可以和HCN、NaHSO3、ROH加成,但不能和X2、HX加成。
2.氧化反应
羧基
乙 酸
Ⅰ:与强氧化剂反应
①燃烧
请写出乙醛燃烧的方程式
【试一试】:将乙醛的化学式改写,指出其耗氧量与哪一者相同?
②乙醛的催化氧化
4、加热时不宜震荡试管
实验注意事项
1、试管内壁要洁净(如有油污,得不到光亮的银,而是黑色沉淀)
2、银氨溶液应随配随用。
3、必须用水浴加热,不能在酒精灯上加热
氧化反应
①银镜反应
【实验探究】
Ⅱ——与弱氧化剂反应
说明:
a、银镜反应方程式的书写 :
反应物:银氨:Ag(NH3)2OH 乙醛
生成物:一水、二银、三氨、乙酸铵
①银镜反应
②与新制Cu(OH)2反应
检验醛基的存在
应用:
四、甲醛和醛类
2、醛的定义:
由烃基和醛基相连而构成的化合物。
②饱和一元醛的通式:
1、甲醛
或
物理性质:甲醛又叫蚁醛,无色、具有强烈刺激性气味的气体,35%—40%的甲醛溶液,叫福尔马林,具有防腐能力。
①通式: 官能团为:
R—CHO
—CHO
CnH2n+1CHO 或CnH2nO
用途:制酚醛树脂,有杀菌防腐功能,可制生物标本
化学性质
化学性质
⑴银镜反应
1mol甲醛最多可以还原得到4molAg。
⑵与碱性的新制氢氧化铜(菲林试剂)反应
⑶还原反应
(4)缩聚反应
甲醛中有2个活泼氢可被氧化
酚醛树脂
单体
单体
★
为求延长保质期 不良奸商竟然给冰鲜鱼浸甲醛保鲜
甲醛有毒,如果用它来浸泡水产,可以固定海鲜、河鲜形态,保持鱼类色泽水发鱿鱼全部含甲醛 食用过量会休克和致癌
儿童房甲醛超标易诱发儿童白血病
给孩子买衣服既要注意款式也要注意安全
去甲醛十大植物高手
吊兰
龙舌兰
醛可看成醛基取代了烃中的氢原子,书写同分异构体时应把醛写成
3. 醛的同分异构体
R-CHO
再判断烃基-R有几种同分异构体
写出C5H10O属于醛类的所有同分异构体
4、醛酮的分类和命名
①按烃基类型不同:
(1)分类
②按烃基中是否含不饱和键分:
①习惯命名法
(2)醛酮的命名
酮根据羰基所连的两个烃基名来命名,把较简单的烃基名称放在前面,较复杂的烃基名称放在后面,最后加“酮”字。
②系统命名法
(1)脂肪族醛酮的命名
选择包含羰基的最长碳链为主链,从靠近羰基的一端开始编号,依次标明碳原子的位次。在名称中要注明羰基的位置。
3-甲基丁醛
2-苯基丙醛
3-戊酮
2,4-戊二酮
3-甲基环戊酮
醛、酮碳原子的位次,除用1,2,3,4,…表示外,也可用α,β,γ…希腊字母表示。α是指官能团羰基旁第一个位置,β是指第二个位置…。酮中一边用α,β,γ…,另一边用α’ β’ γ’…。
β—戊烯醛
(2)不饱和醛、酮的命名
从靠近羰基一端给主链编号。命名称为“某烯醛(酮)”或“某炔醛(酮)”。
2,3-二甲基-4-戊烯醛
3-甲基-4-己烯-2-酮
(3)含醛基、酮基的碳链上的氢被芳环或环烷基取代,就把芳环或环烷基当作主链上的取代基看待:
醛基与芳环、脂环或杂环上的碳原子直接相连时,它们的命名可在相应的环系名称之后加上“醛”字。
2-苯丙醛
1-环己基-1-丙酮
环己醛
1,2-萘二醛
(4)多元醛、酮命名
含有两个以上羰基的化合物,可用二醛、二酮等,醛作取代基时,可用词头“甲酰基”或“氧代”表示;酮作取代时,用词头“氧代”表示。
2,4—戊二酮
3—氧代丁醛
化学性质
(1)和H2加成被还原成醇
(2)氧化反应
a.燃烧
b.催化氧化成羧酸
c.被弱氧化剂氧化
Ⅰ.银镜反应
Ⅱ.与新制的氢氧化铜反应
d.使酸性KMnO4溶液和溴水褪色
小结:醛类的化学性质
还原反应:加氢或失氧
氧化反应:加氧或失氢
有机的氧化还原反应
>C=O称羰基,是酮的官能团,丙酮是最简单的酮。
科学视野
酮:羰基碳原子与两个烃基相连的化合物。
丙酮
丙酮不能被银氨溶液、新制的氢氧化铜等弱氧化剂氧化,但可催化加氢生成醇。
作业 P.59 1、2、3、4
