人教版高中化学选修5第一章:1.4.《研究有机物的一般步骤与方法》课件(共26张PPT)
文档属性
| 名称 | 人教版高中化学选修5第一章:1.4.《研究有机物的一般步骤与方法》课件(共26张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 505.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-02-19 00:00:00 | ||
图片预览








文档简介
(共26张PPT)
第二章 分子结构与性质
第4节 研究有机化合物的一般
步骤和方法
第一章 认识有机化合物
人教版高中化学选修五
1、常用的分离、提纯物质的方法有哪些?
2、下列物质中的杂质(括号中是杂质)分别可以用什么方法除去。
(1)NaCl(泥沙) (2)酒精(水)
(3)溴(水) (4) KNO3 (NaCl)
3、分离、提纯物质的总的原则是什么?
有机物的分离与提纯
过滤、蒸馏 、重结晶、萃取
过滤
蒸馏
萃取
重结晶
不增、不减、易分离、易复原
1、蒸馏:
(2)有机物蒸馏提纯的条件
有机物热稳定性较强;
与杂质的沸点相差较大(一般约大于30℃)
(1)蒸馏的原理
是分离提纯液态有机物的常用方法。利用混合物的沸点不同,除去难挥发或不挥发的杂质。
蒸馏烧瓶
冷凝管
温度计
尾接管
冷水
热水
锥形瓶
蒸馏操作中的注意事项
仪器组装的顺序:“先下后上,由左至右”;
不得直接加热蒸馏烧瓶。其盛装的液体,最多不超过容积的2/3;不得将全部溶液蒸干;
冷凝水水流方向:从下口进水,上口出水
温度计水银球位置应与蒸馏烧瓶支管口齐平,以测量馏出蒸气的温度;
加入素烧瓷片的目的。
含杂质的工业酒精的蒸馏:
1、杂质:水、甲醇等
2、通过蒸馏可获得95.6℅的乙醇和4.4℅水的共沸混合物(
沸点78.15℃)若要得到更纯净的乙醇如何操作呢?
使用前要检查装置的气密性!
二、重结晶
原理:利用固体混合物中目标组分在某种溶剂中的溶解度随温度变化有明显差异,将有机物溶解在热的溶剂中制成饱和溶液,冷却后,由于溶解度减小,溶质又重新成晶体析出。由于产品与杂质在溶剂中的溶解度不同,可以通过过滤将杂质除去,从而达到分离提纯的目的。
选择溶剂的要求:
杂质在溶剂中溶解度很大或很小(前一种情况杂质将留在母液中不析出,后一种情况是使杂质在热过滤时被除去)
目标组分在此溶剂中的溶解度,受温度的影响较大
(该有机物在热溶液中的溶解度较大,在冷溶液中溶解度较小,冷却后易于形成晶体。)
重结晶操作中的使用的仪器:烧杯、三脚架、石棉网、玻璃棒、酒精灯、漏斗、铁架台
实验:粗苯甲酸的重结晶并完成教材中的学与问
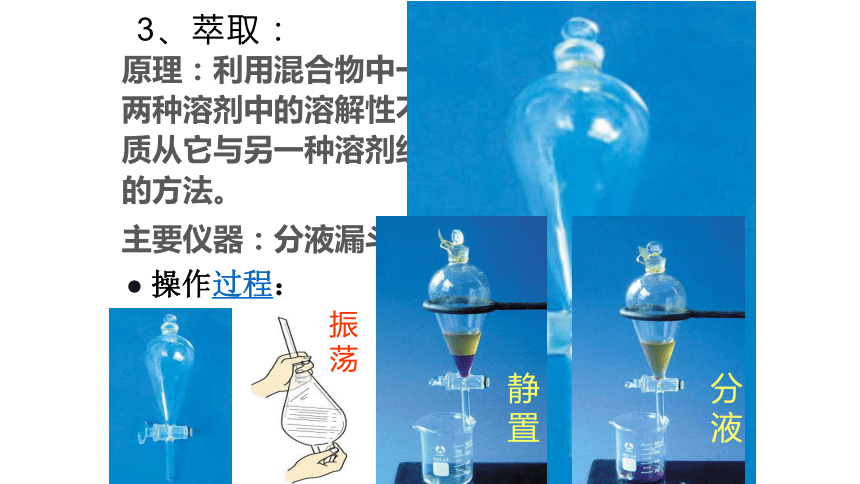
3、萃取:
原理:利用混合物中一种溶质在互不相溶的两种溶剂中的溶解性不同,用一种溶剂把溶质从它与另一种溶剂组成的溶液中提取出来的方法。
主要仪器:分液漏斗、烧杯、铁架台
操作过程:
振荡
静置
分液
3、萃取
萃取剂的选择:
①与原溶剂互不相溶
②被萃取的物质在萃取剂中的溶解度要大得多
常见的有机萃取剂:
乙醚、石油醚、二氯甲烷、四氯化碳……
萃取分类:
1)液—液萃取:是利用有机物在两种互不相溶的溶剂中的溶解性不同,将有机物从一种溶剂转移到另一种溶剂的过程。
2)固—液萃取:是用有机溶剂从固体物质中溶解出有机物的过程 。(专用仪器设备)
4、色谱法:阅读P.19
利用吸附剂对不同有机物吸附作用的不同,分离、提纯有机物的方法。
例如:用粉笔分离色素……
练习2 下列每组中各有三对物质,它们都能用分液漏斗分离的是
A 乙酸乙酯和水,酒精和水,植物油和水
B 四氯化碳和水,溴苯和水,硝基苯和水
C 甘油和水,乙酸和水,乙酸和乙醇
D 汽油和水,苯和水,己烷和水
√
√
练习3 可以用分液漏斗分离的一组液体混和物是
A 溴和四氯化碳 B 苯和溴苯
C 汽油和苯 D 硝基苯和水
√
适当记忆一些有机物质相对与水的密度大小,对于解决萃取分液的实验题是很有帮助的
二、元素分析与相对分子质量的测定
李比希法
现代元素分析仪
分析方法
定量分析的原理:将一定量的有机物燃烧,使其分解为
简单的无机物并作定量测定,通过无机物的质量推算出
组成该有机物元素原子的质量分数。
从而获得有机物的实验式
1、元素分析:
定性分析——有机物的组成元素分析;
定量分析——分子内各元素原子的质量分数
燃烧法
例1、某含C、H、O三种元素的未知物A,经燃烧分析实验测定该未知物中碳的质量分数为52.16%,氢的质量分数为13.14%。(P20)
(1)试求该未知物A的实验式
(2)若要确定它的分子式,还需要什么条件?
未知物的相对分子质量
2、相对分子质量的测定---质谱法
原理:
⑴、质荷比是什么?
⑵、质谱图的作用:
谱图中的质荷比最大的就是未知物的相对分子质量
最右边的分子离子峰的质荷比就是相对分子质量。
分子离子、碎片离子的相对质量与其电荷的比值
下图是例1中有机物A的质谱图,则其相对分子质量为( ),分子式为( )。
46
C2H6O
练习1
则该有机物可能是
A 甲醇 B 甲烷 C 丙烷 D 乙烯
√
三、分子结构的鉴定
结构式
(确定有机物的官能团)
分子式
H—C—O—C—H H—C—C—O—H
H
H
H
H
H
H
H
H
分子式都是C2H6O,能否推测出它的结构?
1、红外光谱
原理:课本P22
用途:推知有机物含有哪些化学键
红外光谱图中不包括C-C键
绝大多数的化学键、官能团、化合物的红外光谱图已建成数据库,通过对比就可直接获得有机物的结构。
三、分子结构的鉴定
读P22红外光谱图,推测例1未知物A的官能团
判断甲酸甲酯、乙酸在红外光谱图有几个振动吸收?
3、4
[练习2]有机物的分子式为C4H10O,确定其属于醇或醚分子结构,请写出该分子的结构简式
C—O—C
对称CH3
对称CH2
CH3CH2OCH2CH3
[例2]下图是一种分子式为C4H8O2的有机物的红外光谱谱图,则该有机物属于酯或羧酸的结构简式为:
C—O—C
C=O
不对称CH3
CH3COOCH2CH3
CH3CH2COOCH3
由图谱获取的是碎片信息,可根据分子组成通式大致判断有机物的类别,再按碳四价的原则对官能团、基团进行合理的拼接。
2、核磁共振氢谱(HNMR)
原理:不同化学环境的氢原子(等效氢原子)因产生共
振时吸收的频率不同,被核磁共振仪记录下来的
吸收峰的面积不同。
用途:由峰的组数可推测等效氢的种类
由峰的强度(包括峰的面积或积分曲线的高度)判断等效氢的相对数目
(读P22图1-19 1-20)
[练习3] 分子式为C3H6O2的二元混合物,如果在核磁共振氢谱上观察到氢原子给出的峰有两种情况。第一种情况峰给出的强度为1︰1;第二种情况峰给出的强度为3︰2︰1。由此推断混合物的组成可能是(写结构简式) 。
CH3COOCH3
CH3CH2COOH
HCOOCH2CH3
研究有机物的一般步骤
分离、提纯
元素定量分析
确定实验式
测定相对分子质量
确定分子式
现代物理实验
方法
确定结构式
练习4、一个有机物的分子量为70,红外光谱表征到碳碳双键和C=O的存在,核磁共振氢谱列如下图:
①写出该有机物的分子式:
②写出该有机物的可能的结构简式:
C4H6O
CH2=CH-C-CH3
O
洗涤沉淀或晶体的方法:用胶头滴管
往晶体上加蒸馏水直至晶体被浸没,
待水完全流出后,重复两至三次,直
至晶体被洗净。
检验洗涤效果:取最后一次的洗出液,
再选择适当的试剂进行检验。
一、蒸馏
1、蒸馏法适用于分离、提纯何类有机物?对该类有机物与杂质的沸点区别有何要求?
2、实验室进行蒸馏实验时,用到的仪器主要有哪些?
3、思考实验1-1的实验步骤,有哪些需要注意的事项?
第二章 分子结构与性质
第4节 研究有机化合物的一般
步骤和方法
第一章 认识有机化合物
人教版高中化学选修五
1、常用的分离、提纯物质的方法有哪些?
2、下列物质中的杂质(括号中是杂质)分别可以用什么方法除去。
(1)NaCl(泥沙) (2)酒精(水)
(3)溴(水) (4) KNO3 (NaCl)
3、分离、提纯物质的总的原则是什么?
有机物的分离与提纯
过滤、蒸馏 、重结晶、萃取
过滤
蒸馏
萃取
重结晶
不增、不减、易分离、易复原
1、蒸馏:
(2)有机物蒸馏提纯的条件
有机物热稳定性较强;
与杂质的沸点相差较大(一般约大于30℃)
(1)蒸馏的原理
是分离提纯液态有机物的常用方法。利用混合物的沸点不同,除去难挥发或不挥发的杂质。
蒸馏烧瓶
冷凝管
温度计
尾接管
冷水
热水
锥形瓶
蒸馏操作中的注意事项
仪器组装的顺序:“先下后上,由左至右”;
不得直接加热蒸馏烧瓶。其盛装的液体,最多不超过容积的2/3;不得将全部溶液蒸干;
冷凝水水流方向:从下口进水,上口出水
温度计水银球位置应与蒸馏烧瓶支管口齐平,以测量馏出蒸气的温度;
加入素烧瓷片的目的。
含杂质的工业酒精的蒸馏:
1、杂质:水、甲醇等
2、通过蒸馏可获得95.6℅的乙醇和4.4℅水的共沸混合物(
沸点78.15℃)若要得到更纯净的乙醇如何操作呢?
使用前要检查装置的气密性!
二、重结晶
原理:利用固体混合物中目标组分在某种溶剂中的溶解度随温度变化有明显差异,将有机物溶解在热的溶剂中制成饱和溶液,冷却后,由于溶解度减小,溶质又重新成晶体析出。由于产品与杂质在溶剂中的溶解度不同,可以通过过滤将杂质除去,从而达到分离提纯的目的。
选择溶剂的要求:
杂质在溶剂中溶解度很大或很小(前一种情况杂质将留在母液中不析出,后一种情况是使杂质在热过滤时被除去)
目标组分在此溶剂中的溶解度,受温度的影响较大
(该有机物在热溶液中的溶解度较大,在冷溶液中溶解度较小,冷却后易于形成晶体。)
重结晶操作中的使用的仪器:烧杯、三脚架、石棉网、玻璃棒、酒精灯、漏斗、铁架台
实验:粗苯甲酸的重结晶并完成教材中的学与问
3、萃取:
原理:利用混合物中一种溶质在互不相溶的两种溶剂中的溶解性不同,用一种溶剂把溶质从它与另一种溶剂组成的溶液中提取出来的方法。
主要仪器:分液漏斗、烧杯、铁架台
操作过程:
振荡
静置
分液
3、萃取
萃取剂的选择:
①与原溶剂互不相溶
②被萃取的物质在萃取剂中的溶解度要大得多
常见的有机萃取剂:
乙醚、石油醚、二氯甲烷、四氯化碳……
萃取分类:
1)液—液萃取:是利用有机物在两种互不相溶的溶剂中的溶解性不同,将有机物从一种溶剂转移到另一种溶剂的过程。
2)固—液萃取:是用有机溶剂从固体物质中溶解出有机物的过程 。(专用仪器设备)
4、色谱法:阅读P.19
利用吸附剂对不同有机物吸附作用的不同,分离、提纯有机物的方法。
例如:用粉笔分离色素……
练习2 下列每组中各有三对物质,它们都能用分液漏斗分离的是
A 乙酸乙酯和水,酒精和水,植物油和水
B 四氯化碳和水,溴苯和水,硝基苯和水
C 甘油和水,乙酸和水,乙酸和乙醇
D 汽油和水,苯和水,己烷和水
√
√
练习3 可以用分液漏斗分离的一组液体混和物是
A 溴和四氯化碳 B 苯和溴苯
C 汽油和苯 D 硝基苯和水
√
适当记忆一些有机物质相对与水的密度大小,对于解决萃取分液的实验题是很有帮助的
二、元素分析与相对分子质量的测定
李比希法
现代元素分析仪
分析方法
定量分析的原理:将一定量的有机物燃烧,使其分解为
简单的无机物并作定量测定,通过无机物的质量推算出
组成该有机物元素原子的质量分数。
从而获得有机物的实验式
1、元素分析:
定性分析——有机物的组成元素分析;
定量分析——分子内各元素原子的质量分数
燃烧法
例1、某含C、H、O三种元素的未知物A,经燃烧分析实验测定该未知物中碳的质量分数为52.16%,氢的质量分数为13.14%。(P20)
(1)试求该未知物A的实验式
(2)若要确定它的分子式,还需要什么条件?
未知物的相对分子质量
2、相对分子质量的测定---质谱法
原理:
⑴、质荷比是什么?
⑵、质谱图的作用:
谱图中的质荷比最大的就是未知物的相对分子质量
最右边的分子离子峰的质荷比就是相对分子质量。
分子离子、碎片离子的相对质量与其电荷的比值
下图是例1中有机物A的质谱图,则其相对分子质量为( ),分子式为( )。
46
C2H6O
练习1
则该有机物可能是
A 甲醇 B 甲烷 C 丙烷 D 乙烯
√
三、分子结构的鉴定
结构式
(确定有机物的官能团)
分子式
H—C—O—C—H H—C—C—O—H
H
H
H
H
H
H
H
H
分子式都是C2H6O,能否推测出它的结构?
1、红外光谱
原理:课本P22
用途:推知有机物含有哪些化学键
红外光谱图中不包括C-C键
绝大多数的化学键、官能团、化合物的红外光谱图已建成数据库,通过对比就可直接获得有机物的结构。
三、分子结构的鉴定
读P22红外光谱图,推测例1未知物A的官能团
判断甲酸甲酯、乙酸在红外光谱图有几个振动吸收?
3、4
[练习2]有机物的分子式为C4H10O,确定其属于醇或醚分子结构,请写出该分子的结构简式
C—O—C
对称CH3
对称CH2
CH3CH2OCH2CH3
[例2]下图是一种分子式为C4H8O2的有机物的红外光谱谱图,则该有机物属于酯或羧酸的结构简式为:
C—O—C
C=O
不对称CH3
CH3COOCH2CH3
CH3CH2COOCH3
由图谱获取的是碎片信息,可根据分子组成通式大致判断有机物的类别,再按碳四价的原则对官能团、基团进行合理的拼接。
2、核磁共振氢谱(HNMR)
原理:不同化学环境的氢原子(等效氢原子)因产生共
振时吸收的频率不同,被核磁共振仪记录下来的
吸收峰的面积不同。
用途:由峰的组数可推测等效氢的种类
由峰的强度(包括峰的面积或积分曲线的高度)判断等效氢的相对数目
(读P22图1-19 1-20)
[练习3] 分子式为C3H6O2的二元混合物,如果在核磁共振氢谱上观察到氢原子给出的峰有两种情况。第一种情况峰给出的强度为1︰1;第二种情况峰给出的强度为3︰2︰1。由此推断混合物的组成可能是(写结构简式) 。
CH3COOCH3
CH3CH2COOH
HCOOCH2CH3
研究有机物的一般步骤
分离、提纯
元素定量分析
确定实验式
测定相对分子质量
确定分子式
现代物理实验
方法
确定结构式
练习4、一个有机物的分子量为70,红外光谱表征到碳碳双键和C=O的存在,核磁共振氢谱列如下图:
①写出该有机物的分子式:
②写出该有机物的可能的结构简式:
C4H6O
CH2=CH-C-CH3
O
洗涤沉淀或晶体的方法:用胶头滴管
往晶体上加蒸馏水直至晶体被浸没,
待水完全流出后,重复两至三次,直
至晶体被洗净。
检验洗涤效果:取最后一次的洗出液,
再选择适当的试剂进行检验。
一、蒸馏
1、蒸馏法适用于分离、提纯何类有机物?对该类有机物与杂质的沸点区别有何要求?
2、实验室进行蒸馏实验时,用到的仪器主要有哪些?
3、思考实验1-1的实验步骤,有哪些需要注意的事项?
