人教版九年级化学下册 8.2金属的化学性质第一课时(共26张PPT)
文档属性
| 名称 | 人教版九年级化学下册 8.2金属的化学性质第一课时(共26张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-02-23 00:00:00 | ||
图片预览




文档简介
(共26张PPT)
第八单元 金属和金属材料
学习目标
1.知道大多数金属都可以与氧气反应,但难易程度不同
2.知道部分金属可以和稀盐酸、稀硫酸反应
3.知道置换反应
4.知道金属在溶液中活动性顺序,
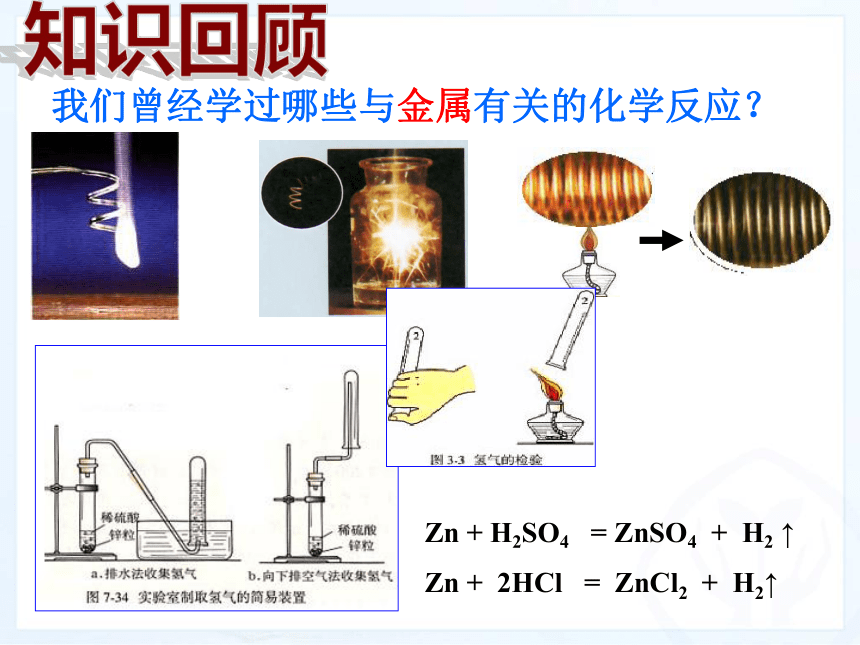
我们曾经学过哪些与金属有关的化学反应?
金属与氧气反应的剧烈程度
火星四射,放热,生成黑色固体
耀眼的白光,放热,生成白色固体
由红色变为黑色
填写【表1】√
不同
√
√
镁在空气中燃烧 √
铁丝在氧气中燃烧
铜在酒精灯上加热
金属与氧气反应的难易
在常温就能与氧气反应,生成致密的氧化铝(Al2O3)膜
在常温就能与氧气反应,生成复杂的氧化膜
铁在氧气浓度比较高时才能被点燃
在常温几乎不与氧气反应,加热时可以(现象平缓)
在高温时也不与氧气反应(真金不怕火炼)
2Mg+O2=2MgO
4Al+3O2=2Al2O3
不同
与氧气反应的条件 ★化学方程式
镁
铝
铁
铜
金
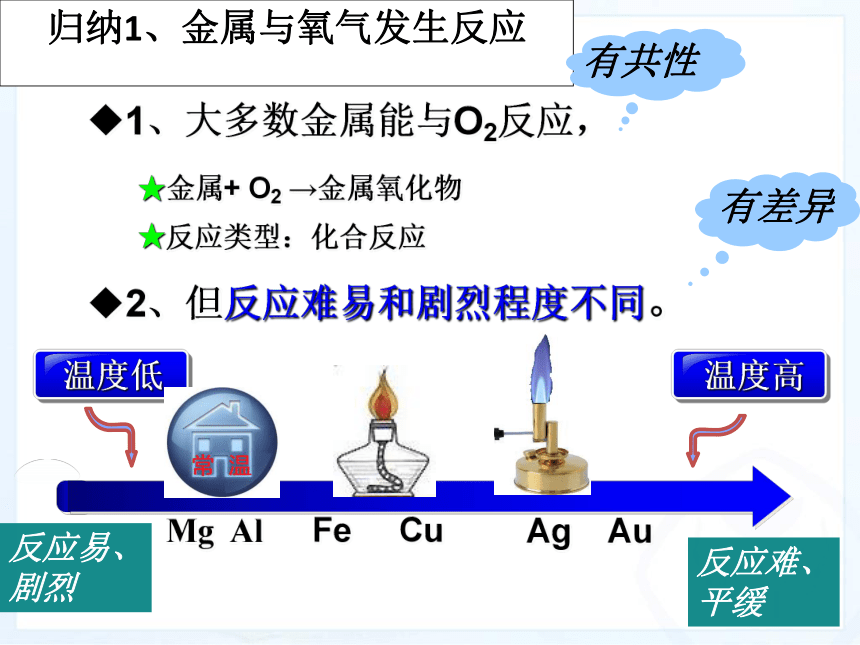
归纳1、金属与氧气发生反应
反应易、
剧烈
反应难、
平缓
1、大多数金属能与O2反应,
★反应类型:化合反应
★金属+ O2 →金属氧化物
2、但反应难易和剧烈程度不同。
Mg Al Fe Cu Ag Au
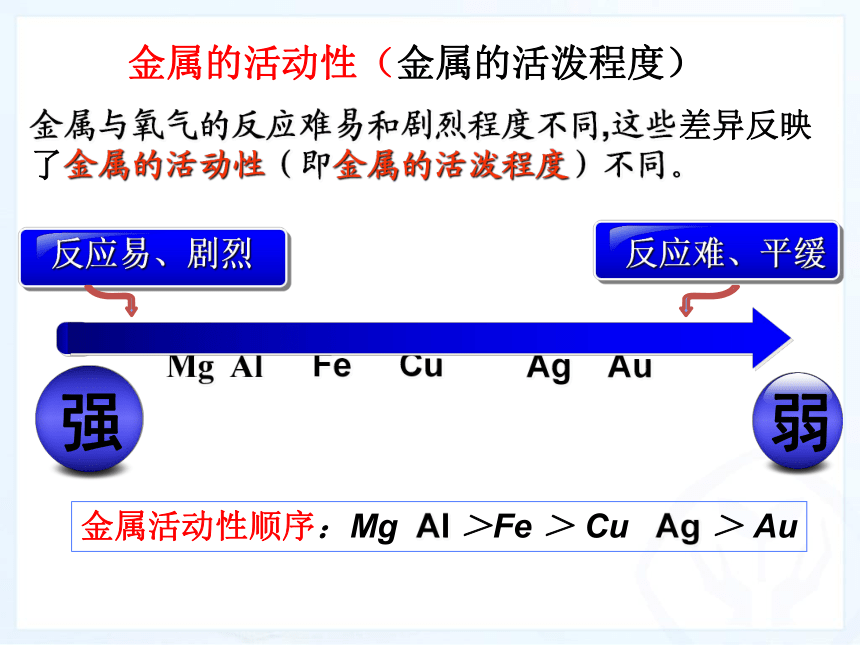
金属与氧气的反应难易和剧烈程度不同,这些差异反映了金属的活动性(即金属的活泼程度)不同。
金属的活动性(金属的活泼程度)
金属活动性顺序:Mg Al >Fe > Cu Ag > Au
Mg Al Fe Cu Ag Au
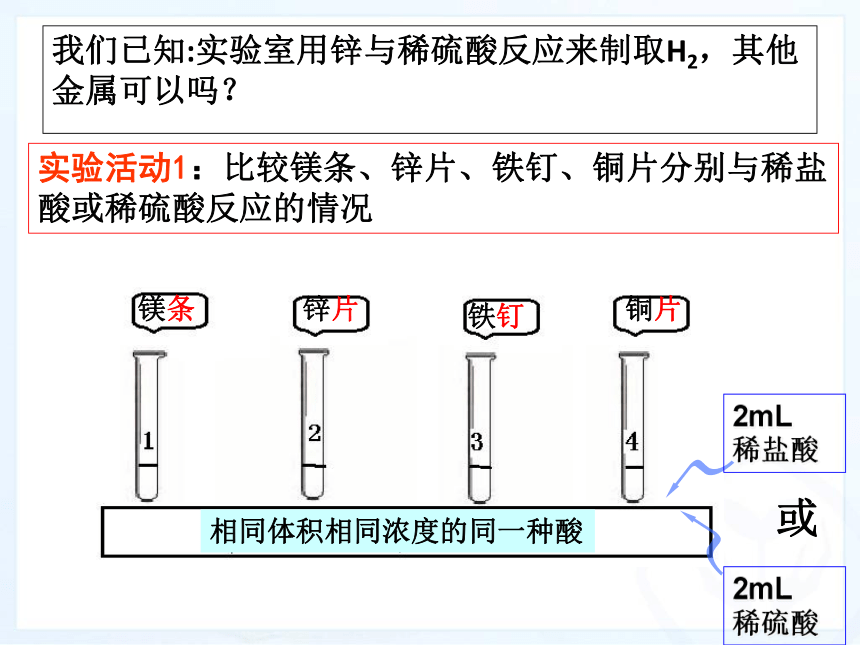
我们已知:实验室用锌与稀硫酸反应来制取H2,其他金属可以吗?
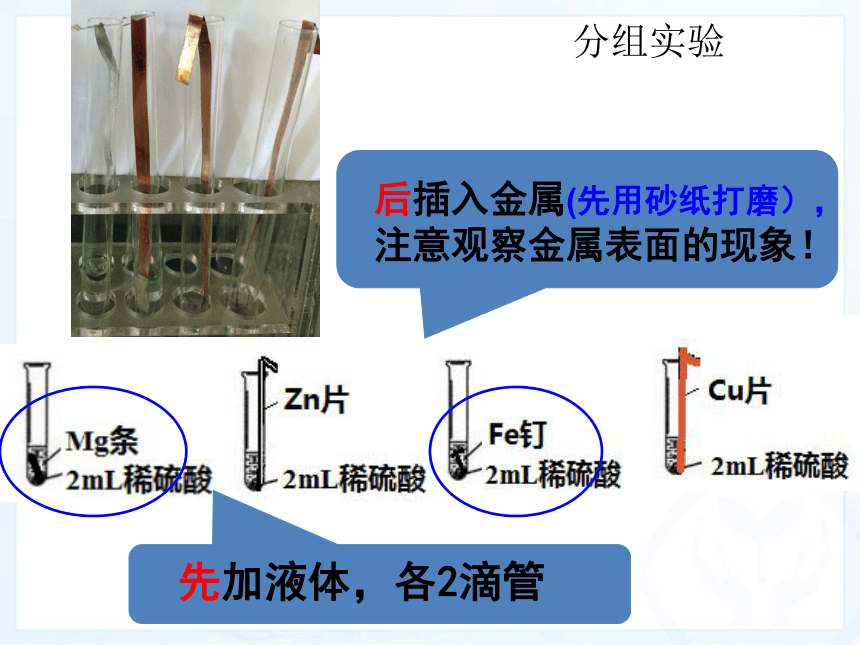
实验活动1:比较镁条、锌片、铁钉、铜片分别与稀盐酸或稀硫酸反应的情况
铜片
铁钉
镁条
锌片
相同体积相同浓度的同一种酸
分组实验
实验现象分析
2mL稀盐酸
Mg
Zn
(无气泡生成)
Fe
Cu
镁、锌、铁、铜与盐酸的反应
Mg
Zn
Fe
Cu
小黑点表表产生的气泡
归纳2:金属与稀盐酸、稀硫酸的反应
1、大多数金属可以和酸发生反应;
2、能和酸反应的金属,其反应的剧烈程度不同。
无明显现象
Fe+2HCl = FeCl2+ H2 ↑
Mg+2HCl= MgCl2 + H2↑
Mg+H2SO4= MgSO4 +H2 ↑
Fe + H2SO4 = FeSO4 + H2 ↑
较慢
较少
剧烈
很多
3、反应类型:置换反应
金属+ 酸 → 金属化合物 + H2 ↑
反应的现象 与盐酸反应
的化学方程式 与硫酸反应
的化学方程式
镁 反应 ,
有 气泡产生
锌 反应较快,
有较多气泡产生 Zn+2HCl==ZnCl2+H2↑ Zn+H2SO4==ZnSO4+H2↑
铁 反应 ,
有 气泡产生
铜
结论
金属与酸的反应也是有共性和有差异!
金属活动性顺序:Mg> Zn > Fe > Cu
常见金属在溶液中的活动性顺序
★
1、金属的位置越靠前,它的活动性就越强
2、位于H前面的金属能置换出盐酸、稀硫酸中的氢
相信你能发现:
1.很多金属都能与盐酸或稀硫酸发生 ,但反应的剧烈程度 。
2.根据金属与酸能否反应以及反应的剧烈程度,判断金属的活泼程度(即金属活动性)。
Mg、Zn、Fe的金属活动性比Cu铜强,能置换出盐酸或稀硫酸中的氢。
置换反应
不相同
【1】在实验室制取氢气,选择锌的理由是什么?
思考:银和铜的金属活动性强弱可以通过加入稀盐酸来比较吗?
可以用稀盐酸来鉴别银镯子和铝镯子。
即:铝和银的金属活动性强弱可以通过加入稀盐酸来比较。
★
★
★
单质 单质
化合物 化合物
它们有什么共同的特征?
置换反应:
一种___一种____反应,生成另
一种 ___和另一种____的反应。
单质
化合物
化合物
单质
置换反应的形式
A +BC ==B +AC
化学反应的基本类型
思考:你知道哪些反应类型请各写出一例?
置换反应:
由一种单质与一种化合物反应,生成另一种单质和化合物的反应
单质+化合物=另一单质+另一化合物
置换反应:A + BC → AC + B
化合反应:A + B + … → AB…(多变一)
分解反应:AB →A + B + … (一变多)
1、下列反应中,属于置换反应的是( )
A. 2H2O2 = 2H2O+ O2↑
B. CuO+CO = Cu+CO2
C. H2+CuO = Cu+H2O
D. CO2+H2O = H2CO3
△
MnO2
△
C
从反应物和生成物的物质类别和种类的角度分析置换反应。
2.小兰家中收藏一件清末的铝制佛像,该佛像至今保存十分完好。其主要原因是( )
A.铝不易发生化学反应
B.铝的氧化物容易发生还原反应
C.铝不易被氧化
D.铝易氧化,但氧化铝具有保护内部铝的作用
D
3、下列反应属于置换反应的是( )
①H2+CuO === Cu+H2O
②2CO+O2===2CO
③Zn+2HCl===ZnCl+H2
④Fe2O3+3CO === 2Fe+3CO2
A、①④ B、②③ C、①③ D、②④
加热
高温
C
4.有两包黑色粉末,分别是铁粉和木炭粉,请你设计多种实验方案加以鉴别,并填写下列实验报告。
用磁铁吸引
能被磁铁吸引的是铁
分别在空气中灼烧
能红热且质量减少的是碳
分别放入酸中
能生成气体的是铁
步骤 现象和结论
方案一
方案二
方案三
1、很多金属能与盐酸、硫酸等发生反应, 但反应的难易和剧烈程度不同,把金属分为活泼金属和不活泼金属
2、置换反应
金属的化学性质
一、金属与氧气的反应
4Al+3O2=2Al2O3
2Mg+O2=2MgO
3Fe+2 O2 Fe3 O4
二、金属与稀盐酸、稀硫酸反应( 置换反应 )
Fe + 2HCl == FeCl2 + H2 ↑
Fe + H2 SO4 == Fe SO4 + H2 ↑
Zn + 2HCl == ZnCl2 + H2 ↑
Zn + H2 SO4 == Zn SO4 + H2 ↑
Mg + 2HCl == MgCl2 + H2 ↑
Mg + H2 SO4 == Mg SO4 + H2 ↑
第八单元 金属和金属材料
学习目标
1.知道大多数金属都可以与氧气反应,但难易程度不同
2.知道部分金属可以和稀盐酸、稀硫酸反应
3.知道置换反应
4.知道金属在溶液中活动性顺序,
我们曾经学过哪些与金属有关的化学反应?
金属与氧气反应的剧烈程度
火星四射,放热,生成黑色固体
耀眼的白光,放热,生成白色固体
由红色变为黑色
填写【表1】√
不同
√
√
镁在空气中燃烧 √
铁丝在氧气中燃烧
铜在酒精灯上加热
金属与氧气反应的难易
在常温就能与氧气反应,生成致密的氧化铝(Al2O3)膜
在常温就能与氧气反应,生成复杂的氧化膜
铁在氧气浓度比较高时才能被点燃
在常温几乎不与氧气反应,加热时可以(现象平缓)
在高温时也不与氧气反应(真金不怕火炼)
2Mg+O2=2MgO
4Al+3O2=2Al2O3
不同
与氧气反应的条件 ★化学方程式
镁
铝
铁
铜
金
归纳1、金属与氧气发生反应
反应易、
剧烈
反应难、
平缓
1、大多数金属能与O2反应,
★反应类型:化合反应
★金属+ O2 →金属氧化物
2、但反应难易和剧烈程度不同。
Mg Al Fe Cu Ag Au
金属与氧气的反应难易和剧烈程度不同,这些差异反映了金属的活动性(即金属的活泼程度)不同。
金属的活动性(金属的活泼程度)
金属活动性顺序:Mg Al >Fe > Cu Ag > Au
Mg Al Fe Cu Ag Au
我们已知:实验室用锌与稀硫酸反应来制取H2,其他金属可以吗?
实验活动1:比较镁条、锌片、铁钉、铜片分别与稀盐酸或稀硫酸反应的情况
铜片
铁钉
镁条
锌片
相同体积相同浓度的同一种酸
分组实验
实验现象分析
2mL稀盐酸
Mg
Zn
(无气泡生成)
Fe
Cu
镁、锌、铁、铜与盐酸的反应
Mg
Zn
Fe
Cu
小黑点表表产生的气泡
归纳2:金属与稀盐酸、稀硫酸的反应
1、大多数金属可以和酸发生反应;
2、能和酸反应的金属,其反应的剧烈程度不同。
无明显现象
Fe+2HCl = FeCl2+ H2 ↑
Mg+2HCl= MgCl2 + H2↑
Mg+H2SO4= MgSO4 +H2 ↑
Fe + H2SO4 = FeSO4 + H2 ↑
较慢
较少
剧烈
很多
3、反应类型:置换反应
金属+ 酸 → 金属化合物 + H2 ↑
反应的现象 与盐酸反应
的化学方程式 与硫酸反应
的化学方程式
镁 反应 ,
有 气泡产生
锌 反应较快,
有较多气泡产生 Zn+2HCl==ZnCl2+H2↑ Zn+H2SO4==ZnSO4+H2↑
铁 反应 ,
有 气泡产生
铜
结论
金属与酸的反应也是有共性和有差异!
金属活动性顺序:Mg> Zn > Fe > Cu
常见金属在溶液中的活动性顺序
★
1、金属的位置越靠前,它的活动性就越强
2、位于H前面的金属能置换出盐酸、稀硫酸中的氢
相信你能发现:
1.很多金属都能与盐酸或稀硫酸发生 ,但反应的剧烈程度 。
2.根据金属与酸能否反应以及反应的剧烈程度,判断金属的活泼程度(即金属活动性)。
Mg、Zn、Fe的金属活动性比Cu铜强,能置换出盐酸或稀硫酸中的氢。
置换反应
不相同
【1】在实验室制取氢气,选择锌的理由是什么?
思考:银和铜的金属活动性强弱可以通过加入稀盐酸来比较吗?
可以用稀盐酸来鉴别银镯子和铝镯子。
即:铝和银的金属活动性强弱可以通过加入稀盐酸来比较。
★
★
★
单质 单质
化合物 化合物
它们有什么共同的特征?
置换反应:
一种___一种____反应,生成另
一种 ___和另一种____的反应。
单质
化合物
化合物
单质
置换反应的形式
A +BC ==B +AC
化学反应的基本类型
思考:你知道哪些反应类型请各写出一例?
置换反应:
由一种单质与一种化合物反应,生成另一种单质和化合物的反应
单质+化合物=另一单质+另一化合物
置换反应:A + BC → AC + B
化合反应:A + B + … → AB…(多变一)
分解反应:AB →A + B + … (一变多)
1、下列反应中,属于置换反应的是( )
A. 2H2O2 = 2H2O+ O2↑
B. CuO+CO = Cu+CO2
C. H2+CuO = Cu+H2O
D. CO2+H2O = H2CO3
△
MnO2
△
C
从反应物和生成物的物质类别和种类的角度分析置换反应。
2.小兰家中收藏一件清末的铝制佛像,该佛像至今保存十分完好。其主要原因是( )
A.铝不易发生化学反应
B.铝的氧化物容易发生还原反应
C.铝不易被氧化
D.铝易氧化,但氧化铝具有保护内部铝的作用
D
3、下列反应属于置换反应的是( )
①H2+CuO === Cu+H2O
②2CO+O2===2CO
③Zn+2HCl===ZnCl+H2
④Fe2O3+3CO === 2Fe+3CO2
A、①④ B、②③ C、①③ D、②④
加热
高温
C
4.有两包黑色粉末,分别是铁粉和木炭粉,请你设计多种实验方案加以鉴别,并填写下列实验报告。
用磁铁吸引
能被磁铁吸引的是铁
分别在空气中灼烧
能红热且质量减少的是碳
分别放入酸中
能生成气体的是铁
步骤 现象和结论
方案一
方案二
方案三
1、很多金属能与盐酸、硫酸等发生反应, 但反应的难易和剧烈程度不同,把金属分为活泼金属和不活泼金属
2、置换反应
金属的化学性质
一、金属与氧气的反应
4Al+3O2=2Al2O3
2Mg+O2=2MgO
3Fe+2 O2 Fe3 O4
二、金属与稀盐酸、稀硫酸反应( 置换反应 )
Fe + 2HCl == FeCl2 + H2 ↑
Fe + H2 SO4 == Fe SO4 + H2 ↑
Zn + 2HCl == ZnCl2 + H2 ↑
Zn + H2 SO4 == Zn SO4 + H2 ↑
Mg + 2HCl == MgCl2 + H2 ↑
Mg + H2 SO4 == Mg SO4 + H2 ↑
同课章节目录
