苏教化学必修2专题1第一单元 原子核外电子排布与元素周期律(共28张PPT)
文档属性
| 名称 | 苏教化学必修2专题1第一单元 原子核外电子排布与元素周期律(共28张PPT) |
|
|
| 格式 | zip | ||
| 文件大小 | 3.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-02-23 00:00:00 | ||
图片预览




文档简介
(共28张PPT)
第一节 原子核外电子的排布
专题1 微观结构与物质的多样性
一.原子结构
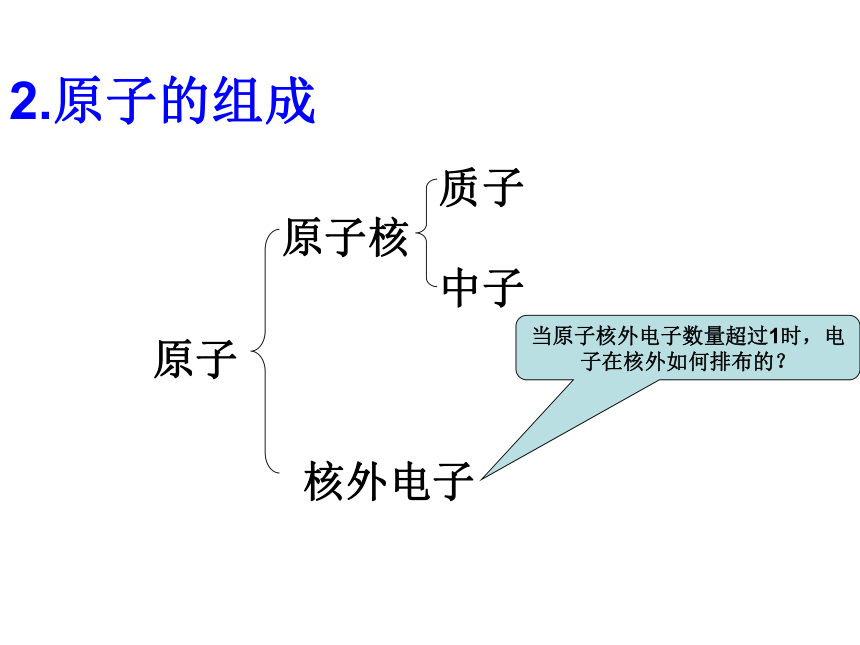
1.元素周期表中的新元素
新华社日内瓦6月8日电(记者张淼)总部位于瑞士苏黎世的国际纯粹与应用化学联合会8日宣布,将合成化学元素第113号(缩写为Nh)、115号(Mc)、117号(Ts)和118号(Og)提名为化学新元素。
该联合会去年年底宣布,确认上述4种新元素的存在。这些元素由俄罗斯、美国和日本的科研团队发现,他们也获得了对这些元素的正式命名权。
2.原子的组成
原子
原子核
核外电子
质子
中子
当原子核外电子数量超过1时,电子在核外如何排布的?
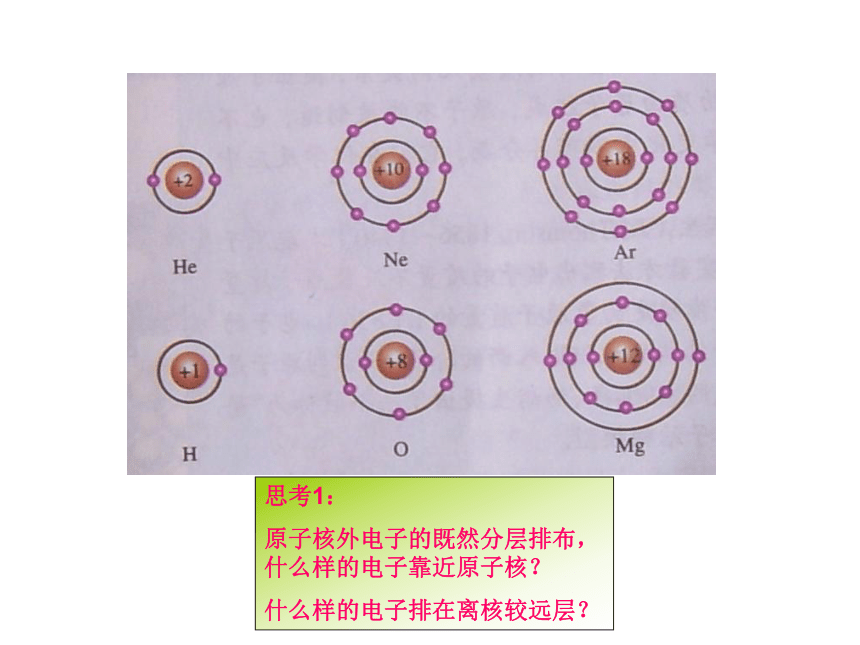
思考1:
原子核外电子的既然分层排布,什么样的电子靠近原子核?
什么样的电子排在离核较远层?
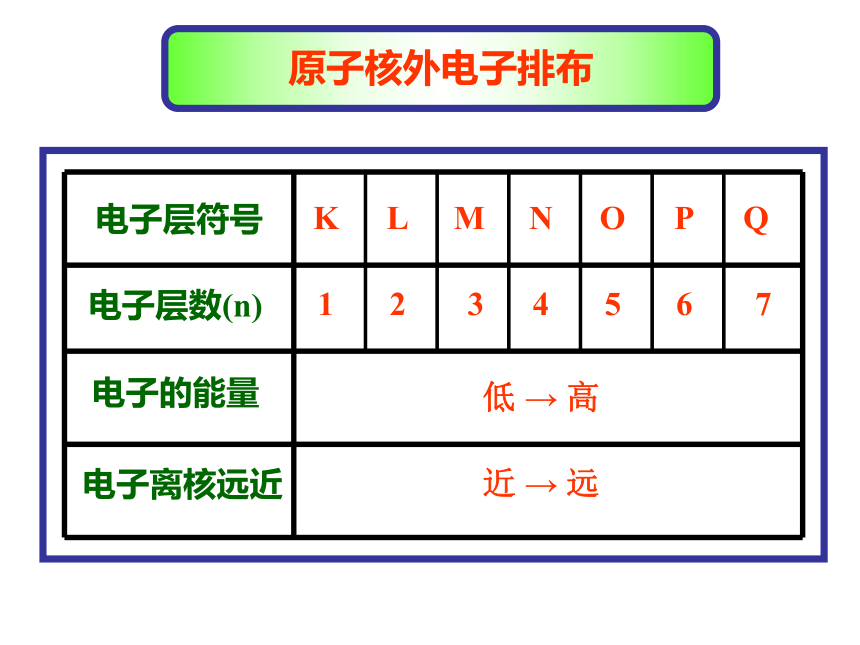
二.原子核外电子的排布(分层排布)
1.电子能量的高低与离核远、近的关系:
电子层
离核远近
能量高低
二 三 四 五 六 七
K L M N O P Q
低 高
近 远
原子核外电子排布
K
L
M
N
O
P
Q
1
2
3
4
5
6
7
低 → 高
近 → 远
2.原子结构示意图
核电荷数
电子层
该电子层上电子数
原子核
核外电子是分层排布的
为了形象、简单的表示原子的结构,人们就创造了“原子结构示意图”这种特殊的图形。
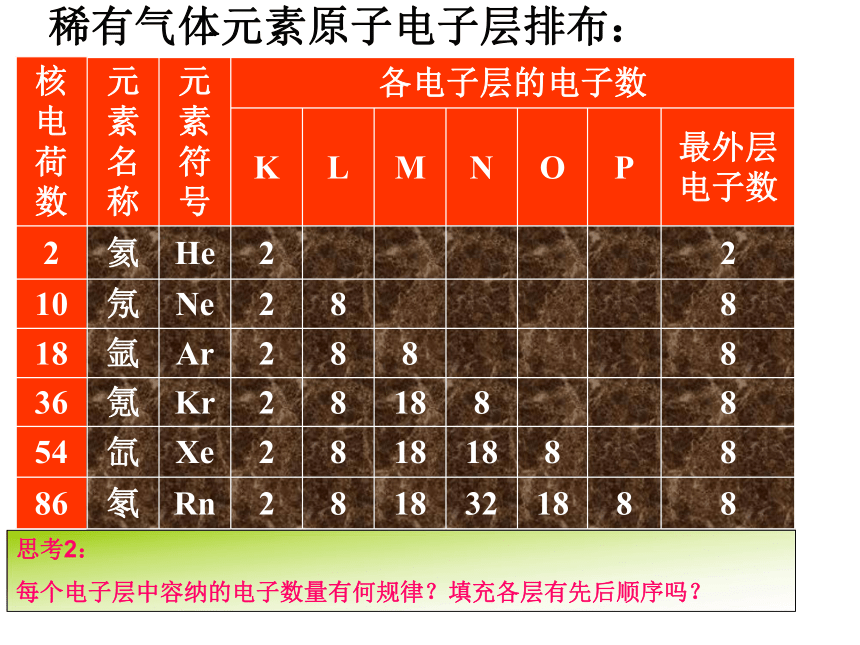
稀有气体元素原子电子层排布:
思考2:
每个电子层中容纳的电子数量有何规律?填充各层有先后顺序吗?
核电荷数 元素名称 元素符号 各电子层的电子数
K L M N O P 最外层电子数
2 氦 He 2 2
10 氖 Ne 2 8 8
18 氩 Ar 2 8 8 8
36 氪 Kr 2 8 18 8 8
54 氙 Xe 2 8 18 18 8 8
86 氡 Rn 2 8 18 32 18 8 8
3.原子核外电子分层排布的一般规律:
a、能量最低原理(K、L、M、N、O、P、Q)
b、每层最多容纳电子数2n2(n表示电子层数)
c、最外层电子数目不超过8个(第一层不超过2个)
d、次外层电子数目不超过18个
e、倒数第三层电子数目不超过32个
原子核外电子排布规律较为复杂,上述规律必须同时符合!
稀有气体元素原子电子层排布:
思考2:
每个电子层中容纳的电子数量有何规律?填充各层有先后顺序吗?
核电荷数 元素名称 元素符号 各电子层的电子数
K L M N O P 最外层电子数
2 氦 He 2 2
10 氖 Ne 2 8 8
18 氩 Ar 2 8 8 8
36 氪 Kr 2 8 18 8 8
54 氙 Xe 2 8 18 18 8 8
86 氡 Rn 2 8 18 32 18 8 8
某元素的原子结构示意图为
该元素的核电荷数为 个,
核外有 个电子层,
第二层上有 个电子,
最外电子层上有 个电子,
该元素符号为 元素。
13
3
8
3
Al
⑴第一层最多容纳___个电子第二层最多容纳__个电子
2
(2)最外层不超过 个电子
8
8
⑶电子先排满能量 的电子层,然后再排能量
稍 的电子层
低
高
请写出34号元素的原子结构示意图。
课堂练习:
硒与人体健康
硒元素是人体所必需的元素,在人体内的含量为6-20mg。
硒参与构成很多酶类,对人体健康具有重要作用,被国内外医药界和营养学界尊称为“生命的火种”,享有“长寿元素”、“抗癌之王”、“心脏守护神”“天然解毒剂”、“明亮的使者” 等美誉。
请写出113、115、117、118号元素的原子结构示意图。
课堂练习:
8个(He为2个)
比较稳定
三.原子结构与性质的关系
元素分类 最外层电子数 元素的化学性质
稀有气体
一般少于4个
易失电子
元素分类 最外层电子数 元素的化学性质
金 属
一般大于或等于4个
易得电子
元素分类 最外层电子数 元素的化学性质
非金属
金属
非金属
稀有气体
稳定结构
极难发生化学反应
元素分类、原子结构与元素化学性质的关系
决定元素化学性质的是 。
决定元素种类的是 。
核电荷数(或质子数)
最外层电子数
不稳定结构
不稳定结构
易失去最外
层电子
易得到电子
<4
≧4
=8 (He为2)
元素分类 最外层电子数 结构的稳性 化学性质
课堂讨论:
请结合原子核外电子排布规律和元素周期表的位置,分析117号元素的性质。(学生分组讨论)
(1)最高化合价
(2)是否为非金属元素
请写出镁离子与铯离子的离子结构示意图
课堂练习:
请写出硫离子与碘离子的离子结构示意图。
课堂练习:
1.下列原子结构示意图中,正确的是( )
2.某元素原子的原子核外有三个电子层,最外层有4个电子,该原子核内的质子数为( ) A.14 B.15 C.16 D.17
B
A
课堂练习:
3.根据下列叙述,写出元素名称并画出原子结构示意图。
(1)A元素原子核外M层电子数是L层电子数的1/2:
________
(2)B元素原子的最外层电子数是次外层电子数的
1.5倍:___ __
(3)C元素的次外层电子数是最外层电子数的1/4:
____________.
课堂练习:
4.原子的核电荷数小于18的某元素X,原子的电子层数为n,最外层电子数为2n+1,原子中的质子数是2n2-1。有关X的说法不正确的是(n为正整数)( )
A.X能形成化学式为X(OH)3的碱
B.X肯定能形成化学式为NaXO3的含氧酸钠盐
C.X原子的最外层电子数和核电荷数肯定为奇数
D.X可能与某些金属元素Y形成Y3X2型化合物
课堂练习:
A
5.在1~18号元素中,最外层电子数等于电子 层数的元素有( )
A.1种 B.2种
C.3种 D.4种
课堂练习:
C
课堂小结
原子核外电子排布规律内容:
a 、能量最低原理(K、L、M、N、O、P、Q)
b、每层最多容纳电子数2n2(n表示电子层数)
c、最外层电子数目不超过8个(第一层不超过2个)
d、次外层电子数目不超过18个,
e、倒数第三层电子数目不超过32个。
排布规律间相互制约
原子结结构能够决定原子的性质(如还原性与氧化性,化合价的规律等)
第一节 原子核外电子的排布
专题1 微观结构与物质的多样性
一.原子结构
1.元素周期表中的新元素
新华社日内瓦6月8日电(记者张淼)总部位于瑞士苏黎世的国际纯粹与应用化学联合会8日宣布,将合成化学元素第113号(缩写为Nh)、115号(Mc)、117号(Ts)和118号(Og)提名为化学新元素。
该联合会去年年底宣布,确认上述4种新元素的存在。这些元素由俄罗斯、美国和日本的科研团队发现,他们也获得了对这些元素的正式命名权。
2.原子的组成
原子
原子核
核外电子
质子
中子
当原子核外电子数量超过1时,电子在核外如何排布的?
思考1:
原子核外电子的既然分层排布,什么样的电子靠近原子核?
什么样的电子排在离核较远层?
二.原子核外电子的排布(分层排布)
1.电子能量的高低与离核远、近的关系:
电子层
离核远近
能量高低
二 三 四 五 六 七
K L M N O P Q
低 高
近 远
原子核外电子排布
K
L
M
N
O
P
Q
1
2
3
4
5
6
7
低 → 高
近 → 远
2.原子结构示意图
核电荷数
电子层
该电子层上电子数
原子核
核外电子是分层排布的
为了形象、简单的表示原子的结构,人们就创造了“原子结构示意图”这种特殊的图形。
稀有气体元素原子电子层排布:
思考2:
每个电子层中容纳的电子数量有何规律?填充各层有先后顺序吗?
核电荷数 元素名称 元素符号 各电子层的电子数
K L M N O P 最外层电子数
2 氦 He 2 2
10 氖 Ne 2 8 8
18 氩 Ar 2 8 8 8
36 氪 Kr 2 8 18 8 8
54 氙 Xe 2 8 18 18 8 8
86 氡 Rn 2 8 18 32 18 8 8
3.原子核外电子分层排布的一般规律:
a、能量最低原理(K、L、M、N、O、P、Q)
b、每层最多容纳电子数2n2(n表示电子层数)
c、最外层电子数目不超过8个(第一层不超过2个)
d、次外层电子数目不超过18个
e、倒数第三层电子数目不超过32个
原子核外电子排布规律较为复杂,上述规律必须同时符合!
稀有气体元素原子电子层排布:
思考2:
每个电子层中容纳的电子数量有何规律?填充各层有先后顺序吗?
核电荷数 元素名称 元素符号 各电子层的电子数
K L M N O P 最外层电子数
2 氦 He 2 2
10 氖 Ne 2 8 8
18 氩 Ar 2 8 8 8
36 氪 Kr 2 8 18 8 8
54 氙 Xe 2 8 18 18 8 8
86 氡 Rn 2 8 18 32 18 8 8
某元素的原子结构示意图为
该元素的核电荷数为 个,
核外有 个电子层,
第二层上有 个电子,
最外电子层上有 个电子,
该元素符号为 元素。
13
3
8
3
Al
⑴第一层最多容纳___个电子第二层最多容纳__个电子
2
(2)最外层不超过 个电子
8
8
⑶电子先排满能量 的电子层,然后再排能量
稍 的电子层
低
高
请写出34号元素的原子结构示意图。
课堂练习:
硒与人体健康
硒元素是人体所必需的元素,在人体内的含量为6-20mg。
硒参与构成很多酶类,对人体健康具有重要作用,被国内外医药界和营养学界尊称为“生命的火种”,享有“长寿元素”、“抗癌之王”、“心脏守护神”“天然解毒剂”、“明亮的使者” 等美誉。
请写出113、115、117、118号元素的原子结构示意图。
课堂练习:
8个(He为2个)
比较稳定
三.原子结构与性质的关系
元素分类 最外层电子数 元素的化学性质
稀有气体
一般少于4个
易失电子
元素分类 最外层电子数 元素的化学性质
金 属
一般大于或等于4个
易得电子
元素分类 最外层电子数 元素的化学性质
非金属
金属
非金属
稀有气体
稳定结构
极难发生化学反应
元素分类、原子结构与元素化学性质的关系
决定元素化学性质的是 。
决定元素种类的是 。
核电荷数(或质子数)
最外层电子数
不稳定结构
不稳定结构
易失去最外
层电子
易得到电子
<4
≧4
=8 (He为2)
元素分类 最外层电子数 结构的稳性 化学性质
课堂讨论:
请结合原子核外电子排布规律和元素周期表的位置,分析117号元素的性质。(学生分组讨论)
(1)最高化合价
(2)是否为非金属元素
请写出镁离子与铯离子的离子结构示意图
课堂练习:
请写出硫离子与碘离子的离子结构示意图。
课堂练习:
1.下列原子结构示意图中,正确的是( )
2.某元素原子的原子核外有三个电子层,最外层有4个电子,该原子核内的质子数为( ) A.14 B.15 C.16 D.17
B
A
课堂练习:
3.根据下列叙述,写出元素名称并画出原子结构示意图。
(1)A元素原子核外M层电子数是L层电子数的1/2:
________
(2)B元素原子的最外层电子数是次外层电子数的
1.5倍:___ __
(3)C元素的次外层电子数是最外层电子数的1/4:
____________.
课堂练习:
4.原子的核电荷数小于18的某元素X,原子的电子层数为n,最外层电子数为2n+1,原子中的质子数是2n2-1。有关X的说法不正确的是(n为正整数)( )
A.X能形成化学式为X(OH)3的碱
B.X肯定能形成化学式为NaXO3的含氧酸钠盐
C.X原子的最外层电子数和核电荷数肯定为奇数
D.X可能与某些金属元素Y形成Y3X2型化合物
课堂练习:
A
5.在1~18号元素中,最外层电子数等于电子 层数的元素有( )
A.1种 B.2种
C.3种 D.4种
课堂练习:
C
课堂小结
原子核外电子排布规律内容:
a 、能量最低原理(K、L、M、N、O、P、Q)
b、每层最多容纳电子数2n2(n表示电子层数)
c、最外层电子数目不超过8个(第一层不超过2个)
d、次外层电子数目不超过18个,
e、倒数第三层电子数目不超过32个。
排布规律间相互制约
原子结结构能够决定原子的性质(如还原性与氧化性,化合价的规律等)
