第三节溶液的酸碱性课件(34张PPT)
图片预览









文档简介
(共34张PPT)
第七单元第三节
溶液的酸碱性
教学目标
1、通过实验探究,学会用酸碱指示剂、石蕊试纸检验溶液酸碱性。
2、通过对溶液酸碱性的分析,知道pH与溶液酸碱性强弱的关系,学会用pH试纸检测溶液酸碱性的强弱程度。
3、通过阅读教材,认识酸碱性对生命活动的重要性,增强对化学学习的情感。
酸
溶于水后解离出的阳离子
全都是氢离子的化合物
碱
溶于水后解离出的阴离子
全都是氢氧根离子的化合物
由金属阳离子(或NH4+)
和酸根阴离子构成的化合物
盐
知识回顾:酸、碱、盐的定义:
1、酸使紫色石蕊试液变红,使酚酞试液不变色;
知识回顾:酸的通性
酸在水溶液中都能解离出相同的氢离子(H+),
因此它们具有相似的化学性质。
2、能与部分金属反应生成盐和氢气;
3、能与金属氧化物反应生成盐和水;
4、能与盐反应生成新酸和新盐;
5、能与碱反应生成盐和水。
1、碱使紫色石蕊试液变蓝,使酚酞试液变红;
知识回顾:碱的通性:
碱在水溶液中都能解离出相同的氢氧根离子
(OH-),因此它们具有相似的化学性质。
2、能与非金属氧化物反应生成盐和水
3、能与盐反应生成新碱和新盐
4、能与酸反应生成盐和水
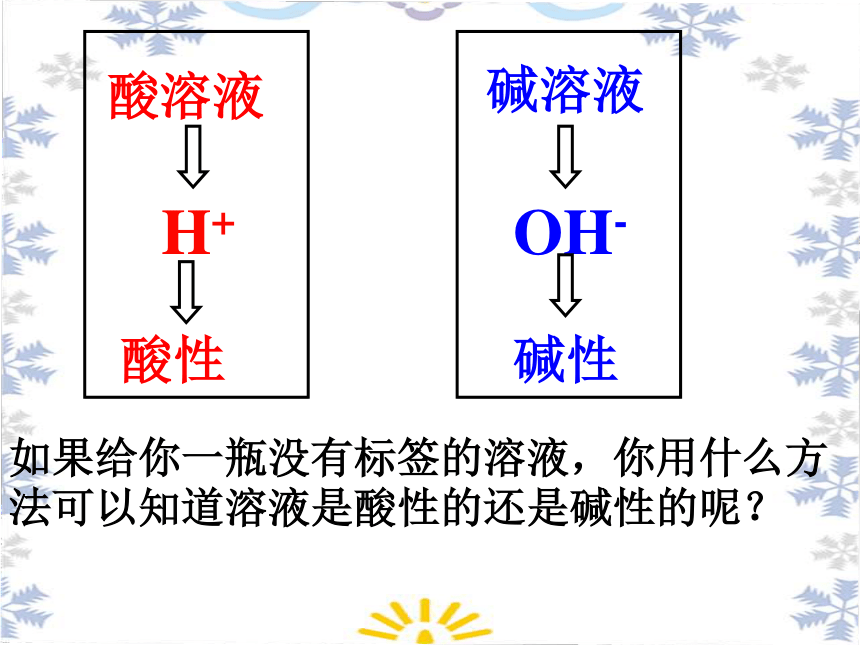
H+
OH-
酸溶液
碱溶液
酸性
碱性
如果给你一瓶没有标签的溶液,你用什么方法可以知道溶液是酸性的还是碱性的呢?
一、如何检验溶液的酸碱性
1、理论依据:根据酸或碱的通性设计实验进行检验;
2、常用方法:将石蕊试液或酚酞试液滴加到待检验的溶液中,根据试液的颜色变化情况来判断溶液的酸碱性,通常把这种方法称为用酸碱指示剂检验溶液的酸碱性;
认识酸碱指示剂
1、定义:遇到酸性或碱性溶液时能发生特定的颜色变化的物质;
2、常用的酸碱指示剂:紫色石蕊试液和无色 酚酞试液
寻找科学家的足迹 (发现酸碱指示剂)
著名化学家罗伯特.波义耳在一次实验中,不小心将盐酸溅到紫罗兰花瓣上,过一会儿,他惊奇地发现,紫色的花瓣上出现了红点点。波义耳对这一意外的发现,做出了各种假设,经过多次实验验证,探究普遍规律,终于获得了成功。
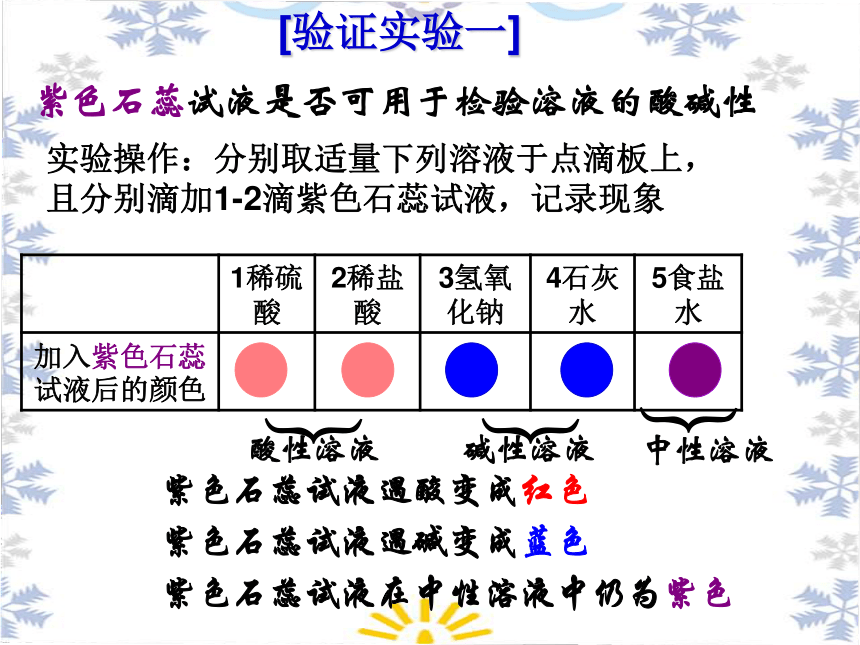
[验证实验一]
紫色石蕊试液是否可用于检验溶液的酸碱性
︸
︸
︸
酸性溶液
中性溶液
碱性溶液
紫色石蕊试液遇酸变成红色
紫色石蕊试液遇碱变成蓝色
紫色石蕊试液在中性溶液中仍为紫色
实验操作:分别取适量下列溶液于点滴板上,
且分别滴加1-2滴紫色石蕊试液,记录现象
1稀硫酸 2稀盐酸 3氢氧化钠 4石灰水 5食盐水
加入紫色石蕊试液后的颜色
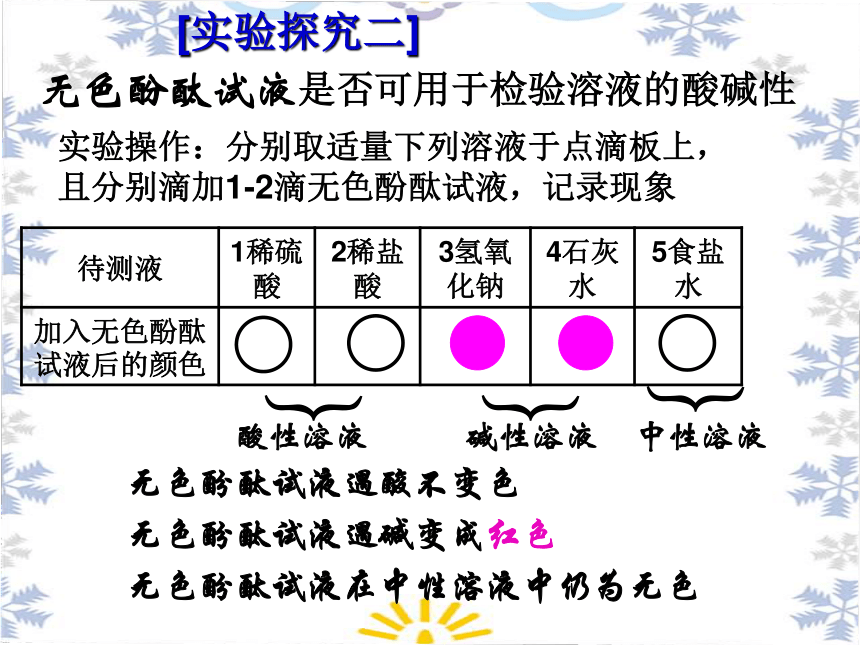
[实验探究二]
无色酚酞试液是否可用于检验溶液的酸碱性
︸
︸
︸
酸性溶液
中性溶液
碱性溶液
无色酚酞试液遇酸不变色
无色酚酞试液遇碱变成红色
无色酚酞试液在中性溶液中仍为无色
实验操作:分别取适量下列溶液于点滴板上,
且分别滴加1-2滴无色酚酞试液,记录现象
待测液 1稀硫酸 2稀盐酸 3氢氧化钠 4石灰水 5食盐水
加入无色酚酞试液后的颜色
总结:
酸碱指示剂可用于检验溶液的酸碱性
如果给你一瓶没有标签的溶液,你用什么方法可以知道溶液是酸性的还是碱性的呢?
取适量溶液于试管中,滴加两滴紫色石蕊试液,
若紫色石蕊试液变红,则说明是 溶液
若紫色石蕊试液变蓝,则说明是 溶液
取适量溶液于试管中,滴加两滴无色酚酞试液,
若酚酞试液变红,则说明是 溶液
若酚酞试液不变色,则说明 溶液
酸性
碱性
碱性
一定不是碱性
H+
OH-
酸溶液
碱溶液
酸性
碱性
酸溶液一定是酸性溶液,但酸性溶液一定是酸溶液吗?
碱溶液一定是碱性溶液,但碱性溶液一定是碱溶液吗?
加入酚酞试液后溶液颜色
变红色
待测液
碳酸钠溶液
实验探究三 酸性溶液是否一定是酸溶液,
碱性溶液是否一定是碱溶液
1、实验操作:取碳酸钠溶液于点滴板上,然后滴加
两滴无色酚酞试液,观察并记录颜色变化;
2、实验现象:
3:实验结论:
酸性溶液不一定是酸溶液,
碱性溶液不一定是碱溶液.
二、怎样判断溶液酸碱性的强弱
我们都有这样的生活经验,如果我们想做一盘木瓜酸,会往木瓜里加入白醋,加入的白醋越多就越酸,也就说明酸性越强,溶液的酸碱性强弱用什么来表示呢?
二、怎样判断溶液酸碱性的强弱
1.溶液酸碱性强弱程度用pH表示
溶液酸碱性的强弱程度跟什么有关?
pH的范围如何规定?
pH的大小与溶液酸碱性有什么关系?
pH如何测定?
阅读提纲
酸性与H+有关,H+的数量越多,酸性越强。
碱性与OH-有关,OH-的数量越多,碱性越强。
pH的范围通常在0~14之间
中性
pH<7 溶液显酸性pH=7 溶液显中性pH>7 溶液显碱性
二、怎样判断溶液酸碱性的强弱
1.溶液酸碱性强弱程度用pH表示
(pH的范围通常在0~14之间)
中性
2.pH的测定——
pH试纸
在玻璃片或白瓷板上放一片pH 试纸,用玻璃棒蘸取被测液滴到试纸上,把试纸显示的颜色立即与标准比色卡比较,即可得出被测液的pH 。
(1)不能直接把pH试纸浸入待测溶液中,以免带入杂质污染试剂;
(2)不能先用水将pH试纸润湿,因为用水润湿是稀释后溶液的pH。
(3)使用的pH试纸测出的pH值是1-14的整数
(4)比较精确的测定溶液的pH,用精密pH试纸和酸度计(pH计)来测量。
(1)各组分别测定稀硫酸、稀盐酸、氢氧化钠溶液、氢氧化钙溶液、氯化钠溶液的pH
(2)把结果写在黑板上,看看哪组做得又快又好。
探究活动四测定溶液的pH
合作探究
测定溶液的pH值
组次 1 2 3 4 5 6 7 8 9 10
稀硫酸
稀盐酸
氢氧化钠
氢氧化钙
氯化钠
结论:用pH试纸可以测定溶液的pH;
酸性溶液pH<7,pH越小酸性越强,
酸性溶液加水稀释后pH变大;
碱性溶液pH>7, pH越大碱性越强, 碱性溶液加水稀释后pH变小;
中性溶液pH=7, 中性溶液加水稀释
后pH不变;
了解生活中一些物质的pH
三、物质的酸碱性对生命活动的意义
人体某些体液的正常pH范围
几种作物生长最适宜的pH范围
西瓜6.0~7.0
苹果树6.0~8.0
小麦6.0~7.0
血液 唾液 胃液 乳汁 尿液
pH 7.35~7.45 6.6~7.1 0.8~1.5 6.4~6.7 5.0~7.0
了解溶液的酸碱性在生活中的应用:
4、化工生产中许多反应必须在一定pH溶液里
才能进行。
2、在农业生产中,农作物一般适宜在pH为7
或接近7的土壤中生长。
3、测定雨水的pH,可以了解空气的污染情况
(正 常雨水的pH约为5.6,酸雨的pH小于5.6)
1、测定人体内或排出的液体的pH,可以了解
人体的健康状况。
二、怎样判断溶液酸碱性的强弱
溶液酸碱性强弱程度用pH表示,用pH试纸测定
(pH的范围通常在0~14之间)
中性
加水
一、如何检验溶液的酸碱性
三、物质的酸碱性对生命活动的意义及应用
课堂总结:
1.下列是某些食物的近似pH,呈碱性的是( )
A B C D
D
2.一些常见食物的近似pH范围如下表:
下列说法正确的是( ) A.葡萄汁能使酚酞试液变红 B.西红柿的酸性比苹果的酸性强 C.胃酸过多的人应少食苹果 D.牛奶的碱性比鸡蛋清的碱性强
C
食物 苹果 鸡蛋清 西红柿 葡萄 牛奶
pH 2.9~3.3 7.6~8.0 4.0~4.4 3.5~4.5 6.3~6.6
3.用石蕊试液和酚酞试液分别滴入同一物质的溶液中,下列现象不可能发生的是( ) A.滴入石蕊试液变红色,滴入酚酞试液不变色 B.滴入石蕊试液不变色,滴入酚酞试液不变色 C.滴入石蕊试液变蓝色,滴入酚酞试液变红色 D.滴入石蕊试液变红色,滴入酚酞试液变红色
D
4.新鲜牛奶的pH约为7,接近 性。储存了一段时间后味道变酸, pH 。
5.有一包可溶性固体粉末,如何检验它是酸性物质还是碱性物质?
中
<7
5.答案:
取适量该固体溶解在水中制成溶液,再用试管取少量该溶液,滴入紫色石蕊试液,若变红色,则为酸性物质,若变蓝色,则为碱性物质。
6.鲜肉是日常主要食品之一,新鲜度可以通过测试pH来判断。据资料,pH与肉的新鲜度的关系为:新鲜肉pH5.8~6.2;次鲜肉pH6.3~6.6;变质肉的pH在6.7以上。新鲜肉在变质的过程中,酸性强弱的变化为( )
A.变弱 B.变强 C.不变 D.无法确定
A
7、下列物质的pH大于7的是(????)?
A.食盐水????????B.食醋???????
C.石灰水???????D.汽水?
C
8、在Ca(OH)2的饱和溶液中加入下列物质,冷却至室温,溶液的pH没有改变的是??(???)?
A.CO2????????????B.CaO??????????C.Cu(NO3)2????? ?D.HCl
B
第七单元第三节
溶液的酸碱性
教学目标
1、通过实验探究,学会用酸碱指示剂、石蕊试纸检验溶液酸碱性。
2、通过对溶液酸碱性的分析,知道pH与溶液酸碱性强弱的关系,学会用pH试纸检测溶液酸碱性的强弱程度。
3、通过阅读教材,认识酸碱性对生命活动的重要性,增强对化学学习的情感。
酸
溶于水后解离出的阳离子
全都是氢离子的化合物
碱
溶于水后解离出的阴离子
全都是氢氧根离子的化合物
由金属阳离子(或NH4+)
和酸根阴离子构成的化合物
盐
知识回顾:酸、碱、盐的定义:
1、酸使紫色石蕊试液变红,使酚酞试液不变色;
知识回顾:酸的通性
酸在水溶液中都能解离出相同的氢离子(H+),
因此它们具有相似的化学性质。
2、能与部分金属反应生成盐和氢气;
3、能与金属氧化物反应生成盐和水;
4、能与盐反应生成新酸和新盐;
5、能与碱反应生成盐和水。
1、碱使紫色石蕊试液变蓝,使酚酞试液变红;
知识回顾:碱的通性:
碱在水溶液中都能解离出相同的氢氧根离子
(OH-),因此它们具有相似的化学性质。
2、能与非金属氧化物反应生成盐和水
3、能与盐反应生成新碱和新盐
4、能与酸反应生成盐和水
H+
OH-
酸溶液
碱溶液
酸性
碱性
如果给你一瓶没有标签的溶液,你用什么方法可以知道溶液是酸性的还是碱性的呢?
一、如何检验溶液的酸碱性
1、理论依据:根据酸或碱的通性设计实验进行检验;
2、常用方法:将石蕊试液或酚酞试液滴加到待检验的溶液中,根据试液的颜色变化情况来判断溶液的酸碱性,通常把这种方法称为用酸碱指示剂检验溶液的酸碱性;
认识酸碱指示剂
1、定义:遇到酸性或碱性溶液时能发生特定的颜色变化的物质;
2、常用的酸碱指示剂:紫色石蕊试液和无色 酚酞试液
寻找科学家的足迹 (发现酸碱指示剂)
著名化学家罗伯特.波义耳在一次实验中,不小心将盐酸溅到紫罗兰花瓣上,过一会儿,他惊奇地发现,紫色的花瓣上出现了红点点。波义耳对这一意外的发现,做出了各种假设,经过多次实验验证,探究普遍规律,终于获得了成功。
[验证实验一]
紫色石蕊试液是否可用于检验溶液的酸碱性
︸
︸
︸
酸性溶液
中性溶液
碱性溶液
紫色石蕊试液遇酸变成红色
紫色石蕊试液遇碱变成蓝色
紫色石蕊试液在中性溶液中仍为紫色
实验操作:分别取适量下列溶液于点滴板上,
且分别滴加1-2滴紫色石蕊试液,记录现象
1稀硫酸 2稀盐酸 3氢氧化钠 4石灰水 5食盐水
加入紫色石蕊试液后的颜色
[实验探究二]
无色酚酞试液是否可用于检验溶液的酸碱性
︸
︸
︸
酸性溶液
中性溶液
碱性溶液
无色酚酞试液遇酸不变色
无色酚酞试液遇碱变成红色
无色酚酞试液在中性溶液中仍为无色
实验操作:分别取适量下列溶液于点滴板上,
且分别滴加1-2滴无色酚酞试液,记录现象
待测液 1稀硫酸 2稀盐酸 3氢氧化钠 4石灰水 5食盐水
加入无色酚酞试液后的颜色
总结:
酸碱指示剂可用于检验溶液的酸碱性
如果给你一瓶没有标签的溶液,你用什么方法可以知道溶液是酸性的还是碱性的呢?
取适量溶液于试管中,滴加两滴紫色石蕊试液,
若紫色石蕊试液变红,则说明是 溶液
若紫色石蕊试液变蓝,则说明是 溶液
取适量溶液于试管中,滴加两滴无色酚酞试液,
若酚酞试液变红,则说明是 溶液
若酚酞试液不变色,则说明 溶液
酸性
碱性
碱性
一定不是碱性
H+
OH-
酸溶液
碱溶液
酸性
碱性
酸溶液一定是酸性溶液,但酸性溶液一定是酸溶液吗?
碱溶液一定是碱性溶液,但碱性溶液一定是碱溶液吗?
加入酚酞试液后溶液颜色
变红色
待测液
碳酸钠溶液
实验探究三 酸性溶液是否一定是酸溶液,
碱性溶液是否一定是碱溶液
1、实验操作:取碳酸钠溶液于点滴板上,然后滴加
两滴无色酚酞试液,观察并记录颜色变化;
2、实验现象:
3:实验结论:
酸性溶液不一定是酸溶液,
碱性溶液不一定是碱溶液.
二、怎样判断溶液酸碱性的强弱
我们都有这样的生活经验,如果我们想做一盘木瓜酸,会往木瓜里加入白醋,加入的白醋越多就越酸,也就说明酸性越强,溶液的酸碱性强弱用什么来表示呢?
二、怎样判断溶液酸碱性的强弱
1.溶液酸碱性强弱程度用pH表示
溶液酸碱性的强弱程度跟什么有关?
pH的范围如何规定?
pH的大小与溶液酸碱性有什么关系?
pH如何测定?
阅读提纲
酸性与H+有关,H+的数量越多,酸性越强。
碱性与OH-有关,OH-的数量越多,碱性越强。
pH的范围通常在0~14之间
中性
pH<7 溶液显酸性pH=7 溶液显中性pH>7 溶液显碱性
二、怎样判断溶液酸碱性的强弱
1.溶液酸碱性强弱程度用pH表示
(pH的范围通常在0~14之间)
中性
2.pH的测定——
pH试纸
在玻璃片或白瓷板上放一片pH 试纸,用玻璃棒蘸取被测液滴到试纸上,把试纸显示的颜色立即与标准比色卡比较,即可得出被测液的pH 。
(1)不能直接把pH试纸浸入待测溶液中,以免带入杂质污染试剂;
(2)不能先用水将pH试纸润湿,因为用水润湿是稀释后溶液的pH。
(3)使用的pH试纸测出的pH值是1-14的整数
(4)比较精确的测定溶液的pH,用精密pH试纸和酸度计(pH计)来测量。
(1)各组分别测定稀硫酸、稀盐酸、氢氧化钠溶液、氢氧化钙溶液、氯化钠溶液的pH
(2)把结果写在黑板上,看看哪组做得又快又好。
探究活动四测定溶液的pH
合作探究
测定溶液的pH值
组次 1 2 3 4 5 6 7 8 9 10
稀硫酸
稀盐酸
氢氧化钠
氢氧化钙
氯化钠
结论:用pH试纸可以测定溶液的pH;
酸性溶液pH<7,pH越小酸性越强,
酸性溶液加水稀释后pH变大;
碱性溶液pH>7, pH越大碱性越强, 碱性溶液加水稀释后pH变小;
中性溶液pH=7, 中性溶液加水稀释
后pH不变;
了解生活中一些物质的pH
三、物质的酸碱性对生命活动的意义
人体某些体液的正常pH范围
几种作物生长最适宜的pH范围
西瓜6.0~7.0
苹果树6.0~8.0
小麦6.0~7.0
血液 唾液 胃液 乳汁 尿液
pH 7.35~7.45 6.6~7.1 0.8~1.5 6.4~6.7 5.0~7.0
了解溶液的酸碱性在生活中的应用:
4、化工生产中许多反应必须在一定pH溶液里
才能进行。
2、在农业生产中,农作物一般适宜在pH为7
或接近7的土壤中生长。
3、测定雨水的pH,可以了解空气的污染情况
(正 常雨水的pH约为5.6,酸雨的pH小于5.6)
1、测定人体内或排出的液体的pH,可以了解
人体的健康状况。
二、怎样判断溶液酸碱性的强弱
溶液酸碱性强弱程度用pH表示,用pH试纸测定
(pH的范围通常在0~14之间)
中性
加水
一、如何检验溶液的酸碱性
三、物质的酸碱性对生命活动的意义及应用
课堂总结:
1.下列是某些食物的近似pH,呈碱性的是( )
A B C D
D
2.一些常见食物的近似pH范围如下表:
下列说法正确的是( ) A.葡萄汁能使酚酞试液变红 B.西红柿的酸性比苹果的酸性强 C.胃酸过多的人应少食苹果 D.牛奶的碱性比鸡蛋清的碱性强
C
食物 苹果 鸡蛋清 西红柿 葡萄 牛奶
pH 2.9~3.3 7.6~8.0 4.0~4.4 3.5~4.5 6.3~6.6
3.用石蕊试液和酚酞试液分别滴入同一物质的溶液中,下列现象不可能发生的是( ) A.滴入石蕊试液变红色,滴入酚酞试液不变色 B.滴入石蕊试液不变色,滴入酚酞试液不变色 C.滴入石蕊试液变蓝色,滴入酚酞试液变红色 D.滴入石蕊试液变红色,滴入酚酞试液变红色
D
4.新鲜牛奶的pH约为7,接近 性。储存了一段时间后味道变酸, pH 。
5.有一包可溶性固体粉末,如何检验它是酸性物质还是碱性物质?
中
<7
5.答案:
取适量该固体溶解在水中制成溶液,再用试管取少量该溶液,滴入紫色石蕊试液,若变红色,则为酸性物质,若变蓝色,则为碱性物质。
6.鲜肉是日常主要食品之一,新鲜度可以通过测试pH来判断。据资料,pH与肉的新鲜度的关系为:新鲜肉pH5.8~6.2;次鲜肉pH6.3~6.6;变质肉的pH在6.7以上。新鲜肉在变质的过程中,酸性强弱的变化为( )
A.变弱 B.变强 C.不变 D.无法确定
A
7、下列物质的pH大于7的是(????)?
A.食盐水????????B.食醋???????
C.石灰水???????D.汽水?
C
8、在Ca(OH)2的饱和溶液中加入下列物质,冷却至室温,溶液的pH没有改变的是??(???)?
A.CO2????????????B.CaO??????????C.Cu(NO3)2????? ?D.HCl
B
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
