第四节酸碱中和反应课件(19张PPT)
图片预览






文档简介
(共19张PPT)
鲁教版化学第七单元 常见的酸和碱
第四节 酸碱中和反应
同学们有这样的经历吗?
马蜂蛰伤
蚊虫叮咬时,在蚊子的口器中分泌出一种有机酸--蚁酸,在家庭中可用浓肥皂涂抹可迅速止痒。
显碱性
情景导入
蚊虫叮咬
如何检验溶液的酸碱性?
1.用___________可以区别溶液的酸碱性。
2.溶液酸碱性的强弱常用 来表示,用 来测定。
酸溶液中含有相同的_____;碱溶液中含有相同的___
pH <7 时,溶液显 性; pH = 7 时,溶液显 性; pH >7 时,溶液显 性。
酸能使紫色石蕊试液变 色,使无色酚酞试液 ;碱能使紫色石蕊试液变 色,使无色酚酞试液变 色。
酸
酸碱指示剂
红
蓝
红
pH
pH试纸
中
碱
H+
OH-
酸的阳离子全部是 H+;碱的阴离子全部是OH-
实验探究
盐酸(HCl)和氢氧化钠(NaOH)溶液能否发生化学反应?
猜想与假设
可能反应?
HCl + NaOH =
可能不反应?
设计实验
给出的药品有:NaOH 溶液,稀HCl,
紫色石蕊试液,无色酚酞试液,PH试纸
(利用给出的药品讨论、设计实验方案)
方案一:往盛有NaOH溶液的试管滴入酚酞试液后再慢慢滴入稀HCl至刚好变为无色。
往盛有稀HCl的试管里滴入几滴紫色石蕊试液,再逐滴滴入NaOH溶液。
方案二:
方案三:往盛有NaOH 溶液的试管加入几滴稀HCl,然后再用PH试纸测定。
讨论
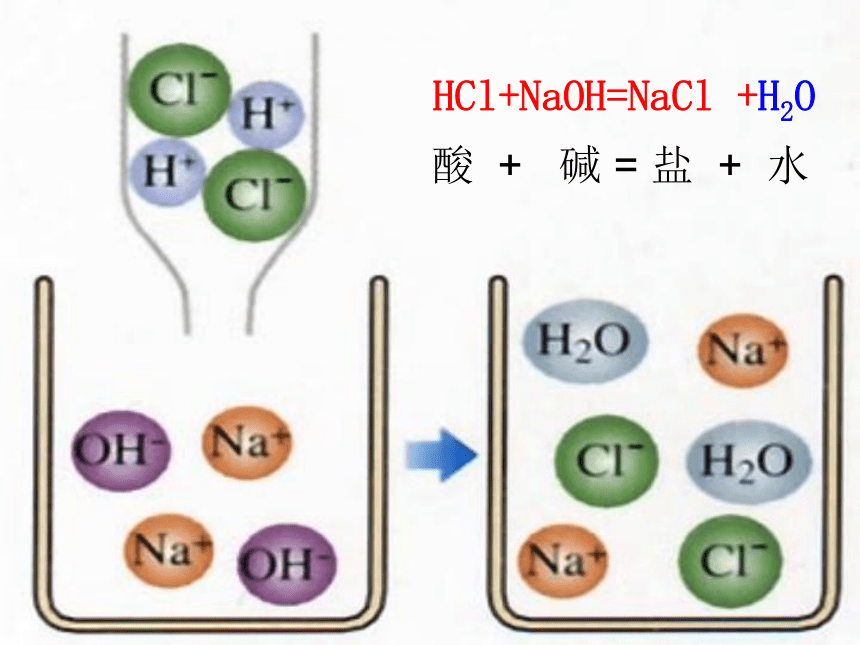
HCl+NaOH=NaCl +H2O
酸 + 碱 = 盐 + 水
活动天地:-----------请试着写一下
盐酸和氢氧化钾:
盐酸和氢氧化钡:
硫酸和氢氧化钠:
硫酸和氢氧化钡:
2HCl + Ba(OH)2 = BaCl2 + 2H2O
HCl + KOH = KCl + H2O
酸 + 碱 = + 水
盐
在线测试:
盐酸与氢氧化钙反应
硫酸与氢氧化钾反应
2HCl + Ca(OH)2 === CaCl2 + 2H2O
H2SO4 +2KOH === K2SO4 +2H2O
思考:酸碱发生中和反应生成盐和水,是否生成盐和水的反应都是中和反应呢?
一、
二、CuO + H2SO4 = CuSO4 + H2O
三、2KOH + H2SO4 = K2SO4+2H2O
CO2+Ca(OH)2= CaCO3↓+H2O
活动天地:图像
向盐酸中滴加氢氧化钠溶液时溶液pH的变化
?
.
.
.
.
.
.
.
.
.
.
。
NaOH溶液与盐酸恰好完全反应,
溶液显中性pH=7
加入烧碱溶液的体积/mL 0 2 4 6 8 10 12 14 16 18
烧杯中溶液的pH 1.1 1.2 1.4 1.6 2.0 7.0 11.0 12.2 12.4 12.5
中和反应在实际中的应用
说明书
成份:氢氧化铝、碘甲基蛋氨酸、颠茄。
作用与用途:
具有制酸、收敛与促进 溃疡愈合的作用。适用于胃溃疡、十二指肠溃疡、急慢性胃炎、胃酸过多、胃痉挛所致的胃痛。
用法与用量:口服,一次1粒,一日3次。
——用于医药
二、改变土壤的酸碱性
植物需要在一定酸碱性的土壤中生长,
但近年来由于不合理使用化肥,或酸雨的形成,破坏土壤的酸碱性,不利于植物的生长。
应怎样去改变酸性土壤?
用熟石灰中和。
2HCl + Ca(OH)2 === CaCl2 + 2H2O
三、处理工厂的废水
某硫酸厂排出的废水中含有硫酸等杂质,严重危害当地的生态环境,你会怎样处理这些废水呢?
应在排放前用碱性物质(例如熟石灰)进行中和处理。
你能写出化学方程式吗?
Ca(OH)2 + H2 SO4 === CaSO4 + 2H2O
在科学实验中,经常需要将溶液的PH控制在一定范围内。如果溶液的酸碱性太强或太弱,都可以用适当的碱或酸调节溶液的PH.
四、调节溶液的酸碱性
请谈谈对本节内容学习你有何收获与感悟?
1.下列反应,属于中和反应的是( )
A Zn +2HCl == ZnCl2 + H2
B CuO + 2HCl == CuCl2 + H2O
C Cu(OH)2 + H2SO4 == CuSO4 + 2H2O
D AgNO3 + HCl == AgCl + HNO3
学以致用
C
4. 2、向NaOH溶液中不断滴加稀盐酸,溶液pH随加入盐酸体积变化与下图相符的是 ( )
鲁教版化学第七单元 常见的酸和碱
第四节 酸碱中和反应
同学们有这样的经历吗?
马蜂蛰伤
蚊虫叮咬时,在蚊子的口器中分泌出一种有机酸--蚁酸,在家庭中可用浓肥皂涂抹可迅速止痒。
显碱性
情景导入
蚊虫叮咬
如何检验溶液的酸碱性?
1.用___________可以区别溶液的酸碱性。
2.溶液酸碱性的强弱常用 来表示,用 来测定。
酸溶液中含有相同的_____;碱溶液中含有相同的___
pH <7 时,溶液显 性; pH = 7 时,溶液显 性; pH >7 时,溶液显 性。
酸能使紫色石蕊试液变 色,使无色酚酞试液 ;碱能使紫色石蕊试液变 色,使无色酚酞试液变 色。
酸
酸碱指示剂
红
蓝
红
pH
pH试纸
中
碱
H+
OH-
酸的阳离子全部是 H+;碱的阴离子全部是OH-
实验探究
盐酸(HCl)和氢氧化钠(NaOH)溶液能否发生化学反应?
猜想与假设
可能反应?
HCl + NaOH =
可能不反应?
设计实验
给出的药品有:NaOH 溶液,稀HCl,
紫色石蕊试液,无色酚酞试液,PH试纸
(利用给出的药品讨论、设计实验方案)
方案一:往盛有NaOH溶液的试管滴入酚酞试液后再慢慢滴入稀HCl至刚好变为无色。
往盛有稀HCl的试管里滴入几滴紫色石蕊试液,再逐滴滴入NaOH溶液。
方案二:
方案三:往盛有NaOH 溶液的试管加入几滴稀HCl,然后再用PH试纸测定。
讨论
HCl+NaOH=NaCl +H2O
酸 + 碱 = 盐 + 水
活动天地:-----------请试着写一下
盐酸和氢氧化钾:
盐酸和氢氧化钡:
硫酸和氢氧化钠:
硫酸和氢氧化钡:
2HCl + Ba(OH)2 = BaCl2 + 2H2O
HCl + KOH = KCl + H2O
酸 + 碱 = + 水
盐
在线测试:
盐酸与氢氧化钙反应
硫酸与氢氧化钾反应
2HCl + Ca(OH)2 === CaCl2 + 2H2O
H2SO4 +2KOH === K2SO4 +2H2O
思考:酸碱发生中和反应生成盐和水,是否生成盐和水的反应都是中和反应呢?
一、
二、CuO + H2SO4 = CuSO4 + H2O
三、2KOH + H2SO4 = K2SO4+2H2O
CO2+Ca(OH)2= CaCO3↓+H2O
活动天地:图像
向盐酸中滴加氢氧化钠溶液时溶液pH的变化
?
.
.
.
.
.
.
.
.
.
.
。
NaOH溶液与盐酸恰好完全反应,
溶液显中性pH=7
加入烧碱溶液的体积/mL 0 2 4 6 8 10 12 14 16 18
烧杯中溶液的pH 1.1 1.2 1.4 1.6 2.0 7.0 11.0 12.2 12.4 12.5
中和反应在实际中的应用
说明书
成份:氢氧化铝、碘甲基蛋氨酸、颠茄。
作用与用途:
具有制酸、收敛与促进 溃疡愈合的作用。适用于胃溃疡、十二指肠溃疡、急慢性胃炎、胃酸过多、胃痉挛所致的胃痛。
用法与用量:口服,一次1粒,一日3次。
——用于医药
二、改变土壤的酸碱性
植物需要在一定酸碱性的土壤中生长,
但近年来由于不合理使用化肥,或酸雨的形成,破坏土壤的酸碱性,不利于植物的生长。
应怎样去改变酸性土壤?
用熟石灰中和。
2HCl + Ca(OH)2 === CaCl2 + 2H2O
三、处理工厂的废水
某硫酸厂排出的废水中含有硫酸等杂质,严重危害当地的生态环境,你会怎样处理这些废水呢?
应在排放前用碱性物质(例如熟石灰)进行中和处理。
你能写出化学方程式吗?
Ca(OH)2 + H2 SO4 === CaSO4 + 2H2O
在科学实验中,经常需要将溶液的PH控制在一定范围内。如果溶液的酸碱性太强或太弱,都可以用适当的碱或酸调节溶液的PH.
四、调节溶液的酸碱性
请谈谈对本节内容学习你有何收获与感悟?
1.下列反应,属于中和反应的是( )
A Zn +2HCl == ZnCl2 + H2
B CuO + 2HCl == CuCl2 + H2O
C Cu(OH)2 + H2SO4 == CuSO4 + 2H2O
D AgNO3 + HCl == AgCl + HNO3
学以致用
C
4. 2、向NaOH溶液中不断滴加稀盐酸,溶液pH随加入盐酸体积变化与下图相符的是 ( )
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
