人教版九年级化学下册 10.1.2 《酸的化学性质》 培优训练
文档属性
| 名称 | 人教版九年级化学下册 10.1.2 《酸的化学性质》 培优训练 |

|
|
| 格式 | zip | ||
| 文件大小 | 196.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-02-28 00:00:00 | ||
图片预览


文档简介
人教版九年级化学下册
10.1.2 酸的化学性质
培优训练
一、选择题 (每小题3分,共36分)
1.下列物质中属于酸的是( )
A.H2CO3 B.NaHCO3
C.P2O5 D.Ba(OH)2
2. 苯甲酸(C6H5COOH)是常见的食品防腐剂。某同学准备进行实验验证苯甲酸具有酸的某一通性,他选择了下列物质,其中不能达到目的的是( )
A.铜 B.铁锈 C.锌粒 D.紫色石蕊溶液
3.大理石雕像很容易被酸雨腐蚀,下列材料代替大理石做雕像比较耐腐蚀的是( )
A.铁 B.铝
C.铜 D.表面镀锌的金属
4.小红学习了酸碱指示剂与常见的酸、碱溶液作用后,归纳总结出如图所示的关系。图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示出的颜色,其中颜色不正确的是( )
A.紫色 B.蓝色 C.红色 D.无色
5. 下列关于酸的说法错误的是( )
A.浓硫酸具有吸水性,浓盐酸具有挥发性
B.稀盐酸和稀硫酸都可用于金属除锈
C.稀盐酸能够使紫色石蕊溶液和无色酚酞溶液都变红色
D.稀硫酸能够与活泼金属反应制取氢气
6. 下列关于H2SO4性质的描述中,不属于酸的通性的是( )
A.使紫色石蕊溶液变红
B.与氧化铁发生反应
C.浓硫酸滴到白纸上使纸变黑
D.与Mg反应放出氢气
7.物质X可发生“X+酸―→化合物+H2O”的反应,则X可能是( )
A.Fe B.CO2 C.H2SO4 D.CuO
8. 将某稀硫酸分成两等份,分别向其中加入锌粉或铁粉,反应结束后剩余的铁比剩余的锌多,产生氢气的质量分别为a g和b g,则a和b的关系是( )
A.a<b B.a=b
C.a>b D.无法判断
9. 下列实验现象的描述正确的是 ( )
A.用盐酸除铁锈时,铁锈逐渐溶解,溶液变成浅绿色
B.铁与稀硫酸反应时有气泡产生,溶液变成黄色
C.将铜片放入稀硫酸中,铜片溶解,形成蓝色溶液
D.氧化铜与稀硫酸反应时,黑色粉末溶解,形成蓝色溶液
10. 小王同学往厨房的纯碱中滴加白醋,发现有气体生成。已知白醋里含3%~5%的醋酸(CH3COOH),醋酸与盐酸的化学性质相似,下列说法不正确的是( )
A.白醋里含有氢离子
B.生成的气体是二氧化碳
C.白醋能使紫色石蕊试液变红
D.白醋不能用来除铁锈
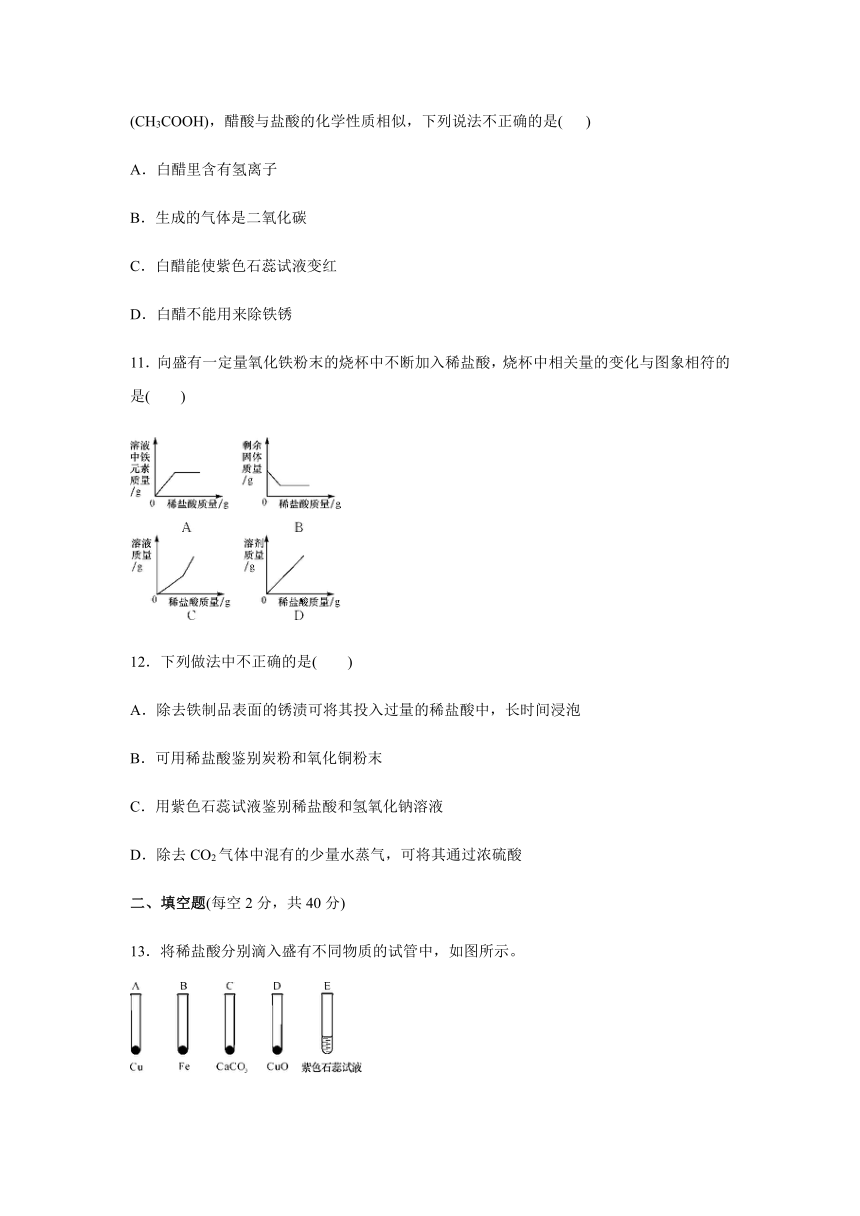
11.向盛有一定量氧化铁粉末的烧杯中不断加入稀盐酸,烧杯中相关量的变化与图象相符的是( )
12.下列做法中不正确的是( )
A.除去铁制品表面的锈渍可将其投入过量的稀盐酸中,长时间浸泡
B.可用稀盐酸鉴别炭粉和氧化铜粉末
C.用紫色石蕊试液鉴别稀盐酸和氢氧化钠溶液
D.除去CO2气体中混有的少量水蒸气,可将其通过浓硫酸
二、填空题(每空2分,共40分)
13.将稀盐酸分别滴入盛有不同物质的试管中,如图所示。
(1)不能发生反应的是__ __(填序号,下同)。
(2)有气泡产生的是__ __。
(3)有浅绿色溶液生成的是__ __。
(4)有蓝色溶液生成的是__ __。
(5)溶液变成红色的是__ __。
14.将表面生锈的铁钉投入到稀硫酸中,开始时观察到的现象是________________________,化学方程式为________________________________;较长时间后观察到的现象是__________________________,化学方程式为________________________。
15. 盐酸是一种重要的化工产品,也是实验室中重要的化学试剂。
(1)增大压强,HCl由气态变为液态,从微观的角度分析该变化过程中改变的是________________________。
(2)在盐酸中加入过量的铁粉充分反应。
①可以看到的现象是___________________________________________________________
________________________________________________________________________。
②如图表示该反应前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号):
________ ________ ________
③下列金属中能与盐酸发生类似反应的是________(填选项)。
A.Cu B.Mg C.Al D.Ag
16.实验时,李华把一枚生锈的铁钉放入足量的稀盐酸中,过一会儿,他看到的现象是____________________________;发生反应的化学方程式为____________________________;过一段时间,他又看到铁钉表面有气泡产生,该反应的化学方程式为_____________________。他又将铝片放入足量的稀盐酸中,奇怪的是开始无明显现象,过一段时间后才看到有气泡冒出,试用学过的知识解释原因___________________,_______________________________(用化学方程式表示)。
三、实验探究题(每空2分,共24分)
17.利用以下装置对酸的化学性质进行探究。
(1)实验Ⅰ中,在点滴板的a、b孔穴中滴入酸溶液后,溶液变红的是______(填“a”或“b”)。
使用点滴板的优点之一是_______________。
(2)实验Ⅱ中,为了验证石灰石中含有碳酸根离子,试剂X的名称是__________________。
(3)实验Ⅲ中,在试管①、②中均可观察到的现象是____________________________________。试管②中发生反应的化学方程式是_______________________________。
18. 利用以下装置对酸的化学性质进行探究。
(1)标号为①的仪器名称是__________。
(2)实验Ⅰ中,在点滴板的a、b穴中滴入酸溶液后,溶液变红的是________(填“a”或“b”)。使用点滴板的优点之一是_________________________________。
(3)实验Ⅱ中,为了验证石灰石中含有碳酸根离子,试剂X的名称是_______________________。
(4)实验Ⅲ中,在仪器①、②中均可观察到的现象是_____________、_____________。仪器②中发生反应的化学方程式是________________________________。
参考答案
一、选择题
1-6AACACC 7-12 DBDDAA
二、填空题
13. (1)A (2)B、C (3)B (4)D (5)E
14. 铁钉表面的铁锈逐渐减少,溶液变成棕黄色
Fe2O3+3H2SO4===Fe2(SO4)3+3H2O
铁钉表面有气泡产生
Fe+H2SO4===FeSO4 + H2↑
15.(1)氯化氢分子之间的间隔 (2)①固体溶解,溶液由无色变为浅绿色,有气泡产生 ②H+ Cl- Fe2+ ③BC
16. 铁锈逐渐消失,溶液变成黄色
Fe2O3+6HCl===2FeCl3+3H2O
Fe+2HCl===FeCl2+H2↑
Al2O3+6HCl===2AlCl3+3H2O
2Al+6HCl===2AlCl3+3H2↑
三、实验探究题
17. (1)a 节约药品
(2)澄清石灰水
(3)红棕色固体逐渐消失、溶液逐渐变成黄色 Fe2O3+3H2SO4===Fe2(SO4)3+3H2O
18. (1)试管
(2)a 节约试剂(合理即可)
(3)澄清石灰水
(4)固体逐渐溶解 得到黄色溶液 Fe2O3+3H2SO4===Fe2(SO4)3+3H2O
同课章节目录
