2020人教版九年级化学下册《酸和碱的中和反应》同步测试提高题
文档属性
| 名称 | 2020人教版九年级化学下册《酸和碱的中和反应》同步测试提高题 |

|
|
| 格式 | zip | ||
| 文件大小 | 191.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-03 00:00:00 | ||
图片预览



文档简介
《酸和碱的中和反应》同步测试提高题
一、选择题
1.一定温度下,向含有适量酚酞溶液的氢氧化钠溶液中慢慢滴加稀盐酸,溶液温度随加入稀盐酸的质量如图所示。下列叙述正确的是( )
A.M点时溶液呈无色
B.P点时,溶液中至少含两种溶质
C.N点时溶液的pH最大
D.从M﹣N点反应放出的热量逐渐增大,随后逐渐减少
2.某同学用盐酸与氢氧化钠按照如图的方式进行中和反应实验。溶液由红色变为无色。以下证明盐酸过量的操作及实验现象的叙述正确的是( )
A.滴加石蕊溶液,搅拌,溶液变蓝
B.滴加少量氢氧化钠溶液,搅拌,溶液变红色
C.加入蒸馏水,搅拌,溶液颜色不变
D.加入金属Zn片,产生气泡
3.室温时,在氢氧化钠溶液与盐酸反应中,测得溶液的pH随滴入溶液体积变化情况如图。下列说法错误的是( )
A.所得溶液的pH随加入溶液体积的变化是不均匀的
B.该实验是将盐酸逐滴加入一定量的氢氧化钠溶液中
C.当滴入溶液体积为5mL时,所得溶液中含有两种溶质
D.当滴入溶液体积为20mL时,所得溶液能使酚酞试液变红色
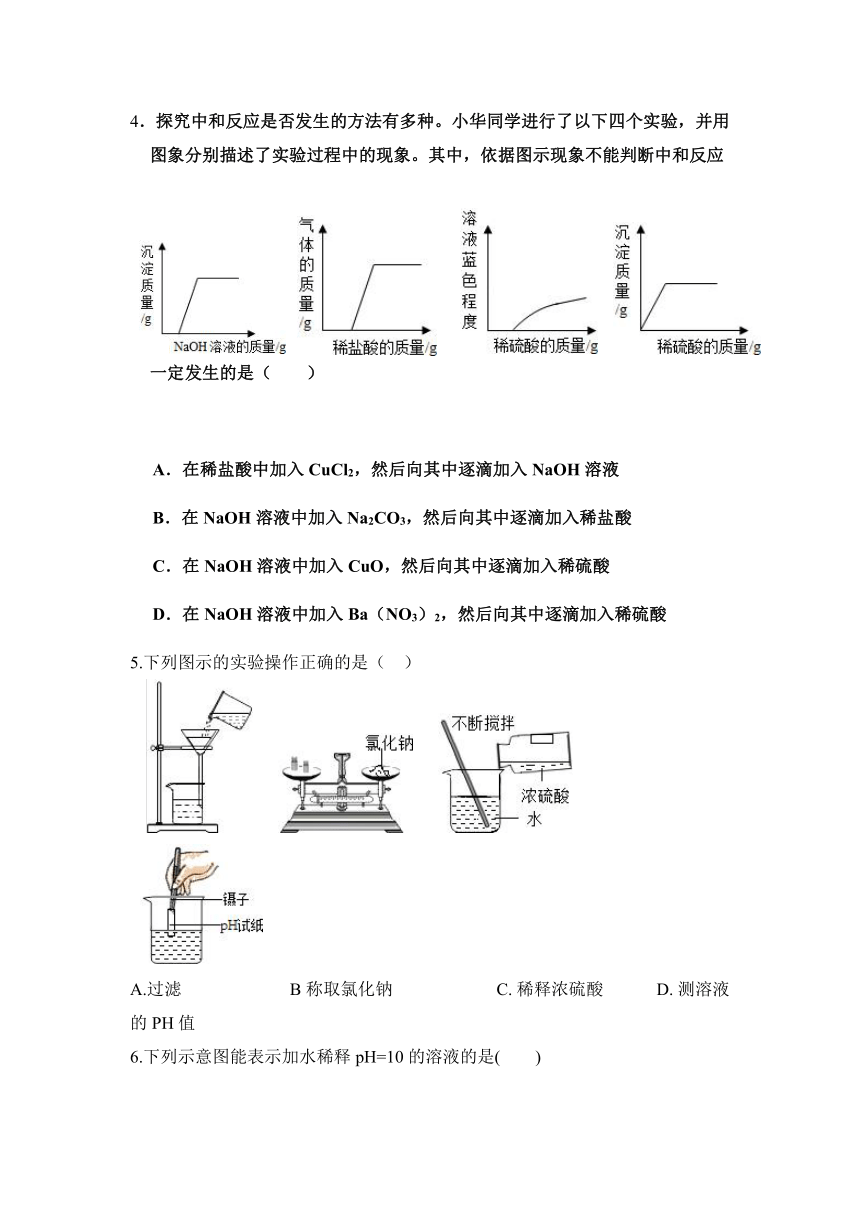
4.探究中和反应是否发生的方法有多种。小华同学进行了以下四个实验,并用图象分别描述了实验过程中的现象。其中,依据图示现象不能判断中和反应一定发生的是( )
A.在稀盐酸中加入CuCl2,然后向其中逐滴加入NaOH溶液
B.在NaOH溶液中加入Na2CO3,然后向其中逐滴加入稀盐酸
C.在NaOH溶液中加入CuO,然后向其中逐滴加入稀硫酸
D.在NaOH溶液中加入Ba(NO3)2,然后向其中逐滴加入稀硫酸
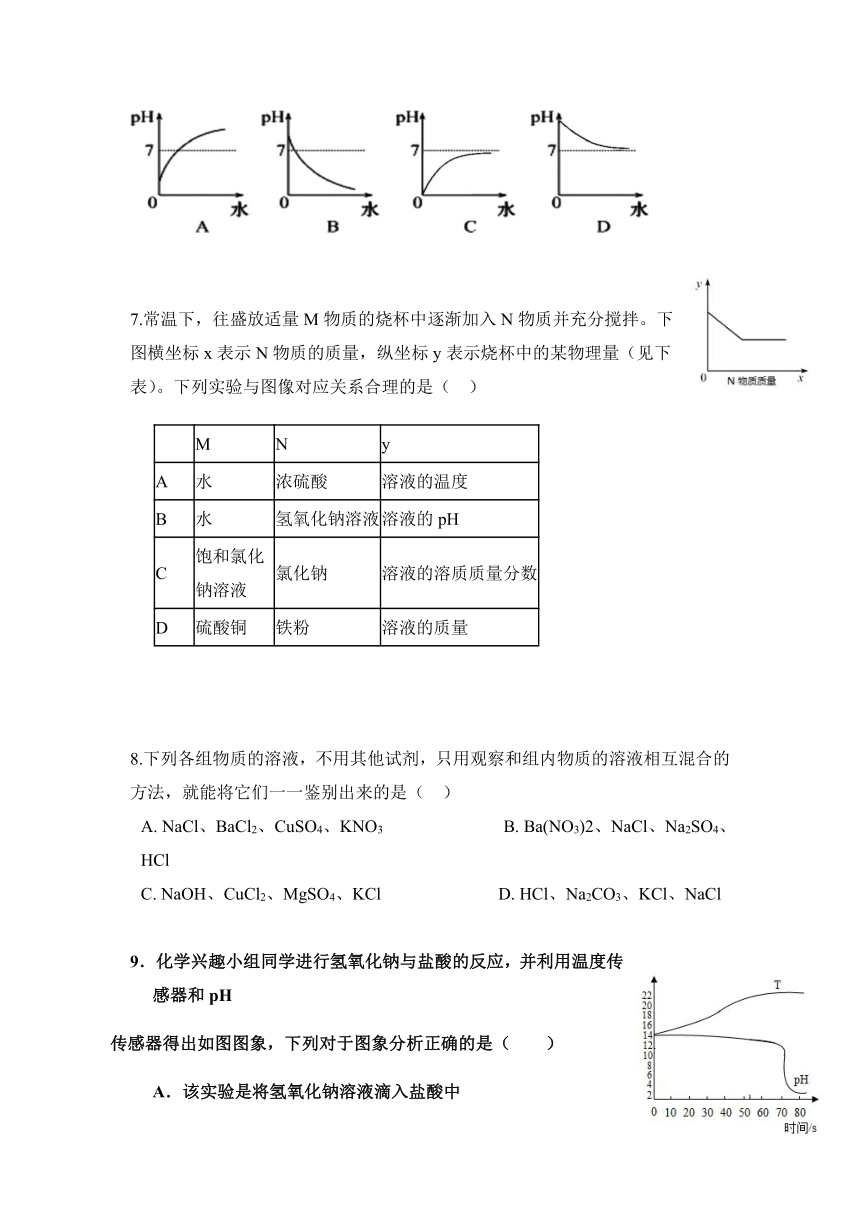
5.下列图示的实验操作正确的是(?? )
?
A.过滤?? ?B称取氯化钠 C.?稀释浓硫酸?? D.?测溶液的PH值
6.下列示意图能表示加水稀释pH=10的溶液的是( )
7.常温下,往盛放适量M物质的烧杯中逐渐加入N物质并充分搅拌。下图横坐标x表示N物质的质量,纵坐标y表示烧杯中的某物理量(见下表)。下列实验与图像对应关系合理的是(?? )
M N y
A 水 浓硫酸 溶液的温度
B 水 氢氧化钠溶液 溶液的pH
C 饱和氯化钠溶液 氯化钠 溶液的溶质质量分数
D 硫酸铜 铁粉 溶液的质量
8.下列各组物质的溶液,不用其他试剂,只用观察和组内物质的溶液相互混合的方法,就能将它们一一鉴别出来的是( ??)
A.?NaCl、BaCl2、CuSO4、KNO3 ??????????????????????????B.?Ba(NO3)2、NaCl、Na2SO4、HCl
C.?NaOH、CuCl2、MgSO4、KCl???????????????????????????D.?HCl、Na2CO3、KCl、NaCl
9.化学兴趣小组同学进行氢氧化钠与盐酸的反应,并利用温度传感器和pH
传感器得出如图图象,下列对于图象分析正确的是( )
A.该实验是将氢氧化钠溶液滴入盐酸中
B.约70秒时恰好完全反应
C.温度的变化能够直接证明二者发生化学变化
D.中和反应放热,所以放热的反应一定是中和反应
10.向盛有稀盐酸的烧杯中滴加氢氧化钠溶液,对反应前后烧杯中溶液的分析,错误的是( )
A.氯离子减少 B.钠离子增加 C.酸性减弱 D.温度升高
二、填空题
11.酸和碱作用生成盐和水的反应,叫做中和反应。它在工农业生产和日常生活中有广泛的用途。写出下列应用所对应的化学方程式。
(1)用熟石灰〔Ca(OH)2〕改良酸性土壤(盐酸) ________________________________________。
(2)服用含Al(OH)3的药物治疗胃酸过多________________。
(3)用氢氧化钠溶液洗涤石油产品中残余的硫酸_______________。
12.工厂排出的无色废水经测定pH=3.如果往此废水中滴入紫色石蕊试液,溶液变成红色.由于治污染需要,欲将此废水调节为微碱性,可在石灰石、生石灰、铁屑这几种物质中选择________以达到目的.
13氢氧化钠密封保存的原因:________;________.涉及的化学方程式是________
14.以氢氧化钠溶液为例,归纳小结碱的共同性质。填写下表:
碱的共同性质 结论或化学方程式
(1)与酸碱指示剂反应 无色酚酞试液遇碱变____________色紫色石蕊试液遇碱变____________色
(2)非金属氧化物+碱→盐+水
(3)酸+碱→盐+水 HCl+NaOH====NaCl+H2O
(4)(某些)盐+碱→另盐+另碱
15.小明在一种未知溶液中滴入几滴酚酞试液,振荡后发现溶液不变红。请完成下列问题:
(1)该溶液一定呈酸性吗?____________,理由是____________________________________;
(2)你将如何解决这一问题? ______________________________________。
3、实验探究题
16.如右图所示,田绘同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂。为了确定盐酸与氢氧化钠是否恰好完全反应,田绘从烧杯中取少量反应后的溶液放于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡后观察到酚酞试液不变色。于是她得出“两种物质已恰好完全中和”的结论。
(1)你认为她得出的结论是否正确?____________,理由是:___________________________。
(2)写出该中和反应的化学方程式____________________________。
(3)请你另设计一个实验,探究上述烧杯中的溶液是否恰好完全中和,填写下表:
实验方法 可能观察到的现象 结论
17.某化学兴趣小组围绕“酸和碱的中和反应”的学习,进行了如下实验:
实验一:取10g质量分数2%的氢氧化钠溶液于烧杯中,滴入几滴酚酞溶液,可观察到现象为 ,然后加入稀盐酸,用玻璃棒搅拌,溶液褪为无色.有关的反应方程式
实验二:对实验一反应后溶液中的溶质进行探究.
(1)【提出猜想】
猜想一:只有NaCl 猜想二:有NaCl和NaOH 猜想三:有NaCl和HCl
你认为猜想 不合理,其理由是 .
(2)【设计实验】
实验操作 实验现象 实验结论
方案一,取反应后的溶液于试管中,向其中加入 猜想三成立
方案二,取反应后的溶液于试管中,向其中加入 猜想三成立
(3)该实验当溶液pH=7时,共用去稀盐酸7.3g,则实验所用的稀盐酸的溶质质量分数为 .(写出计算过程)
18.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动。以下是教学片段,请你参与学习并帮助填写空格(包括表中空格)。
【演示实验】将一定量的稀H2SO4加入盛有NaOH溶液的小烧杯中。
【学生板演】该反应的化学方程式 。
【提出问题】实验未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
【猜想假设】针对疑问,大家纷纷提出猜想。甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的。不合理的猜想及其理由是 。
【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有 。
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,进行如下三个方案的探究。
实验方案 测溶液pH 滴加Na2CO3溶液 滴加BaCl2溶液
实验操作
实验现象 试纸变色,对比比色卡,pH 7(选填“>”“<”或“=”) 产生白色沉淀
实验结论 溶液中有H2SO4 溶液中有H2SO4 溶液中有H2SO4
【得出结论】通过探究,全班同学一致确定猜想二是正确的。
【评价反思】老师对同学们用多种方法进行探究,并得出正确结论给予肯定。同时指出实验探究(2)中存在两处明显错误,请大家反思。同学们经过反思发现了两处错误:
(1)实验操作中的错误是 。
(2)实验方案中有一个是错误的,写出能说明实验方案错误原因的化学方程式
是 。
答案:
1.B2.D3.B。4. D5.C 6. D 7. D 8.C 9. B。10.A。
11.(1)Ca(OH)2+2HCl====CaCl2+2H2O
(2)Al(OH)3+3HCl====AlCl3+3H2O
(3)2NaOH+H2SO4====Na2SO4+2H2O
12. 生石灰
13.能吸收空气中的水分发生潮解;与空气中的二氧化碳反应;CO2+2NaOH=Na2CO3+H2O
14.(1)红 蓝
(2)Ca(OH)2+CO2====CaCO3↓+H2O(或2NaOH+SO2Na2SO3+H2O等)
(4)CuSO4+2NaOH====Cu(OH)2↓+Na2SO4〔或Ca(OH)2+Na2====CO3CaCO3↓+2NaOH等〕
15.(1)不一定 无色酚酞试液在酸性和中性溶液中都不变色
16.(1)不正确 滴加的稀盐酸过量,酚酞试液也不会变色
(2)NaOH+HCl====NaCl+H2O
(3)以下方法任写一种均可:
实验方法 实验现象 结论
①取样,滴加紫色石蕊试液 试液变红 盐酸过量
②取样,滴加紫色石蕊试液 试液不变红 恰好中和
③取样,滴加碳酸钠溶液 有气泡产生 盐酸过量
④取样,滴加碳酸钠溶液 无气泡产生 恰好中和
⑤取样,加入锌粒等活泼?金属 有气泡产生 盐酸过量
⑥取样,加入锌粒等活泼?金属 无气泡产生 恰好中和
17.故答案为:溶液变为红色
反应方程式 NaOH+HCl═NaCl+H2O
(1)猜想 二,其理由是 若有氢氧化钠,溶液应呈红色
(2)【设计实验】(其他合理方案均可)
实验操作 实验现象 实验结论
方案一,向其中加入 紫色石蕊试液 溶液变红 猜想三成立
方案二,向其中加入 锌粒 有气泡产生 猜想三成立
(3)2.5%
.
18.【学生板演】H2SO4+2NaOH=Na2SO4+2H2O;
【猜想假设】Na2SO4和H2SO4,猜想四不正确,H2SO4和NaOH还会继续反应;
【实验探究】(1)NaOH或氢氧化钠;
(2)<,有气泡产生;
【评价反思】(1)pH试纸浸入溶液中;
(2)BaCl2+Na2SO4=BaSO4↓+2NaCl
同课章节目录
