高中生物人教版必修一第五章酶的作用和本质 PPT(28张PPT)
文档属性
| 名称 | 高中生物人教版必修一第五章酶的作用和本质 PPT(28张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 生物学 | ||
| 更新时间 | 2020-03-02 00:00:00 | ||
图片预览







文档简介
(共29张PPT)
降低化学反应
活化能的酶
细胞代谢: 细胞中各种化学反应的总称
意义:细胞生命活动的基础
一、细胞代谢
1、原理
二、实验:比较H2O2在不同条件下的分解
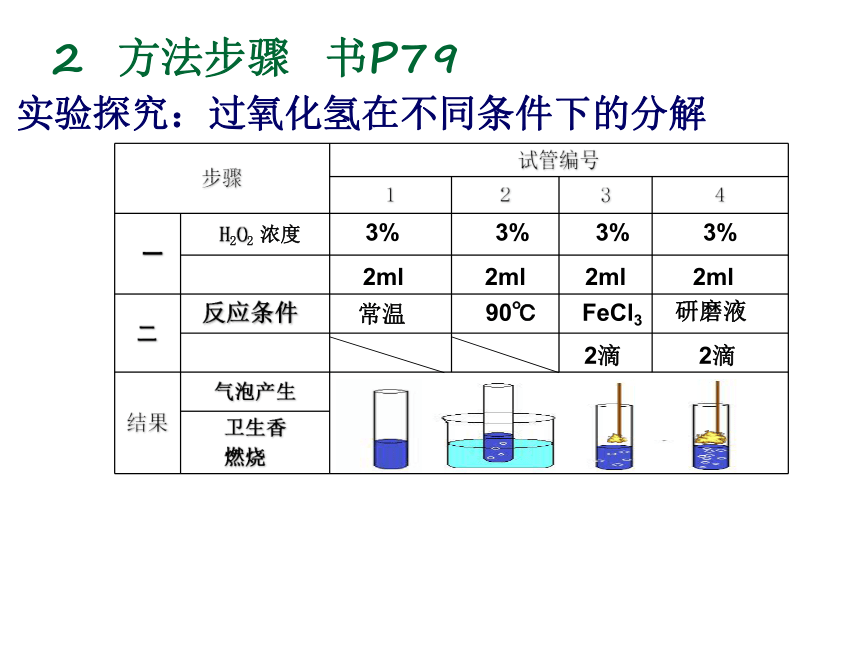
2 方法步骤 书P79
实验探究:过氧化氢在不同条件下的分解
反应条件
2ml
2ml
2ml
2ml
3%
3%
3%
3%
常温
90℃
FeCl3
研磨液
2滴
2滴
步骤 试管编号
1 2 3 4
一 H2O2 浓度
二
结果 气泡产生
卫生香
燃烧
3 实验结果
不明显
少量
大量
迅速复燃
复燃
较多
1号 2号 3号 4号
气泡产生
卫生香复燃
1号试管与2号试管对照,说明
1号试管与3号试管对照,说明
1号试管与4号试管对照,说明
3号试管与4号试管对照,说明
4 实验结论
加热能加快H2O2分解
Fe3+能加快H2O2分解
H2O2酶能加快H2O2的分解
H2O2酶的催化效率比Fe3+高
——酶有
催化作用
——酶有
高效性
三、控制变量
1、自变量:实验中人为改变的变量
因变量:随着自变量的变化而变化的变量
控制自变量
观察或检测因变量
①气泡目测法 ②卫生香复燃法
无关变量:除自变量外,实验中对实验结果造成影响的变量
消除无关变量 随机均分 等量且适量 相同且适宜
如实验中的不同反应条件
如实验中H2O2用量、浓度、室温、催化剂的浓度及用量
如实验中H2O2分解的速率
2、对照实验
除一个因素外,其余因素都保持不变的实验
对照组:
实验组:
1号
2、3、4号
空白对照:
相互对照:
1号与2、3、4号
2、3、4号
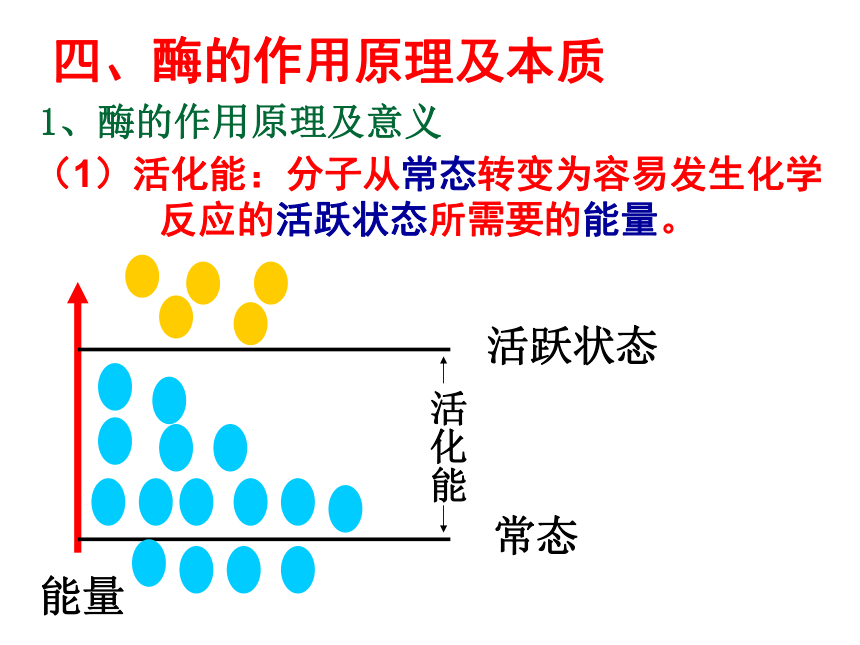
四、酶的作用原理及本质
1、酶的作用原理及意义
(1)活化能:分子从常态转变为容易发生化学反应的活跃状态所需要的能量。
常态分子 活跃状态分子
活化能
加热:
Fe3+:
酶:
提高分子的能量
降低化学反应的活化能
更显著地降低化学反应的活化能
(2)作用原理
(3)意义
使细胞代谢能在温和的条件下快速进行
a:无催化剂
b:无机催化剂
c:酶
A
B
C
D
AD:反应所需活化能
CD: 无机催化剂降低的活化能
BD: 酶降低的活化能
2、酶本质的探索历程
资料
巴斯德
李比希
毕希纳
萨姆纳
切赫
奥特曼
用3分钟的时间阅读课本P81-82“关于酶本质的探索”
他们在酶的认识历程中分别有什么发现?
思考
巴斯德之前
发酵是纯化学反应,与生命活动无关
巴斯德
发酵与活细胞有关,发酵是整个细胞而不是细胞中某些物质起作用
引起发酵的是细胞中的某些物质,但这些物质只有在酵母细胞死亡并裂解后才能发挥作用
毕希纳
酵母细胞中的某些物质能够在酵母细胞破碎后继续起催化作用,就像在活酵母细胞中一样
萨姆纳
脲酶是蛋白质
李比希
切赫、奥特曼
少数RNA也具有生物催化功能
3、酶的概念
酶是活细胞产生的具有催化作用的有机物,大多数是蛋白质,少数是RNA。
酶的产生场所
酶的作用
酶的化学本质
酶的作用场所:
细胞内、外或生物体内外均可
五、酶的特性
1、高效性 酶的催化效率大约是无机催化剂的107~13 倍
2、专一性 每种酶只能催化一种或一类化学反应
3、作用条件温和 适宜的温度、PH
A
A
B
B
C
C
A
B
C
A‘
B’
C‘
过酸、过碱、高温都会使酶的空间结构遭到破坏,使酶永久失活。
而低温,酶的活性很低,但酶的空间结构稳定,在适宜的温度下酶的活性可以升高。
酶制剂适于低温(0~4℃)下保存。
B点:该酶的最适温度
A—B:当温度低于最适温度,酶的活性随着温度升高而升高
B—C:当温度高于最适温度,酶的活性随着温度升高而降低,甚至失活。
A
A
B
B
C
C
A
B
C
A‘
B’
C‘
六、实验
1、酶活性:酶对化学反应的催化效率
观察或检测指标:
单位时间内反应物的减少量或产物的增加量
2、探究温度对淀粉酶活性的影响
自变量:
因变量:
控制自变量:
观察或检测因变量:
温度
酶活性的大小
0℃ 60℃ 100℃
用碘液检验
注意:①底物不能用H2O2 (因为高温能加快H2O2分解)
②不能用斐林试剂检验
只有在一定温度下酶的催化效率最好
只有在一定温度下酶的催化效率最好
实验步骤 1 1’ 2 2’ 3 3’
一 2mL淀粉溶液 2mL淀粉酶溶液 2mL淀粉溶液 2mL淀粉酶溶液 2mL淀粉溶液 2mL淀粉酶溶液
二 在冰水中
水浴5分钟 在60℃
水浴中5分钟 在沸水中
水浴5分钟
三 1与1’试管
混合均匀 2与2’试管
混合均匀 3与3’试管
混合均匀
四 在冰水中
水浴数分钟 在60℃水中
水浴数分钟 在沸水中
水浴数分钟
五 取出试管,分别滴加2滴碘液摇匀观察现象
现象 呈蓝色 无蓝色出现 呈蓝色
结论
3、探究PH对H2O2酶活性的影响
自变量:
因变量:
控制自变量:
观察或检测因变量:
PH
酶活性的大小
酸性 中性 碱性
观察气泡产生速率
或卫生香的复燃程度
注意:底物不能用淀粉(因为酸和碱都能催化淀粉水解)
1号试管
2号试管
3号试管
加入2ml水
试管各加入1mL H2O2酶溶液
生成大量气泡
加入2ml H2O2溶液,并在适宜温度下水浴
观察3支试管中气泡的产生情况
只有在适合的pH下酶的催化效率最好
无明显变化
无明显变化
探究pH对H2O2酶活性的影响
加入2mlHCl
加入2mlNaOH
过氧化氢溶液
实验步骤 一
二
三
四
实验现象
结论
4、验证酶的专一性
自变量:
因变量:
控制自变量:
观察或检测因变量:
不同底物
底物能否被淀粉酶水解
一组用淀粉,一组用蔗糖
用斐林试剂检验
注意:不能用碘液检验(不能检测出
蔗糖是否水解)
加入等量且适量淀粉酶,振荡摇匀,置于相同且适宜的条件下,反应一段时间
2号试管中加入等量
蔗糖溶液
加入斐林试剂
振荡
约60℃水浴2min
1号试管中加入适量
淀粉溶液
浅蓝色
无变化
砖红色沉淀
淀粉酶只能催化淀粉水解,不能催化蔗糖水解。
探究淀粉酶对淀粉和蔗糖的水解作用
1号试管 2号试管
实验步骤 一
二
三
实验现象
结论
影响酶促反应速率的因素:
1、温度
3、酶的浓度:反应速率随
酶浓度的升高而加快。
4、底物浓度:在一定浓度
范围内,反应速率随浓
度的升高而加快,但达
到一定浓度,反应速率
不再变化
酶量一定
2、pH
底物充足
温度、PH
激活剂或抑制剂
酶浓度、底物浓度
影响
酶活性
影响
酶与底物的接触面积
影响
酶促反应速率
酶促反应速率≠酶活性
谢
谢!
降低化学反应
活化能的酶
细胞代谢: 细胞中各种化学反应的总称
意义:细胞生命活动的基础
一、细胞代谢
1、原理
二、实验:比较H2O2在不同条件下的分解
2 方法步骤 书P79
实验探究:过氧化氢在不同条件下的分解
反应条件
2ml
2ml
2ml
2ml
3%
3%
3%
3%
常温
90℃
FeCl3
研磨液
2滴
2滴
步骤 试管编号
1 2 3 4
一 H2O2 浓度
二
结果 气泡产生
卫生香
燃烧
3 实验结果
不明显
少量
大量
迅速复燃
复燃
较多
1号 2号 3号 4号
气泡产生
卫生香复燃
1号试管与2号试管对照,说明
1号试管与3号试管对照,说明
1号试管与4号试管对照,说明
3号试管与4号试管对照,说明
4 实验结论
加热能加快H2O2分解
Fe3+能加快H2O2分解
H2O2酶能加快H2O2的分解
H2O2酶的催化效率比Fe3+高
——酶有
催化作用
——酶有
高效性
三、控制变量
1、自变量:实验中人为改变的变量
因变量:随着自变量的变化而变化的变量
控制自变量
观察或检测因变量
①气泡目测法 ②卫生香复燃法
无关变量:除自变量外,实验中对实验结果造成影响的变量
消除无关变量 随机均分 等量且适量 相同且适宜
如实验中的不同反应条件
如实验中H2O2用量、浓度、室温、催化剂的浓度及用量
如实验中H2O2分解的速率
2、对照实验
除一个因素外,其余因素都保持不变的实验
对照组:
实验组:
1号
2、3、4号
空白对照:
相互对照:
1号与2、3、4号
2、3、4号
四、酶的作用原理及本质
1、酶的作用原理及意义
(1)活化能:分子从常态转变为容易发生化学反应的活跃状态所需要的能量。
常态分子 活跃状态分子
活化能
加热:
Fe3+:
酶:
提高分子的能量
降低化学反应的活化能
更显著地降低化学反应的活化能
(2)作用原理
(3)意义
使细胞代谢能在温和的条件下快速进行
a:无催化剂
b:无机催化剂
c:酶
A
B
C
D
AD:反应所需活化能
CD: 无机催化剂降低的活化能
BD: 酶降低的活化能
2、酶本质的探索历程
资料
巴斯德
李比希
毕希纳
萨姆纳
切赫
奥特曼
用3分钟的时间阅读课本P81-82“关于酶本质的探索”
他们在酶的认识历程中分别有什么发现?
思考
巴斯德之前
发酵是纯化学反应,与生命活动无关
巴斯德
发酵与活细胞有关,发酵是整个细胞而不是细胞中某些物质起作用
引起发酵的是细胞中的某些物质,但这些物质只有在酵母细胞死亡并裂解后才能发挥作用
毕希纳
酵母细胞中的某些物质能够在酵母细胞破碎后继续起催化作用,就像在活酵母细胞中一样
萨姆纳
脲酶是蛋白质
李比希
切赫、奥特曼
少数RNA也具有生物催化功能
3、酶的概念
酶是活细胞产生的具有催化作用的有机物,大多数是蛋白质,少数是RNA。
酶的产生场所
酶的作用
酶的化学本质
酶的作用场所:
细胞内、外或生物体内外均可
五、酶的特性
1、高效性 酶的催化效率大约是无机催化剂的107~13 倍
2、专一性 每种酶只能催化一种或一类化学反应
3、作用条件温和 适宜的温度、PH
A
A
B
B
C
C
A
B
C
A‘
B’
C‘
过酸、过碱、高温都会使酶的空间结构遭到破坏,使酶永久失活。
而低温,酶的活性很低,但酶的空间结构稳定,在适宜的温度下酶的活性可以升高。
酶制剂适于低温(0~4℃)下保存。
B点:该酶的最适温度
A—B:当温度低于最适温度,酶的活性随着温度升高而升高
B—C:当温度高于最适温度,酶的活性随着温度升高而降低,甚至失活。
A
A
B
B
C
C
A
B
C
A‘
B’
C‘
六、实验
1、酶活性:酶对化学反应的催化效率
观察或检测指标:
单位时间内反应物的减少量或产物的增加量
2、探究温度对淀粉酶活性的影响
自变量:
因变量:
控制自变量:
观察或检测因变量:
温度
酶活性的大小
0℃ 60℃ 100℃
用碘液检验
注意:①底物不能用H2O2 (因为高温能加快H2O2分解)
②不能用斐林试剂检验
只有在一定温度下酶的催化效率最好
只有在一定温度下酶的催化效率最好
实验步骤 1 1’ 2 2’ 3 3’
一 2mL淀粉溶液 2mL淀粉酶溶液 2mL淀粉溶液 2mL淀粉酶溶液 2mL淀粉溶液 2mL淀粉酶溶液
二 在冰水中
水浴5分钟 在60℃
水浴中5分钟 在沸水中
水浴5分钟
三 1与1’试管
混合均匀 2与2’试管
混合均匀 3与3’试管
混合均匀
四 在冰水中
水浴数分钟 在60℃水中
水浴数分钟 在沸水中
水浴数分钟
五 取出试管,分别滴加2滴碘液摇匀观察现象
现象 呈蓝色 无蓝色出现 呈蓝色
结论
3、探究PH对H2O2酶活性的影响
自变量:
因变量:
控制自变量:
观察或检测因变量:
PH
酶活性的大小
酸性 中性 碱性
观察气泡产生速率
或卫生香的复燃程度
注意:底物不能用淀粉(因为酸和碱都能催化淀粉水解)
1号试管
2号试管
3号试管
加入2ml水
试管各加入1mL H2O2酶溶液
生成大量气泡
加入2ml H2O2溶液,并在适宜温度下水浴
观察3支试管中气泡的产生情况
只有在适合的pH下酶的催化效率最好
无明显变化
无明显变化
探究pH对H2O2酶活性的影响
加入2mlHCl
加入2mlNaOH
过氧化氢溶液
实验步骤 一
二
三
四
实验现象
结论
4、验证酶的专一性
自变量:
因变量:
控制自变量:
观察或检测因变量:
不同底物
底物能否被淀粉酶水解
一组用淀粉,一组用蔗糖
用斐林试剂检验
注意:不能用碘液检验(不能检测出
蔗糖是否水解)
加入等量且适量淀粉酶,振荡摇匀,置于相同且适宜的条件下,反应一段时间
2号试管中加入等量
蔗糖溶液
加入斐林试剂
振荡
约60℃水浴2min
1号试管中加入适量
淀粉溶液
浅蓝色
无变化
砖红色沉淀
淀粉酶只能催化淀粉水解,不能催化蔗糖水解。
探究淀粉酶对淀粉和蔗糖的水解作用
1号试管 2号试管
实验步骤 一
二
三
实验现象
结论
影响酶促反应速率的因素:
1、温度
3、酶的浓度:反应速率随
酶浓度的升高而加快。
4、底物浓度:在一定浓度
范围内,反应速率随浓
度的升高而加快,但达
到一定浓度,反应速率
不再变化
酶量一定
2、pH
底物充足
温度、PH
激活剂或抑制剂
酶浓度、底物浓度
影响
酶活性
影响
酶与底物的接触面积
影响
酶促反应速率
酶促反应速率≠酶活性
谢
谢!
同课章节目录
- 第一章 走近细胞
- 第1节 从生物圈到细胞
- 第2节 细胞的多样性和统一性
- 第二章 组成细胞的分子
- 第1节 细胞中的元素和化合物
- 第2节 生命活动的主要承担者──蛋白质
- 第3节 遗传信息的携带者──核酸
- 第4节 细胞中的糖类和脂质
- 第5节 细胞中的无机物
- 第三章 细胞的基本结构
- 第1节 细胞膜──系统的边界
- 第2节 细胞器──系统内的分工合作
- 第3节 细胞核──系统的控制中心
- 第四章 细胞的物质输入和输出
- 第1节 物质跨膜运输的实例
- 第2节 生物膜的流动镶嵌模型
- 第3节 物质跨膜运输的方式
- 第五章 细胞的能量供应和利用
- 第1节 降低化学反应活化能的酶
- 第2节 细胞的能量“通货”──ATP
- 第3节 ATP的主要来源──细胞呼吸
- 第4节 能量之源——光与光合作用
- 第六章 细胞的生命历程
- 第1节 细胞的增殖
- 第2节 细胞的分化
- 第3节 细胞的衰老和凋亡
- 第4节 细胞的癌变
