高中化学人教版 (2019)必修 第一册 1.3 氧化还原反应(共20张ppt)
文档属性
| 名称 | 高中化学人教版 (2019)必修 第一册 1.3 氧化还原反应(共20张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 11.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-03 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
氧化还原反应
理解氧化还原反应的特征、本质
学会用化合价升降、电子得失或电子转移的角度来理解氧化还原反应
培养由现象到本质的科学探究意识
教学重难点
从化合价升降、电子得失或电子转移角度理解氧化还原反应
教学目标
下图中的铜狮子、铜壶、铁链为什么会生锈?你能用化学知识来解释一下吗?
导入新课
初中学过的四大基本反应类型都有哪些?
分解反应 化合反应 置换反应 复分解反应
高温
思考:
2CuO+C 2Cu+CO2 属于四大基本反应类型中的哪一种?
温故知新
教学过程
课前准备
课堂实施
课后提升
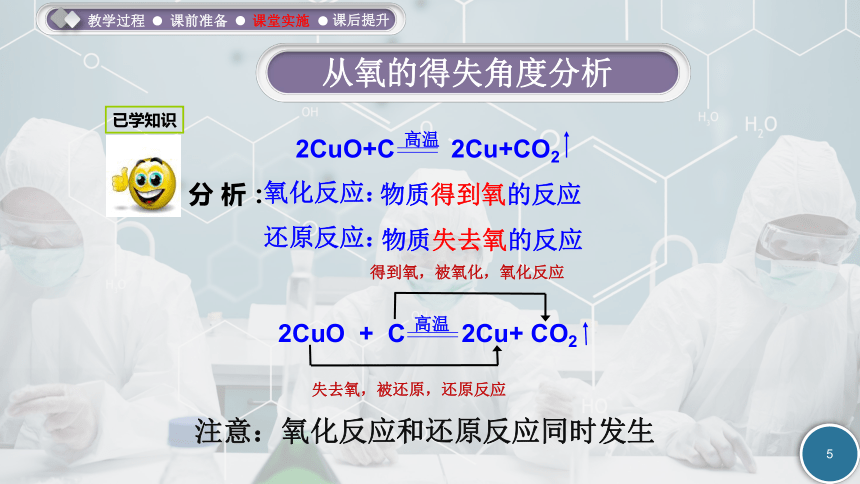
得到氧,被氧化,氧化反应
失去氧,被还原,还原反应
2CuO+C 2Cu+CO2
2CuO + C 2Cu+ CO2
分 析:
氧化反应:
还原反应:
已学知识
注意:氧化反应和还原反应同时发生
物质得到氧的反应
物质失去氧的反应
教学过程
课前准备
课堂实施
课后提升
高温
高温
从氧的得失角度分析
从得失氧的角度可得出氧化还原反应的定义:
一种物质失去氧,同时另一种物质得到氧的反应,叫做氧化还原反应。
结论1
教学过程
课前准备
课堂实施
课后提升
标出下列氧化还原反应中的各个元素的化合价,观察化合价有无变化,变化有无规律?
H2+CuO====Cu+H2O
2Mg+O2====2MgO
CO+CuO====Cu+CO2
△
△
点燃
合作与探究
教学过程
课前准备
课堂实施
课后提升
CO+CuO====Cu+CO2
2Mg+O2====2MgO
H2 + CuO ==== H2O + Cu
失氧,被还原,化合价降低,还原反应
+2
0
得氧,被氧化,化合价升高,氧化反应
0
+1
点燃
(1)
(2)
(3)
分 析:
被氧化,化合价升高
0
+2
被还原,化合价降低
0
-2
被还原,化合价降低
+2
0
+2
被氧化,化合价升高
+4
教学过程
课前准备
课堂实施
课后提升
从化合价升降的角度定义
有元素化合价升降的反应,叫氧化还原反应。
氧化还原反应的特征:有元素化合价的升降
结论2
重点:
(氧化还原反应的判断依据)
教学过程
课前准备
课堂实施
课后提升
练习:判断下列反应是否属于氧化还原反应?
+7 -2 +6 +4 0
⑴ 2KMnO4 == K2MnO4 + MnO2 + O2↑
+5 -2 -1 0
⑵ 2KClO3 == 2KCl+3O2↑
⑶ Na2CO3+2HCl==2NaCl+ H2O + CO2↑
0 +1 +2 0
⑷ Fe+2HCl== 2FeCl2 + H2↑
+3 +2 0 +4
⑸ Fe2O3 + 3CO === 2Fe + 3CO2
(6) CaO+H2O==Ca(OH)2
√
√
√
×
×
√
MnO2
高温
化合价升高
化合价降低
先分析钠与
氯气的反应吧
思考:
在反应过程中元素化合价为什么会发生变化呢?氧化还原反应的本质是什么?
0
0
+1 -1
2Na+Cl2 ==== 2Na Cl
点燃
从化合价升降角度分析
教学过程
课前准备
课堂实施
课后提升
2Na + Cl2 ==== 2NaCl
点燃
化合价的升降——电子的得失
化合价变化本质原因的分析
教学过程
课前准备
课堂实施
课后提升
H Cl
+17
+1
+1
+17
H Cl
δ+ δ-
H
Cl
HCl
化合价的升降—共用电子对的偏移
教学过程
课前准备
课堂实施
课后提升
有电子转移(得失或偏移)的反应都是氧化还原反应。
结论3
氧化还原反应的本质:有电子转移(得失或偏移)
重点:
教学过程
课前准备
课堂实施
课后提升
知识线
口诀
升失氧 降得还
(特征)
—
化合价升高
化合价降低
被还原
被氧化
氧化反应
还原反应
失电子
(共用电子对偏离)
得电子
(共用电子对偏向)
—
—
—
—
—
(本质)
教学过程
课前准备
课堂实施
课后提升
1.下列反应属于氧化还原反应的是( )
A. CaCO3+2HCl==CaCl2+H2O+CO2↑
B. CaCO3====CaO+CO2↑
C. Na2O+H2O==2NaOH
D. Mg+2HCl==MgCl2+H2↑
高温
D
教学过程
课前准备
课堂实施
课后提升
巩固提升
2.某元素在化学反应中由化合态(化合物)变为 游离态(单质),则该元素( )
A.一定被氧化
B.一定被还原
C.可能被氧化,也可能被还原
D.以上都不是
C
教学过程
课前准备
课堂实施
课后提升
巩固提升
3. 氧化还原反应的实质是( )
A.化合价的升降
B.分子中各原子重新组合
C.电子的得失或共用电子对的偏移
D.原子的得失
C
教学过程
课前准备
课堂实施
课后提升
巩固提升
step 01
得失氧角度
step 02
化合价升降角度
step 03
电子转移角度
step 04
特征:元素化合价发生变化
step 05
本质:有电子转移(得失或偏移)
氧化还原反应
归纳小结
谢谢欣赏
氧化还原反应
理解氧化还原反应的特征、本质
学会用化合价升降、电子得失或电子转移的角度来理解氧化还原反应
培养由现象到本质的科学探究意识
教学重难点
从化合价升降、电子得失或电子转移角度理解氧化还原反应
教学目标
下图中的铜狮子、铜壶、铁链为什么会生锈?你能用化学知识来解释一下吗?
导入新课
初中学过的四大基本反应类型都有哪些?
分解反应 化合反应 置换反应 复分解反应
高温
思考:
2CuO+C 2Cu+CO2 属于四大基本反应类型中的哪一种?
温故知新
教学过程
课前准备
课堂实施
课后提升
得到氧,被氧化,氧化反应
失去氧,被还原,还原反应
2CuO+C 2Cu+CO2
2CuO + C 2Cu+ CO2
分 析:
氧化反应:
还原反应:
已学知识
注意:氧化反应和还原反应同时发生
物质得到氧的反应
物质失去氧的反应
教学过程
课前准备
课堂实施
课后提升
高温
高温
从氧的得失角度分析
从得失氧的角度可得出氧化还原反应的定义:
一种物质失去氧,同时另一种物质得到氧的反应,叫做氧化还原反应。
结论1
教学过程
课前准备
课堂实施
课后提升
标出下列氧化还原反应中的各个元素的化合价,观察化合价有无变化,变化有无规律?
H2+CuO====Cu+H2O
2Mg+O2====2MgO
CO+CuO====Cu+CO2
△
△
点燃
合作与探究
教学过程
课前准备
课堂实施
课后提升
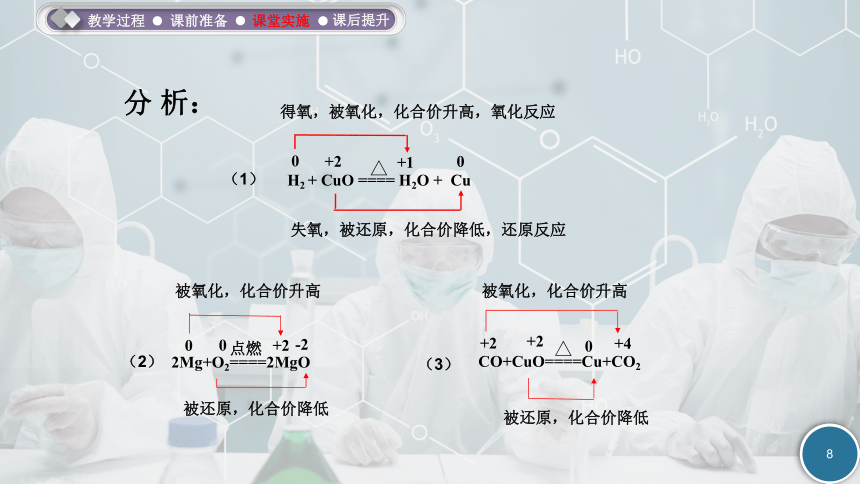
CO+CuO====Cu+CO2
2Mg+O2====2MgO
H2 + CuO ==== H2O + Cu
失氧,被还原,化合价降低,还原反应
+2
0
得氧,被氧化,化合价升高,氧化反应
0
+1
点燃
(1)
(2)
(3)
分 析:
被氧化,化合价升高
0
+2
被还原,化合价降低
0
-2
被还原,化合价降低
+2
0
+2
被氧化,化合价升高
+4
教学过程
课前准备
课堂实施
课后提升
从化合价升降的角度定义
有元素化合价升降的反应,叫氧化还原反应。
氧化还原反应的特征:有元素化合价的升降
结论2
重点:
(氧化还原反应的判断依据)
教学过程
课前准备
课堂实施
课后提升
练习:判断下列反应是否属于氧化还原反应?
+7 -2 +6 +4 0
⑴ 2KMnO4 == K2MnO4 + MnO2 + O2↑
+5 -2 -1 0
⑵ 2KClO3 == 2KCl+3O2↑
⑶ Na2CO3+2HCl==2NaCl+ H2O + CO2↑
0 +1 +2 0
⑷ Fe+2HCl== 2FeCl2 + H2↑
+3 +2 0 +4
⑸ Fe2O3 + 3CO === 2Fe + 3CO2
(6) CaO+H2O==Ca(OH)2
√
√
√
×
×
√
MnO2
高温
化合价升高
化合价降低
先分析钠与
氯气的反应吧
思考:
在反应过程中元素化合价为什么会发生变化呢?氧化还原反应的本质是什么?
0
0
+1 -1
2Na+Cl2 ==== 2Na Cl
点燃
从化合价升降角度分析
教学过程
课前准备
课堂实施
课后提升
2Na + Cl2 ==== 2NaCl
点燃
化合价的升降——电子的得失
化合价变化本质原因的分析
教学过程
课前准备
课堂实施
课后提升
H Cl
+17
+1
+1
+17
H Cl
δ+ δ-
H
Cl
HCl
化合价的升降—共用电子对的偏移
教学过程
课前准备
课堂实施
课后提升
有电子转移(得失或偏移)的反应都是氧化还原反应。
结论3
氧化还原反应的本质:有电子转移(得失或偏移)
重点:
教学过程
课前准备
课堂实施
课后提升
知识线
口诀
升失氧 降得还
(特征)
—
化合价升高
化合价降低
被还原
被氧化
氧化反应
还原反应
失电子
(共用电子对偏离)
得电子
(共用电子对偏向)
—
—
—
—
—
(本质)
教学过程
课前准备
课堂实施
课后提升
1.下列反应属于氧化还原反应的是( )
A. CaCO3+2HCl==CaCl2+H2O+CO2↑
B. CaCO3====CaO+CO2↑
C. Na2O+H2O==2NaOH
D. Mg+2HCl==MgCl2+H2↑
高温
D
教学过程
课前准备
课堂实施
课后提升
巩固提升
2.某元素在化学反应中由化合态(化合物)变为 游离态(单质),则该元素( )
A.一定被氧化
B.一定被还原
C.可能被氧化,也可能被还原
D.以上都不是
C
教学过程
课前准备
课堂实施
课后提升
巩固提升
3. 氧化还原反应的实质是( )
A.化合价的升降
B.分子中各原子重新组合
C.电子的得失或共用电子对的偏移
D.原子的得失
C
教学过程
课前准备
课堂实施
课后提升
巩固提升
step 01
得失氧角度
step 02
化合价升降角度
step 03
电子转移角度
step 04
特征:元素化合价发生变化
step 05
本质:有电子转移(得失或偏移)
氧化还原反应
归纳小结
谢谢欣赏
