第九单元 课题1溶液的形成 同步练习(解析版)
文档属性
| 名称 | 第九单元 课题1溶液的形成 同步练习(解析版) |

|
|
| 格式 | zip | ||
| 文件大小 | 62.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-05 00:00:00 | ||
图片预览



文档简介
第九单元课题1溶液的形成同步练习(解析版)
1.下列关于溶液的说法,正确的是
A.溶液都是无色透明的 B.面粉与水混合可形成溶液
C.饱和溶液不能再溶解任何物质 D.硝酸铵溶解在水中,溶液温度会降低
2.衣服上沾有碘很难洗净,碘在下列四种不同溶剂中的溶解性如下表所示:
溶质
碘
溶剂
水
酒精
汽油
苯(有毒)
溶解性
微溶
可溶
易溶
易溶
由表中提供的信息判断,洗净衣服上的碘污渍的最佳选择是
A.水 B.酒精 C.汽油 D.苯
3.厨房中的物质放入足量的水中,充分搅拌,不能形成溶液的是
A.食用油 B.白醋 C.白糖 D.食盐
4.调味剂是重要的食品添加剂,将下列调味剂加入水中,不能形成溶液的是( )
A.食盐 B.蔗糖 C.味精 D.芝麻油
5.将少量下列调味品加入水中,不能形成溶液的是
A.食盐 B.蔗糖 C.味精 D.芝麻油
6.下列有关溶液的叙述正确的是
A.均一、稳定的液体一定是溶液 B.洗涤剂去油污是乳化现象
C.豆浆、牛奶都是溶液 D.溶液都是无色的
7.如图,往烧杯中加入一定量的某固体,会引起试管内白磷燃烧,该固体可能是
A.氢氧化钠 B.硝酸铵
C.氯化钠 D.碳酸钙
8.将一定质量的食盐溶解在 10mL 水中,下列等式一定成立的是( )
A.食盐质量+水的质量=溶液的质量
B.食盐体积+水的体积=溶液的体积
C.溶质质量+水的质量=溶液的质量
D.食盐密度+水的密度=溶液的密度
9.下列物质加入水中,能形成溶液的是
A.植物油 B.牛奶 C.食盐 D.生铁
10.配制溶液时,下列溶剂中最常用的是( )
A.酒精 B.植物油 C.汽油 D.水
11.张华为了探究溶液的质量分数与溶液颜色之间的关系,进行了实验并将数据 记录表中,根据表中的信息回答问题:
试管编号
①
②
③
水的体积/mL
5
10
15
(1)向三支试管中各加入 0.5g 硫酸铜粉末,完全溶解后,溶液颜色最深的是编号(_______)试管.
(2)由此实验可得出:溶质的质量分数越大,有色溶液的颜色越______选填“浅”或“深”).
12.已知蔗糖的溶解度随温度升高而变大。现在20℃下用蔗糖进行如下图所示的实验,该蔗糖溶液________(填“一定”或“不一定”)是饱和溶液,若要让试管中的蔗糖固体全部溶解,下列办法不可行的是_____(填序号)。
①试管内加入适量水 ②烧杯内加入适量氢氧化钠固体
③烧杯内加入适量生石灰 ④烧杯内加入适量硝酸铵固体
13.要使不饱和的氯化钠溶液变为饱和溶液的方法有__________________;_____________.(任意填两种即可)
14.某同学进行“物质溶解的吸热或放热”的探究实验.他取三支试管,向试管中分别注入水,测得水的初温为,再分别向三支试管中各加入、、固体,振荡.
“振荡”试管的目的是________.
用温度计分别测三支试管中溶液的温度,高于的是________溶液,这是因______.
装有溶液的试管外壁有水珠产生,原因是________.
由此探究实验可知________溶于水温度没有明显的变化.
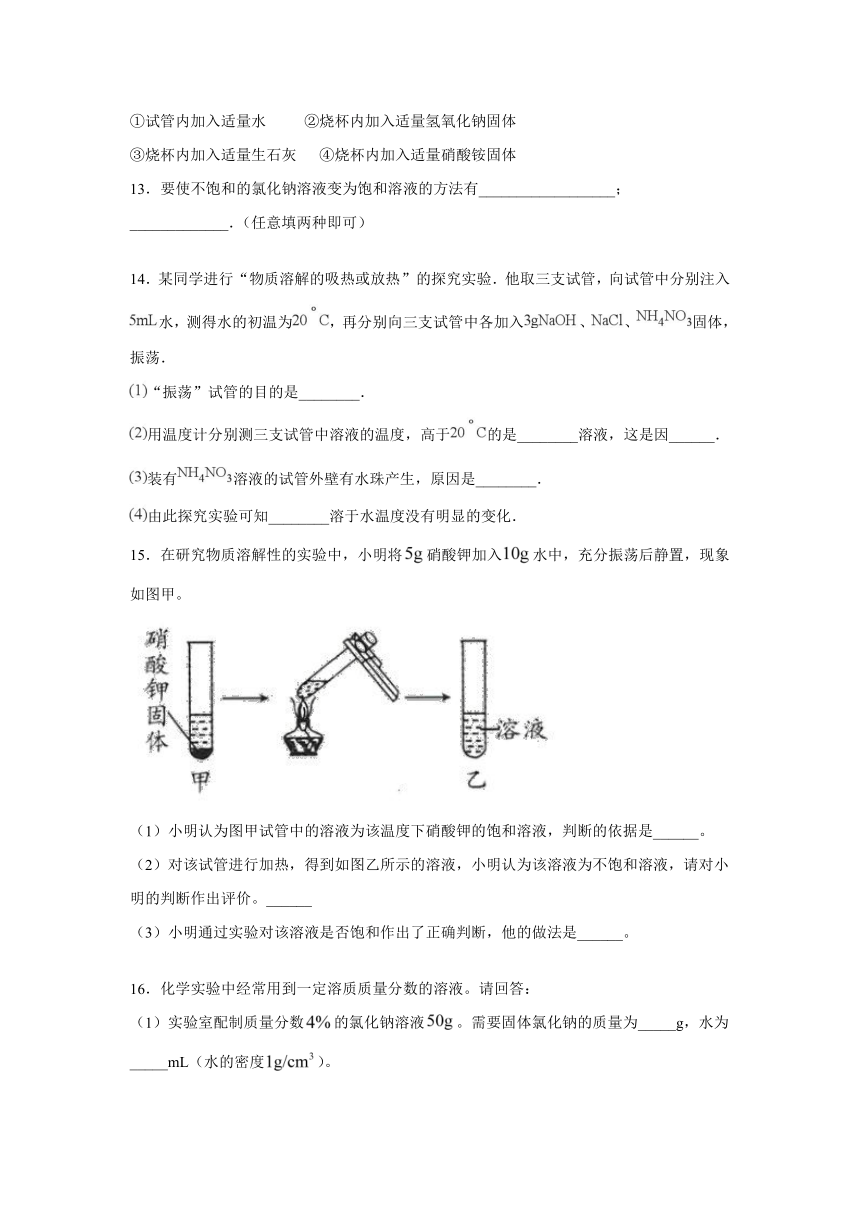
15.在研究物质溶解性的实验中,小明将硝酸钾加入水中,充分振荡后静置,现象如图甲。
(1)小明认为图甲试管中的溶液为该温度下硝酸钾的饱和溶液,判断的依据是______。
(2)对该试管进行加热,得到如图乙所示的溶液,小明认为该溶液为不饱和溶液,请对小明的判断作出评价。______
(3)小明通过实验对该溶液是否饱和作出了正确判断,他的做法是______。
16.化学实验中经常用到一定溶质质量分数的溶液。请回答:
(1)实验室配制质量分数的氯化钠溶液。需要固体氯化钠的质量为_____g,水为_____mL(水的密度)。
(2)若用质量分数为的氯化钠溶液配制质量分数为的氯化钠溶液。
①需要的氯化钠溶液的质量为_____g。
②该溶液配制过程中除用到量筒、玻璃棒和胶头滴管外,还需要的仪器是_____。
参考答案
1.D
【解析】
A、溶液不一定无色,例如硫酸铜溶液是蓝色,故A错;
B、面粉不溶于水,与水混合形成的是悬浊液,不均一、不稳定,故B错;
C、饱和溶液是指在一定温度下,一定量的溶剂里,不能再溶解某一溶质的溶液叫做这种溶质的饱和溶液,此时还可以溶解其它溶质,故C错;
D、硝酸铵溶于水吸热,溶液温度会降低,故D正确.
2.C
【解析】
为洗净碘,需要的物质应能溶解较多的碘。根据题意可知碘易溶于汽油和苯,但苯有毒,故选C。
3.A
【解析】
溶液的特点:1.均一性:溶液各处的密度、组成和性质完全一样;
2.稳定性:温度不变,溶剂量不变时,溶质和溶剂长期不会分离(透明);
3混合物:溶液一定是混合物。
A食用油不能溶于水,混合后一段时间后,油飘浮在水的上面,不具有均一、稳定的特点。此项错误。
B白醋与水混合后,可溶于水,形成均一、稳定的混合物。此项正确。
C白糖与水混合后,可溶于水,形成均一、稳定的混合物。此项正确。
D食盐与水混合后,可溶于水,形成均一、稳定的混合物。此项正确。
4.D
【解析】
A、食盐溶于水中形成均一稳定的混合物,属于溶液,故A错误;
B、蔗糖溶于水中形成均一稳定的混合物,属于溶液,故B错误;
C、味精溶于水中形成均一稳定的混合物,属于溶液,故C错误;
D、芝麻油与水混合形成的混合物不均一、不稳定,属于乳浊液,故D正确,故选D。
5.D
【解析】
试题分析:溶液的概念:一种或几种物质分散到另一种物质里形成的均一的、稳定的混合物,叫做溶液;
芝麻油不溶于水,不能形成溶液,故选D
6.B
【解析】A、溶液是指将一种或几种物质分散到其它的物质中形成的均一稳定的混合物,溶液必须是混合物,故错误;
B、洗涤剂具有乳化功能,可以去除油污,正确;
C、豆浆、牛奶不是均一、稳定的混合物,错误;
D、溶液具有均一性和稳定性,溶液不一定都是无色的,比如硫酸铜溶液是蓝色的,错误。故选B。
7.A
【解析】
物质溶于烧杯中的冷水,能引起白磷燃烧,说明了物质在溶于水时能放出热量,据此分析解答。
【详解】
A、氢氧化钠溶于水放出热量,使容器内温度升高,达到白磷的着火点,引起试管内白磷燃烧,选项正确;B、硝酸铵溶于水吸热,使容器内温度降低,选项错误;C、氯化钠溶于水容器内温度基本不变,选项错误;D、碳酸钙难溶于水,容器内温度基本不变,选项错误。故选A。
8.C
【解析】
A、被溶解的物质叫溶质。若食盐水不能完全溶解话,食盐质量+水的质量≠溶液的质量; 故本选项错误;
B、密度不同的两种物质混合后,总体积减少,因为微粒间存在间隔,所以,食盐体积+水的体积≠溶 液的体积,故本选项错误;
C、溶液是由溶质和溶剂组成的,所以溶质质量+水的质量=溶液的质量,故本选 项正确;
D、溶液中溶质和溶剂的质量可以相加,但密度不可以相加;故本选项错误。
9.C
【解析】
A、植物油不溶于水,不能和水形成均一、稳定的混合物,不能够形成溶液,错误; B、牛奶是不溶性的小液滴等分散到液体中形成的,不能和水形成均一、稳定的混合物,不能够形成溶液,错误;C、食盐易溶于水,能形成均一、稳定的混合物,属于溶液,正确;
D、生铁不溶于水,不能和水形成均一、稳定的混合物,不能够形成溶液,错误。故选C。
点睛:溶液的判定主要看其是否是均一、稳定的混合物。
10.D
【解析】
配制溶液时,如无特殊要求,一般采用水作为溶剂,水是最常用的溶剂,汽油、酒精、植物油都属于有机溶剂,故选D。
11.① 深.
【解析】
(1)由表中的数据可知,向三支试管中各加入 0.5g 硫酸铜粉末, 完全溶解后,溶液①的质量分数最大,颜色最深.
(2)由此实验可得出:溶质的质量分数越大,有色溶液的颜色越深. 故答为:(1)①;(2)深.
12.一定 ④
【解析】
由图示可知,有未溶解的蔗糖,该蔗糖溶液一定是饱和溶液;
①试管内加入适量水,能溶解蔗糖,故可行;
②烧杯内加入适量氢氧化钠固体,氢氧化钠溶于水放出大量的热,能溶解蔗糖,故可行;
③烧杯内加入适量生石灰,生石灰与水反应放出大量的热,能溶解蔗糖,故可行;
④烧杯内加入适量硝酸铵固体,硝酸铵溶于水吸热,会析出的蔗糖,故不可行。
13.继续加入少量的氯化钠 恒温蒸发水分.
【解析】
饱和溶液是在一定温度下、一定量的溶剂里不能再溶解某物质的溶液叫该物质的饱和溶液,反之为不饱和溶液。氯化钠的溶解度随温度的升高而增大,故要把其不饱和溶液转化为 饱和溶液,可采取的方法有:①继续加入少量的氯化钠;②恒温蒸发水分;③降 温。
14.加速固体的溶解氢氧化钠固体溶于水放热硝酸铵溶解吸热,使空气中的水蒸气凝结成小水珠氯化钠
【解析】
(1)振荡可以加速固体的溶解。
(2)氢氧化钠溶于水温度升高,故温度高于20℃的是氢氧化钠。
(3)硝酸铵溶于水温度降低,试管外部的温度降低,使空气中的水蒸气预冷液化为小水珠。
(4)氯化钠溶液水温度几乎不变。
15.试管底部有硝酸钾固体未溶解 小明的判断不正确,因为该溶液可能恰好为饱和溶液 向该溶液中加入少量的硝酸钾晶体,看其能否继续溶解
【解析】
饱和溶液是在一定温度下、一定量的溶剂里不能再溶解某物质的溶液叫该物质的饱和溶液,反之为不饱和溶液。
(1)图甲试管中的溶液为该温度下硝酸钾的饱和溶液,判断的依据是试管底部有硝酸钾固体未溶解,说明该条件下,溶液不能再溶解硝酸钾,
(2)对该试管进行加热,得到如图乙所示的溶液,小明认为该溶液为不饱和溶液,小明的判断不正确,因为该溶液可能恰好为饱和溶液,因为刚好饱和的溶液和不饱和溶液都是澄清溶液;
(3)判断该溶液是否饱和的做法是向该溶液中加入少量的硝酸钾晶体,看其能否继续溶解,溶解,原溶液是不饱和溶液;不溶,则是饱和溶液。
16.2 48 25 烧杯
【解析】
(1)实验室配制质量分数4%的氯化钠溶液50g,则需要固体氯化钠的质量为50g×4%=2g,需水为50g-2g=48g,即48mL,故填:2 48;
(2)设需要8%的氯化钠溶液的质量为x,8%x=50g×4%,x=25g
溶液配制过程中除用到量筒、玻璃棒和胶头滴管外,还需要烧杯盛放溶液,故填:25 烧杯。
1.下列关于溶液的说法,正确的是
A.溶液都是无色透明的 B.面粉与水混合可形成溶液
C.饱和溶液不能再溶解任何物质 D.硝酸铵溶解在水中,溶液温度会降低
2.衣服上沾有碘很难洗净,碘在下列四种不同溶剂中的溶解性如下表所示:
溶质
碘
溶剂
水
酒精
汽油
苯(有毒)
溶解性
微溶
可溶
易溶
易溶
由表中提供的信息判断,洗净衣服上的碘污渍的最佳选择是
A.水 B.酒精 C.汽油 D.苯
3.厨房中的物质放入足量的水中,充分搅拌,不能形成溶液的是
A.食用油 B.白醋 C.白糖 D.食盐
4.调味剂是重要的食品添加剂,将下列调味剂加入水中,不能形成溶液的是( )
A.食盐 B.蔗糖 C.味精 D.芝麻油
5.将少量下列调味品加入水中,不能形成溶液的是
A.食盐 B.蔗糖 C.味精 D.芝麻油
6.下列有关溶液的叙述正确的是
A.均一、稳定的液体一定是溶液 B.洗涤剂去油污是乳化现象
C.豆浆、牛奶都是溶液 D.溶液都是无色的
7.如图,往烧杯中加入一定量的某固体,会引起试管内白磷燃烧,该固体可能是
A.氢氧化钠 B.硝酸铵
C.氯化钠 D.碳酸钙
8.将一定质量的食盐溶解在 10mL 水中,下列等式一定成立的是( )
A.食盐质量+水的质量=溶液的质量
B.食盐体积+水的体积=溶液的体积
C.溶质质量+水的质量=溶液的质量
D.食盐密度+水的密度=溶液的密度
9.下列物质加入水中,能形成溶液的是
A.植物油 B.牛奶 C.食盐 D.生铁
10.配制溶液时,下列溶剂中最常用的是( )
A.酒精 B.植物油 C.汽油 D.水
11.张华为了探究溶液的质量分数与溶液颜色之间的关系,进行了实验并将数据 记录表中,根据表中的信息回答问题:
试管编号
①
②
③
水的体积/mL
5
10
15
(1)向三支试管中各加入 0.5g 硫酸铜粉末,完全溶解后,溶液颜色最深的是编号(_______)试管.
(2)由此实验可得出:溶质的质量分数越大,有色溶液的颜色越______选填“浅”或“深”).
12.已知蔗糖的溶解度随温度升高而变大。现在20℃下用蔗糖进行如下图所示的实验,该蔗糖溶液________(填“一定”或“不一定”)是饱和溶液,若要让试管中的蔗糖固体全部溶解,下列办法不可行的是_____(填序号)。
①试管内加入适量水 ②烧杯内加入适量氢氧化钠固体
③烧杯内加入适量生石灰 ④烧杯内加入适量硝酸铵固体
13.要使不饱和的氯化钠溶液变为饱和溶液的方法有__________________;_____________.(任意填两种即可)
14.某同学进行“物质溶解的吸热或放热”的探究实验.他取三支试管,向试管中分别注入水,测得水的初温为,再分别向三支试管中各加入、、固体,振荡.
“振荡”试管的目的是________.
用温度计分别测三支试管中溶液的温度,高于的是________溶液,这是因______.
装有溶液的试管外壁有水珠产生,原因是________.
由此探究实验可知________溶于水温度没有明显的变化.
15.在研究物质溶解性的实验中,小明将硝酸钾加入水中,充分振荡后静置,现象如图甲。
(1)小明认为图甲试管中的溶液为该温度下硝酸钾的饱和溶液,判断的依据是______。
(2)对该试管进行加热,得到如图乙所示的溶液,小明认为该溶液为不饱和溶液,请对小明的判断作出评价。______
(3)小明通过实验对该溶液是否饱和作出了正确判断,他的做法是______。
16.化学实验中经常用到一定溶质质量分数的溶液。请回答:
(1)实验室配制质量分数的氯化钠溶液。需要固体氯化钠的质量为_____g,水为_____mL(水的密度)。
(2)若用质量分数为的氯化钠溶液配制质量分数为的氯化钠溶液。
①需要的氯化钠溶液的质量为_____g。
②该溶液配制过程中除用到量筒、玻璃棒和胶头滴管外,还需要的仪器是_____。
参考答案
1.D
【解析】
A、溶液不一定无色,例如硫酸铜溶液是蓝色,故A错;
B、面粉不溶于水,与水混合形成的是悬浊液,不均一、不稳定,故B错;
C、饱和溶液是指在一定温度下,一定量的溶剂里,不能再溶解某一溶质的溶液叫做这种溶质的饱和溶液,此时还可以溶解其它溶质,故C错;
D、硝酸铵溶于水吸热,溶液温度会降低,故D正确.
2.C
【解析】
为洗净碘,需要的物质应能溶解较多的碘。根据题意可知碘易溶于汽油和苯,但苯有毒,故选C。
3.A
【解析】
溶液的特点:1.均一性:溶液各处的密度、组成和性质完全一样;
2.稳定性:温度不变,溶剂量不变时,溶质和溶剂长期不会分离(透明);
3混合物:溶液一定是混合物。
A食用油不能溶于水,混合后一段时间后,油飘浮在水的上面,不具有均一、稳定的特点。此项错误。
B白醋与水混合后,可溶于水,形成均一、稳定的混合物。此项正确。
C白糖与水混合后,可溶于水,形成均一、稳定的混合物。此项正确。
D食盐与水混合后,可溶于水,形成均一、稳定的混合物。此项正确。
4.D
【解析】
A、食盐溶于水中形成均一稳定的混合物,属于溶液,故A错误;
B、蔗糖溶于水中形成均一稳定的混合物,属于溶液,故B错误;
C、味精溶于水中形成均一稳定的混合物,属于溶液,故C错误;
D、芝麻油与水混合形成的混合物不均一、不稳定,属于乳浊液,故D正确,故选D。
5.D
【解析】
试题分析:溶液的概念:一种或几种物质分散到另一种物质里形成的均一的、稳定的混合物,叫做溶液;
芝麻油不溶于水,不能形成溶液,故选D
6.B
【解析】A、溶液是指将一种或几种物质分散到其它的物质中形成的均一稳定的混合物,溶液必须是混合物,故错误;
B、洗涤剂具有乳化功能,可以去除油污,正确;
C、豆浆、牛奶不是均一、稳定的混合物,错误;
D、溶液具有均一性和稳定性,溶液不一定都是无色的,比如硫酸铜溶液是蓝色的,错误。故选B。
7.A
【解析】
物质溶于烧杯中的冷水,能引起白磷燃烧,说明了物质在溶于水时能放出热量,据此分析解答。
【详解】
A、氢氧化钠溶于水放出热量,使容器内温度升高,达到白磷的着火点,引起试管内白磷燃烧,选项正确;B、硝酸铵溶于水吸热,使容器内温度降低,选项错误;C、氯化钠溶于水容器内温度基本不变,选项错误;D、碳酸钙难溶于水,容器内温度基本不变,选项错误。故选A。
8.C
【解析】
A、被溶解的物质叫溶质。若食盐水不能完全溶解话,食盐质量+水的质量≠溶液的质量; 故本选项错误;
B、密度不同的两种物质混合后,总体积减少,因为微粒间存在间隔,所以,食盐体积+水的体积≠溶 液的体积,故本选项错误;
C、溶液是由溶质和溶剂组成的,所以溶质质量+水的质量=溶液的质量,故本选 项正确;
D、溶液中溶质和溶剂的质量可以相加,但密度不可以相加;故本选项错误。
9.C
【解析】
A、植物油不溶于水,不能和水形成均一、稳定的混合物,不能够形成溶液,错误; B、牛奶是不溶性的小液滴等分散到液体中形成的,不能和水形成均一、稳定的混合物,不能够形成溶液,错误;C、食盐易溶于水,能形成均一、稳定的混合物,属于溶液,正确;
D、生铁不溶于水,不能和水形成均一、稳定的混合物,不能够形成溶液,错误。故选C。
点睛:溶液的判定主要看其是否是均一、稳定的混合物。
10.D
【解析】
配制溶液时,如无特殊要求,一般采用水作为溶剂,水是最常用的溶剂,汽油、酒精、植物油都属于有机溶剂,故选D。
11.① 深.
【解析】
(1)由表中的数据可知,向三支试管中各加入 0.5g 硫酸铜粉末, 完全溶解后,溶液①的质量分数最大,颜色最深.
(2)由此实验可得出:溶质的质量分数越大,有色溶液的颜色越深. 故答为:(1)①;(2)深.
12.一定 ④
【解析】
由图示可知,有未溶解的蔗糖,该蔗糖溶液一定是饱和溶液;
①试管内加入适量水,能溶解蔗糖,故可行;
②烧杯内加入适量氢氧化钠固体,氢氧化钠溶于水放出大量的热,能溶解蔗糖,故可行;
③烧杯内加入适量生石灰,生石灰与水反应放出大量的热,能溶解蔗糖,故可行;
④烧杯内加入适量硝酸铵固体,硝酸铵溶于水吸热,会析出的蔗糖,故不可行。
13.继续加入少量的氯化钠 恒温蒸发水分.
【解析】
饱和溶液是在一定温度下、一定量的溶剂里不能再溶解某物质的溶液叫该物质的饱和溶液,反之为不饱和溶液。氯化钠的溶解度随温度的升高而增大,故要把其不饱和溶液转化为 饱和溶液,可采取的方法有:①继续加入少量的氯化钠;②恒温蒸发水分;③降 温。
14.加速固体的溶解氢氧化钠固体溶于水放热硝酸铵溶解吸热,使空气中的水蒸气凝结成小水珠氯化钠
【解析】
(1)振荡可以加速固体的溶解。
(2)氢氧化钠溶于水温度升高,故温度高于20℃的是氢氧化钠。
(3)硝酸铵溶于水温度降低,试管外部的温度降低,使空气中的水蒸气预冷液化为小水珠。
(4)氯化钠溶液水温度几乎不变。
15.试管底部有硝酸钾固体未溶解 小明的判断不正确,因为该溶液可能恰好为饱和溶液 向该溶液中加入少量的硝酸钾晶体,看其能否继续溶解
【解析】
饱和溶液是在一定温度下、一定量的溶剂里不能再溶解某物质的溶液叫该物质的饱和溶液,反之为不饱和溶液。
(1)图甲试管中的溶液为该温度下硝酸钾的饱和溶液,判断的依据是试管底部有硝酸钾固体未溶解,说明该条件下,溶液不能再溶解硝酸钾,
(2)对该试管进行加热,得到如图乙所示的溶液,小明认为该溶液为不饱和溶液,小明的判断不正确,因为该溶液可能恰好为饱和溶液,因为刚好饱和的溶液和不饱和溶液都是澄清溶液;
(3)判断该溶液是否饱和的做法是向该溶液中加入少量的硝酸钾晶体,看其能否继续溶解,溶解,原溶液是不饱和溶液;不溶,则是饱和溶液。
16.2 48 25 烧杯
【解析】
(1)实验室配制质量分数4%的氯化钠溶液50g,则需要固体氯化钠的质量为50g×4%=2g,需水为50g-2g=48g,即48mL,故填:2 48;
(2)设需要8%的氯化钠溶液的质量为x,8%x=50g×4%,x=25g
溶液配制过程中除用到量筒、玻璃棒和胶头滴管外,还需要烧杯盛放溶液,故填:25 烧杯。
同课章节目录
