第二节 碱及其性质 第2课时课件(18张PPT)
文档属性
| 名称 | 第二节 碱及其性质 第2课时课件(18张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 539.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-05 00:00:00 | ||
图片预览




文档简介
(共18张PPT)
鲁教2011课标版
化学 九年级下册
(1)认识氢氧化钠、氢氧化钙的化学性质、
用途。
(2)掌握碱的通性,理解碱具有相似化学性质的原因是溶液中都含有氢氧根离子。
【学习目标】
(3)进一步认识复分解反应,会书写常见复分解反应的化学方程式。
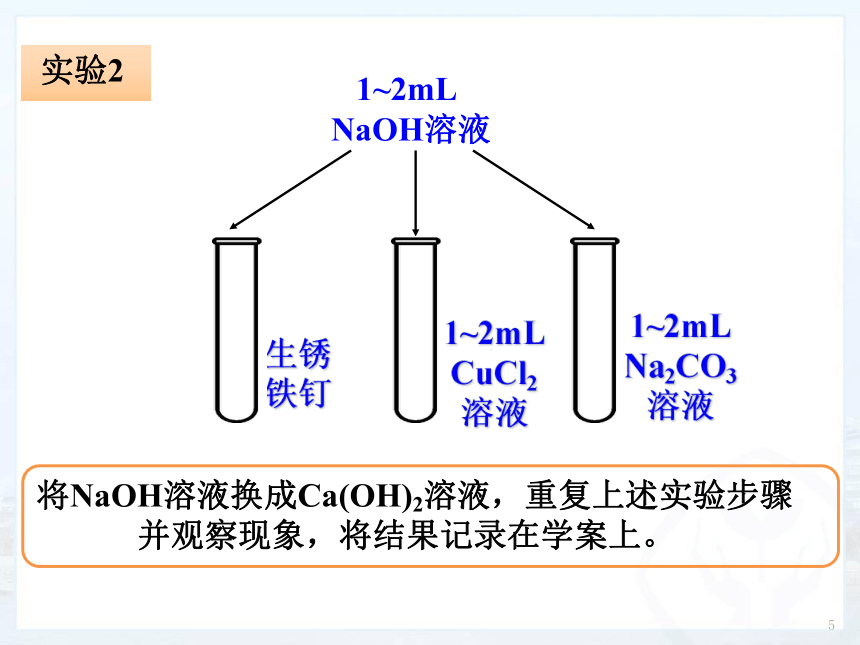
将NaOH溶液换成Ca(OH)2溶液,重复上述实验步骤并观察现象,将结果记录在学案上。
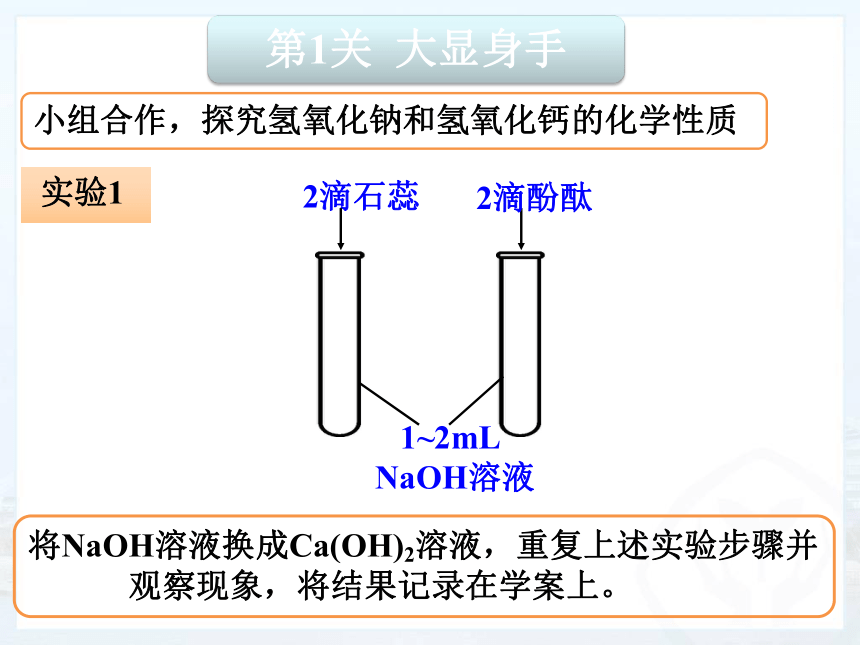
小组合作,探究氢氧化钠和氢氧化钙的化学性质
结论1
碱溶液都能使紫色石蕊试液变蓝,使无色酚酞试液变红。
*
生锈铁钉
1~2mLCuCl2溶液
1~2mLNa2CO3溶液
1~2mL
NaOH溶液
将NaOH溶液换成Ca(OH)2溶液,重复上述实验步骤并观察现象,将结果记录在学案上。
结论2
Cl
Na
Cu
2
(
)
2
碱能与某些盐反应
生成另一种盐和另一种碱。
OH
+
NaOH + CuCl2 Cu(OH)2↓+ NaCl
2
2
Ca(OH)2 + CuCl2 = Cu(OH)2↓ + CaCl2
Ca(OH)2 + Na2CO3 = CaCO3↓+ 2NaOH
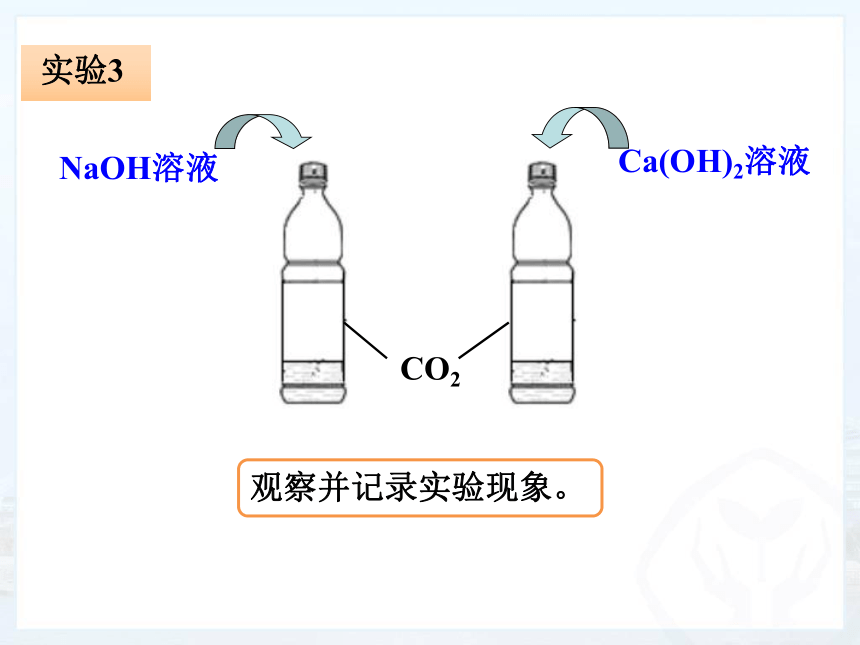
CO2
NaOH溶液
Ca(OH)2溶液
观察并记录实验现象。
你同意这种观点吗?
有的同学认为,“实验3中矿泉水瓶变瘪,不足以证明二氧化碳和氢氧化钠或氢氧化钙溶液发生了化学反应,因为二氧化碳溶解在水中也会产生类似的现象”。
加入氢氧化钠溶液没有沉淀产生,是氢氧化钠和二氧化碳反应使矿泉水瓶变瘪,还是二氧化碳溶于水,造成矿泉水瓶变瘪?
【作出猜想】
【设计实验】
氢氧化钠和二氧化碳反应使矿泉水瓶变瘪
往2个集满二氧化碳
的矿泉水瓶中加入
等体积的水和氢氧
化钠溶液
加入氢氧化钠
溶液的矿泉水
瓶瘪的程度更
大
氢氧化钠和
二氧化碳发
生了反应
【提出问题】
二氧化碳中加入氢氧化钙溶液产生了沉淀,
实验操作 现象 结论
我来设计
结论3
碱能与某些非金属氧化物反应
2NaOH+CO2=Na2CO3+H2O
Ca(OH)2+CO2=CaCO3↓+H2O
生成盐和水。
化学反应伴随着新物质的生成,能不能从验证
生成物的角度来证明氢氧化钠与二氧化碳发生了反应呢?
实验方案:取变瘪后瓶中的溶液加入稀盐酸,若
有气泡,说明生成了新物质,氢氧化钠与二氧化
碳发生了反应。
NaOH = Na+ + OH-
Ca(OH)2 = Ca2+ + 2OH-
碱具有相似化学性质的原因是:溶液中都含有OH-。
不同的碱性质存在差异的原因是:解离出的阳离子不同。
SO2
Na2CO3
CuSO4
Fe2O3
FeCl3
1、将下列卡片中能与NaOH反应的物质找出来,并写出相关的化学方程式。
(1)2NaOH + SO2 = Na2SO3 + H2O
(2)CuSO4 + 2NaOH = Cu(OH)2↓+ Na2SO4
(3)FeCl3 + 3NaOH = Fe(OH)3↓+ 3NaCl
K
K
K
K
K
K
K
NaOH
K
方法一:取少量3种无色溶液于3支试管中,滴加
2滴石蕊溶液,若变红,则是稀硫酸;若变蓝,
是氢氧化钙溶液;无明显现象的是蒸馏水。
方法二:取少量3种无色溶液于3支试管中,滴加
适量碳酸钠溶液,若产生气泡,则是稀硫酸;若
产生沉淀,是氢氧化钙溶液;无明显现象的是蒸
馏水。
解释以下事实
1、氢氧化钠固体可做某些气体的干燥剂,但不能用来干燥二氧化碳。
3、工业上用熟石灰制烧碱。
2、有人用石灰乳【主要成分是Ca(OH)2】刷墙,并在室内烧一个炭火盆,开始墙面变得潮湿,过几天墙壁就变得又硬又白了。
碱具有相似化学性质的原因
碱的通性
不同碱性质差异的原因
与某些盐
碱的化学性质
与某些非金属氧化物
与指示剂
微观解释
鲁教2011课标版
化学 九年级下册
(1)认识氢氧化钠、氢氧化钙的化学性质、
用途。
(2)掌握碱的通性,理解碱具有相似化学性质的原因是溶液中都含有氢氧根离子。
【学习目标】
(3)进一步认识复分解反应,会书写常见复分解反应的化学方程式。
将NaOH溶液换成Ca(OH)2溶液,重复上述实验步骤并观察现象,将结果记录在学案上。
小组合作,探究氢氧化钠和氢氧化钙的化学性质
结论1
碱溶液都能使紫色石蕊试液变蓝,使无色酚酞试液变红。
*
生锈铁钉
1~2mLCuCl2溶液
1~2mLNa2CO3溶液
1~2mL
NaOH溶液
将NaOH溶液换成Ca(OH)2溶液,重复上述实验步骤并观察现象,将结果记录在学案上。
结论2
Cl
Na
Cu
2
(
)
2
碱能与某些盐反应
生成另一种盐和另一种碱。
OH
+
NaOH + CuCl2 Cu(OH)2↓+ NaCl
2
2
Ca(OH)2 + CuCl2 = Cu(OH)2↓ + CaCl2
Ca(OH)2 + Na2CO3 = CaCO3↓+ 2NaOH
CO2
NaOH溶液
Ca(OH)2溶液
观察并记录实验现象。
你同意这种观点吗?
有的同学认为,“实验3中矿泉水瓶变瘪,不足以证明二氧化碳和氢氧化钠或氢氧化钙溶液发生了化学反应,因为二氧化碳溶解在水中也会产生类似的现象”。
加入氢氧化钠溶液没有沉淀产生,是氢氧化钠和二氧化碳反应使矿泉水瓶变瘪,还是二氧化碳溶于水,造成矿泉水瓶变瘪?
【作出猜想】
【设计实验】
氢氧化钠和二氧化碳反应使矿泉水瓶变瘪
往2个集满二氧化碳
的矿泉水瓶中加入
等体积的水和氢氧
化钠溶液
加入氢氧化钠
溶液的矿泉水
瓶瘪的程度更
大
氢氧化钠和
二氧化碳发
生了反应
【提出问题】
二氧化碳中加入氢氧化钙溶液产生了沉淀,
实验操作 现象 结论
我来设计
结论3
碱能与某些非金属氧化物反应
2NaOH+CO2=Na2CO3+H2O
Ca(OH)2+CO2=CaCO3↓+H2O
生成盐和水。
化学反应伴随着新物质的生成,能不能从验证
生成物的角度来证明氢氧化钠与二氧化碳发生了反应呢?
实验方案:取变瘪后瓶中的溶液加入稀盐酸,若
有气泡,说明生成了新物质,氢氧化钠与二氧化
碳发生了反应。
NaOH = Na+ + OH-
Ca(OH)2 = Ca2+ + 2OH-
碱具有相似化学性质的原因是:溶液中都含有OH-。
不同的碱性质存在差异的原因是:解离出的阳离子不同。
SO2
Na2CO3
CuSO4
Fe2O3
FeCl3
1、将下列卡片中能与NaOH反应的物质找出来,并写出相关的化学方程式。
(1)2NaOH + SO2 = Na2SO3 + H2O
(2)CuSO4 + 2NaOH = Cu(OH)2↓+ Na2SO4
(3)FeCl3 + 3NaOH = Fe(OH)3↓+ 3NaCl
K
K
K
K
K
K
K
NaOH
K
方法一:取少量3种无色溶液于3支试管中,滴加
2滴石蕊溶液,若变红,则是稀硫酸;若变蓝,
是氢氧化钙溶液;无明显现象的是蒸馏水。
方法二:取少量3种无色溶液于3支试管中,滴加
适量碳酸钠溶液,若产生气泡,则是稀硫酸;若
产生沉淀,是氢氧化钙溶液;无明显现象的是蒸
馏水。
解释以下事实
1、氢氧化钠固体可做某些气体的干燥剂,但不能用来干燥二氧化碳。
3、工业上用熟石灰制烧碱。
2、有人用石灰乳【主要成分是Ca(OH)2】刷墙,并在室内烧一个炭火盆,开始墙面变得潮湿,过几天墙壁就变得又硬又白了。
碱具有相似化学性质的原因
碱的通性
不同碱性质差异的原因
与某些盐
碱的化学性质
与某些非金属氧化物
与指示剂
微观解释
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
