第二节 元素 课件(26张PPT)
文档属性
| 名称 | 第二节 元素 课件(26张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 5.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-07 00:00:00 | ||
图片预览







文档简介
(共26张PPT)
元
要素
素
基本
音乐元素
do,re,mi,fa,so,la,si
英语元素
a b c d e f g h i j k l m n o p q r s t u v w x y z
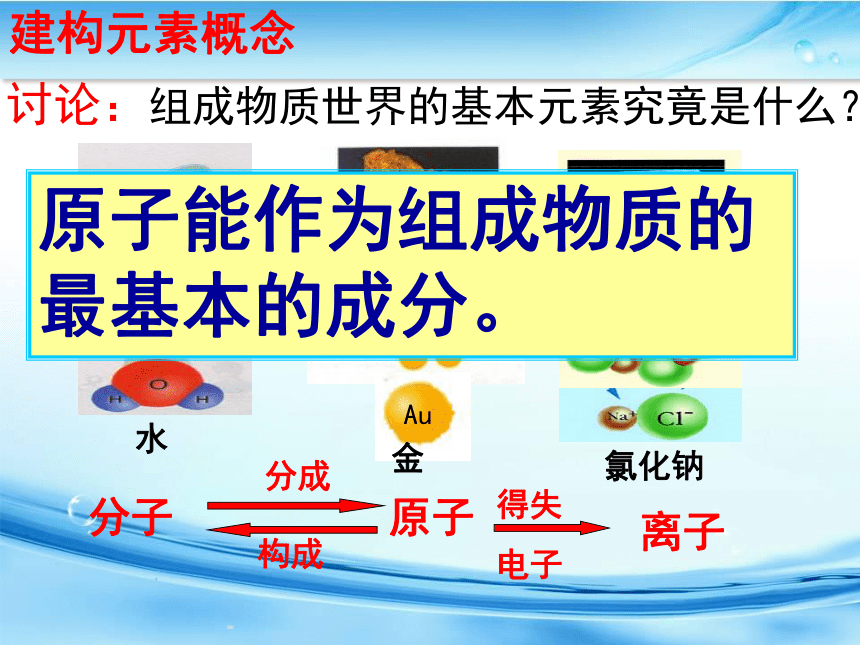
分子
原子
建构元素概念
讨论:组成物质世界的基本元素究竟是什么?
原子能作为组成物质的最基本的成分。
建构元素概念
动一动:
拆分微粒的模型,对原子进行归类,
说出同一类原子来自于哪种分子或物质。
结论:元素是一类原子的总称
元素是宏观概念,
只讲种类,不讲个数。
同种元素的原子在结构上有什么相同点?
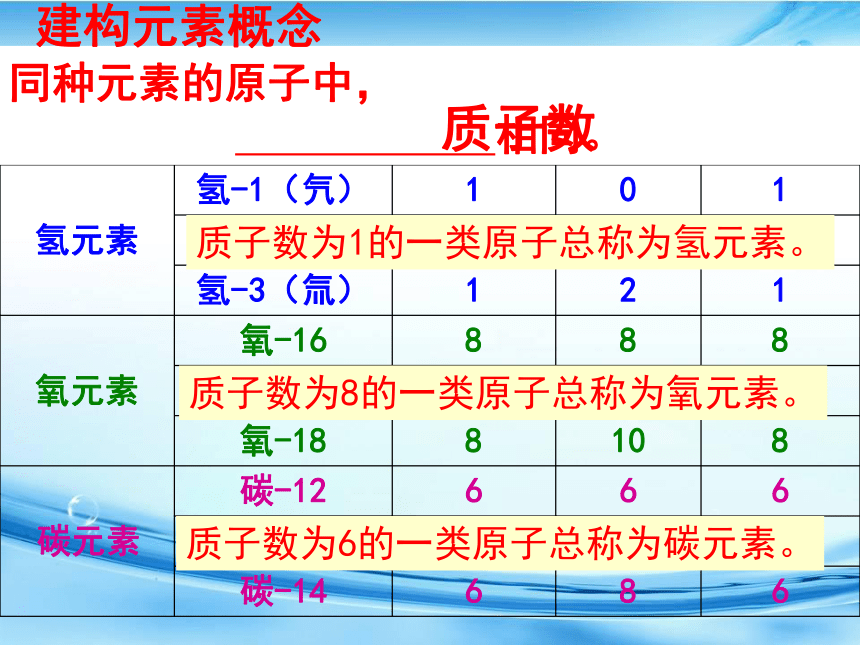
建构元素概念
质子数为1的一类原子总称为氢元素。
质子数为8的一类原子总称为氧元素。
质子数为6的一类原子总称为碳元素。
同种元素的原子中,
相同。
质子数
元素种类 原子名称 质子数 中子数 电子数
氢元素 氢-1(氕) 1 0 1
氢-2(氘) 1 1 1
氢-3(氚) 1 2 1
氧元素 氧-16 8 8 8
氧-17 8 9 8
氧-18 8 10 8
碳元素 碳-12 6 6 6
碳-13 6 7 6
碳-14 6 8 6
建构元素概念
元素是一类原子总称,
元素的概念:
具有相同质子数的一类原子的总称
原子中的质子数决定了元素种类。
元素组成物质。
元素是宏观概念,
只讲种类,不讲个数。
元素是具有相同质子数
的一类原子的总称。
原子是化学变化中的
的最小粒子。
原子是微观概念,
既讲种类,又讲个数。
原子构成物质或分子。
元素 原子
联系
区别
深化元素概念——元素分类
请查看课本61页的表格
思考:
1、不同元素的本质区别是什么?
2、这些元素可以分成哪几类?观察每一类元素的名称书写有什么特点?
3、同一类元素的原子结构有什么共同特点?
不同元素,原子的质子数不同
深化元素概念——元素分类
钾
钙
2、这些元素可以分成哪几类?
观察每一类元素的名称书写有什么特点?
金属元素
深化元素概念——元素分类
原子的最外层电子数一般小于4
非金属元素
稀有气体
元素
原子的最外层电子数一般大于或等于4
一般“钅”
字旁
一般“石”
“气”字旁
“气”
原子的最外层电子数一般8(氦为2)
钠镁铝钙
碳硅氧氯
氦氖氩
同一类元素的原子结构有什么共同特点?
分类法研究化学,可以化繁为简。
元素分类
实例 元素名称
书写特点
分类依据
铜
氧化镁
二氧化碳
氢气
水
氧气
认识元素——元素组成物质
氯化钠
思考:你能否对这些纯净物进行分类?说出分类依据。
组成纯净物的元素种类
是否相同
都是纯净物
认识元素——元素组成物质
单质
纯净物
化合物
一种元素组成的纯净物
两种或两种以上元素组成的
纯净物
分类法研究化学,
可化繁为简。
单质 化合物
联系
区别
认识元素——元素组成物质
动一动:
将原子模型进行组合,你能组合出哪些物质的微观粒子?
目前已发现的物质有数千万种,但组成这些物质的元素只有一百多种,为什么呢?
元素的有限性
物质的多样性
原子以不同的数量、不同种类、按照不同方式结合,构成了多种多样的物质。
再认识元素——元素的分布
龙口北皂煤矿
——中国唯一的海底煤矿已关停
主要成分碳酸钙
地壳中的元素分布(按质量分数计算)
再认识元素——元素的分布
再认识元素——元素的分布
生活处处有元素
元素
再认识元素——元素的分布
元素的表示——元素符号
1---20号元素的名称及符号
氢 氦 锂 铍 硼
碳 氮 氧 氟 氖
钠 镁 铝 硅 磷
硫 氯 氩 钾 钙
H He Li Be B
C N O F Ne
Na Mg Al Si P
S Cl Ar K Ca
元素的表示——元素符号
元素符号的意义
O
一个氧原子
元素符号意义
表示一种元素
表示该元素的一个原子
氧元素
宏观意义
微观意义
说出下列符号的表示意义:
H 、 Mg、2H、5C
注意:
元素符号前有系数时:
只有微观含义
元素的表示——元素符号
物质
元素
原子总称
元素符号
宏观微观
相联系
符号魅力
纯净物
分类思想
单质、化合物
元素分类
金属、非金属、
稀有气体
学有所获
七个简单的音符谱写出了脍炙人口的音乐,一百多种元素组成了丰富多彩的物质世界。用知识和智慧去探索,我们会更好地改造和创造这个物质世界,使我们的生活更加美好!
寄语:
元
要素
素
基本
音乐元素
do,re,mi,fa,so,la,si
英语元素
a b c d e f g h i j k l m n o p q r s t u v w x y z
分子
原子
建构元素概念
讨论:组成物质世界的基本元素究竟是什么?
原子能作为组成物质的最基本的成分。
建构元素概念
动一动:
拆分微粒的模型,对原子进行归类,
说出同一类原子来自于哪种分子或物质。
结论:元素是一类原子的总称
元素是宏观概念,
只讲种类,不讲个数。
同种元素的原子在结构上有什么相同点?
建构元素概念
质子数为1的一类原子总称为氢元素。
质子数为8的一类原子总称为氧元素。
质子数为6的一类原子总称为碳元素。
同种元素的原子中,
相同。
质子数
元素种类 原子名称 质子数 中子数 电子数
氢元素 氢-1(氕) 1 0 1
氢-2(氘) 1 1 1
氢-3(氚) 1 2 1
氧元素 氧-16 8 8 8
氧-17 8 9 8
氧-18 8 10 8
碳元素 碳-12 6 6 6
碳-13 6 7 6
碳-14 6 8 6
建构元素概念
元素是一类原子总称,
元素的概念:
具有相同质子数的一类原子的总称
原子中的质子数决定了元素种类。
元素组成物质。
元素是宏观概念,
只讲种类,不讲个数。
元素是具有相同质子数
的一类原子的总称。
原子是化学变化中的
的最小粒子。
原子是微观概念,
既讲种类,又讲个数。
原子构成物质或分子。
元素 原子
联系
区别
深化元素概念——元素分类
请查看课本61页的表格
思考:
1、不同元素的本质区别是什么?
2、这些元素可以分成哪几类?观察每一类元素的名称书写有什么特点?
3、同一类元素的原子结构有什么共同特点?
不同元素,原子的质子数不同
深化元素概念——元素分类
钾
钙
2、这些元素可以分成哪几类?
观察每一类元素的名称书写有什么特点?
金属元素
深化元素概念——元素分类
原子的最外层电子数一般小于4
非金属元素
稀有气体
元素
原子的最外层电子数一般大于或等于4
一般“钅”
字旁
一般“石”
“气”字旁
“气”
原子的最外层电子数一般8(氦为2)
钠镁铝钙
碳硅氧氯
氦氖氩
同一类元素的原子结构有什么共同特点?
分类法研究化学,可以化繁为简。
元素分类
实例 元素名称
书写特点
分类依据
铜
氧化镁
二氧化碳
氢气
水
氧气
认识元素——元素组成物质
氯化钠
思考:你能否对这些纯净物进行分类?说出分类依据。
组成纯净物的元素种类
是否相同
都是纯净物
认识元素——元素组成物质
单质
纯净物
化合物
一种元素组成的纯净物
两种或两种以上元素组成的
纯净物
分类法研究化学,
可化繁为简。
单质 化合物
联系
区别
认识元素——元素组成物质
动一动:
将原子模型进行组合,你能组合出哪些物质的微观粒子?
目前已发现的物质有数千万种,但组成这些物质的元素只有一百多种,为什么呢?
元素的有限性
物质的多样性
原子以不同的数量、不同种类、按照不同方式结合,构成了多种多样的物质。
再认识元素——元素的分布
龙口北皂煤矿
——中国唯一的海底煤矿已关停
主要成分碳酸钙
地壳中的元素分布(按质量分数计算)
再认识元素——元素的分布
再认识元素——元素的分布
生活处处有元素
元素
再认识元素——元素的分布
元素的表示——元素符号
1---20号元素的名称及符号
氢 氦 锂 铍 硼
碳 氮 氧 氟 氖
钠 镁 铝 硅 磷
硫 氯 氩 钾 钙
H He Li Be B
C N O F Ne
Na Mg Al Si P
S Cl Ar K Ca
元素的表示——元素符号
元素符号的意义
O
一个氧原子
元素符号意义
表示一种元素
表示该元素的一个原子
氧元素
宏观意义
微观意义
说出下列符号的表示意义:
H 、 Mg、2H、5C
注意:
元素符号前有系数时:
只有微观含义
元素的表示——元素符号
物质
元素
原子总称
元素符号
宏观微观
相联系
符号魅力
纯净物
分类思想
单质、化合物
元素分类
金属、非金属、
稀有气体
学有所获
七个简单的音符谱写出了脍炙人口的音乐,一百多种元素组成了丰富多彩的物质世界。用知识和智慧去探索,我们会更好地改造和创造这个物质世界,使我们的生活更加美好!
寄语:
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
