第三节 物质组成的表示——化学式的书写、意义、计算 课件(18张PPT)
文档属性
| 名称 | 第三节 物质组成的表示——化学式的书写、意义、计算 课件(18张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 778.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-07 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
原
到
延迟符
化
学
式
子
从
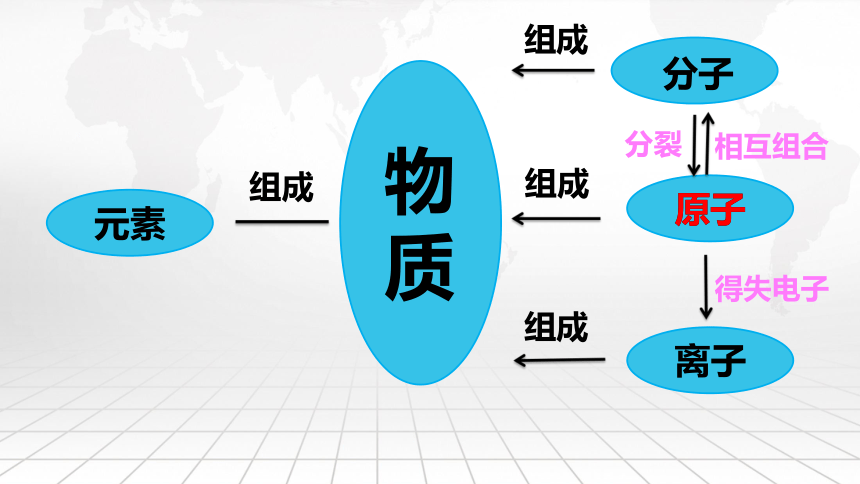
物
质
元素
组成
分子
原子
离子
组成
组成
组成
分裂
相互组合
得失电子
原子
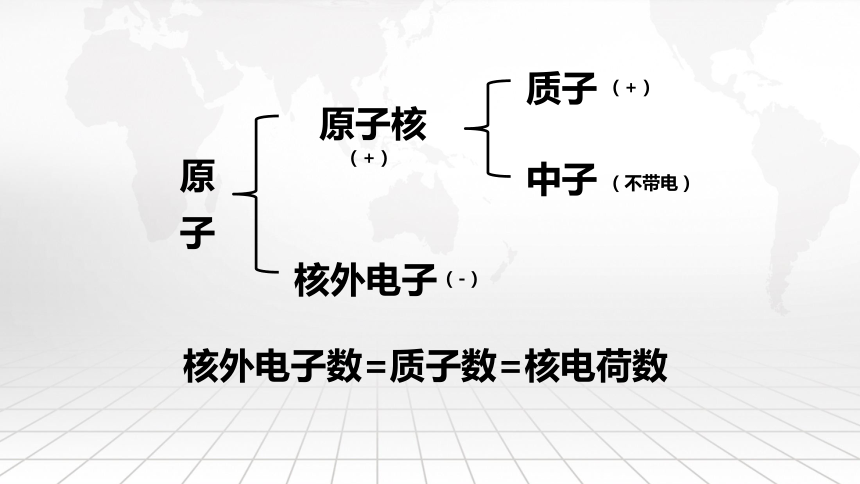
原 子
原子核
核外电子
质子
中子
(+)
(+)
(不带电)
(-)
核外电子数=质子数=核电荷数
原子核外的电子是分层排布的:
1.每层最多容纳的电子数是2n2;
2.排满第一层,再排第二层;排满第二层,再排第三层;
3.最外层不超过8个电子(若只有一层电子,则不超过2个)。
元素又是什么呢?
和原子是什么关系呢?
元素的化学性质又和什么相关呢?
元素的化学性质与其原子的最外层电子数密切相关:
稀有气体元素:最外层电子数=8(He为2),
稳定结构;
金 属 元 素:最外层电子数<4,
易失去电子达到稳定结构;
非 金 属 元素:最外层电子数>4,
易得到电子达到稳定结构。
而原子得失电子之后就变成了离子(即带电的原子或原子团)。
离子
阳离子:带正电(原子失去电子所得)
阴离子:带负电(原子得到电子所得)
Na
Na1+
失去1e-
Cl
得到1e-
Cl1-
Na+
Cl-
离子
OH-
NO3-
SO42-
CO32-
NH4+
在元素符号的右上角标出
离子所带的电荷数及电性。
Na
Na+
失去1e-
Cl
得到1e-
Cl-
1e-
得失电子数相等,得Na+:Cl-=1:1
(静电)NaCl
所以氯化钠的化学式为:NaCl
Cl
得到1e-
Cl-
(静电)MgCl2
所以氯化镁的化学式为:MgCl2
得失电子数相等,得Mg:Cl=1:2
2e-
需要2个Cl原子来捕获
Mg
Mg2+
失去2e-
通过原子得失电子数可以写出物质的化学式。
而原子形成离子时,所带电荷数就是它们与不同种元素相互化合时所显示的化合价(标在元素符号的正上方)。单质,化合价均为0.
则形成化合物时,Na;
+1
如:Na
失去1e-
Na+,
Mg
失去2e-
Mg2+,
则形成化合物时,Mg.
+2
我们也可以通过化合价书写物质的化学式。
+1
Na
-1
Cl
1
1
NaCl
+2
Mg
-1
Cl
1
2
MgCl2
+5
P
-2
O
2
5
P2O5
+1
Na
-1
OH
1
1
+2
Ca
-1
OH
( )
1
2
+3
Al
-2
SO4
( )
2
3
NaOH
Ca(OH)2
Al2(SO4)3
依据化合价书写化学式口诀:
正在前,负在后,
化合价标上头,
先约简,后交叉,
代数和等于零。
化学式:用元素符号和数字组合表示纯净物组成的式子。
书
写
方
法
通过原子得失电子数可以写出物质的化学式。
书写原则:得失电子数相等
我们也可以通过化合价书写物质的化学式。
书写原则:化合价代数和为零
同学们,通过这节课你们有何收获啊?
畅谈收获
从原子到化学式,
你明白了吗?
原
到
延迟符
化
学
式
子
从
物
质
元素
组成
分子
原子
离子
组成
组成
组成
分裂
相互组合
得失电子
原子
原 子
原子核
核外电子
质子
中子
(+)
(+)
(不带电)
(-)
核外电子数=质子数=核电荷数
原子核外的电子是分层排布的:
1.每层最多容纳的电子数是2n2;
2.排满第一层,再排第二层;排满第二层,再排第三层;
3.最外层不超过8个电子(若只有一层电子,则不超过2个)。
元素又是什么呢?
和原子是什么关系呢?
元素的化学性质又和什么相关呢?
元素的化学性质与其原子的最外层电子数密切相关:
稀有气体元素:最外层电子数=8(He为2),
稳定结构;
金 属 元 素:最外层电子数<4,
易失去电子达到稳定结构;
非 金 属 元素:最外层电子数>4,
易得到电子达到稳定结构。
而原子得失电子之后就变成了离子(即带电的原子或原子团)。
离子
阳离子:带正电(原子失去电子所得)
阴离子:带负电(原子得到电子所得)
Na
Na1+
失去1e-
Cl
得到1e-
Cl1-
Na+
Cl-
离子
OH-
NO3-
SO42-
CO32-
NH4+
在元素符号的右上角标出
离子所带的电荷数及电性。
Na
Na+
失去1e-
Cl
得到1e-
Cl-
1e-
得失电子数相等,得Na+:Cl-=1:1
(静电)NaCl
所以氯化钠的化学式为:NaCl
Cl
得到1e-
Cl-
(静电)MgCl2
所以氯化镁的化学式为:MgCl2
得失电子数相等,得Mg:Cl=1:2
2e-
需要2个Cl原子来捕获
Mg
Mg2+
失去2e-
通过原子得失电子数可以写出物质的化学式。
而原子形成离子时,所带电荷数就是它们与不同种元素相互化合时所显示的化合价(标在元素符号的正上方)。单质,化合价均为0.
则形成化合物时,Na;
+1
如:Na
失去1e-
Na+,
Mg
失去2e-
Mg2+,
则形成化合物时,Mg.
+2
我们也可以通过化合价书写物质的化学式。
+1
Na
-1
Cl
1
1
NaCl
+2
Mg
-1
Cl
1
2
MgCl2
+5
P
-2
O
2
5
P2O5
+1
Na
-1
OH
1
1
+2
Ca
-1
OH
( )
1
2
+3
Al
-2
SO4
( )
2
3
NaOH
Ca(OH)2
Al2(SO4)3
依据化合价书写化学式口诀:
正在前,负在后,
化合价标上头,
先约简,后交叉,
代数和等于零。
化学式:用元素符号和数字组合表示纯净物组成的式子。
书
写
方
法
通过原子得失电子数可以写出物质的化学式。
书写原则:得失电子数相等
我们也可以通过化合价书写物质的化学式。
书写原则:化合价代数和为零
同学们,通过这节课你们有何收获啊?
畅谈收获
从原子到化学式,
你明白了吗?
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
