人教版九年级化学第十单元 酸和碱课题1常见的酸和碱第4课时常见的碱同步导学精练
文档属性
| 名称 | 人教版九年级化学第十单元 酸和碱课题1常见的酸和碱第4课时常见的碱同步导学精练 |

|
|
| 格式 | zip | ||
| 文件大小 | 450.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-08 00:00:00 | ||
图片预览


文档简介
第十单元 酸和碱
课题1 常见的酸和碱
第4课时 几种常见的碱
【学习目标】
1.知道NaOH和Ca(OH)2的主要性质和用途;
2.认识NaOH和Ca(OH)2的腐蚀性及使用时的安全注意事项;
3.理解潮解的概念,知道NaOH、Ca(OH)2等物质的保存方法。
【名师导学】
1.氢氧化钠:
(1)氢氧化钠有____性,所以,它的俗名叫做____、_____或_____。如果不慎将碱液沾到皮肤上,要先__________,后__________________。
(2)氢氧化钠为___色固体,将氢氧化钠放在表面皿上放置一会儿产生的现象为___________,这种现象叫做_____,产生这种现象的原因为__________________________。将NaOH放入盛有少量水的试管里,并用手触摸试管外壁,产生的现象为________,该实验说明NaOH_______________________________。
(3)氢氧化钠广泛应用于__________、___________、__________、_________和_________等工业,在生活中可用于____________。
2.氢氧化钙:氢氧化钙是____色_____状固体,俗称_______或_________,它可由________与水反应得到,反应中_______(填“放出”或“吸收”)热量,反应方程式为____________________________________。
3.其它常见的碱:氨水___________(写化学式,下同)、氢氧化钾___________、氢氧化钡____________。
4.碱的化学性质
(1)碱溶液+酚酞溶液→变______色, 碱溶液+紫色石蕊溶液→变_______色;
如: 氨水+酚酞→变________色 KOH溶液+紫色石蕊溶液→________色
(2)非金属氧化物+碱溶液→_________ 如:
Ca(OH)2+CO2=________________ 2NaOH+CO2=_____________________
SO3+2NaOH=_________________ Ba(OH)2+CO2=____________________
【课时作业】
1. 下列关于氢氧化钠的叙述不正确的是( )
A.固体氢氧化钠要密封保存
B.氢氧化钠的俗名叫做苛性钠、火碱或烧碱
C.固体氢氧化钠可作CO2和SO2等气体的干燥剂
D.氢氧化钠溶液对皮肤、纸张、织物有强腐蚀性
2.下列关于氢氧化钙的叙述中,不正确的是 (???)
A.氢氧化钙溶液敞放在空气中会变质?????
B.氢氧化钙的溶解度随温度的升高而升高
C.氢氧化钙在农业上可改良酸性土壤
D.氢氧化钙的俗名叫做熟石灰、消石灰
3.下列有关氢氧化钠性质的说法错误的是( )
A.氢氧化钠有腐蚀性 B.固体氢氧化钠有挥发性
C.氢氧化钠能吸收二氧化碳而变质 D.固体氢氧化钠能吸收水蒸气而潮解
4.生活中的许多变化都能产生热量,下列放热现象主要由物理变化引起的是()
A生石灰与水作用放出大量的热 B.氢氧化钠与盐酸混合放出大量的热
C.白炽灯泡通电后发热 D.铝与盐酸作用放出大量的热
5.下列方法很难区别氢氧化钠溶液和饱和澄清石灰水的是( )
A.加热溶液 B.通入CO2气体 C.滴入紫色石蕊溶液 D.加入少量CaO
6.下列现象的产生,与空气成分无关的是( )
A.烧碱露置空气中变重 B.浓盐酸露至空气中变轻
C.酥脆饼干置于空气中变软 D.菜刀置于潮湿空气中生锈
7.右图橡皮塞上装有试管和U形管,若观察到U形管中a处的液面下降,则试管中加入的物质是( )
①CaO固体 ②NaOH固体 ③浓H2SO4 ④NH4NO3固体
A.①②③ B.②③④ C.①②④ D.全部
8.下列对实验意外事故的处理错误的是( )
A.若不慎将燃着的酒精灯碰倒,洒出的酒精在桌上燃烧,应立刻用湿抹布扑盖
B.若不慎将烧碱溶液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液
C.若不慎将腐蚀性药液溅入眼睛,要先用手揉眼睛,再立即用水冲洗
D.若不慎将浓硫酸沾到皮肤或衣服上,应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液
9.从H、O、N、Ca、Na、Cu六种元素中,选择适当的元素组成符合下列要求的物质,并用化学符号表示:
(1)在空气中易潮解的碱_______;(2)溶解度随温度升高而减小的碱_________;
(3)只由非金属元素组成的碱____________;4)不溶性碱_________;
(5)碱有相似化学性质的原因是溶液中含有______。
10.小黎同学为了进一步加深对“碱的化学性质”的理解,特邀你协助完成下列活动与探究:?(1) 如右图所示,在白色点滴板上进行实验,请将实验现象填入下表:
氢氧化钠溶液 氢氧化钙溶液
加紫色石蕊溶液 __________ __________
(2)回忆检验二氧化碳气体的反应,写出该反应的化学方程____________________________________。
(3)三氧化硫(SO3)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式____________________________________。?
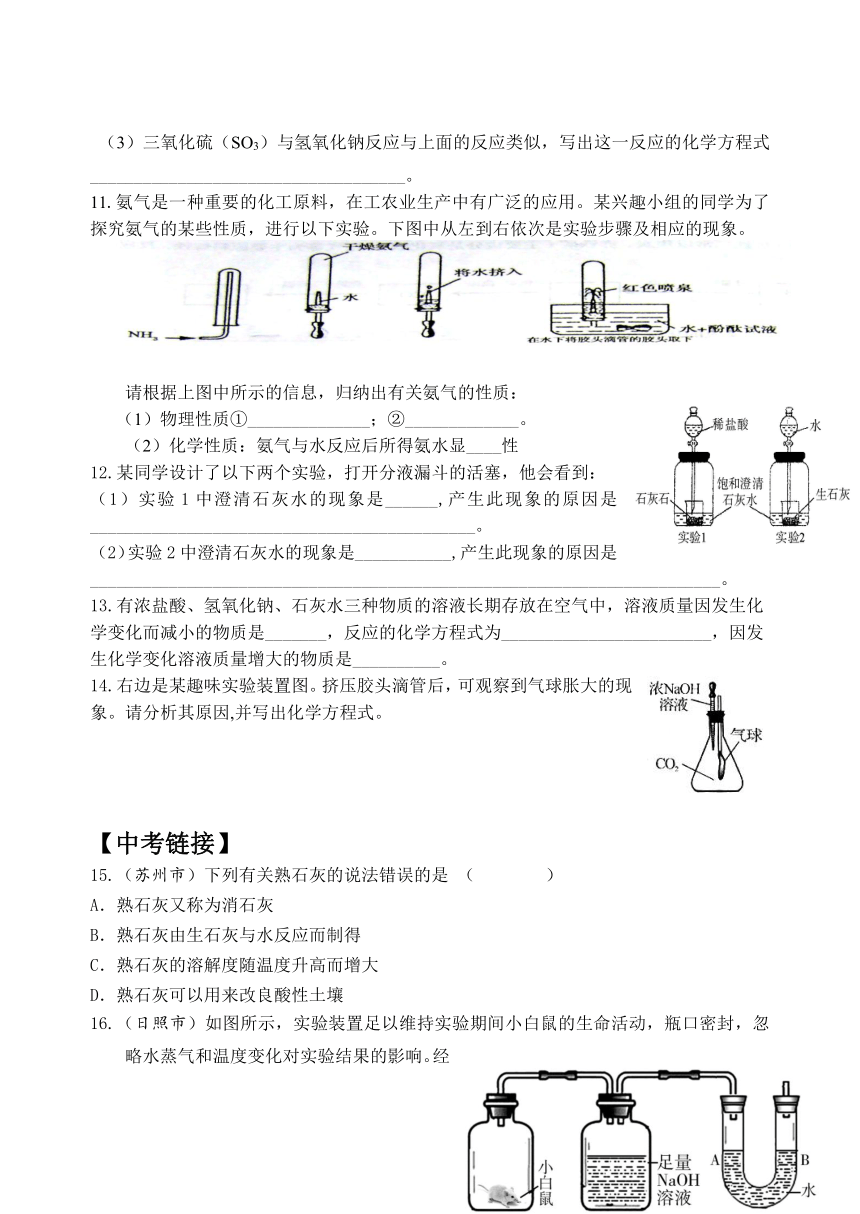
11.氨气是一种重要的化工原料,在工农业生产中有广泛的应用。某兴趣小组的同学为了探究氨气的某些性质,进行以下实验。下图中从左到右依次是实验步骤及相应的现象。
请根据上图中所示的信息,归纳出有关氨气的性质:
(1)物理性质①______________;②_____________。
(2)化学性质:氨气与水反应后所得氨水显____性
12.某同学设计了以下两个实验,打开分液漏斗的活塞,他会看到:
(1)实验1中澄清石灰水的现象是______,产生此现象的原因是____________________________________________。
(2)实验2中澄清石灰水的现象是___________,产生此现象的原因是________________________________________________________________________。
13.有浓盐酸、氢氧化钠、石灰水三种物质的溶液长期存放在空气中,溶液质量因发生化学变化而减小的物质是_______,反应的化学方程式为________________________,因发生化学变化溶液质量增大的物质是__________。
14.右边是某趣味实验装置图。挤压胶头滴管后,可观察到气球胀大的现象。请分析其原因,并写出化学方程式。
【中考链接】
15.(苏州市)下列有关熟石灰的说法错误的是 ( )
A.熟石灰又称为消石灰
B.熟石灰由生石灰与水反应而制得
C.熟石灰的溶解度随温度升高而增大
D.熟石灰可以用来改良酸性土壤
16.(日照市)如图所示,实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响。经数小时实验后,U形管A、B两处的液面会出现下列哪种情况 ( )
A.A处下降,B处上升
B.A、B两处都下降
C.A处上升,B处下降
D.A、B两处都不变
17.(内江市)将稀硫酸滴入一定量的氧化铜粉末中,使固体刚好溶解后滴入适量的氢氧化钠溶液至反应完全.请依次写出相关的化学反应方程式:
18.(宿迁市)化学课堂上要学习碱的化学性质,老师让两位同学和他共同做实验,要求两位同学分别向澄清石灰水和氢氧化钠溶液中吹气,如图①②所示,老师告诉同学们,呼出的气体中只有二氧化碳有可能与澄清石灰水和氢氧化钠溶液反应.
同学们在吹气后观察到①中澄清石灰水边浑浊,②中氢氧化钠溶液无明显现象.观察实验现象后老师问,通过实验现象的观察,检验二氧化碳气体应该使用_________________,针对②中的情况,师生共同开始探究之旅.
【提出问题】二氧化碳通入氢氧化钠溶液中无明显现象,两者是否发生了化学反应?
【猜想假设】猜想A:两者发生了化学反应;猜想B:两者没有发生化学反应.
【实验探究】
(1)小明设计了如图所示的③、④两个实验.
实验现象:③中的软塑料瓶变瘪,④中 ________________________________.
(2)小亮认为小明的实验是可行的,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低,小光同学却对此提出了质疑,他认为小明的实验不严谨,若仍利用该装置,需要补做的对比实验是_________________________________________.
(3)小光设计的是通过检验生成物来验证猜想,请帮他填写实验报告:
实验步骤 实验现象 实验结论
取③实验后的溶液少许,再向其加入 ________________________________ _________________________________________ 验证了二氧化碳和氢氧化钠溶液反应
【实验结论】二氧化碳和氢氧化钠溶液发生了化学反应.
【反思拓展】探究结束老师说,通过此探究实验我们发现,对于没有明显现象的化学反应,可以从不同的角度证明反应的发生,这些角度可以是:
①通过检验反应物减少证明反应发生;②通过________________证明反应的发生.
19.(昆明市)为测定某CuSO4溶液的溶质质量分数,化学小组的同学取CuSO4溶液100g,向其中滴加一定浓度的NaOH溶液,至不再产生沉淀为止,共用去NaOH溶液80g,过滤,得到滤液175.1g.请计算:
(1)该反应生成沉淀 4.9 g;
(2)该CuSO4溶液中溶质的质量分数.
参考答案
【名师导学】
1.氢氧化钠:
(1)氢氧化钠有_腐蚀__性,所以,它的俗名叫做_火碱__、_烧碱 _或_ 苛性钠_。如果不慎将碱液沾到皮肤上,要先__用水冲洗___,后___涂上硼酸溶液_________。
(2)氢氧化钠为__白_色固体,将氢氧化钠放在表面皿上放置一会儿产生的现象为___表面变潮湿___,这种现象叫做_潮解___,产生这种现象的原因为__NaOH吸收空气中水蒸气_____。将NaOH放入盛有少量水的试管里,并用手触摸试管外壁,产生的现象为试管烫热__,该实验说明NaOH__溶于水时放出热量________________。
(3)氢氧化钠广泛应用于__肥皂___、__石油____、__造纸___、__纺织___和__印染___等工业,在生活中可用于__去除油污______。
2.氢氧化钙:氢氧化钙是__白__色___ 粉___状固体,俗称_消石灰__或_熟石灰____,它可由__CaO___与水反应得到,反应中_放出______(填“放出”或“吸收”)热量,反应方程式为__CaO+H2O=Ca(OH)2 ______________。
3.其它常见的碱:氨水 NH3·H2O (写化学式,下同)、氢氧化钾 KOH 、氢氧化钡 Ba(OH)2 。
4.碱的化学性质
(1)碱溶液+酚酞溶液→变__红___色, 碱溶液+紫色石蕊溶液→变_蓝____色;
如: 氨水+酚酞→变__红____色 KOH溶液+紫色石蕊溶液→_蓝_____色
(2)非金属氧化物+碱溶液→_盐+水______ 如:
Ca(OH)2+CO2=CaCO3↓+H2O 2NaOH+CO2=Na2CO3+H2O
SO3+2NaOH=Na2SO4+H2O Ba(OH)2+CO2=BaCO3↓+H2O
【课时作业】
1.C 2.B??3.B 4.C 5.C 6.B 7.A 8.C
9.(1)NaOH(2)Ca(OH)2 (3)NH3·H2O;(4)Cu(OH)2 ;(5)OH-
10. (1)变蓝色 变蓝色
(2)Ca(OH)2+CO2=CaCO3↓+H2O
(3)SO3+2NaOH=Na2SO4+H2O?
11. (1)①密度比空气小 ②易溶于水
(2)碱
12.(1)变浑浊 生成的CO2与Ca(OH)2反应生成的CaCO3不溶于水
(2)变浑浊 CaO与H2O反应放出热量 Ca(OH)2的溶解度随温度的升高而减小,有Ca(OH)2析出 。
13.石灰水 CO2+Ca(OH)2=CaCO3↓+H2O 氢氧化钠
14.CO2被浓NaOH溶液吸收,锥形瓶内的气压成小,外界大气压大于锥形瓶内的气压,使气球胀大。 2NaOH+CO2=Na2CO3+H2O
【中考链接】
15.C 16.C
17.(1)CuO+H2SO4═CuSO4+H2O
(2)CuSO4+2NaOH═Cu(OH)2↓+Na2SO4
18. 澄清的石灰水
(1)气球变大(合理说法均可)
(2)将氢氧化钠溶液换成等体积的水,与加入氢氧化钠溶液的实验现象进行对比
(3)
实验步骤 实验现象 实验结论
取③实验后的溶液少许,再向其加入 稀盐酸(或氯化钙溶液等) 有气泡产生(或有白色沉淀生成等) 验证了二氧化碳和氢氧化钠溶液反应
② 检验生成物
19.(1)4.9g (2)8%
课题1 常见的酸和碱
第4课时 几种常见的碱
【学习目标】
1.知道NaOH和Ca(OH)2的主要性质和用途;
2.认识NaOH和Ca(OH)2的腐蚀性及使用时的安全注意事项;
3.理解潮解的概念,知道NaOH、Ca(OH)2等物质的保存方法。
【名师导学】
1.氢氧化钠:
(1)氢氧化钠有____性,所以,它的俗名叫做____、_____或_____。如果不慎将碱液沾到皮肤上,要先__________,后__________________。
(2)氢氧化钠为___色固体,将氢氧化钠放在表面皿上放置一会儿产生的现象为___________,这种现象叫做_____,产生这种现象的原因为__________________________。将NaOH放入盛有少量水的试管里,并用手触摸试管外壁,产生的现象为________,该实验说明NaOH_______________________________。
(3)氢氧化钠广泛应用于__________、___________、__________、_________和_________等工业,在生活中可用于____________。
2.氢氧化钙:氢氧化钙是____色_____状固体,俗称_______或_________,它可由________与水反应得到,反应中_______(填“放出”或“吸收”)热量,反应方程式为____________________________________。
3.其它常见的碱:氨水___________(写化学式,下同)、氢氧化钾___________、氢氧化钡____________。
4.碱的化学性质
(1)碱溶液+酚酞溶液→变______色, 碱溶液+紫色石蕊溶液→变_______色;
如: 氨水+酚酞→变________色 KOH溶液+紫色石蕊溶液→________色
(2)非金属氧化物+碱溶液→_________ 如:
Ca(OH)2+CO2=________________ 2NaOH+CO2=_____________________
SO3+2NaOH=_________________ Ba(OH)2+CO2=____________________
【课时作业】
1. 下列关于氢氧化钠的叙述不正确的是( )
A.固体氢氧化钠要密封保存
B.氢氧化钠的俗名叫做苛性钠、火碱或烧碱
C.固体氢氧化钠可作CO2和SO2等气体的干燥剂
D.氢氧化钠溶液对皮肤、纸张、织物有强腐蚀性
2.下列关于氢氧化钙的叙述中,不正确的是 (???)
A.氢氧化钙溶液敞放在空气中会变质?????
B.氢氧化钙的溶解度随温度的升高而升高
C.氢氧化钙在农业上可改良酸性土壤
D.氢氧化钙的俗名叫做熟石灰、消石灰
3.下列有关氢氧化钠性质的说法错误的是( )
A.氢氧化钠有腐蚀性 B.固体氢氧化钠有挥发性
C.氢氧化钠能吸收二氧化碳而变质 D.固体氢氧化钠能吸收水蒸气而潮解
4.生活中的许多变化都能产生热量,下列放热现象主要由物理变化引起的是()
A生石灰与水作用放出大量的热 B.氢氧化钠与盐酸混合放出大量的热
C.白炽灯泡通电后发热 D.铝与盐酸作用放出大量的热
5.下列方法很难区别氢氧化钠溶液和饱和澄清石灰水的是( )
A.加热溶液 B.通入CO2气体 C.滴入紫色石蕊溶液 D.加入少量CaO
6.下列现象的产生,与空气成分无关的是( )
A.烧碱露置空气中变重 B.浓盐酸露至空气中变轻
C.酥脆饼干置于空气中变软 D.菜刀置于潮湿空气中生锈
7.右图橡皮塞上装有试管和U形管,若观察到U形管中a处的液面下降,则试管中加入的物质是( )
①CaO固体 ②NaOH固体 ③浓H2SO4 ④NH4NO3固体
A.①②③ B.②③④ C.①②④ D.全部
8.下列对实验意外事故的处理错误的是( )
A.若不慎将燃着的酒精灯碰倒,洒出的酒精在桌上燃烧,应立刻用湿抹布扑盖
B.若不慎将烧碱溶液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液
C.若不慎将腐蚀性药液溅入眼睛,要先用手揉眼睛,再立即用水冲洗
D.若不慎将浓硫酸沾到皮肤或衣服上,应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液
9.从H、O、N、Ca、Na、Cu六种元素中,选择适当的元素组成符合下列要求的物质,并用化学符号表示:
(1)在空气中易潮解的碱_______;(2)溶解度随温度升高而减小的碱_________;
(3)只由非金属元素组成的碱____________;4)不溶性碱_________;
(5)碱有相似化学性质的原因是溶液中含有______。
10.小黎同学为了进一步加深对“碱的化学性质”的理解,特邀你协助完成下列活动与探究:?(1) 如右图所示,在白色点滴板上进行实验,请将实验现象填入下表:
氢氧化钠溶液 氢氧化钙溶液
加紫色石蕊溶液 __________ __________
(2)回忆检验二氧化碳气体的反应,写出该反应的化学方程____________________________________。
(3)三氧化硫(SO3)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式____________________________________。?
11.氨气是一种重要的化工原料,在工农业生产中有广泛的应用。某兴趣小组的同学为了探究氨气的某些性质,进行以下实验。下图中从左到右依次是实验步骤及相应的现象。
请根据上图中所示的信息,归纳出有关氨气的性质:
(1)物理性质①______________;②_____________。
(2)化学性质:氨气与水反应后所得氨水显____性
12.某同学设计了以下两个实验,打开分液漏斗的活塞,他会看到:
(1)实验1中澄清石灰水的现象是______,产生此现象的原因是____________________________________________。
(2)实验2中澄清石灰水的现象是___________,产生此现象的原因是________________________________________________________________________。
13.有浓盐酸、氢氧化钠、石灰水三种物质的溶液长期存放在空气中,溶液质量因发生化学变化而减小的物质是_______,反应的化学方程式为________________________,因发生化学变化溶液质量增大的物质是__________。
14.右边是某趣味实验装置图。挤压胶头滴管后,可观察到气球胀大的现象。请分析其原因,并写出化学方程式。
【中考链接】
15.(苏州市)下列有关熟石灰的说法错误的是 ( )
A.熟石灰又称为消石灰
B.熟石灰由生石灰与水反应而制得
C.熟石灰的溶解度随温度升高而增大
D.熟石灰可以用来改良酸性土壤
16.(日照市)如图所示,实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响。经数小时实验后,U形管A、B两处的液面会出现下列哪种情况 ( )
A.A处下降,B处上升
B.A、B两处都下降
C.A处上升,B处下降
D.A、B两处都不变
17.(内江市)将稀硫酸滴入一定量的氧化铜粉末中,使固体刚好溶解后滴入适量的氢氧化钠溶液至反应完全.请依次写出相关的化学反应方程式:
18.(宿迁市)化学课堂上要学习碱的化学性质,老师让两位同学和他共同做实验,要求两位同学分别向澄清石灰水和氢氧化钠溶液中吹气,如图①②所示,老师告诉同学们,呼出的气体中只有二氧化碳有可能与澄清石灰水和氢氧化钠溶液反应.
同学们在吹气后观察到①中澄清石灰水边浑浊,②中氢氧化钠溶液无明显现象.观察实验现象后老师问,通过实验现象的观察,检验二氧化碳气体应该使用_________________,针对②中的情况,师生共同开始探究之旅.
【提出问题】二氧化碳通入氢氧化钠溶液中无明显现象,两者是否发生了化学反应?
【猜想假设】猜想A:两者发生了化学反应;猜想B:两者没有发生化学反应.
【实验探究】
(1)小明设计了如图所示的③、④两个实验.
实验现象:③中的软塑料瓶变瘪,④中 ________________________________.
(2)小亮认为小明的实验是可行的,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低,小光同学却对此提出了质疑,他认为小明的实验不严谨,若仍利用该装置,需要补做的对比实验是_________________________________________.
(3)小光设计的是通过检验生成物来验证猜想,请帮他填写实验报告:
实验步骤 实验现象 实验结论
取③实验后的溶液少许,再向其加入 ________________________________ _________________________________________ 验证了二氧化碳和氢氧化钠溶液反应
【实验结论】二氧化碳和氢氧化钠溶液发生了化学反应.
【反思拓展】探究结束老师说,通过此探究实验我们发现,对于没有明显现象的化学反应,可以从不同的角度证明反应的发生,这些角度可以是:
①通过检验反应物减少证明反应发生;②通过________________证明反应的发生.
19.(昆明市)为测定某CuSO4溶液的溶质质量分数,化学小组的同学取CuSO4溶液100g,向其中滴加一定浓度的NaOH溶液,至不再产生沉淀为止,共用去NaOH溶液80g,过滤,得到滤液175.1g.请计算:
(1)该反应生成沉淀 4.9 g;
(2)该CuSO4溶液中溶质的质量分数.
参考答案
【名师导学】
1.氢氧化钠:
(1)氢氧化钠有_腐蚀__性,所以,它的俗名叫做_火碱__、_烧碱 _或_ 苛性钠_。如果不慎将碱液沾到皮肤上,要先__用水冲洗___,后___涂上硼酸溶液_________。
(2)氢氧化钠为__白_色固体,将氢氧化钠放在表面皿上放置一会儿产生的现象为___表面变潮湿___,这种现象叫做_潮解___,产生这种现象的原因为__NaOH吸收空气中水蒸气_____。将NaOH放入盛有少量水的试管里,并用手触摸试管外壁,产生的现象为试管烫热__,该实验说明NaOH__溶于水时放出热量________________。
(3)氢氧化钠广泛应用于__肥皂___、__石油____、__造纸___、__纺织___和__印染___等工业,在生活中可用于__去除油污______。
2.氢氧化钙:氢氧化钙是__白__色___ 粉___状固体,俗称_消石灰__或_熟石灰____,它可由__CaO___与水反应得到,反应中_放出______(填“放出”或“吸收”)热量,反应方程式为__CaO+H2O=Ca(OH)2 ______________。
3.其它常见的碱:氨水 NH3·H2O (写化学式,下同)、氢氧化钾 KOH 、氢氧化钡 Ba(OH)2 。
4.碱的化学性质
(1)碱溶液+酚酞溶液→变__红___色, 碱溶液+紫色石蕊溶液→变_蓝____色;
如: 氨水+酚酞→变__红____色 KOH溶液+紫色石蕊溶液→_蓝_____色
(2)非金属氧化物+碱溶液→_盐+水______ 如:
Ca(OH)2+CO2=CaCO3↓+H2O 2NaOH+CO2=Na2CO3+H2O
SO3+2NaOH=Na2SO4+H2O Ba(OH)2+CO2=BaCO3↓+H2O
【课时作业】
1.C 2.B??3.B 4.C 5.C 6.B 7.A 8.C
9.(1)NaOH(2)Ca(OH)2 (3)NH3·H2O;(4)Cu(OH)2 ;(5)OH-
10. (1)变蓝色 变蓝色
(2)Ca(OH)2+CO2=CaCO3↓+H2O
(3)SO3+2NaOH=Na2SO4+H2O?
11. (1)①密度比空气小 ②易溶于水
(2)碱
12.(1)变浑浊 生成的CO2与Ca(OH)2反应生成的CaCO3不溶于水
(2)变浑浊 CaO与H2O反应放出热量 Ca(OH)2的溶解度随温度的升高而减小,有Ca(OH)2析出 。
13.石灰水 CO2+Ca(OH)2=CaCO3↓+H2O 氢氧化钠
14.CO2被浓NaOH溶液吸收,锥形瓶内的气压成小,外界大气压大于锥形瓶内的气压,使气球胀大。 2NaOH+CO2=Na2CO3+H2O
【中考链接】
15.C 16.C
17.(1)CuO+H2SO4═CuSO4+H2O
(2)CuSO4+2NaOH═Cu(OH)2↓+Na2SO4
18. 澄清的石灰水
(1)气球变大(合理说法均可)
(2)将氢氧化钠溶液换成等体积的水,与加入氢氧化钠溶液的实验现象进行对比
(3)
实验步骤 实验现象 实验结论
取③实验后的溶液少许,再向其加入 稀盐酸(或氯化钙溶液等) 有气泡产生(或有白色沉淀生成等) 验证了二氧化碳和氢氧化钠溶液反应
② 检验生成物
19.(1)4.9g (2)8%
同课章节目录
