7.2碱及其性质 同步练习(解析版)
图片预览



文档简介
7.2碱及其性质
同步练习(解析版)
1.氧化钙常用作食品干燥剂,其俗称是
A.生石灰 B.熟石灰 C.消石灰 D.石灰石
2.下列溶液在空气中敞口放置后,溶液质量因发生化学反应而减小的是
A.石灰水 B.浓硫酸 C.浓盐酸 D.烧碱溶液
3.使用酸、碱等腐蚀性药品时,必须按照操作规程进行。下列处理方法错误的是( )
A.有腐蚀性的药液溅入眼睛内,要立即用水冲洗,切不可用手揉搓
B.稀酸飞溅到皮肤上,立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液
C.不小心打翻了燃着的酒精灯,应立即浇水来熄灭桌子上燃着的酒精
D.氢氧化钠溶液溅在皮肤上,先用水冲洗后,再涂上硼酸溶液
4.下列各组物质中,按酸、碱和单质的顺序排列的是( )
A.硫酸钙、氨水、锌 B.硫酸、熟石灰、氮气
C.盐酸、纯碱、金刚石 D.硝酸、烧碱、氨气
5.氢氧化钠是重要的化工原料,下列不是其俗称的是
A.纯碱 B.烧碱
C.苛性钠 D.火碱
6.碱溶液中都含有OH—,因此不同的碱表现出一些共同的性质。下列关于Ba(OH)2性质的描述中不属于碱的共同性质的是( )
A.能使紫色石蕊溶液变蓝色
B.能与盐酸反应生成水
C.能与Na2SO4溶液反应生成BaSO4沉淀
D.能与CO2反应生成水
7.向含有MgCl2和HCl的混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,所加NaOH溶液质量与生成沉淀的质量关系如下图所示。下列说法中正确的是( )
A.M点溶液中的溶质只有一种
B.整个反应过程中,氯离子质量分数不变
C.沉淀完全时,x的数值为80
D.N点溶液中氯化钠的质量为17.55g
8.下列物质在所述方法操作后溶液质量变大的是( )
A.在稀盐酸中加入少量碳酸钙 B.将澄清石灰水敞口放置一段时间
C.在饱和石灰水中加入少量生石灰 D.在硫酸亚铁溶液中加入少量铜
9.现有盐酸和氯化镁的混合溶液,向其中逐滴滴入氢氧化钠溶液,生成沉淀质量与滴入氢氧化钠溶液质量的变化关系如图所示。下列说法错误的是( )
A.滴加氢氧化钠液质量为a﹣cg时,溶液中发生的反应为:
B.滴加氢氧化钠溶液质量至ag时,溶液中溶质质量比原混合溶液中溶质质量大
C.滴加氢氧化钠溶液质量至bg时,溶液中含三种溶质
D.滴加氢氧化钠溶液质量至cg时,溶液呈中性
10.下列关于水的说法中错误的是( )
A.长期饮用纯净水不利于身体健康
B.可用水鉴别两种白色固体:生石灰和熟石灰
C.用水壶将含可溶性钙、镁化合物较多的地下水煮沸,水壶内易产生水垢
D.淡水资源是取之不尽用之不竭的
11.物质的用途是由它们的性质决定的,下列有关碱的用途中,哪些可以归为一类,请你写出分类的依据。①用熟石灰制波尔多液②用碱溶液吸收二氧化硫③用氢氧化钠溶液洗涤石油产品中残余的硫酸 ④用熟石灰改良酸性土壤 ⑤用石灰水鉴定二氧化碳 ⑥用含氢氧化铝的药物治疗胃酸过多症
(1)分类(填序号):_____;依据_____;
(2)写出用途⑥所发生的化学反应方程式_____。
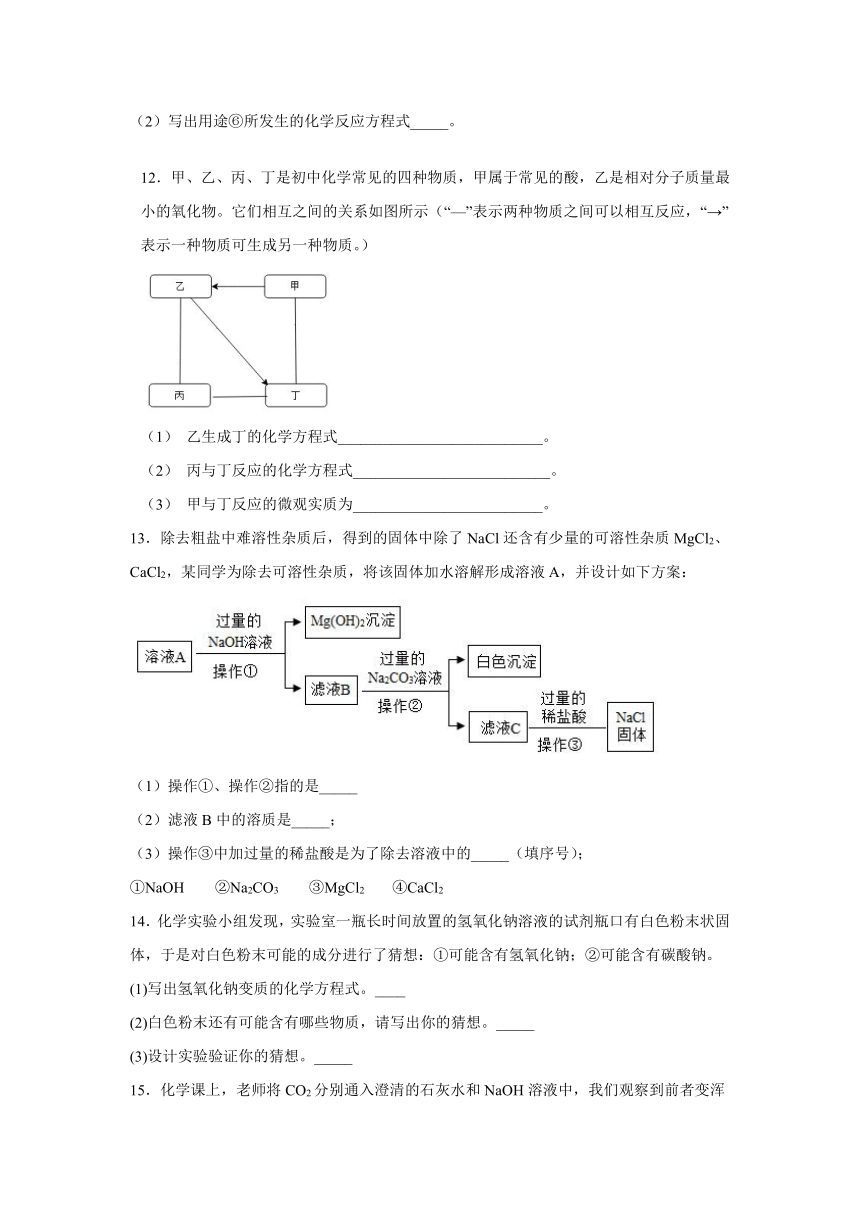
12.甲、乙、丙、丁是初中化学常见的四种物质,甲属于常见的酸,乙是相对分子质量最小的氧化物。它们相互之间的关系如图所示(“—”表示两种物质之间可以相互反应,“→”表示一种物质可生成另一种物质。)
(1) 乙生成丁的化学方程式___________________________。
(2) 丙与丁反应的化学方程式__________________________。
(3) 甲与丁反应的微观实质为_________________________。
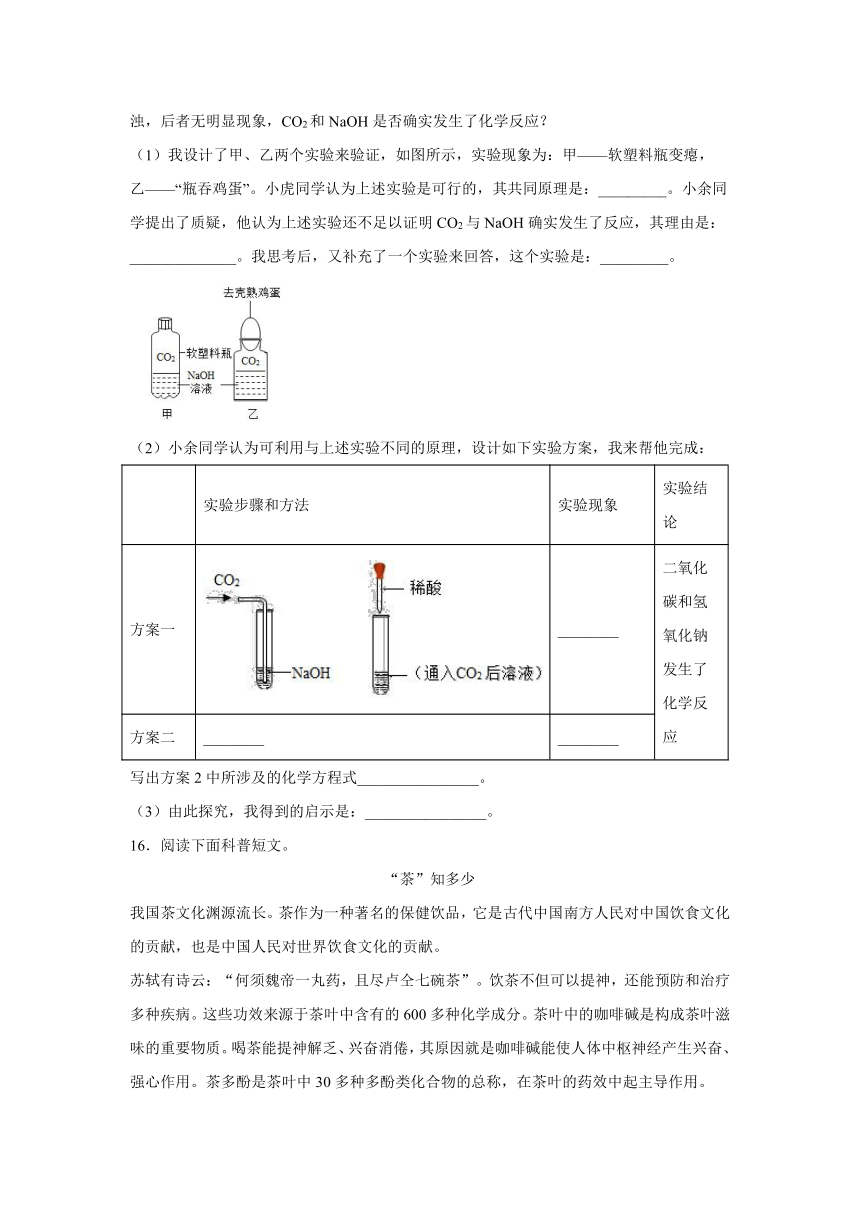
13.除去粗盐中难溶性杂质后,得到的固体中除了NaCl还含有少量的可溶性杂质MgCl2、CaCl2,某同学为除去可溶性杂质,将该固体加水溶解形成溶液A,并设计如下方案:
(1)操作①、操作②指的是_____
(2)滤液B中的溶质是_____;
(3)操作③中加过量的稀盐酸是为了除去溶液中的_____(填序号);
①NaOH ②Na2CO3 ③MgCl2 ④CaCl2
14.化学实验小组发现,实验室一瓶长时间放置的氢氧化钠溶液的试剂瓶口有白色粉末状固体,于是对白色粉末可能的成分进行了猜想:①可能含有氢氧化钠;②可能含有碳酸钠。
(1)写出氢氧化钠变质的化学方程式。____
(2)白色粉末还有可能含有哪些物质,请写出你的猜想。_____
(3)设计实验验证你的猜想。_____
15.化学课上,老师将CO2分别通入澄清的石灰水和NaOH溶液中,我们观察到前者变浑浊,后者无明显现象,CO2和NaOH是否确实发生了化学反应?
(1)我设计了甲、乙两个实验来验证,如图所示,实验现象为:甲——软塑料瓶变瘪,乙——“瓶吞鸡蛋”。小虎同学认为上述实验是可行的,其共同原理是:_________。小余同学提出了质疑,他认为上述实验还不足以证明CO2与NaOH确实发生了反应,其理由是:______________。我思考后,又补充了一个实验来回答,这个实验是:_________。
(2)小余同学认为可利用与上述实验不同的原理,设计如下实验方案,我来帮他完成:
实验步骤和方法
实验现象
实验结论
方案一
________
二氧化碳和氢氧化钠发生了化学反应
方案二
________
________
写出方案2中所涉及的化学方程式________________。
(3)由此探究,我得到的启示是:________________。
16.阅读下面科普短文。
“茶”知多少
我国茶文化渊源流长。茶作为一种著名的保健饮品,它是古代中国南方人民对中国饮食文化的贡献,也是中国人民对世界饮食文化的贡献。
苏轼有诗云:“何须魏帝一丸药,且尽卢仝七碗茶”。饮茶不但可以提神,还能预防和治疗多种疾病。这些功效来源于茶叶中含有的600多种化学成分。茶叶中的咖啡碱是构成茶叶滋味的重要物质。喝茶能提神解乏、兴奋消倦,其原因就是咖啡碱能使人体中枢神经产生兴奋、强心作用。茶多酚是茶叶中30多种多酚类化合物的总称,在茶叶的药效中起主导作用。
茶树适宜生长在pH4.5~6.5的土壤中,并且品种和环境不同,茶叶中的茶多酚含量不同。大叶种含的茶多酚较小叶种多。一般而言,温度越高,光线越强的地方,所种的茶中茶多酚较多。通常而言,在500米海拔以上,相对低海拔所产的茶比高海拔产的茶所含的茶多酚要多。
茶的品质和对人体的保健功效主要取决于茶水浸出物中茶多酚的含量。茶汤越浓、刺激性越强、收敛性越明显、越苦涩、回甘越好就说明茶汤中含的茶多酚浓度越大。不同的泡茶方法影响着茶多酚的溶解。以龙井茶为例进行研究,下图为水温及浸泡时间对茶多酚溶解率的影响。
除了控制水温和浸泡时间外,多次浸泡也可提高茶多酚的溶解率。
茶虽有多种保健功效,但有些人是不宜饮茶的。如:缺铁性贫血的人;溃疡病患者;发热病人;经常失眠的人在睡前不宜饮茶;儿童不宜饮浓茶;高血压病人不宜多饮茶。
请依据文章内容回答下列问题:
(1)茶叶中能起到提神解乏、兴奋消倦的物质是_____。
(2)茶树适宜生长在_____(填“酸性”“碱性”或“中性”)。
(3)茶杯中的滤网可使茶叶与茶水分离,其分离方法相当于实验基本操作中的_____。
(4)洗茶应采用低温水(50℃左右)短时间快速冲洗的方法,目的是_____。
(5)下列说法正确的是_____。
A在茶叶的药效中起主导作用的是茶多酚
B南方茶产区种的茶比北方茶产区种的茶所含茶多酚相对含量要高
C分析上图得到的结论是:泡茶时水温越高,时间越长,茶多酚溶解越多
D为使茶多酚溶解率达到80%以上,冲泡龙井茶水温首选90℃,并至少浸泡10min后再饮用
参考答案
1.A
【解析】
A. 生石灰是氧化钙的俗称; B. 熟石灰是氢氧化钙的俗称; C. 消石灰是氢氧化钙的俗称; D. 石灰石是主要成分是碳酸钙的矿石的俗称。故选A。
2.A
【解析】
A.石灰水与二氧化碳反应生成碳酸钙和水;每生成100g碳酸钙的质量,反应而吸收的质量为44g,所以溶液的质量减少; B.浓硫酸 吸水,溶液质量增加; C.浓盐酸挥发使溶液的质量减少,但是物理变化;D.烧碱溶液吸收二氧化碳反应生成碳酸钠,得碳酸钠溶液,溶液质量增加。选A
3.C
【解析】
A、有腐蚀性的药液溅入眼睛内,要立即用水冲洗,切不可用手揉搓洒,正确,不符合题意; B、稀酸飞溅到皮肤上,立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液,正确,不符合题意;
C、酒精灯着火用湿抹布盖灭,而不是用水扑灭,错误,符合题意;
D、 氢氧化钠溶液溅在皮肤上,先用水冲洗后,再涂上硼酸溶液,正确,不符合题意。
4.B
【解析】
A、硫酸钙属于盐,氨水属于碱,锌属于单质,选项错误;
B、硫酸属于酸,熟石灰属于碱,氮气属于单质,选项正确;
C、盐酸属于酸,纯碱属于盐,金刚石属于单质,选项错误;
D、硝酸属于酸,烧碱属于碱,氨气属于化合物,选项错误,故选B。
5.A
【解析】
氢氧化钠俗称烧碱、火碱、苛性钠;纯碱是碳酸钠的俗称。故选A。
6.C
【解析】
碱溶液中都含有OH-,所以各种碱溶液具有相似的性质。
A、Ba(OH)2溶液使紫色石蕊溶液变蓝色,是Ba(OH)2溶液中的OH-与石蕊发生反应所致,属于碱的通性;
B、Ba(OH)2溶液能与盐酸反应生成水,是Ba(OH)2溶液中的OH-与盐酸中的H+反应生成水,属于碱的通性;
C、Ba(OH)2与Na2SO4溶液反应的实质是钡离子与硫酸根离子结合生成沉淀的缘故,与OH-无关,不属于碱的通性;
D、Ba(OH)2溶液能与CO2反应生成水,与溶液中的OH-有关,属于碱的通性。故选C。
7.D
【解析】
由图中信息可知,向含有MgCl2和HCl的混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,氢氧化钠先和盐酸反应,当盐酸完全反应后,再和氯化镁反应。A、氢氧化钠先和盐酸反应生成氯化钠和水,M点时,氢氧化钠和盐酸恰好完全反应生成氯化钠和水,M点溶液中的溶质是氯化镁和氯化钠,故A错误;B、整个反应过程中,盐酸和氢氧化钠反应生成氯化钠和水,氯化镁和氢氧化钠反应生成氢氧化钠和氯化钠,溶液中的氯离子质量不变,但溶液的质量增加,因此质量分数减小,故B错误;C、设:氯化镁消耗的氢氧化钠的质量为x,生成的氯化钠的质量为y。
x=8g
y=11.7g
氢氧化钠溶液的质量=,所以沉淀完全时,x的数值为40+80=120,故C错误;D、设:盐酸和氢氧化钠反应生成氯化钠的质量为z。
z=5.85,所以N点溶液中氯化钠的质量5.85g+11.7g=17.55g,故D正确。故选D。
8.A
【解析】
A、碳酸钙与稀盐酸生成了氯化钙、水和二氧化碳,参加反应的碳酸钙的质量大于生成的二氧化碳的质量,反应后溶液的总质量变大,选项A正确;
B、将澄清石灰水敞口放置一段时间,石灰石与空气中的二氧化碳反应生成了碳酸钙沉淀,溶液的总质量减少,选项B不正确;
C、由于氧化钙与饱和溶液中的水发生反应而使溶液因此减少了水,饱和溶液的溶剂减少会造成溶质析出;溶液的溶质、溶剂都在减少,溶液的质量也在减少,选项C不正确;
D、铜无法置换出硫酸亚铁中的铁,故溶液质量不变,选项D不正确;
9.C
【解析】
向盐酸和氯化镁的混合溶液中逐滴滴入NaOH溶液,则开始是氢氧化钠和盐酸反应,盐酸反应完氢氧化钠和氯化镁反应产生沉淀。
A、滴加氢氧化钠溶液质量为a~c克时,溶液中发生反应为:,故正确;
B、滴加氢氧化钠溶液质量至ag时,发生的反应是稀盐酸和氢氧化钠反应生成了氯化钠和水,氯化氢变成了氯化钠,溶质质量增大,故正确;
C、滴加氢氧化钠溶液质量至b克时,含有的溶质有氯化钠和氯化镁两种,不是三种,故错误;
D、滴加氢氧化钠溶液质量至c克时,盐酸反应完了,氢氧化钠和氯化镁恰好完全反应,故溶液呈中性,故正确。
10.D
【解析】
A.纯净水中不含人体需要的各种矿物质离子,长期饮用不利于身体健康,说法正确;
B.生石灰遇水放出大量热量,熟石灰遇水放热不明显,可用水区别二者,说法正确;
C.含可溶性钙、镁化合物较多的地下水是硬水,煮沸时能生成碳酸钙和氢氧化镁沉淀,即水壶内易产生水垢,说法正确;
D. 淡水资源在地球上含量是非常少的,如果不节约使用,很快就会耗尽,说法错误。
11.②⑤ 碱溶液能与某些非金属氧化物反应(或③④⑥;碱能与酸发生中和反应) Al(OH)3+3HCl=AlCl3+3H2O
【解析】
(1)用熟石灰制波尔多液、利用的是熟石灰能与硫酸铜等盐溶液发生反应;用碱溶液吸收二氧化硫,利用的是碱能与非金属氧化物反应生成盐和水;用氢氧化钠溶液洗涤石油产品中残余的硫酸,利用的是硫酸能与氢氧化钠溶液发生反应生成硫酸钠和水;用熟石灰改良酸性土壤,利用的熟石灰能与酸发生中和反应;用石灰水鉴定二氧化碳,利用的是氢氧化钙能与二氧化碳反应生成碳酸钙沉淀和水;用含氢氧化铝的药物治疗胃酸过多症,利用的是氢氧化铝和胃酸中的盐酸发生中和反应生成氯化铝和水;故填:②⑤,碱溶液能与某些非金属氧化物反应(或③④⑥,碱能与酸发生中和反应)
(2)用途⑥,利用的是氢氧化铝和胃酸中的盐酸反应生成氯化铝和水,反应的化学方程式为:Al(OH)3+3HCl═AlCl3+3H2O。
12.CaO+H2O = Ca(OH)2(其他合理答案均可) CO2+Ca(OH)2= CaCO3↓+H2O (或SO2+ 2NaOH=Na2SO3 + H2O)(其他合理答案均可) 氢离子与氢氧根离子生成水(其他合理描述均可)
【解析】
乙是相对分子质量最小的氧化物,则乙是水,甲、乙、丙、丁是初中化学常见的四种物质,甲属于常见的酸,结合图中各物质间的转化或反应关系,可推知:甲可能是盐酸,丁是氢氧化钙、丙是二氧化碳,因二氧化碳和水反应生成碳酸,水和氧化钙生成氢氧化钙,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,氢氧化钙和盐酸反应生成氯化钙和水;(其他合理答案均可)。
(1) 乙生成丁的化学方程式CaO+H2O = Ca(OH)2(其他合理答案均可);
(2) 丙与丁反应的化学方程式CO2+Ca(OH)2= CaCO3↓+H2O (或SO2+ 2NaOH=Na2SO3 + H2O)(其他合理答案均可)
(3) 甲与丁反应是中和反应,微观实质为氢离子与氢氧根离子生成水。
13.过滤 氯化钠、氢氧化钠、氯化钙 ①②
【解析】
(1)操作①、操作②均是将沉淀与滤液分离,指的是过滤;
(2)过量的氢氧化钠溶液与氯化镁溶液反应生成氢氧化镁沉淀和氯化钠,滤液B中的溶质是氯化钠、氢氧化钠、氯化钙;
(3)滤液C是含有氯化钠、氢氧化钠和碳酸钠,操作③中加过量的稀盐酸,目的是除去溶液中的NaOH、Na2CO3。
14.CO2+2NaOH=Na2CO3+H2O 氢氧化钠和碳酸钠 取少量白色粉末与烧杯中,加入适量水使固体全部溶解;然后加入过量的氯化钙溶液,若有白色沉淀产生,说明原溶液中有碳酸钠;过滤后向滤液中再滴入几滴酚酞溶液,若溶液变为红色,说明溶液显碱性,则原溶液中一定有氢氧化钠。
【解析】
(1)氢氧化钠与二氧化碳反应产生碳酸钠和水的化学方程式:CO2+2NaOH=Na2CO3+H2O;
(2)白色粉末还有可能同时含有氢氧化钠和碳酸钠;
(3)取少量白色粉末与烧杯中,加入适量水使固体全部溶解;然后加入过量的氯化钙溶液,若有白色沉淀产生,说明原溶液中有碳酸钠;过滤后向滤液中再滴入几滴酚酞溶液,若溶液变为红色,说明溶液显碱性,则原溶液中一定有氢氧化钠。
15.在密闭的体系里消耗CO2,使气体压强减小 NaOH溶液中有水,CO2又能溶于水且可以与水反应 取一个与甲装置同样大小和质地的软塑料瓶,充满CO2后,注入与NaOH溶液体积相同的水,振荡,比较瓶子变瘪的程度 有气泡产生 将CO2通入NaOH溶液后,再向溶液中滴加CaCl2溶液[或石灰水或BaCl2溶液或Ba(OH)2溶液] 出现白色浑浊(或产生白色沉淀) CO2+2NaOH═Na2CO3+H2O,Na2CO3+CaCl2═CaCO3↓+2NaCl(合理即可) 对于无明显现象的化学反应,可通过改变实验装置,创新的情境来观察明显的反应现象判断反应的发生
【解析】
(1)图甲、图乙,在密闭的容器内使氢氧化钠溶液吸收二氧化碳气体,容器内气体减少压强减小,图甲中的塑料瓶变瘪,图乙中的鸡蛋落入瓶中,都是在密闭的体系里消耗CO2,使气体压强减小,从而观察到明显现象;
由于氢氧化钠溶液中含有大量的水,气体二氧化碳不但能溶于水且可以和水发生反应,因此二氧化碳气体的减少原因在此又难以确切判断:究竟是CO2溶于水使气压减小,还是CO2与NaOH反应使气压减小;
为了说明二氧化碳的减少和氢氧化钠有很大关系,可取同量的水做对比实验,会发现仅是水,气体减少的体积明显小于氢氧化钠溶液。做一个对比实验:取一个与甲装置同样大小和质地的软塑料瓶,充满CO2后,注入与NaOH溶液体积相同的水,振荡,比较瓶子变瘪的程度即可判断;
(2)可以采取验证溶液中含有碳酸钠的方法说明二氧化碳与氢氧化钠发生了反应.虽然碳酸钠溶液呈碱性,但反应前的氢氧化钠溶液也呈碱性,因此不能使用酚酞变红的方法来检验是否生成碳酸钠.可以考虑常用的碳酸盐的检验方法来实现检验.如方法一滴加稀盐酸,也可以向反应后溶液中滴加氯化钙溶液(或氯化钡、氢氧化钡等溶液),使溶液中的碳酸钠变成沉淀;实验过程如下:
实验步骤和方法
实验现象
实验结论
方案一
有气泡产生
二氧化碳和氢氧化钠发生了化学反应
方案二
将CO2通入NaOH溶液后,再向溶液中滴加CaCl2溶液[或石灰水或BaCl2溶液或Ba(OH)2溶液]
出现白色浑浊(或产生白色沉淀)
方案2中所涉及的反应是二氧化碳与氢氧化钠反应生成碳酸钠和水,以及碳酸钠与氯化钙反应生成碳酸钙和氯化钠,反应的化学方程式分别为:CO2+2NaOH═Na2CO3+H2O,Na2CO3+CaCl2═CaCO3↓+2NaCl;
(3)由此探究,我得到的启示是:对于无明显现象的化学反应,可通过改变实验装置,创新的情境来观察明显的反应现象判断反应的发生。
16.咖啡碱 酸性 过滤 减少茶多酚流失 ABCD
【解析】
(1)因为咖啡碱能使人体中枢神经产生兴奋、强心作用,所以茶叶中能起到提神解乏、兴奋消倦的物质是 咖啡碱;
(2)pH?4.5~6.5的土壤属于 酸性;
(3)茶杯内的纱网能滤去茶叶,和过滤器除去水中泥沙原理是一样的;
(4)洗茶应采用低温水(50℃左右)短时间快速冲洗的方法,目的是 减少茶多酚流失;
(5)A、茶多酚是茶叶中30多种多酚类化合物的总称,在茶叶的药效中起主导作用,故正确;
B、一般而言,温度越高,光线越强的地方,所种的茶中茶多酚较多。所以南方茶产区种的茶比北方茶产区种的茶所含茶多酚相对含量要高,故正确;
C、分析上图得到的结论是:泡茶时水温越高,时间越长,茶多酚溶解越多,故正确;
D、由图中的信息知,为使茶多酚溶解率达到80%以上,冲泡龙井茶水温首选90℃,并至少浸泡10min后再饮用,故正确。
同步练习(解析版)
1.氧化钙常用作食品干燥剂,其俗称是
A.生石灰 B.熟石灰 C.消石灰 D.石灰石
2.下列溶液在空气中敞口放置后,溶液质量因发生化学反应而减小的是
A.石灰水 B.浓硫酸 C.浓盐酸 D.烧碱溶液
3.使用酸、碱等腐蚀性药品时,必须按照操作规程进行。下列处理方法错误的是( )
A.有腐蚀性的药液溅入眼睛内,要立即用水冲洗,切不可用手揉搓
B.稀酸飞溅到皮肤上,立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液
C.不小心打翻了燃着的酒精灯,应立即浇水来熄灭桌子上燃着的酒精
D.氢氧化钠溶液溅在皮肤上,先用水冲洗后,再涂上硼酸溶液
4.下列各组物质中,按酸、碱和单质的顺序排列的是( )
A.硫酸钙、氨水、锌 B.硫酸、熟石灰、氮气
C.盐酸、纯碱、金刚石 D.硝酸、烧碱、氨气
5.氢氧化钠是重要的化工原料,下列不是其俗称的是
A.纯碱 B.烧碱
C.苛性钠 D.火碱
6.碱溶液中都含有OH—,因此不同的碱表现出一些共同的性质。下列关于Ba(OH)2性质的描述中不属于碱的共同性质的是( )
A.能使紫色石蕊溶液变蓝色
B.能与盐酸反应生成水
C.能与Na2SO4溶液反应生成BaSO4沉淀
D.能与CO2反应生成水
7.向含有MgCl2和HCl的混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,所加NaOH溶液质量与生成沉淀的质量关系如下图所示。下列说法中正确的是( )
A.M点溶液中的溶质只有一种
B.整个反应过程中,氯离子质量分数不变
C.沉淀完全时,x的数值为80
D.N点溶液中氯化钠的质量为17.55g
8.下列物质在所述方法操作后溶液质量变大的是( )
A.在稀盐酸中加入少量碳酸钙 B.将澄清石灰水敞口放置一段时间
C.在饱和石灰水中加入少量生石灰 D.在硫酸亚铁溶液中加入少量铜
9.现有盐酸和氯化镁的混合溶液,向其中逐滴滴入氢氧化钠溶液,生成沉淀质量与滴入氢氧化钠溶液质量的变化关系如图所示。下列说法错误的是( )
A.滴加氢氧化钠液质量为a﹣cg时,溶液中发生的反应为:
B.滴加氢氧化钠溶液质量至ag时,溶液中溶质质量比原混合溶液中溶质质量大
C.滴加氢氧化钠溶液质量至bg时,溶液中含三种溶质
D.滴加氢氧化钠溶液质量至cg时,溶液呈中性
10.下列关于水的说法中错误的是( )
A.长期饮用纯净水不利于身体健康
B.可用水鉴别两种白色固体:生石灰和熟石灰
C.用水壶将含可溶性钙、镁化合物较多的地下水煮沸,水壶内易产生水垢
D.淡水资源是取之不尽用之不竭的
11.物质的用途是由它们的性质决定的,下列有关碱的用途中,哪些可以归为一类,请你写出分类的依据。①用熟石灰制波尔多液②用碱溶液吸收二氧化硫③用氢氧化钠溶液洗涤石油产品中残余的硫酸 ④用熟石灰改良酸性土壤 ⑤用石灰水鉴定二氧化碳 ⑥用含氢氧化铝的药物治疗胃酸过多症
(1)分类(填序号):_____;依据_____;
(2)写出用途⑥所发生的化学反应方程式_____。
12.甲、乙、丙、丁是初中化学常见的四种物质,甲属于常见的酸,乙是相对分子质量最小的氧化物。它们相互之间的关系如图所示(“—”表示两种物质之间可以相互反应,“→”表示一种物质可生成另一种物质。)
(1) 乙生成丁的化学方程式___________________________。
(2) 丙与丁反应的化学方程式__________________________。
(3) 甲与丁反应的微观实质为_________________________。
13.除去粗盐中难溶性杂质后,得到的固体中除了NaCl还含有少量的可溶性杂质MgCl2、CaCl2,某同学为除去可溶性杂质,将该固体加水溶解形成溶液A,并设计如下方案:
(1)操作①、操作②指的是_____
(2)滤液B中的溶质是_____;
(3)操作③中加过量的稀盐酸是为了除去溶液中的_____(填序号);
①NaOH ②Na2CO3 ③MgCl2 ④CaCl2
14.化学实验小组发现,实验室一瓶长时间放置的氢氧化钠溶液的试剂瓶口有白色粉末状固体,于是对白色粉末可能的成分进行了猜想:①可能含有氢氧化钠;②可能含有碳酸钠。
(1)写出氢氧化钠变质的化学方程式。____
(2)白色粉末还有可能含有哪些物质,请写出你的猜想。_____
(3)设计实验验证你的猜想。_____
15.化学课上,老师将CO2分别通入澄清的石灰水和NaOH溶液中,我们观察到前者变浑浊,后者无明显现象,CO2和NaOH是否确实发生了化学反应?
(1)我设计了甲、乙两个实验来验证,如图所示,实验现象为:甲——软塑料瓶变瘪,乙——“瓶吞鸡蛋”。小虎同学认为上述实验是可行的,其共同原理是:_________。小余同学提出了质疑,他认为上述实验还不足以证明CO2与NaOH确实发生了反应,其理由是:______________。我思考后,又补充了一个实验来回答,这个实验是:_________。
(2)小余同学认为可利用与上述实验不同的原理,设计如下实验方案,我来帮他完成:
实验步骤和方法
实验现象
实验结论
方案一
________
二氧化碳和氢氧化钠发生了化学反应
方案二
________
________
写出方案2中所涉及的化学方程式________________。
(3)由此探究,我得到的启示是:________________。
16.阅读下面科普短文。
“茶”知多少
我国茶文化渊源流长。茶作为一种著名的保健饮品,它是古代中国南方人民对中国饮食文化的贡献,也是中国人民对世界饮食文化的贡献。
苏轼有诗云:“何须魏帝一丸药,且尽卢仝七碗茶”。饮茶不但可以提神,还能预防和治疗多种疾病。这些功效来源于茶叶中含有的600多种化学成分。茶叶中的咖啡碱是构成茶叶滋味的重要物质。喝茶能提神解乏、兴奋消倦,其原因就是咖啡碱能使人体中枢神经产生兴奋、强心作用。茶多酚是茶叶中30多种多酚类化合物的总称,在茶叶的药效中起主导作用。
茶树适宜生长在pH4.5~6.5的土壤中,并且品种和环境不同,茶叶中的茶多酚含量不同。大叶种含的茶多酚较小叶种多。一般而言,温度越高,光线越强的地方,所种的茶中茶多酚较多。通常而言,在500米海拔以上,相对低海拔所产的茶比高海拔产的茶所含的茶多酚要多。
茶的品质和对人体的保健功效主要取决于茶水浸出物中茶多酚的含量。茶汤越浓、刺激性越强、收敛性越明显、越苦涩、回甘越好就说明茶汤中含的茶多酚浓度越大。不同的泡茶方法影响着茶多酚的溶解。以龙井茶为例进行研究,下图为水温及浸泡时间对茶多酚溶解率的影响。
除了控制水温和浸泡时间外,多次浸泡也可提高茶多酚的溶解率。
茶虽有多种保健功效,但有些人是不宜饮茶的。如:缺铁性贫血的人;溃疡病患者;发热病人;经常失眠的人在睡前不宜饮茶;儿童不宜饮浓茶;高血压病人不宜多饮茶。
请依据文章内容回答下列问题:
(1)茶叶中能起到提神解乏、兴奋消倦的物质是_____。
(2)茶树适宜生长在_____(填“酸性”“碱性”或“中性”)。
(3)茶杯中的滤网可使茶叶与茶水分离,其分离方法相当于实验基本操作中的_____。
(4)洗茶应采用低温水(50℃左右)短时间快速冲洗的方法,目的是_____。
(5)下列说法正确的是_____。
A在茶叶的药效中起主导作用的是茶多酚
B南方茶产区种的茶比北方茶产区种的茶所含茶多酚相对含量要高
C分析上图得到的结论是:泡茶时水温越高,时间越长,茶多酚溶解越多
D为使茶多酚溶解率达到80%以上,冲泡龙井茶水温首选90℃,并至少浸泡10min后再饮用
参考答案
1.A
【解析】
A. 生石灰是氧化钙的俗称; B. 熟石灰是氢氧化钙的俗称; C. 消石灰是氢氧化钙的俗称; D. 石灰石是主要成分是碳酸钙的矿石的俗称。故选A。
2.A
【解析】
A.石灰水与二氧化碳反应生成碳酸钙和水;每生成100g碳酸钙的质量,反应而吸收的质量为44g,所以溶液的质量减少; B.浓硫酸 吸水,溶液质量增加; C.浓盐酸挥发使溶液的质量减少,但是物理变化;D.烧碱溶液吸收二氧化碳反应生成碳酸钠,得碳酸钠溶液,溶液质量增加。选A
3.C
【解析】
A、有腐蚀性的药液溅入眼睛内,要立即用水冲洗,切不可用手揉搓洒,正确,不符合题意; B、稀酸飞溅到皮肤上,立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液,正确,不符合题意;
C、酒精灯着火用湿抹布盖灭,而不是用水扑灭,错误,符合题意;
D、 氢氧化钠溶液溅在皮肤上,先用水冲洗后,再涂上硼酸溶液,正确,不符合题意。
4.B
【解析】
A、硫酸钙属于盐,氨水属于碱,锌属于单质,选项错误;
B、硫酸属于酸,熟石灰属于碱,氮气属于单质,选项正确;
C、盐酸属于酸,纯碱属于盐,金刚石属于单质,选项错误;
D、硝酸属于酸,烧碱属于碱,氨气属于化合物,选项错误,故选B。
5.A
【解析】
氢氧化钠俗称烧碱、火碱、苛性钠;纯碱是碳酸钠的俗称。故选A。
6.C
【解析】
碱溶液中都含有OH-,所以各种碱溶液具有相似的性质。
A、Ba(OH)2溶液使紫色石蕊溶液变蓝色,是Ba(OH)2溶液中的OH-与石蕊发生反应所致,属于碱的通性;
B、Ba(OH)2溶液能与盐酸反应生成水,是Ba(OH)2溶液中的OH-与盐酸中的H+反应生成水,属于碱的通性;
C、Ba(OH)2与Na2SO4溶液反应的实质是钡离子与硫酸根离子结合生成沉淀的缘故,与OH-无关,不属于碱的通性;
D、Ba(OH)2溶液能与CO2反应生成水,与溶液中的OH-有关,属于碱的通性。故选C。
7.D
【解析】
由图中信息可知,向含有MgCl2和HCl的混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,氢氧化钠先和盐酸反应,当盐酸完全反应后,再和氯化镁反应。A、氢氧化钠先和盐酸反应生成氯化钠和水,M点时,氢氧化钠和盐酸恰好完全反应生成氯化钠和水,M点溶液中的溶质是氯化镁和氯化钠,故A错误;B、整个反应过程中,盐酸和氢氧化钠反应生成氯化钠和水,氯化镁和氢氧化钠反应生成氢氧化钠和氯化钠,溶液中的氯离子质量不变,但溶液的质量增加,因此质量分数减小,故B错误;C、设:氯化镁消耗的氢氧化钠的质量为x,生成的氯化钠的质量为y。
x=8g
y=11.7g
氢氧化钠溶液的质量=,所以沉淀完全时,x的数值为40+80=120,故C错误;D、设:盐酸和氢氧化钠反应生成氯化钠的质量为z。
z=5.85,所以N点溶液中氯化钠的质量5.85g+11.7g=17.55g,故D正确。故选D。
8.A
【解析】
A、碳酸钙与稀盐酸生成了氯化钙、水和二氧化碳,参加反应的碳酸钙的质量大于生成的二氧化碳的质量,反应后溶液的总质量变大,选项A正确;
B、将澄清石灰水敞口放置一段时间,石灰石与空气中的二氧化碳反应生成了碳酸钙沉淀,溶液的总质量减少,选项B不正确;
C、由于氧化钙与饱和溶液中的水发生反应而使溶液因此减少了水,饱和溶液的溶剂减少会造成溶质析出;溶液的溶质、溶剂都在减少,溶液的质量也在减少,选项C不正确;
D、铜无法置换出硫酸亚铁中的铁,故溶液质量不变,选项D不正确;
9.C
【解析】
向盐酸和氯化镁的混合溶液中逐滴滴入NaOH溶液,则开始是氢氧化钠和盐酸反应,盐酸反应完氢氧化钠和氯化镁反应产生沉淀。
A、滴加氢氧化钠溶液质量为a~c克时,溶液中发生反应为:,故正确;
B、滴加氢氧化钠溶液质量至ag时,发生的反应是稀盐酸和氢氧化钠反应生成了氯化钠和水,氯化氢变成了氯化钠,溶质质量增大,故正确;
C、滴加氢氧化钠溶液质量至b克时,含有的溶质有氯化钠和氯化镁两种,不是三种,故错误;
D、滴加氢氧化钠溶液质量至c克时,盐酸反应完了,氢氧化钠和氯化镁恰好完全反应,故溶液呈中性,故正确。
10.D
【解析】
A.纯净水中不含人体需要的各种矿物质离子,长期饮用不利于身体健康,说法正确;
B.生石灰遇水放出大量热量,熟石灰遇水放热不明显,可用水区别二者,说法正确;
C.含可溶性钙、镁化合物较多的地下水是硬水,煮沸时能生成碳酸钙和氢氧化镁沉淀,即水壶内易产生水垢,说法正确;
D. 淡水资源在地球上含量是非常少的,如果不节约使用,很快就会耗尽,说法错误。
11.②⑤ 碱溶液能与某些非金属氧化物反应(或③④⑥;碱能与酸发生中和反应) Al(OH)3+3HCl=AlCl3+3H2O
【解析】
(1)用熟石灰制波尔多液、利用的是熟石灰能与硫酸铜等盐溶液发生反应;用碱溶液吸收二氧化硫,利用的是碱能与非金属氧化物反应生成盐和水;用氢氧化钠溶液洗涤石油产品中残余的硫酸,利用的是硫酸能与氢氧化钠溶液发生反应生成硫酸钠和水;用熟石灰改良酸性土壤,利用的熟石灰能与酸发生中和反应;用石灰水鉴定二氧化碳,利用的是氢氧化钙能与二氧化碳反应生成碳酸钙沉淀和水;用含氢氧化铝的药物治疗胃酸过多症,利用的是氢氧化铝和胃酸中的盐酸发生中和反应生成氯化铝和水;故填:②⑤,碱溶液能与某些非金属氧化物反应(或③④⑥,碱能与酸发生中和反应)
(2)用途⑥,利用的是氢氧化铝和胃酸中的盐酸反应生成氯化铝和水,反应的化学方程式为:Al(OH)3+3HCl═AlCl3+3H2O。
12.CaO+H2O = Ca(OH)2(其他合理答案均可) CO2+Ca(OH)2= CaCO3↓+H2O (或SO2+ 2NaOH=Na2SO3 + H2O)(其他合理答案均可) 氢离子与氢氧根离子生成水(其他合理描述均可)
【解析】
乙是相对分子质量最小的氧化物,则乙是水,甲、乙、丙、丁是初中化学常见的四种物质,甲属于常见的酸,结合图中各物质间的转化或反应关系,可推知:甲可能是盐酸,丁是氢氧化钙、丙是二氧化碳,因二氧化碳和水反应生成碳酸,水和氧化钙生成氢氧化钙,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,氢氧化钙和盐酸反应生成氯化钙和水;(其他合理答案均可)。
(1) 乙生成丁的化学方程式CaO+H2O = Ca(OH)2(其他合理答案均可);
(2) 丙与丁反应的化学方程式CO2+Ca(OH)2= CaCO3↓+H2O (或SO2+ 2NaOH=Na2SO3 + H2O)(其他合理答案均可)
(3) 甲与丁反应是中和反应,微观实质为氢离子与氢氧根离子生成水。
13.过滤 氯化钠、氢氧化钠、氯化钙 ①②
【解析】
(1)操作①、操作②均是将沉淀与滤液分离,指的是过滤;
(2)过量的氢氧化钠溶液与氯化镁溶液反应生成氢氧化镁沉淀和氯化钠,滤液B中的溶质是氯化钠、氢氧化钠、氯化钙;
(3)滤液C是含有氯化钠、氢氧化钠和碳酸钠,操作③中加过量的稀盐酸,目的是除去溶液中的NaOH、Na2CO3。
14.CO2+2NaOH=Na2CO3+H2O 氢氧化钠和碳酸钠 取少量白色粉末与烧杯中,加入适量水使固体全部溶解;然后加入过量的氯化钙溶液,若有白色沉淀产生,说明原溶液中有碳酸钠;过滤后向滤液中再滴入几滴酚酞溶液,若溶液变为红色,说明溶液显碱性,则原溶液中一定有氢氧化钠。
【解析】
(1)氢氧化钠与二氧化碳反应产生碳酸钠和水的化学方程式:CO2+2NaOH=Na2CO3+H2O;
(2)白色粉末还有可能同时含有氢氧化钠和碳酸钠;
(3)取少量白色粉末与烧杯中,加入适量水使固体全部溶解;然后加入过量的氯化钙溶液,若有白色沉淀产生,说明原溶液中有碳酸钠;过滤后向滤液中再滴入几滴酚酞溶液,若溶液变为红色,说明溶液显碱性,则原溶液中一定有氢氧化钠。
15.在密闭的体系里消耗CO2,使气体压强减小 NaOH溶液中有水,CO2又能溶于水且可以与水反应 取一个与甲装置同样大小和质地的软塑料瓶,充满CO2后,注入与NaOH溶液体积相同的水,振荡,比较瓶子变瘪的程度 有气泡产生 将CO2通入NaOH溶液后,再向溶液中滴加CaCl2溶液[或石灰水或BaCl2溶液或Ba(OH)2溶液] 出现白色浑浊(或产生白色沉淀) CO2+2NaOH═Na2CO3+H2O,Na2CO3+CaCl2═CaCO3↓+2NaCl(合理即可) 对于无明显现象的化学反应,可通过改变实验装置,创新的情境来观察明显的反应现象判断反应的发生
【解析】
(1)图甲、图乙,在密闭的容器内使氢氧化钠溶液吸收二氧化碳气体,容器内气体减少压强减小,图甲中的塑料瓶变瘪,图乙中的鸡蛋落入瓶中,都是在密闭的体系里消耗CO2,使气体压强减小,从而观察到明显现象;
由于氢氧化钠溶液中含有大量的水,气体二氧化碳不但能溶于水且可以和水发生反应,因此二氧化碳气体的减少原因在此又难以确切判断:究竟是CO2溶于水使气压减小,还是CO2与NaOH反应使气压减小;
为了说明二氧化碳的减少和氢氧化钠有很大关系,可取同量的水做对比实验,会发现仅是水,气体减少的体积明显小于氢氧化钠溶液。做一个对比实验:取一个与甲装置同样大小和质地的软塑料瓶,充满CO2后,注入与NaOH溶液体积相同的水,振荡,比较瓶子变瘪的程度即可判断;
(2)可以采取验证溶液中含有碳酸钠的方法说明二氧化碳与氢氧化钠发生了反应.虽然碳酸钠溶液呈碱性,但反应前的氢氧化钠溶液也呈碱性,因此不能使用酚酞变红的方法来检验是否生成碳酸钠.可以考虑常用的碳酸盐的检验方法来实现检验.如方法一滴加稀盐酸,也可以向反应后溶液中滴加氯化钙溶液(或氯化钡、氢氧化钡等溶液),使溶液中的碳酸钠变成沉淀;实验过程如下:
实验步骤和方法
实验现象
实验结论
方案一
有气泡产生
二氧化碳和氢氧化钠发生了化学反应
方案二
将CO2通入NaOH溶液后,再向溶液中滴加CaCl2溶液[或石灰水或BaCl2溶液或Ba(OH)2溶液]
出现白色浑浊(或产生白色沉淀)
方案2中所涉及的反应是二氧化碳与氢氧化钠反应生成碳酸钠和水,以及碳酸钠与氯化钙反应生成碳酸钙和氯化钠,反应的化学方程式分别为:CO2+2NaOH═Na2CO3+H2O,Na2CO3+CaCl2═CaCO3↓+2NaCl;
(3)由此探究,我得到的启示是:对于无明显现象的化学反应,可通过改变实验装置,创新的情境来观察明显的反应现象判断反应的发生。
16.咖啡碱 酸性 过滤 减少茶多酚流失 ABCD
【解析】
(1)因为咖啡碱能使人体中枢神经产生兴奋、强心作用,所以茶叶中能起到提神解乏、兴奋消倦的物质是 咖啡碱;
(2)pH?4.5~6.5的土壤属于 酸性;
(3)茶杯内的纱网能滤去茶叶,和过滤器除去水中泥沙原理是一样的;
(4)洗茶应采用低温水(50℃左右)短时间快速冲洗的方法,目的是 减少茶多酚流失;
(5)A、茶多酚是茶叶中30多种多酚类化合物的总称,在茶叶的药效中起主导作用,故正确;
B、一般而言,温度越高,光线越强的地方,所种的茶中茶多酚较多。所以南方茶产区种的茶比北方茶产区种的茶所含茶多酚相对含量要高,故正确;
C、分析上图得到的结论是:泡茶时水温越高,时间越长,茶多酚溶解越多,故正确;
D、由图中的信息知,为使茶多酚溶解率达到80%以上,冲泡龙井茶水温首选90℃,并至少浸泡10min后再饮用,故正确。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
