5.1生活中的酸和碱 课时作业(解析版)
文档属性
| 名称 | 5.1生活中的酸和碱 课时作业(解析版) |

|
|
| 格式 | zip | ||
| 文件大小 | 110.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-08 00:00:00 | ||
图片预览


文档简介
5.1生活中的酸和碱
课时作业(解析版)
1.氢氧化钙可用于改良酸性土壤,其俗称是( )
A.小苏打
B.熟石灰
C.生石灰
D.纯碱
2.使用酸、碱等腐蚀性药品时,必须按照操作规程进行。下列处理方法中有错误的是( )
A.有腐蚀性的药液溅入眼睛内,要立即用水冲洗,切不可用手揉搓洒
B.稀酸飞溅到皮肤上,立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液
C.配制稀硫酸时,可先在量筒中加入一定量的浓硫酸,再慢慢注入水并不断搅拌
D.氢氧化钠溶液洒在衣服上,先用水冲洗后,再涂上硼酸溶液
3.下列物质敞口放置,质量会减轻的是
A.氢氧化钠 B.浓硫酸 C.浓盐酸 D.碳酸钙
4.氢氧化钠是重要的化工原料,其俗称是
A.纯碱 B.烧碱 C.小苏打 D.熟石灰
5.存放下列物品的区域不需要张贴 的是( )
A.浓硫酸 B.氢氧化钠固体 C.汽油 D.纯净水
6.下列说法符合安全要求的是( )
A.家中燃气泄漏,立即开灯检查
B.稀释浓硫酸时,将水沿烧杯壁缓缓注入盛有浓硫酸的烧杯中
C.不慎碰倒酒精灯,洒出的酒精在桌上燃烧,立即用水浇灭
D.逃离火灾现场时,可用湿毛巾捂住口鼻,并尽量贴近地面
7.下列说法正确的是( )
A.浓盐酸在空气中会形成白烟
B.醋酸溶液可使紫色石蕊溶液变蓝
C.稀释浓硫酸时,一定要把水注入浓硫酸中
D.浓硫酸露置于空气中,溶质质量分数会变小
8.下列物质敞口放置一段时间后,因发生化学变化而使溶液质量减小的是( )
A.浓盐酸 B.氢氧化钙溶液 C.浓硫酸 D.氢氧化钠溶液
9.下列关于氢氧化钠的说法中错误的是( )
A.易溶于水,溶解时放出热量 B.它的俗称叫火碱、烧碱或苛性钠
C.它的水溶液能使石蕊试液变红色 D.它能与酸发生中和反应
10.下列操作能达到目的是( )
A.稀释浓硫酸时,将水沿容器壁慢慢注入浓硫酸中,并不断搅拌
B.溶解食盐时用玻璃棒搅拌以增大氯化钠的溶解度
C.用湿润的pH试纸测量酸雨的酸碱度
D.蒸发操作中,当蒸发中出现较多固体时,停止加热
11.根据下列事实说明空气中存在的物质,请将此物质的化学式填写在空格内:
(1)天然气能在空气中燃烧,说明空气中有_____;
(2)长期敞口存放在空气中的澄清石灰水表面有一层白膜,说明空气中有_____。
12.某化学小组进行“酸和碱的中和反应”实验:将盐酸滴入一定量的澄清石灰水中,实验无明显现象,取反应后的部分溶液测其酸碱度、加热、蒸干、得到白色固体。已知CaCl2溶液呈中性。
(1)怎样用pH试纸测定反应后溶液的酸碱度?____
(2)若得到的白色固体为CaCl2,请分析反应后溶液中溶质成分。____
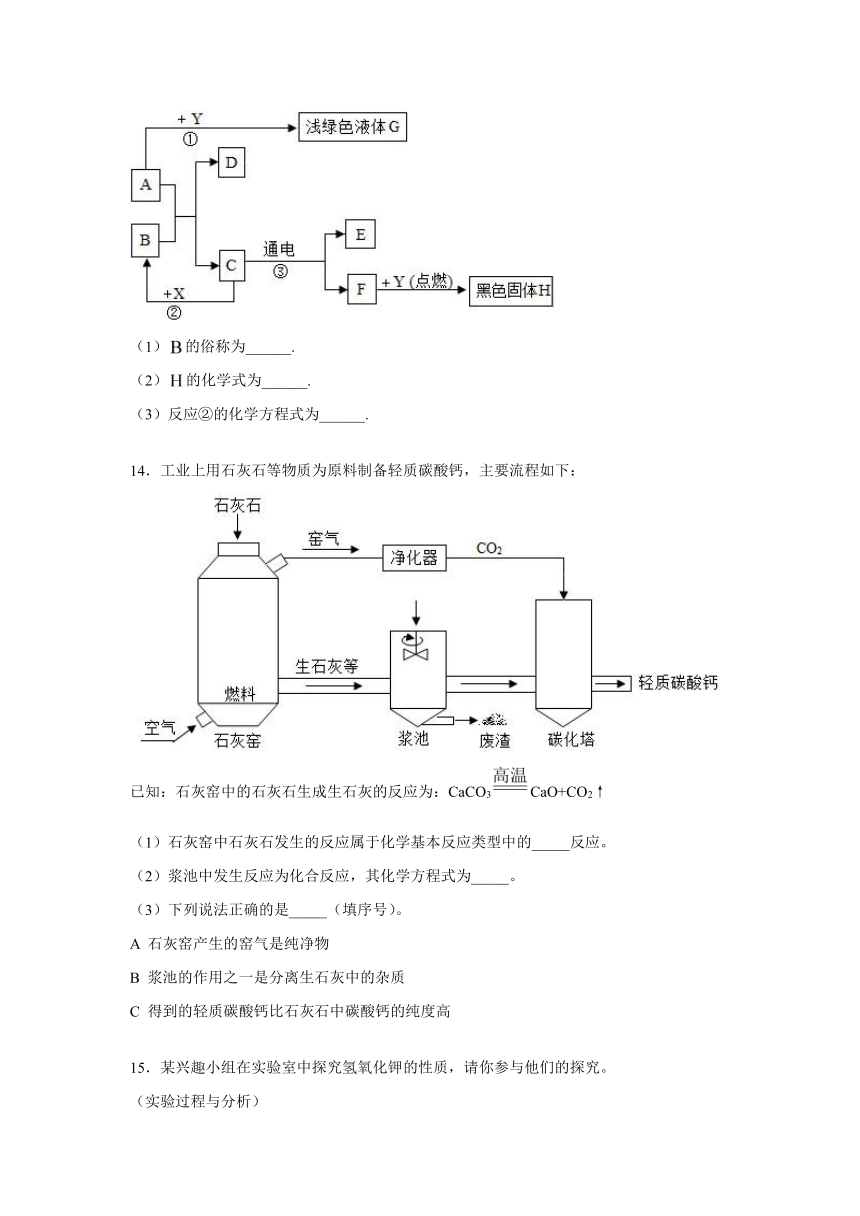
13.如图所示,是初中化学常见的物质,和可发生中和反应,常用作食品干燥剂,为单质.根据图示回答下列问题.
(1)的俗称为______.
(2)的化学式为______.
(3)反应②的化学方程式为______.
14.工业上用石灰石等物质为原料制备轻质碳酸钙,主要流程如下:
已知:石灰窑中的石灰石生成生石灰的反应为:CaCO3CaO+CO2↑
(1)石灰窑中石灰石发生的反应属于化学基本反应类型中的_____反应。
(2)浆池中发生反应为化合反应,其化学方程式为_____。
(3)下列说法正确的是_____(填序号)。
A 石灰窑产生的窑气是纯净物
B 浆池的作用之一是分离生石灰中的杂质
C 得到的轻质碳酸钙比石灰石中碳酸钙的纯度高
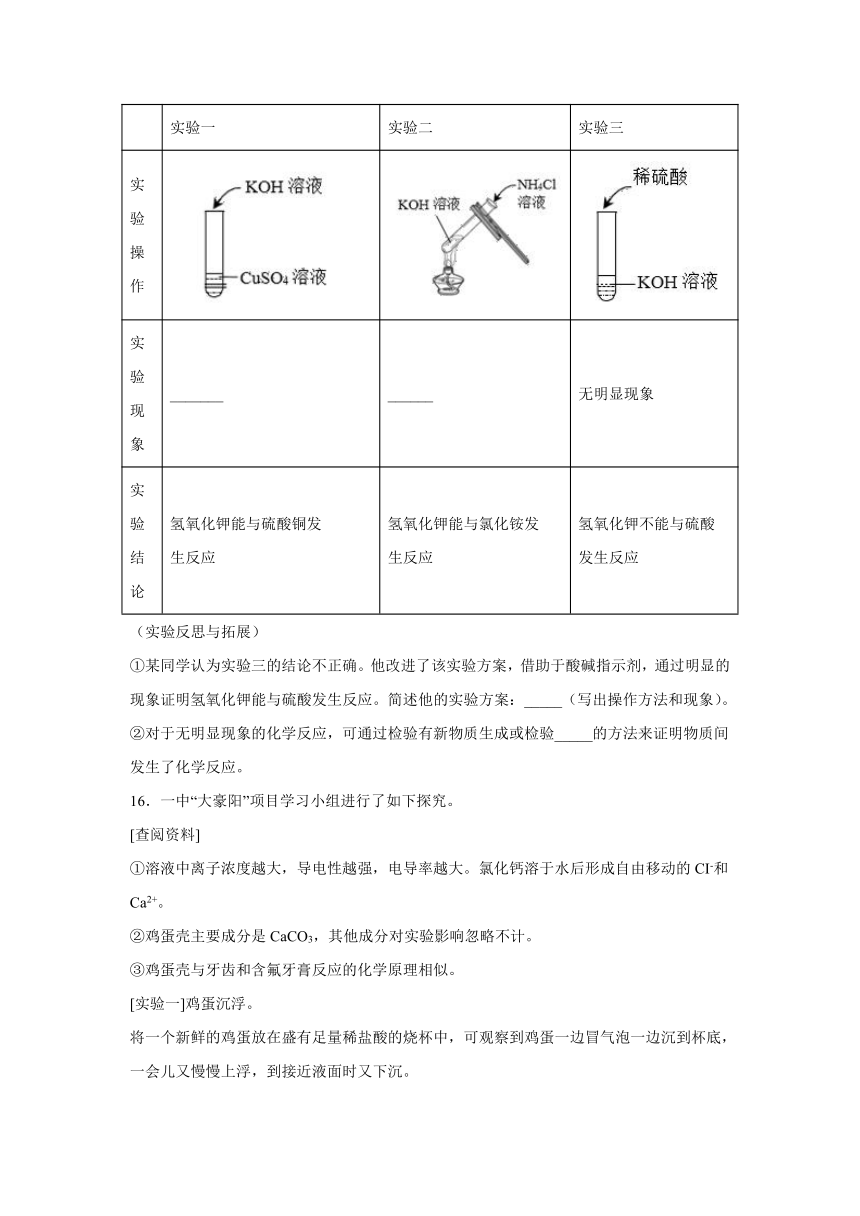
15.某兴趣小组在实验室中探究氢氧化钾的性质,请你参与他们的探究。
(实验过程与分析)
实验一
实验二
实验三
实验操作
实验现象
_______
______
无明显现象
实验结论
氢氧化钾能与硫酸铜发
生反应
氢氧化钾能与氯化铵发
生反应
氢氧化钾不能与硫酸
发生反应
(实验反思与拓展)
①某同学认为实验三的结论不正确。他改进了该实验方案,借助于酸碱指示剂,通过明显的现象证明氢氧化钾能与硫酸发生反应。简述他的实验方案:_____(写出操作方法和现象)。
②对于无明显现象的化学反应,可通过检验有新物质生成或检验_____的方法来证明物质间发生了化学反应。
16.一中“大豪阳”项目学习小组进行了如下探究。
[查阅资料]
①溶液中离子浓度越大,导电性越强,电导率越大。氯化钙溶于水后形成自由移动的CI-和Ca2+。
②鸡蛋壳主要成分是CaCO3,其他成分对实验影响忽略不计。
③鸡蛋壳与牙齿和含氟牙膏反应的化学原理相似。
[实验一]鸡蛋沉浮。
将一个新鲜的鸡蛋放在盛有足量稀盐酸的烧杯中,可观察到鸡蛋一边冒气泡一边沉到杯底,一会儿又慢慢上浮,到接近液面时又下沉。
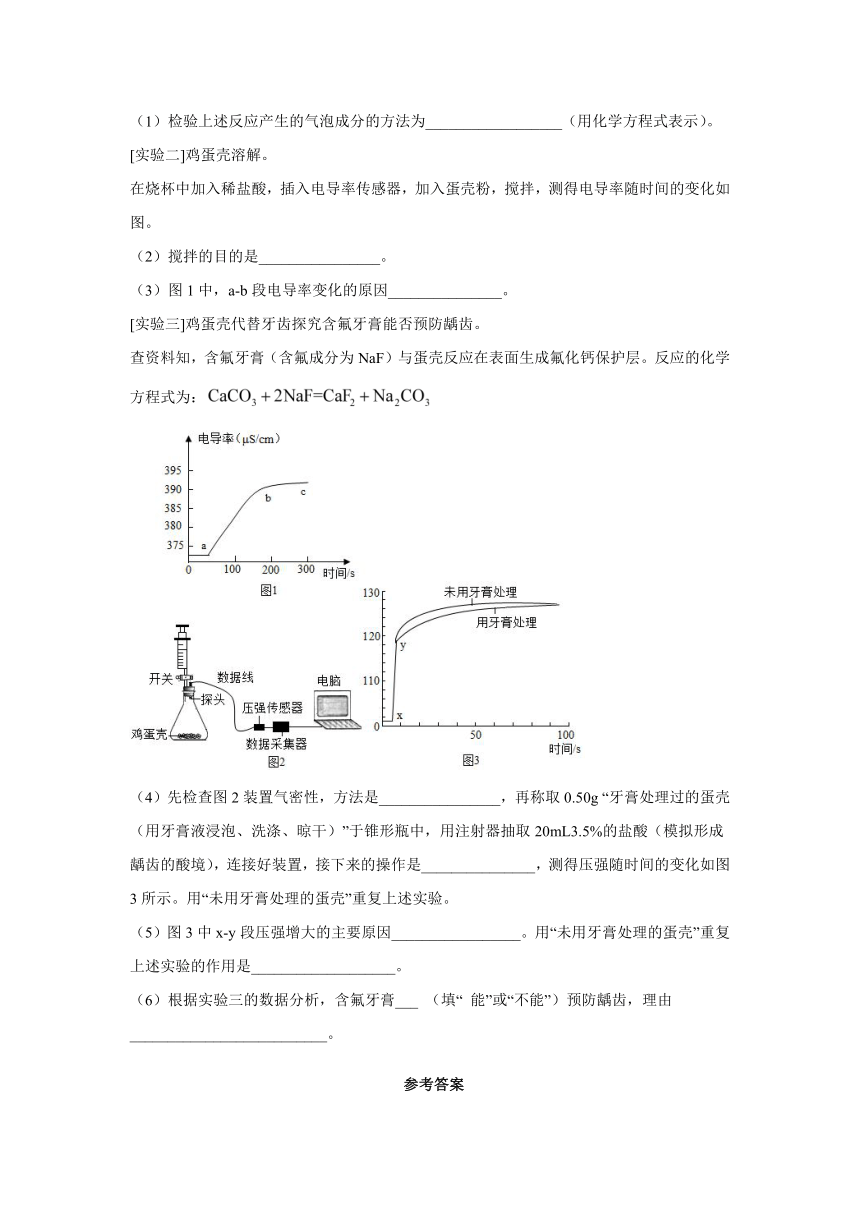
(1)检验上述反应产生的气泡成分的方法为__________________(用化学方程式表示)。
[实验二]鸡蛋壳溶解。
在烧杯中加入稀盐酸,插入电导率传感器,加入蛋壳粉,搅拌,测得电导率随时间的变化如图。
(2)搅拌的目的是________________。
(3)图1中,a-b段电导率变化的原因_______________。
[实验三]鸡蛋壳代替牙齿探究含氟牙膏能否预防龋齿。
查资料知,含氟牙膏(含氟成分为NaF)与蛋壳反应在表面生成氟化钙保护层。反应的化学方程式为:
(4)先检查图2装置气密性,方法是________________,再称取0.50g “牙膏处理过的蛋壳(用牙膏液浸泡、洗涤、晾干)”于锥形瓶中,用注射器抽取20mL3.5%的盐酸(模拟形成龋齿的酸境),连接好装置,接下来的操作是_______________,测得压强随时间的变化如图3所示。用“未用牙膏处理的蛋壳”重复上述实验。
(5)图3中x-y段压强增大的主要原因_________________。用“未用牙膏处理的蛋壳”重复上述实验的作用是___________________。
(6)根据实验三的数据分析,含氟牙膏___ (填“ 能”或“不能”)预防龋齿,理由__________________________。
参考答案
1.B
【解析】
氢氧化钙可用于改良酸性土壤,其俗称是熟石灰。故选B.
2.C
【解析】
A、有腐蚀性的药液溅入眼睛内,要立即用水冲洗,切不可用手揉搓洒,正确,不符合题意; B、稀酸飞溅到皮肤上,立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液,正确,不符合题意; C、稀释浓硫酸不能再量筒中进行,且不能将水倒进浓硫酸中,错误,符合题意; D、氢氧化钠溶液洒在衣服上,先用水冲洗后,再涂上硼酸溶液,正确,不符合题意;
3.C
【解析】
氢氧化钠吸收空气中的水和二氧化碳,质量增加;浓硫酸具有吸水性,敞口放置质量增加;浓盐酸具有挥发性,质量减小;碳酸钙性质稳定,在空气中质量不变.
4.B
【解析】
A、纯碱是碳酸钠的俗称,故A错误;
B、氢氧化钠俗称火碱、烧碱、苛性钠,故B正确;
C、小苏打为碳酸氢钠的俗称,故C错误;
D、熟石灰是氢氧化钙的俗称,故D错误.
5.D
【解析】
A、浓硫酸具有较强的腐蚀性,属于危险物品;需要张贴,故不符合题意;
B、氢氧化钠固体容易潮解,也就有较强的腐蚀性,属于危险物品;需要张贴,故不符合题意;
C、汽油容易燃烧,遇到明火容易发生爆炸,属于危险物品;需要张贴,故不符合题意;
D、纯净水无毒无污染,人可饮用,不属于危险物品;不需要张贴,故符合题意;
故选D
6.D
【解析】
A、家中燃气泄漏,不能立即开灯检查,以防止产生的电火花引发爆炸,故A不正确;
B、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时的扩散;一定不能把水注入浓硫酸中,故B不正确;
C、不慎碰倒酒精灯,洒出的酒精在桌上燃烧,不能立即用水浇灭,应用湿抹布扑盖,故C不正确;
D、湿毛巾有类似防毒面具作用,用湿毛巾捂住口鼻能防止吸入燃烧时生成的烟尘;气体受热密度变小,有毒气体上升聚集在高处,故要尽量贴近地面,寻找安全出口,故D正确。故选D。
7.D
【解析】A、浓盐酸具有挥发性,打开盛浓盐酸的试剂瓶,瓶口会产生白雾,而不是白烟,错误;
B、醋酸能使紫色石蕊溶液变红色,错误;
C、浓硫酸溶于水放出大量的热,稀释浓硫酸时,一定要把浓硫酸注入水中,错误;
D、浓硫酸具有吸水性,浓硫酸露置于空气中,溶质的质量不变,溶剂的质量增加,溶质的质量分数变小,正确。故选D。
8.B
【解析】
A、浓盐酸具有挥发性,敞口放置会使溶质氯化氢挥发出来,溶液质量减少,但属于物理变化,故不符合题意;
B、氢氧化钙溶液敞口放置吸收空气中的二氧化碳,发生化学反应,生成沉淀和水,使溶液质量减小,故符合题意。
C、浓硫酸敞口放置吸收空气中的水蒸气,没发生化学变化,溶液质量增大,故不符合题意;
D、氢氧化钠溶液敞口放置吸收空气中的二氧化碳,发生化学反应,生成碳酸钠和水,使溶液质量增大,故不符合题意。
9.C
【解析】
A、氢氧化钠易溶于水,溶于水时放出大量的热,故A说法正确;
B、由于氢氧化钠具有较强的腐蚀性,氢氧化钠俗称叫火碱、烧碱或苛性钠,故B说法正确;
C、氢氧化钠的水溶液显碱性,能使石蕊试液变蓝,故C说法错误;
D、酸和碱反应生成盐和水的反应是中和反应,氢氧化钠属于碱,能与酸发生中和反应,故D说法正确。
10.D
【解析】
A、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散,一定不能把水注入浓硫酸中,错误;B、溶解食盐时用玻璃棒搅拌,目的是加快溶解速率,而不是增大氯化钠的溶解度,错误;C、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH,不能用水湿润pH试纸,否则稀释了待测溶液,使酸雨的酸性减弱,测定结果偏大,,错误;D、蒸发时,待蒸发皿中出现较多量的固体时,应停止加热,利用余热将剩余液体蒸干,正确。故选D。
11.O2 CO2
【解析】
(1)天然气能在空气中燃烧,说明空气中有氧气,因为氧气能支持燃烧;故表示为:O2;
(2)长期敞口存放在空气中的澄清石灰水表面有一层白膜,说明空气中有二氧化碳;故表示为:CO2。
12.用玻璃棒蘸取待测溶液少许滴到pH试纸上,将试纸显示颜色与标准比色卡对照,读出pH值 一定含有氯化钙,可能含有氯化氢
【解析】
(1)用pH试纸测定反应后溶液的酸碱度的方法是:用玻璃棒蘸取待测溶液少许滴到pH试纸上,将试纸显示颜色与标准比色卡对照,读出pH值;
(2)盐酸具有挥发性,氢氧化钙和盐酸反应生成氯化钙和水,所以得到的白色固体为CaCl2,反应后溶液中溶质成分是:一定含有氯化钙,可能含有氯化氢。
13.熟石灰(或消石灰)
【解析】
C为生活中最常见的液体,故C是水,F可支持燃烧,故F是氧气,C通电生成的E是氢气,X常用作食品干燥剂,故X是氧化钙,能与水反应生成氢氧化钙,故B是氢氧化钙,A和B可发生中和反应,故A是酸,能与单质Y反应生成浅绿色溶液G,则Y是铁,铁能在氧气中燃烧生成四氧化三铁,故H是四氧化三铁,代入框图,推断合理。
【详解】
(1)B是氢氧化钙,俗称熟石灰或消石灰;
(2)H是四氧化三铁,化学式为:Fe3O4;
(3)反应②是氧化钙与水反应生成氢氧化钙的反应,化学方程式为:CaO+H2O=Ca(OH)2。
14.分解 CaO+H2O=Ca(OH)2 BC
【解析】
【详解】
(1)石灰窑中石灰石在高温条件下生成氧化钙和二氧化碳,该反应的特征是一变多,属于分解反应,故填:分解。
(2)浆池中生石灰和水反应生成氢氧化钙,其化学方程式为:CaO+H2O=Ca(OH)2。故填:CaO+H2O=Ca(OH)2。
(3)A.窑气中含有氮气、氧气、二氧化碳等,属于混合物,故选项说法错误。 B.浆池中能分离出废渣,浆池的作用之一是分离生石灰中的杂质,故选项说法正确。 C.石灰石的主要成分是碳酸钙,含有杂质,得到的轻质碳酸钙比石灰石中碳酸钙的纯度高,故选项说法正确。
15.出现蓝色沉淀 试管中冒气泡 取少量氢氧化钾于试管中,滴加无色酚酞溶液,观察到溶液变红,加入硫酸溶液变为无色,证明氢氧化钾溶液与稀硫酸发生了化学反应 反应物减少
【解析】
氢氧化钾和硫酸铜反应生成氢氧化铜蓝色沉淀和硫酸钾,氢氧化钾和氯化铵反应生成氯化钾和水和氨气,稀硫酸和氢氧化钾反应生成硫酸钾和水。
[实验过程与分析]
实验一
实验二
实验三
实验操作
实验现象
出现蓝色沉淀
试管中冒气泡
无明显现象
实验结论
氢氧化钾能与硫酸铜发
生反应
氢氧化钾能与氯化铵发
生反应
氢氧化钾不能与硫酸
发生反应
[实验反思与拓展]
①某同学认为实验三的结论不正确。他改进了该实验方案,借助于酸碱指示剂,通过明显的现象证明氢氧化钾能与硫酸发生反应。实验方案为取少量氢氧化钾于试管中,滴加无色酚酞溶液,观察到溶液变红,加入硫酸溶液变为无色,证明氢氧化钾溶液与稀硫酸发生了化学反应。
②对于无明显现象的化学反应,可通过检验有新物质生成或检验反应物减少的方法来证明物质间发生了化学反应。
【点睛】
16.Ca(OH)2+CO2=CaCO3↓+H2O 增大接触面积,加快反应速率 蛋壳中部分碳酸钙逐渐溶解,溶液中离子浓度增大,电导率增强 打开开关,拉动(或“推动”也可)注射器活塞,松开后,活塞回到原位,说明气密性良好 打开开关,将盐酸快速压入锥形瓶,关闭开关 碳酸盐与盐酸反应产生了二氧化碳气体,使瓶内压强增大 对比 能 相同条件下,使用含氟牙膏处理后的鸡蛋壳,反应能产生的气体更少,压强更小,消耗的鸡蛋壳更少
【解析】
(1)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O; (2)搅拌是为了增大接触面积,加快反应速率; (3)图1中,a-b段电导率变化的原因:蛋壳中部分碳酸钙逐渐溶解,溶液中离子浓度增大,电导率增强; (4)检验装置气密性利用装置内外的压强差检验,所以检查图2装置气密性,方法:打开开关,拉动注射器活塞,松开后,活塞回到原位,说明气密性良好,连接好装置,接下来的操作是:打开开关,将盐酸快速压入锥形瓶,关闭开关,测得压强随时间的变化如图3所 示; (5)碳酸盐和酸反应会生成二氧化碳,所以对比图3中x-y段压强增大的主要原因:碳酸盐与盐酸反应产生了二氧化碳气体,使瓶内压强增大;用“未用牙膏处理的蛋壳”重复上述实验的作用是对比; (6)根据图3的数据分析,含氟牙膏能预防龋齿,这是因为单位时间内用牙膏处理过的蛋壳产生二氧化碳较少。 故答案为:(1)Ca(OH)2+CO2=CaCO3↓+H2O; (2)增大接触面积,加快溶解速率; (3)蛋壳中部分碳酸钙逐渐溶解,溶液中离子浓度增大,电导率增强; (4)打开开关,拉动(或“推动”也可)注射器活塞,松开后,活塞回到原位,说明气密性良好;打开开关,将盐酸快速压入锥形瓶,关闭开关; (5)碳酸盐与盐酸反应产生了二氧化碳气体,使瓶内压强增大;对比; (6)能;相同条件下,使用含氟牙膏处理后的鸡蛋壳,反应能产生的气体更少,压强更小,消耗的鸡蛋壳更少。
课时作业(解析版)
1.氢氧化钙可用于改良酸性土壤,其俗称是( )
A.小苏打
B.熟石灰
C.生石灰
D.纯碱
2.使用酸、碱等腐蚀性药品时,必须按照操作规程进行。下列处理方法中有错误的是( )
A.有腐蚀性的药液溅入眼睛内,要立即用水冲洗,切不可用手揉搓洒
B.稀酸飞溅到皮肤上,立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液
C.配制稀硫酸时,可先在量筒中加入一定量的浓硫酸,再慢慢注入水并不断搅拌
D.氢氧化钠溶液洒在衣服上,先用水冲洗后,再涂上硼酸溶液
3.下列物质敞口放置,质量会减轻的是
A.氢氧化钠 B.浓硫酸 C.浓盐酸 D.碳酸钙
4.氢氧化钠是重要的化工原料,其俗称是
A.纯碱 B.烧碱 C.小苏打 D.熟石灰
5.存放下列物品的区域不需要张贴 的是( )
A.浓硫酸 B.氢氧化钠固体 C.汽油 D.纯净水
6.下列说法符合安全要求的是( )
A.家中燃气泄漏,立即开灯检查
B.稀释浓硫酸时,将水沿烧杯壁缓缓注入盛有浓硫酸的烧杯中
C.不慎碰倒酒精灯,洒出的酒精在桌上燃烧,立即用水浇灭
D.逃离火灾现场时,可用湿毛巾捂住口鼻,并尽量贴近地面
7.下列说法正确的是( )
A.浓盐酸在空气中会形成白烟
B.醋酸溶液可使紫色石蕊溶液变蓝
C.稀释浓硫酸时,一定要把水注入浓硫酸中
D.浓硫酸露置于空气中,溶质质量分数会变小
8.下列物质敞口放置一段时间后,因发生化学变化而使溶液质量减小的是( )
A.浓盐酸 B.氢氧化钙溶液 C.浓硫酸 D.氢氧化钠溶液
9.下列关于氢氧化钠的说法中错误的是( )
A.易溶于水,溶解时放出热量 B.它的俗称叫火碱、烧碱或苛性钠
C.它的水溶液能使石蕊试液变红色 D.它能与酸发生中和反应
10.下列操作能达到目的是( )
A.稀释浓硫酸时,将水沿容器壁慢慢注入浓硫酸中,并不断搅拌
B.溶解食盐时用玻璃棒搅拌以增大氯化钠的溶解度
C.用湿润的pH试纸测量酸雨的酸碱度
D.蒸发操作中,当蒸发中出现较多固体时,停止加热
11.根据下列事实说明空气中存在的物质,请将此物质的化学式填写在空格内:
(1)天然气能在空气中燃烧,说明空气中有_____;
(2)长期敞口存放在空气中的澄清石灰水表面有一层白膜,说明空气中有_____。
12.某化学小组进行“酸和碱的中和反应”实验:将盐酸滴入一定量的澄清石灰水中,实验无明显现象,取反应后的部分溶液测其酸碱度、加热、蒸干、得到白色固体。已知CaCl2溶液呈中性。
(1)怎样用pH试纸测定反应后溶液的酸碱度?____
(2)若得到的白色固体为CaCl2,请分析反应后溶液中溶质成分。____
13.如图所示,是初中化学常见的物质,和可发生中和反应,常用作食品干燥剂,为单质.根据图示回答下列问题.
(1)的俗称为______.
(2)的化学式为______.
(3)反应②的化学方程式为______.
14.工业上用石灰石等物质为原料制备轻质碳酸钙,主要流程如下:
已知:石灰窑中的石灰石生成生石灰的反应为:CaCO3CaO+CO2↑
(1)石灰窑中石灰石发生的反应属于化学基本反应类型中的_____反应。
(2)浆池中发生反应为化合反应,其化学方程式为_____。
(3)下列说法正确的是_____(填序号)。
A 石灰窑产生的窑气是纯净物
B 浆池的作用之一是分离生石灰中的杂质
C 得到的轻质碳酸钙比石灰石中碳酸钙的纯度高
15.某兴趣小组在实验室中探究氢氧化钾的性质,请你参与他们的探究。
(实验过程与分析)
实验一
实验二
实验三
实验操作
实验现象
_______
______
无明显现象
实验结论
氢氧化钾能与硫酸铜发
生反应
氢氧化钾能与氯化铵发
生反应
氢氧化钾不能与硫酸
发生反应
(实验反思与拓展)
①某同学认为实验三的结论不正确。他改进了该实验方案,借助于酸碱指示剂,通过明显的现象证明氢氧化钾能与硫酸发生反应。简述他的实验方案:_____(写出操作方法和现象)。
②对于无明显现象的化学反应,可通过检验有新物质生成或检验_____的方法来证明物质间发生了化学反应。
16.一中“大豪阳”项目学习小组进行了如下探究。
[查阅资料]
①溶液中离子浓度越大,导电性越强,电导率越大。氯化钙溶于水后形成自由移动的CI-和Ca2+。
②鸡蛋壳主要成分是CaCO3,其他成分对实验影响忽略不计。
③鸡蛋壳与牙齿和含氟牙膏反应的化学原理相似。
[实验一]鸡蛋沉浮。
将一个新鲜的鸡蛋放在盛有足量稀盐酸的烧杯中,可观察到鸡蛋一边冒气泡一边沉到杯底,一会儿又慢慢上浮,到接近液面时又下沉。
(1)检验上述反应产生的气泡成分的方法为__________________(用化学方程式表示)。
[实验二]鸡蛋壳溶解。
在烧杯中加入稀盐酸,插入电导率传感器,加入蛋壳粉,搅拌,测得电导率随时间的变化如图。
(2)搅拌的目的是________________。
(3)图1中,a-b段电导率变化的原因_______________。
[实验三]鸡蛋壳代替牙齿探究含氟牙膏能否预防龋齿。
查资料知,含氟牙膏(含氟成分为NaF)与蛋壳反应在表面生成氟化钙保护层。反应的化学方程式为:
(4)先检查图2装置气密性,方法是________________,再称取0.50g “牙膏处理过的蛋壳(用牙膏液浸泡、洗涤、晾干)”于锥形瓶中,用注射器抽取20mL3.5%的盐酸(模拟形成龋齿的酸境),连接好装置,接下来的操作是_______________,测得压强随时间的变化如图3所示。用“未用牙膏处理的蛋壳”重复上述实验。
(5)图3中x-y段压强增大的主要原因_________________。用“未用牙膏处理的蛋壳”重复上述实验的作用是___________________。
(6)根据实验三的数据分析,含氟牙膏___ (填“ 能”或“不能”)预防龋齿,理由__________________________。
参考答案
1.B
【解析】
氢氧化钙可用于改良酸性土壤,其俗称是熟石灰。故选B.
2.C
【解析】
A、有腐蚀性的药液溅入眼睛内,要立即用水冲洗,切不可用手揉搓洒,正确,不符合题意; B、稀酸飞溅到皮肤上,立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液,正确,不符合题意; C、稀释浓硫酸不能再量筒中进行,且不能将水倒进浓硫酸中,错误,符合题意; D、氢氧化钠溶液洒在衣服上,先用水冲洗后,再涂上硼酸溶液,正确,不符合题意;
3.C
【解析】
氢氧化钠吸收空气中的水和二氧化碳,质量增加;浓硫酸具有吸水性,敞口放置质量增加;浓盐酸具有挥发性,质量减小;碳酸钙性质稳定,在空气中质量不变.
4.B
【解析】
A、纯碱是碳酸钠的俗称,故A错误;
B、氢氧化钠俗称火碱、烧碱、苛性钠,故B正确;
C、小苏打为碳酸氢钠的俗称,故C错误;
D、熟石灰是氢氧化钙的俗称,故D错误.
5.D
【解析】
A、浓硫酸具有较强的腐蚀性,属于危险物品;需要张贴,故不符合题意;
B、氢氧化钠固体容易潮解,也就有较强的腐蚀性,属于危险物品;需要张贴,故不符合题意;
C、汽油容易燃烧,遇到明火容易发生爆炸,属于危险物品;需要张贴,故不符合题意;
D、纯净水无毒无污染,人可饮用,不属于危险物品;不需要张贴,故符合题意;
故选D
6.D
【解析】
A、家中燃气泄漏,不能立即开灯检查,以防止产生的电火花引发爆炸,故A不正确;
B、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时的扩散;一定不能把水注入浓硫酸中,故B不正确;
C、不慎碰倒酒精灯,洒出的酒精在桌上燃烧,不能立即用水浇灭,应用湿抹布扑盖,故C不正确;
D、湿毛巾有类似防毒面具作用,用湿毛巾捂住口鼻能防止吸入燃烧时生成的烟尘;气体受热密度变小,有毒气体上升聚集在高处,故要尽量贴近地面,寻找安全出口,故D正确。故选D。
7.D
【解析】A、浓盐酸具有挥发性,打开盛浓盐酸的试剂瓶,瓶口会产生白雾,而不是白烟,错误;
B、醋酸能使紫色石蕊溶液变红色,错误;
C、浓硫酸溶于水放出大量的热,稀释浓硫酸时,一定要把浓硫酸注入水中,错误;
D、浓硫酸具有吸水性,浓硫酸露置于空气中,溶质的质量不变,溶剂的质量增加,溶质的质量分数变小,正确。故选D。
8.B
【解析】
A、浓盐酸具有挥发性,敞口放置会使溶质氯化氢挥发出来,溶液质量减少,但属于物理变化,故不符合题意;
B、氢氧化钙溶液敞口放置吸收空气中的二氧化碳,发生化学反应,生成沉淀和水,使溶液质量减小,故符合题意。
C、浓硫酸敞口放置吸收空气中的水蒸气,没发生化学变化,溶液质量增大,故不符合题意;
D、氢氧化钠溶液敞口放置吸收空气中的二氧化碳,发生化学反应,生成碳酸钠和水,使溶液质量增大,故不符合题意。
9.C
【解析】
A、氢氧化钠易溶于水,溶于水时放出大量的热,故A说法正确;
B、由于氢氧化钠具有较强的腐蚀性,氢氧化钠俗称叫火碱、烧碱或苛性钠,故B说法正确;
C、氢氧化钠的水溶液显碱性,能使石蕊试液变蓝,故C说法错误;
D、酸和碱反应生成盐和水的反应是中和反应,氢氧化钠属于碱,能与酸发生中和反应,故D说法正确。
10.D
【解析】
A、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散,一定不能把水注入浓硫酸中,错误;B、溶解食盐时用玻璃棒搅拌,目的是加快溶解速率,而不是增大氯化钠的溶解度,错误;C、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH,不能用水湿润pH试纸,否则稀释了待测溶液,使酸雨的酸性减弱,测定结果偏大,,错误;D、蒸发时,待蒸发皿中出现较多量的固体时,应停止加热,利用余热将剩余液体蒸干,正确。故选D。
11.O2 CO2
【解析】
(1)天然气能在空气中燃烧,说明空气中有氧气,因为氧气能支持燃烧;故表示为:O2;
(2)长期敞口存放在空气中的澄清石灰水表面有一层白膜,说明空气中有二氧化碳;故表示为:CO2。
12.用玻璃棒蘸取待测溶液少许滴到pH试纸上,将试纸显示颜色与标准比色卡对照,读出pH值 一定含有氯化钙,可能含有氯化氢
【解析】
(1)用pH试纸测定反应后溶液的酸碱度的方法是:用玻璃棒蘸取待测溶液少许滴到pH试纸上,将试纸显示颜色与标准比色卡对照,读出pH值;
(2)盐酸具有挥发性,氢氧化钙和盐酸反应生成氯化钙和水,所以得到的白色固体为CaCl2,反应后溶液中溶质成分是:一定含有氯化钙,可能含有氯化氢。
13.熟石灰(或消石灰)
【解析】
C为生活中最常见的液体,故C是水,F可支持燃烧,故F是氧气,C通电生成的E是氢气,X常用作食品干燥剂,故X是氧化钙,能与水反应生成氢氧化钙,故B是氢氧化钙,A和B可发生中和反应,故A是酸,能与单质Y反应生成浅绿色溶液G,则Y是铁,铁能在氧气中燃烧生成四氧化三铁,故H是四氧化三铁,代入框图,推断合理。
【详解】
(1)B是氢氧化钙,俗称熟石灰或消石灰;
(2)H是四氧化三铁,化学式为:Fe3O4;
(3)反应②是氧化钙与水反应生成氢氧化钙的反应,化学方程式为:CaO+H2O=Ca(OH)2。
14.分解 CaO+H2O=Ca(OH)2 BC
【解析】
【详解】
(1)石灰窑中石灰石在高温条件下生成氧化钙和二氧化碳,该反应的特征是一变多,属于分解反应,故填:分解。
(2)浆池中生石灰和水反应生成氢氧化钙,其化学方程式为:CaO+H2O=Ca(OH)2。故填:CaO+H2O=Ca(OH)2。
(3)A.窑气中含有氮气、氧气、二氧化碳等,属于混合物,故选项说法错误。 B.浆池中能分离出废渣,浆池的作用之一是分离生石灰中的杂质,故选项说法正确。 C.石灰石的主要成分是碳酸钙,含有杂质,得到的轻质碳酸钙比石灰石中碳酸钙的纯度高,故选项说法正确。
15.出现蓝色沉淀 试管中冒气泡 取少量氢氧化钾于试管中,滴加无色酚酞溶液,观察到溶液变红,加入硫酸溶液变为无色,证明氢氧化钾溶液与稀硫酸发生了化学反应 反应物减少
【解析】
氢氧化钾和硫酸铜反应生成氢氧化铜蓝色沉淀和硫酸钾,氢氧化钾和氯化铵反应生成氯化钾和水和氨气,稀硫酸和氢氧化钾反应生成硫酸钾和水。
[实验过程与分析]
实验一
实验二
实验三
实验操作
实验现象
出现蓝色沉淀
试管中冒气泡
无明显现象
实验结论
氢氧化钾能与硫酸铜发
生反应
氢氧化钾能与氯化铵发
生反应
氢氧化钾不能与硫酸
发生反应
[实验反思与拓展]
①某同学认为实验三的结论不正确。他改进了该实验方案,借助于酸碱指示剂,通过明显的现象证明氢氧化钾能与硫酸发生反应。实验方案为取少量氢氧化钾于试管中,滴加无色酚酞溶液,观察到溶液变红,加入硫酸溶液变为无色,证明氢氧化钾溶液与稀硫酸发生了化学反应。
②对于无明显现象的化学反应,可通过检验有新物质生成或检验反应物减少的方法来证明物质间发生了化学反应。
【点睛】
16.Ca(OH)2+CO2=CaCO3↓+H2O 增大接触面积,加快反应速率 蛋壳中部分碳酸钙逐渐溶解,溶液中离子浓度增大,电导率增强 打开开关,拉动(或“推动”也可)注射器活塞,松开后,活塞回到原位,说明气密性良好 打开开关,将盐酸快速压入锥形瓶,关闭开关 碳酸盐与盐酸反应产生了二氧化碳气体,使瓶内压强增大 对比 能 相同条件下,使用含氟牙膏处理后的鸡蛋壳,反应能产生的气体更少,压强更小,消耗的鸡蛋壳更少
【解析】
(1)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O; (2)搅拌是为了增大接触面积,加快反应速率; (3)图1中,a-b段电导率变化的原因:蛋壳中部分碳酸钙逐渐溶解,溶液中离子浓度增大,电导率增强; (4)检验装置气密性利用装置内外的压强差检验,所以检查图2装置气密性,方法:打开开关,拉动注射器活塞,松开后,活塞回到原位,说明气密性良好,连接好装置,接下来的操作是:打开开关,将盐酸快速压入锥形瓶,关闭开关,测得压强随时间的变化如图3所 示; (5)碳酸盐和酸反应会生成二氧化碳,所以对比图3中x-y段压强增大的主要原因:碳酸盐与盐酸反应产生了二氧化碳气体,使瓶内压强增大;用“未用牙膏处理的蛋壳”重复上述实验的作用是对比; (6)根据图3的数据分析,含氟牙膏能预防龋齿,这是因为单位时间内用牙膏处理过的蛋壳产生二氧化碳较少。 故答案为:(1)Ca(OH)2+CO2=CaCO3↓+H2O; (2)增大接触面积,加快溶解速率; (3)蛋壳中部分碳酸钙逐渐溶解,溶液中离子浓度增大,电导率增强; (4)打开开关,拉动(或“推动”也可)注射器活塞,松开后,活塞回到原位,说明气密性良好;打开开关,将盐酸快速压入锥形瓶,关闭开关; (5)碳酸盐与盐酸反应产生了二氧化碳气体,使瓶内压强增大;对比; (6)能;相同条件下,使用含氟牙膏处理后的鸡蛋壳,反应能产生的气体更少,压强更小,消耗的鸡蛋壳更少。
