仁爱版化学九年级下册专题八 金属和金属材料测试题(含答案)
文档属性
| 名称 | 仁爱版化学九年级下册专题八 金属和金属材料测试题(含答案) |
|
|
| 格式 | zip | ||
| 文件大小 | 229.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 仁爱科普版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-10 00:00:00 | ||
图片预览




文档简介
专题8《金属和金属材料》测试题
一、单选题(每小题只有一个正确答案)
1.下列哪个是可回收标志( )
A. B. C. D.
2.下列物质不属于合金的是( )
A.黄铜 B.硬铝 C.金刚石 D.生铁
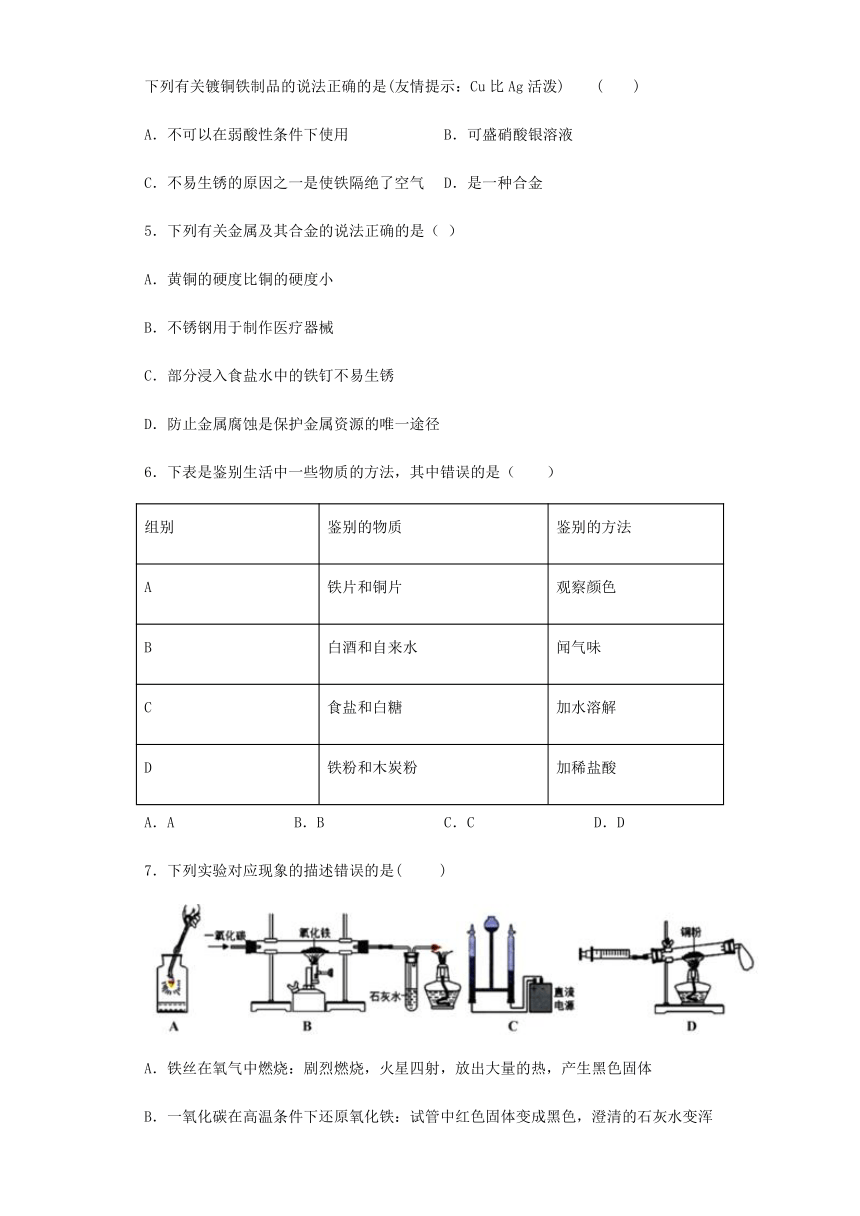
3.如图中的图象能正确反映对应的变化关系的是( )
A.向一定量的水中加入生石灰
B.向一定量的氧化铁中通入CO并持续高温
C.水的电解
D.向一定量的盐酸和氯化铁混合溶液中滴入NaOH溶液
4.铁制品在通常情况下极易生锈,制造时常常在铁制品表面电镀一层铜起防锈作用。下列有关镀铜铁制品的说法正确的是(友情提示:Cu比Ag活泼) ( )
A.不可以在弱酸性条件下使用 B.可盛硝酸银溶液
C.不易生锈的原因之一是使铁隔绝了空气 D.是一种合金
5.下列有关金属及其合金的说法正确的是( )
A.黄铜的硬度比铜的硬度小
B.不锈钢用于制作医疗器械
C.部分浸入食盐水中的铁钉不易生锈
D.防止金属腐蚀是保护金属资源的唯一途径
6.下表是鉴别生活中一些物质的方法,其中错误的是( )
组别 鉴别的物质 鉴别的方法
A 铁片和铜片 观察颜色
B 白酒和自来水 闻气味
C 食盐和白糖 加水溶解
D 铁粉和木炭粉 加稀盐酸
A.A B.B C.C D.D
7.下列实验对应现象的描述错误的是( )
A.铁丝在氧气中燃烧:剧烈燃烧,火星四射,放出大量的热,产生黑色固体
B.一氧化碳在高温条件下还原氧化铁:试管中红色固体变成黑色,澄清的石灰水变浑浊
C.电解水的实验:两个电极上产生大量的气泡,正极上产生的是氢气,负极上产生的是氧气
D.测定空气成分的实验:玻璃管内红色的固体粉末变成黑色,气体的总体积减少了约五分之一
8.化学是一门以实验为基础的科学。下列有关实验现象的描述正确的是
A.红磷在氧气中燃烧发出耀眼的白光,并产生大量的白雾
B.细铁丝在氧气中燃烧火星四射,生成四氧化三铁
C.木炭在氧气中燃烧产生白色火焰,生成黑色固体
D.某同学在做一氧化碳还原氧化铁的实验过程中,观察到红棕色粉末逐渐变黑
9.下列说法中不正确的是
A.合金的硬度一般比各成分金属小
B.用肥皂水可以区分硬水和软水
C.含有碳元素的物质不一定是有机物
D.在钢铁表面涂油可以防止生锈
10.将一定量的锌粉加入到硫酸镁和硫酸铜的混合溶液中,反应一段时间后过滤,得无色滤液和滤渣。滤渣的成分可能是
A.锌 、铜 B.镁、铜 C.锌 D.镁、锌、铜
11.下列实验操作不能达到实验目的的是
选项 实验目的 实验操作
A 鉴别真假黄金 在空气中灼烧
B 鉴别过氧化氢溶液和水 加入二氧化锰
C 分离铜粉和铁粉 用磁铁吸引
D 除去氮气中的氧气 通入澄清石灰水
A.A B.B C.C D.D
12.将金属与金属(或非金属)加热熔合在一起就能形成合金.根据下列金属的熔点、沸点,其不能形成合金的是( )
Na Cu Al Fe
熔点/℃ 97.81 1083 660 1535
沸点/℃ 882.9 2595 2467 3000
A.Cu Na B.Al Fe C.Fe Cu D.Al Na
13.下列事实和解释相符的是( )
A.CO冶炼金属--CO有可燃性 B.铝比铁耐腐蚀--铝不及铁活泼
C.气体热胀冷缩--分子大小改变 D.作气体肥料--能参与光合作用
14.金属镍(Ni)与物质X的溶液发生反应的化学方程式为:Ni+X === Cu+NiSO4 ,则下列说法错误的是
A.Ni的化合价由0价变为+2价
B.X的化学式为CuSO4
C.该反应前后原子种类没有发生改变
D.Cu的金属活动性比Ni强
15.下列除杂所选用的除杂试剂与操作方法均正确的是
选项 物质(括号内为杂质) 除杂试剂 操作方法
A CaO(CaCO3) 水 溶解、过滤
B CO2(HCl) NaOH溶液 洗气
C Cu(Fe) 过量CuCl2溶液 过滤、洗涤、干燥
D NaCl(Na2CO3) 足量稀硫酸 蒸发结晶
A.A B.B C.C D.D
二、填空题
16.(1)举出两条保护金属资源的有效途径:_____
(2)金刚石和石墨物理性质差异很大的原因是_____。
(3)保持水的化学性质的微粒是_____。
(4)在加热的条件下,一氧化碳与氧化铜发生氧化还原反应的化学方程式是_____。
17.如图是小明画的某密闭容器中某反应的微观示意图,“”和“”分别表示不同的原子.
(1)完整的该反应的微观示意图应该在反应后的方框内再填入1个__________微粒(选字母).
A. B. C. D.
(2)反应过程中,参加反应的“”与“”微粒数之比为:__________.
(3)有关该反应的下列说法正确的是___________(填字母).
A.该反应前后各元素化合价均发生了改变 B.反应前后原子种类、分子种类均不变
C.原子是化学变化中最小的微粒 D.该反应的基本反应类型属于置换反应
18.炼铁的主要原料是_________、_________、_________,表示炼铁的主要化学反应方程式是_______________________.其中___________被__________还原为铁.在实验室进行这一反应时,尾气中的有害气体可采用___________的方法除去.
19.按要求书写化学方程式。
1)有水参加的化合反应 ;
2)有水生成的分解反应 ;
3)有水参加的分解反应 ;
4)有水生成的复分解反应 。
20.铁是目前使用最广泛的金属,请回答:
(1)铁可以用来制作炊具,受热后炊具温度能较快升高,这是利用了铁的_____性;油罐车的尾部经常有一条铁链拖到地上,用来防止静电引起火灾,这是利用了铁的_________性。
(2)金属腐蚀造成的损失巨大,钢铁防腐尤为重要。下列钢铁制品的防护措施不合理的是________。
A在车船的表面喷涂油漆 B将使用后的菜刀用布擦干
C在铁制品表面镀上一层锌 D用洗涤剂把铁制品表面的油膜洗净
(3)实验室模拟炼铁的实验装置如图所示。试回答下列问题:
①写出有标号仪器的名称:a._______,b.__________。
②实验中看到A装置中的实验现象为:玻璃管中的粉末___________。
③A装置玻璃管中反应的化学方程式为______________。
④C装置的作用是____________。
三、推断题
21.已知铜在潮湿的环境中也会生绣,铜锈的主要成分俗称“铜绿”化学式[Cu2(OH)2CO3],加热时铜绿分解生成A、B、C三种常见的氧化物,下面是有关物质之间的转化关系图示。
(1)试通过分析推断,确定下列物质并写出化学式:
B_________,D_________,E________,G_______。
(2)写出下列变化的化学方程式:
C→H:________________。
C→F:_________________。
22.已知A、B、C、D、E为初三常见的化类物质,其中A、B是同一类别的物质,C、D是同一类别的物质。E是目前年产量最大的金属,“—”表示相互反应,“→”表示转化生成,部分反应物、生成物已省略。则:
(1)C的化学式为______________
(2)D—B的化学方程式为________________
四、实验题
23.某学习小组用下列装置进行CO2的制取及性质探究实验.
资料卡片:20°C时,碳酸钠在乙醇中几乎不溶解,氢氧化钠在乙醇中的溶解度为17.3g,20°C时,碳酸钠、碳酸氢钠在水中的溶解度分别为21.8g和9.6g。请根据如图回答下列问题:
(1)图中装置A是用大理石制CO2的装置,仪器a的名称是 ______ ;装置A中发生反应的化学方程式是 ______ ;在b处检验是否有CO2逸出的操作是 ______ .
(2)装置C中放有干和湿的pH试纸各一张,当通入CO2一段时间后,湿pH试纸显示pH约为6,干pH试纸显示pH仍为7,实验结论是 ______ .
(3)当通入CO2一段时间后,装置D中观察到溶液中有白色沉淀(NaHCO3)出现,则反应的化学方程式是 ______.
(4)当通入CO2一段时间后,装置E中观察到的实验现象是 ______ .
24.模拟实验是重要的实验手段之一。在实验室中模拟炼铁的原理可用下图表示:
该装置的设计有一明显不当之处,你的改进方案是_____。
(1)试写出一氧化碳和氧化铁在高温下生成铁的化学反应方程式_____;
(2)实验一段时间后,观察到B处澄清石灰水_____,A处红棕色固体逐渐变为黑色,小明将所得的黑色固体与足量的_____充分反应,观察到固体减少并有气泡冒出,说明黑色固体物质含有铁。
五、计算题
25.早在西汉时期,我国劳动人民就利用铁与硫酸铜溶液反应制取铜,称为“湿法炼铜”,若用该方法制得铜16 kg,理论上需要硫酸铜多少千克?
26.某钢铁厂日产含杂质4%的生铁1 000 t,试计算该厂每天至少需含Fe2O3 80%的赤铁矿石多少吨?
参考答案
1.C 2.C 3.D 4.C 5.B 6.C 7.C 8.D 9.A 10.A 11.D 12.A 13.D 14.D 15.C 16.放在干燥环境中、金属表面刷油漆 碳原子的排列方式不同 水分子
17.B 2:1 AC
18. 铁矿石 焦炭 石灰石 Fe2O3+3CO2Fe+3CO2 Fe2O3 CO 点燃
19.H2O+CaO=Ca(OH)2;H2CO3==H2O+CO2↑;2H2O2H2↑+O2↑;HCl+NaOH=NaCl+H2O
20.导热 导电 D 铁架台 导管 由红色变为黑色 3CO+Fe2O33CO2↑+2Fe 处理尾气,防止其污染环境
21.CuO O2 H2 Cu CO2 +Ca(OH)2 ==CaCO3↓+ H2O C + CO2 2CO
22.H2SO4 HCl+AgNO3=AgCl↓+HNO3
23.长颈漏斗 CaCO3+2HCl=CaCl2+H2O+CO2 将燃着的木条放在导气管口,观察木条是否熄灭 CO2与水反应后的溶液显酸性 Na2CO3+CO2+H2O=2NaHCO3 出现白色沉淀或浑浊
24.在装置末端增加点燃的酒精灯或气球灯尾气处理装置 变浑浊 稀盐酸或稀硫酸
25.40 kg
26.生铁中纯铁的质量为1 000 t×(1-4%)=960 t
设需赤铁矿石的质量为x。
Fe2O3+3CO2Fe+3CO2
160 112
80%×x 960 t
= x=1 714.3 t
答:该厂每天至少需含Fe2O3 80%的赤铁矿石1 714.3 t。
