课题2 原子的构成 第2课时 原子核外电子的排布 课件(21张PPT)
文档属性
| 名称 | 课题2 原子的构成 第2课时 原子核外电子的排布 课件(21张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-12 00:00:00 | ||
图片预览



文档简介
(共21张PPT)
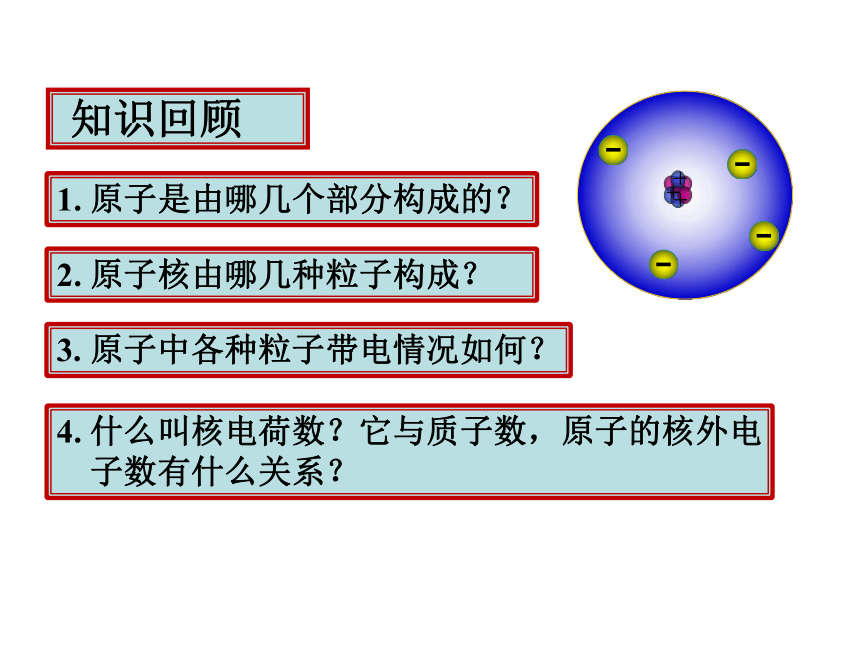
知识回顾
1. 原子是由哪几个部分构成的?
2. 原子核由哪几种粒子构成?
3. 原子中各种粒子带电情况如何?
4. 什么叫核电荷数?它与质子数,原子的核外电
子数有什么关系?
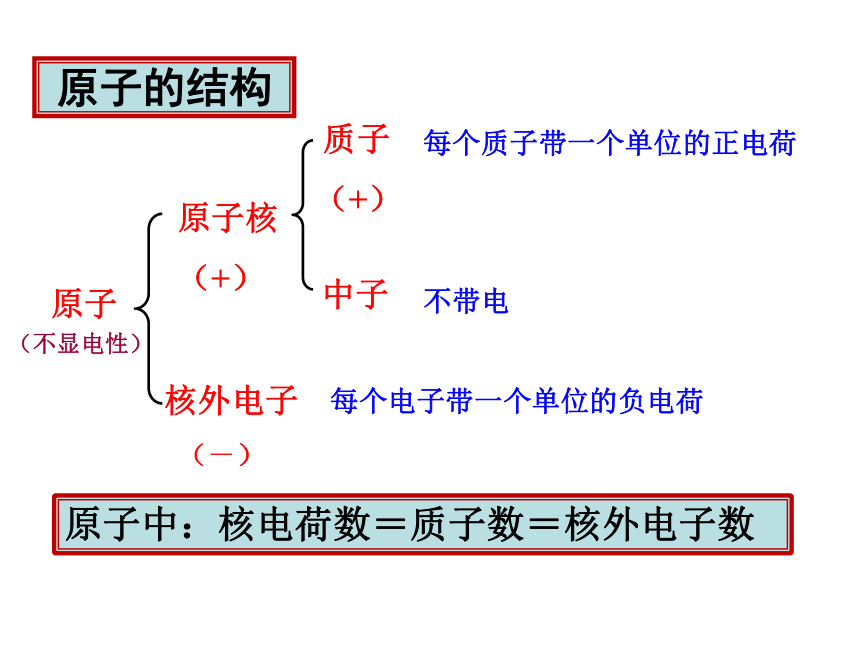
原子的结构
原子
每个质子带一个单位的正电荷
不带电
每个电子带一个单位的负电荷
原子中:核电荷数=质子数=核外电子数
(不显电性)
虽然空间很大,但我和我的同伴总想挣脱原子核的吸引。可是原子核这个小老头很有能耐,虽然只占原子的一丁点空间,里面却由质子和中子构成。中子不带电,质子带正电,正好把我身上的负电深深地吸引… 哎!大家猜一猜,我和我的同伴在原子里除了高速运动还进行怎样的运动呢?
【情景激活】
我是一个小小的电子,我在原子里围绕着正中心的原子核不停地高速运动。
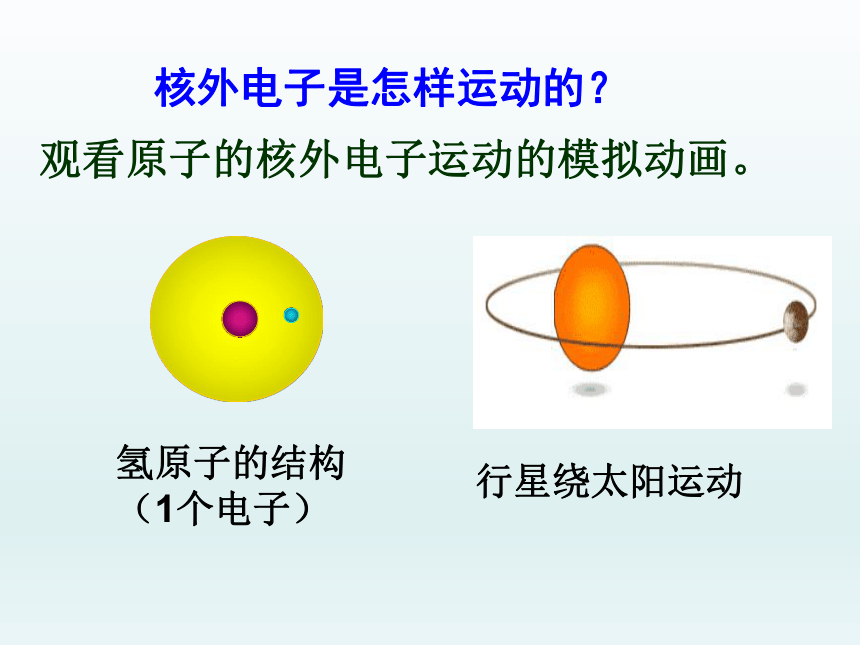
核外电子是怎样运动的?
观看原子的核外电子运动的模拟动画。
氢原子的结构
(1个电子)
行星绕太阳运动
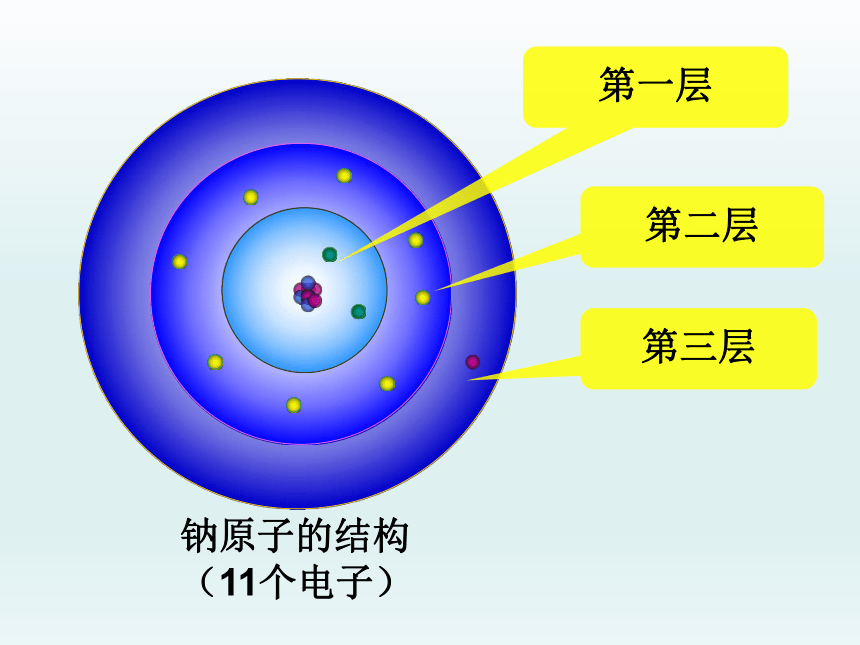
第一层
第二层
第三层
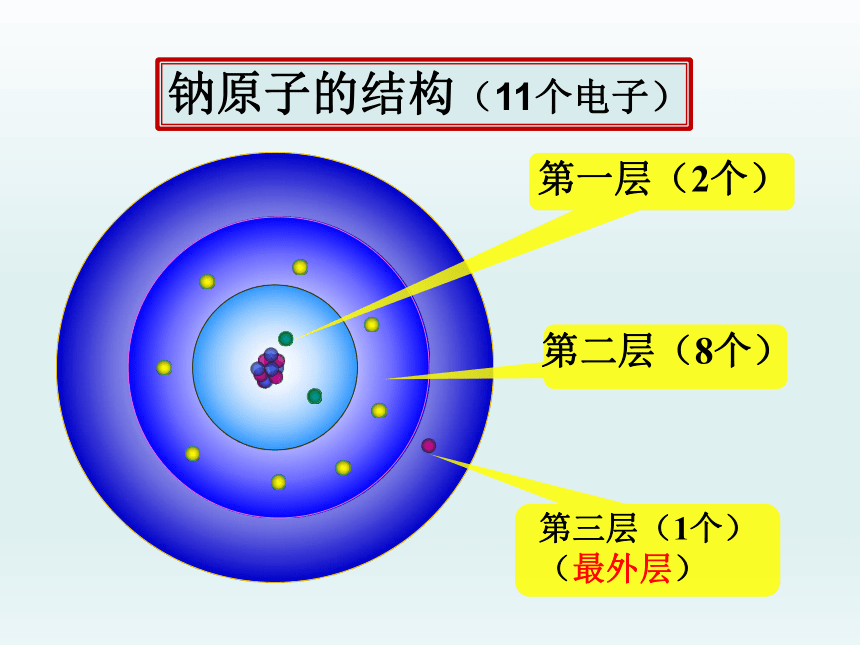
钠原子的结构
(11个电子)
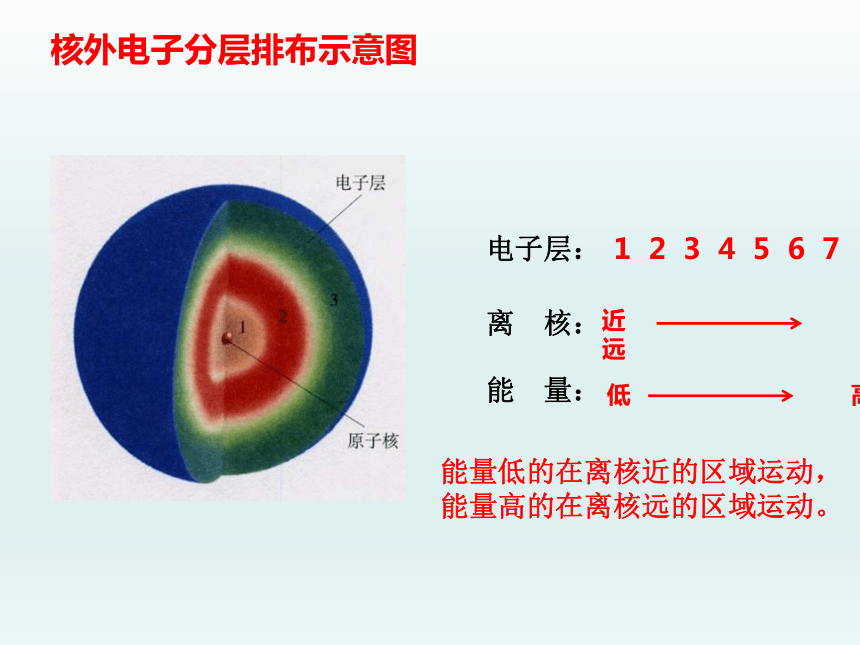
1 2 3 4 5 6 7
能量低的在离核近的区域运动,
能量高的在离核远的区域运动。
电子层:
离 核:
能 量:
第一层(2个)
第二层(8个)
第三层(1个)
(最外层)
钠原子的结构(11个电子)
+11
原子结构示意图:
电子层
原子核
质子数
各电子层上的电子数
原子核带正电
最外层电子数
2 8 1
上图为硫原子的原子结构示意图,该原子的核电荷数为 ,核外有 个电子层,第二层上有 个电子,最外电子层上有 个电子。
16
3
8
6
第一层(2个)
第二层(6个)
(最外层)
【亲手尝试】根据氧原子的结构图画出结构示意图
探究一:原子核外电子的排布有什么规律?
核外电子的分层排布规律
(3)最外层最多排8电子.
②核外电子总是尽先排布在能量稍低的电子层里.
(1)第一层最多排2电子.
(2)第二层最多排8电子.
(若第一层为最外层最多排2电子)
注:①每层最多容纳电子数为2n2个
2、8、8规则
氢 H 氦He
锂 Li 铍 Be 硼 B 碳 C 氮N 氧O 氟 F 氖Ne
钠Na 镁Mg 铝Al 硅Si 磷P 硫 S 氯Cl 氩Ar
金属原子
非金属原子
稀有气体原子
这三大类元素的原子最外层电子数有什么特点?
探究二:
金属元素的原子最外层电子数一般少于4个
非金属元素的原子最外层电子数一般多于4个
稀有气体元素的原子最外层电子数为8个(He为2)
结论:
【稳定结构】像稀有气体元素原子这样的结构 叫8电子稳定结构。
若只有一个电子层,则2电子是稳定结构(如:He)。
化学反应中原子有趋向于稳定结构的特点。那什么样的结构才是原子的稳定结构呢?
氢 H 氦He
锂 Li 铍 Be 硼 B 碳 C 氮N 氧O 氟 F 氖Ne
钠Na 镁Mg 铝Al 硅Si 磷P 硫 S 氯Cl 氩Ar
金属原子
非金属原子
稀有气体原子
一般少于4
易失电子
不稳定
较活泼
一般多于4
不稳定
易得电子
较活泼
较稳定
小结:三类不同元素的原子结构特点与化学性质的关系
【结论】元素的化学性质与原子结构尤其原子最外层电子数有密切关系。一般来说,最外层电子数相同,元素的化学性质相似.
8(He为2)
稳 定
不易得失
元素分类 最外层
电子数 原子结构的稳定性 电子的 得失 化学性质
金属
非金属
稀有气体
电子层 1,2,3,4,5,6,7
离 核:近 远
能 量:低 高
电子的分层排布规律2,8,8
原子结构与化学性质的关系
课堂小结
原子核外电子分层排布
知识回顾
1. 原子是由哪几个部分构成的?
2. 原子核由哪几种粒子构成?
3. 原子中各种粒子带电情况如何?
4. 什么叫核电荷数?它与质子数,原子的核外电
子数有什么关系?
原子的结构
原子
每个质子带一个单位的正电荷
不带电
每个电子带一个单位的负电荷
原子中:核电荷数=质子数=核外电子数
(不显电性)
虽然空间很大,但我和我的同伴总想挣脱原子核的吸引。可是原子核这个小老头很有能耐,虽然只占原子的一丁点空间,里面却由质子和中子构成。中子不带电,质子带正电,正好把我身上的负电深深地吸引… 哎!大家猜一猜,我和我的同伴在原子里除了高速运动还进行怎样的运动呢?
【情景激活】
我是一个小小的电子,我在原子里围绕着正中心的原子核不停地高速运动。
核外电子是怎样运动的?
观看原子的核外电子运动的模拟动画。
氢原子的结构
(1个电子)
行星绕太阳运动
第一层
第二层
第三层
钠原子的结构
(11个电子)
1 2 3 4 5 6 7
能量低的在离核近的区域运动,
能量高的在离核远的区域运动。
电子层:
离 核:
能 量:
第一层(2个)
第二层(8个)
第三层(1个)
(最外层)
钠原子的结构(11个电子)
+11
原子结构示意图:
电子层
原子核
质子数
各电子层上的电子数
原子核带正电
最外层电子数
2 8 1
上图为硫原子的原子结构示意图,该原子的核电荷数为 ,核外有 个电子层,第二层上有 个电子,最外电子层上有 个电子。
16
3
8
6
第一层(2个)
第二层(6个)
(最外层)
【亲手尝试】根据氧原子的结构图画出结构示意图
探究一:原子核外电子的排布有什么规律?
核外电子的分层排布规律
(3)最外层最多排8电子.
②核外电子总是尽先排布在能量稍低的电子层里.
(1)第一层最多排2电子.
(2)第二层最多排8电子.
(若第一层为最外层最多排2电子)
注:①每层最多容纳电子数为2n2个
2、8、8规则
氢 H 氦He
锂 Li 铍 Be 硼 B 碳 C 氮N 氧O 氟 F 氖Ne
钠Na 镁Mg 铝Al 硅Si 磷P 硫 S 氯Cl 氩Ar
金属原子
非金属原子
稀有气体原子
这三大类元素的原子最外层电子数有什么特点?
探究二:
金属元素的原子最外层电子数一般少于4个
非金属元素的原子最外层电子数一般多于4个
稀有气体元素的原子最外层电子数为8个(He为2)
结论:
【稳定结构】像稀有气体元素原子这样的结构 叫8电子稳定结构。
若只有一个电子层,则2电子是稳定结构(如:He)。
化学反应中原子有趋向于稳定结构的特点。那什么样的结构才是原子的稳定结构呢?
氢 H 氦He
锂 Li 铍 Be 硼 B 碳 C 氮N 氧O 氟 F 氖Ne
钠Na 镁Mg 铝Al 硅Si 磷P 硫 S 氯Cl 氩Ar
金属原子
非金属原子
稀有气体原子
一般少于4
易失电子
不稳定
较活泼
一般多于4
不稳定
易得电子
较活泼
较稳定
小结:三类不同元素的原子结构特点与化学性质的关系
【结论】元素的化学性质与原子结构尤其原子最外层电子数有密切关系。一般来说,最外层电子数相同,元素的化学性质相似.
8(He为2)
稳 定
不易得失
元素分类 最外层
电子数 原子结构的稳定性 电子的 得失 化学性质
金属
非金属
稀有气体
电子层 1,2,3,4,5,6,7
离 核:近 远
能 量:低 高
电子的分层排布规律2,8,8
原子结构与化学性质的关系
课堂小结
原子核外电子分层排布
同课章节目录
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的构成
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题1 质量守恒定律
- 课题2 如何正确书写化学方程式
- 课题3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动3 燃烧的条件
- 旧版目录
- 第五单元 物质组成的表示
- 课题2 燃料和热量
- 课题3 使用燃料对环境的影响
