人教版初中化学九年级下 10.1常见的酸和碱(共32张PPT)
文档属性
| 名称 | 人教版初中化学九年级下 10.1常见的酸和碱(共32张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 9.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-13 00:00:00 | ||
图片预览









文档简介
(共32张PPT)
课题1 常见的酸和碱
教学目标:
1.学会用酸碱指示剂来检验溶液的酸碱性
2.知道浓盐酸和浓硫酸的物理性质
3.了解浓硫酸的特性
4.知道盐酸硫酸的用途
重点:
浓盐酸,浓硫酸的特性;浓硫酸的稀释
难点:
浓硫酸的吸水性和腐蚀性
1.生活中的酸有哪些?
“酸”一词从有酸味的酒而来。最早,在制酒的时候,有时把比较珍贵的酒放在窖中保存,在微生物的作用下,产生了酸。
2.生活中的碱有哪些?
“碱”一词在阿拉伯语中表示灰。人们将草木灰放到水中,利用灰汁洗浴、印染等。
生活中的酸有:食醋中的醋酸(CH3COOH); 水果中的果酸,如杨梅很酸(望梅止渴)、苹果中有苹果酸,柠檬、柑桔等水果中有柠檬酸等。
生活中的碱有:石灰水中有氢氧化钙,炉具清洁剂中含有氢氧化钠,它们都是碱。吃的皮蛋中也有碱。
3.常见的酸有盐酸(HCl)、硫酸(H2SO4)、硝酸(HNO3)、还有磷酸(H3PO4)、碳酸(H2CO3)、醋酸(CH3COOH)等。
4.常见的碱有氢氧化钠(NaOH)、氢氧化钙[Ca(OH)2]、氢氧化钾(KOH)、氢氧化铜[Cu(OH)2]、氨水(NH3·H2O)等。
从名称上看它们最后一个字都是“酸”,从结构上看都含有氢元素。
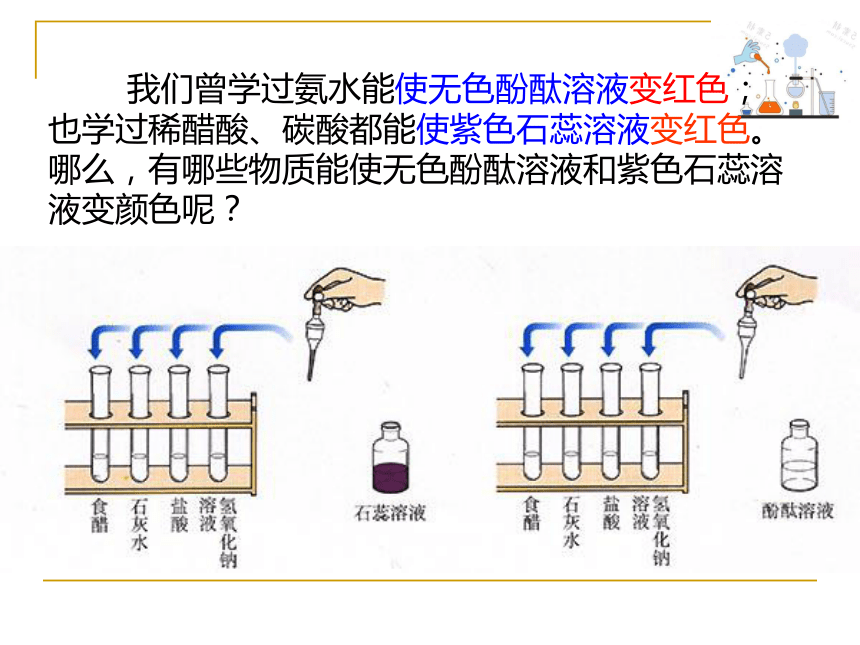
我们曾学过氨水能使无色酚酞溶液变红色;也学过稀醋酸、碳酸都能使紫色石蕊溶液变红色。哪么,有哪些物质能使无色酚酞溶液和紫色石蕊溶液变颜色呢?
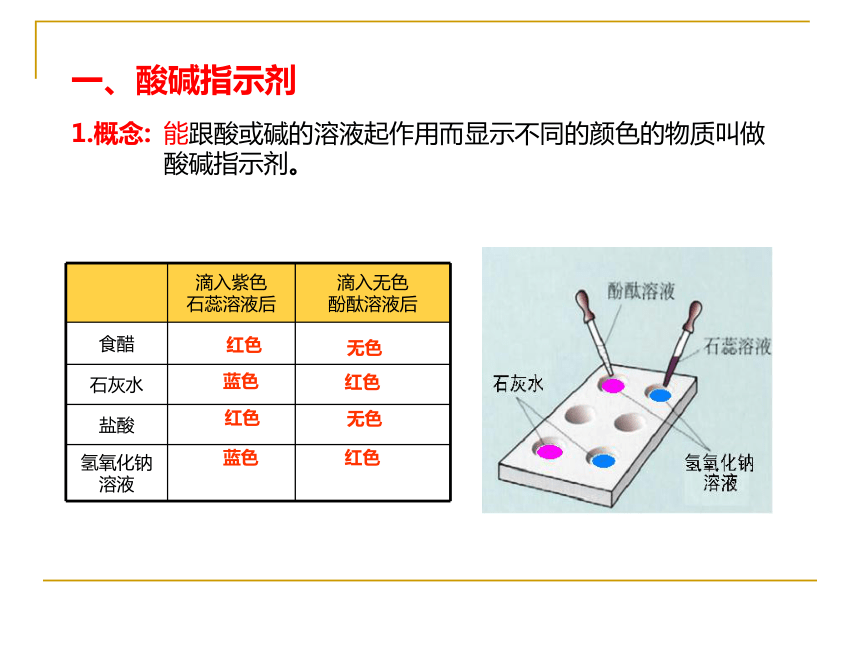
1.概念:
能跟酸或碱的溶液起作用而显示不同的颜色的物质叫做酸碱指示剂。
一、酸碱指示剂
滴入紫色
石蕊溶液后 滴入无色
酚酞溶液后
食醋
石灰水
盐酸
氢氧化钠溶液
食醋和盐酸是酸溶液。
石灰水和氢氧化钠溶液是碱溶液。
石蕊试纸的使用方法:
将石蕊试纸放在表面皿上,用玻璃棒蘸取试样溶液沾在石蕊试纸上,然后观察试纸颜色的变化。
指示剂注意事项:
1.酸碱指示剂遇酸,碱变色是化学变化,变色的物质是 指示剂,而不是酸或碱.
2.不溶于水的酸或碱不能使指示剂变色,如氢氧化铜.
3.只要在酸碱溶液中显示不同的颜色,就可作酸碱指示剂.
4.某溶液中滴入无色酚酞中不变色,该溶液不一定是酸性溶液,也可能是中性溶液,如氯化钠溶液.
5.简记方法:酸 蕊红酚蓝 碱 蕊无酚红
误区警示:
1.碱溶液一定显碱性,碱性溶液不一定是碱溶液,如NaOH溶液和Na2CO3溶液
2.酸溶液一定显酸性,酸性溶液不一定是酸溶液,如盐酸溶液和CuSO4溶液
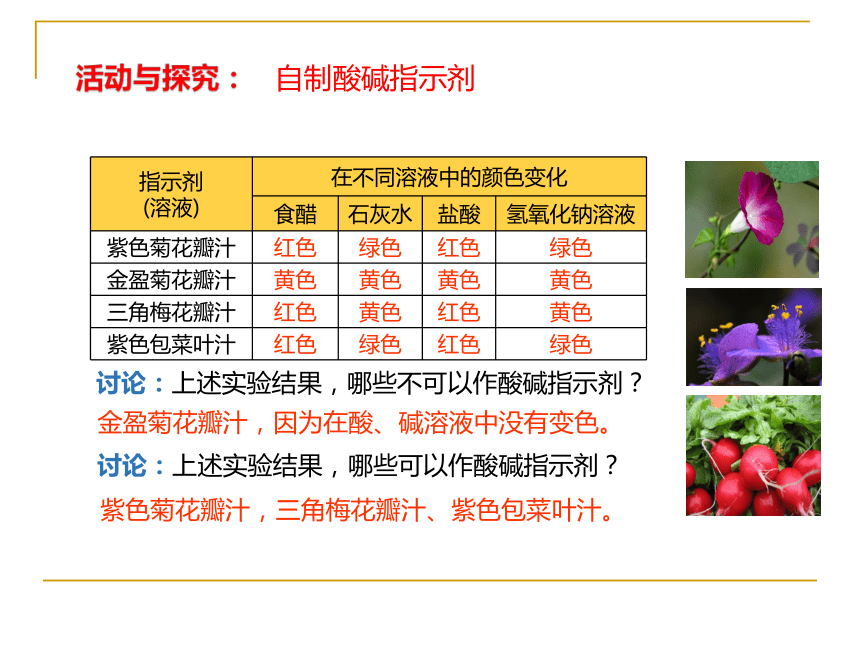
自制酸碱指示剂
⑴取几种植物的花瓣或果实(如牵牛花、月季花、紫卷心菜、胡萝卜等),分别在研钵中捣烂,加入酒精(乙醇与水的体积比为1∶1)浸泡;
⑵用纱布将浸泡出的汁液过滤或挤出,得到指示剂;
⑶试验指示剂在上述4种溶液中的颜色变化。
指示剂
(溶液) 在不同溶液中的颜色变化
食醋 石灰水 盐酸 氢氧化钠溶液
讨论:上述实验结果,哪些不可以作酸碱指示剂?
讨论:上述实验结果,哪些可以作酸碱指示剂?
金盈菊花瓣汁,因为在酸、碱溶液中没有变色。
紫色菊花瓣汁,三角梅花瓣汁、紫色包菜叶汁。
自制酸碱指示剂
指示剂
(溶液) 在不同溶液中的颜色变化
食醋 石灰水 盐酸 氢氧化钠溶液
紫色菊花瓣汁 红色 绿色 红色 绿色
金盈菊花瓣汁 黄色 黄色 黄色 黄色
三角梅花瓣汁 红色 黄色 红色 黄色
紫色包菜叶汁 红色 绿色 红色 绿色
巩固练习:
1.盐酸是酸溶液,它使紫色石蕊溶液变______,
遇无色酚酞溶液_______。
2.氢氧化钠溶液是碱溶液,它使石蕊溶液变____,使酚酞溶液变______。
红色
仍无色
蓝色
红色
3.紫色石蕊溶液滴入碱溶液(如石灰水)变_____,
将紫色石蕊溶液滴入酸溶液(如稀硫酸)变______。
4.无色酚酞溶液滴入碱溶液(如石灰水)变____,
将无色酚酞溶液滴入酸溶液(如稀硫酸)显_____。
蓝色
红色
红色
无色
注意:是指示剂在变色,不是酸溶液和碱溶液在变色。如说石蕊溶液使盐酸变红色的说法是错误的。
巩固练习:
5.下表是四种花的提取液实验(酒精用于提取花中的色素)
⑴上表中能做酸碱指示剂的花汁是____________ ;
⑵将厨房中的少量白醋滴入大红花的花汁中,可以看到的现象是_________;
⑶若将紫罗兰提取液滴入氯化钠溶液中,则可看到的现象是____________。
大红花、紫罗兰
橙色
紫色
酒精中 酸溶液中 碱溶液中
大红花 粉红色 橙色 绿色
紫罗兰 紫色 红色 蓝色
万寿菊 黄色 黄色 黄色
巩固练习:
6.能使紫色石蕊溶液变蓝的溶液,它能使无色酚酞溶液 ( )
A.变红色 B.变蓝色 C.呈无色 D.变紫色
A
7.下列物质的水溶液能使紫色石蕊溶液变红色的是 ( )
A.NaCl B.NH3 C.HCl D.NaOH
C
盐类、中性
变成氨水
后是碱类
盐酸是酸类
是碱类
巩固练习:
8.化学兴趣学习小组的同学采集了三种植物的花瓣,将它们分别放在研钵中研磨,加入酒精充分浸泡后过滤,得到了三种溶液。将三种溶液分别滴加到下列液体中,得到以下信息:
试回答: ⑴如果用所制得的溶液检验花盆中土壤的酸碱性,你会建议选择__________花的酒精溶液来作酸碱指示剂;在上述三种酒精溶液中,酒精属于_________。(填“溶质”或“溶剂”)
⑵如果得知花盆中的土壤显酸性,某种花卉适合微碱性条件下生长,你会建议选择上表中的__________来进行改良。
玫瑰
溶剂
石灰水
花的种类 所制成溶液的颜色 有关试剂呈现的颜色
白醋 蒸馏水 石灰水
玫瑰 粉红色 红色 粉红色 绿色
黄菊 黄色 黄色 黄色 黄色
雏菊 无色 无色 无色 黄色
1.常见的酸:盐酸(HCl)、硫酸(H2SO4)、硝酸(HNO3)、磷酸(H3PO4)、碳酸(H2CO3)、醋酸(CH3COOH,简写为HAc)等。
从名称上看它们最后一个字都是“酸”,
从结构上看都含有氢元素。
二、常见的酸
【实验 】
(1)观察盐酸、硫酸的颜色、状态;
(2)分别打开盛有盐酸、硫酸的试剂瓶的瓶盖,观察现象并闻气味。
1.常见的酸
浓盐酸(HCl)HCl气体的水溶液
无色液体
瓶口有白雾,有挥发性
有强烈的刺激性气味、有酸味
浓盐酸
颜色状态
打开瓶盖后的现象
气味
浓硫酸:
无色、粘稠、油状的液体
无明显现象,无挥发性
无刺激性气味
浓硫酸
颜色状态
打开瓶盖
气味
2.酸的物理性质
HCl
有刺激性气味
瓶口冒白雾
有
无
有
密封
H2SO4
无气味
无
有
有
密封
不易挥发
浓盐酸 浓硫酸
溶质
气味
打开试剂瓶
挥发性
吸水性
腐蚀性
保存方法
3 .浓盐酸的特性
① 浓盐酸有强挥发性,为物理性质
② HCl气体极易溶于水(1∶500), 质量分数〈38%
1.为何制备H2、CO2不用浓盐酸?
2.为何制备的CO2气体不能使Ca(OH)2变浑浊?
思考:
制得的气体不纯,有HCl杂质气体
CO2中的杂质气体HCl和Ca(OH)2反应成易溶
于水的CaCl2,而不是不溶于水的CaCO3.
思考:
3.浓HCl瓶塞打开,质量如何变化?质量分数如何变化?
4.不饱和溶液变为饱和溶液可采用蒸发溶剂的方式,盐酸也可以吗?
溶质HCl挥发,溶质,溶液质量都减少,
质量分数减少
不可以,溶质HCl易挥发,加热溶质挥发
速度大于溶剂蒸发速度
4 .浓硫酸的特性
(1)吸水性
为物理性质
(2)腐蚀性(脱水性)
为化学性质
(3)溶于水放热,为物理性质
(4)强氧化性
为化学性质
用途:可作气体干燥剂
常期暴露于空气中:溶质质量分数减小
浓硫酸能将有机物中的氢和氧元素按水的组成比脱去
加热时,浓硫酸能与大多数金属反应,
但都没有氢气生成。
4 .浓硫酸的特性
(1)吸水性
(2)脱水性
(3)溶于水放热
(4)强氧化性
用途:可作气体干燥剂
常期暴露于空气中:溶质质量分数减小
浓硫酸能将有机物中的氢和
氧元素按水的组成比脱去
加热时,浓硫酸能与大多数金属反应,
但都没有氢气生成。
浓硫酸脱水性
5.浓硫酸的稀释
将浓硫酸沿烧杯壁缓慢地注入盛有水的烧杯里,
发热或烫
浓硫酸溶于水放热
属于物理变化
用玻璃棒不断搅动,并用手接触烧杯外壁。
“酸入水”
“不断搅”
稀释口诀:
酸入水、沿杯壁
缓慢注、不断搅
手的感觉
分 析
1.你知道稀释浓硫酸时为什么不能将水倒进
浓硫酸里,而是要将浓硫酸沿着器壁慢慢注
入水中,而且还不断搅拌吗?
应立即用大量水冲洗,然后涂上3%~5%的碳
酸氢钠溶液。
2.如果不慎将浓硫酸沾到皮肤或衣服上,应如何处理?
浓硫酸溶于水放出大量热,溶于水暴沸,不断搅拌,是为了降低温度
思考:
6、酸的用途
在实验室和化工生产中常用的酸还
有硝酸HNO3,醋酸CH3COOH等.
另外,生活中常见的许多物质中也
含有酸.
两种酸 酸的用途
盐 酸
HCl 重要的化工产品;用于金属表面除锈、制造药物(如盐酸麻黄素、氯化锌)等;人体胃液中有盐酸,可帮助消化。
硫 酸
H2SO4 重要的化工原料。用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等。
浓硫酸有吸水性,在实验室中常用它做干燥剂。
1.盐酸与硫酸的比较
巩固练习:
浓硫酸 浓盐酸
溶质的化学式 HCl H2SO4
颜色 无色 无色
状态 水状 油状
气味 刺激性气味 无味
密度(与水比较) 大于水 大于水
打开瓶口的现象 瓶口有白雾生成 无现象
其它 挥发性 吸水性,腐蚀性
巩固练习:
2.按下图所示的装置打开分液漏斗的活塞,让水滴入锥形瓶中,可以看到锥形瓶中出现______、的现象,同时在U型管中_____________。这个事实告诉我们:为了防止发生事故。在稀释浓硫酸时,一定要将浓硫酸沿着器壁慢慢注入水中,并不断搅动。
1.某学生在化学晚会上表演如下下魔术:用毛笔蘸取一种无色液体在一张白纸上书写了“化学魔术”四个字,然后再喷上一种无色液体,白纸上立即出现了红色的“化学魔术”四个字。该学生先后所用的无色液体可能是 ( )
A.紫色石蕊溶液和盐酸 B.氢氧化钠溶液和盐酸
C.无色酚酞溶液和盐酸 D.无色酚酞溶液和氢氧化钠溶液
D
沸腾
液面乙高甲低
课外小实验:
将两朵红色或紫色的鲜花分别插入白醋的稀溶液和石灰水中,注意每天观察鲜花并更换溶液。几天后鲜花有什么变化?
课后作业:
完成导学75-79
课题1 常见的酸和碱
教学目标:
1.学会用酸碱指示剂来检验溶液的酸碱性
2.知道浓盐酸和浓硫酸的物理性质
3.了解浓硫酸的特性
4.知道盐酸硫酸的用途
重点:
浓盐酸,浓硫酸的特性;浓硫酸的稀释
难点:
浓硫酸的吸水性和腐蚀性
1.生活中的酸有哪些?
“酸”一词从有酸味的酒而来。最早,在制酒的时候,有时把比较珍贵的酒放在窖中保存,在微生物的作用下,产生了酸。
2.生活中的碱有哪些?
“碱”一词在阿拉伯语中表示灰。人们将草木灰放到水中,利用灰汁洗浴、印染等。
生活中的酸有:食醋中的醋酸(CH3COOH); 水果中的果酸,如杨梅很酸(望梅止渴)、苹果中有苹果酸,柠檬、柑桔等水果中有柠檬酸等。
生活中的碱有:石灰水中有氢氧化钙,炉具清洁剂中含有氢氧化钠,它们都是碱。吃的皮蛋中也有碱。
3.常见的酸有盐酸(HCl)、硫酸(H2SO4)、硝酸(HNO3)、还有磷酸(H3PO4)、碳酸(H2CO3)、醋酸(CH3COOH)等。
4.常见的碱有氢氧化钠(NaOH)、氢氧化钙[Ca(OH)2]、氢氧化钾(KOH)、氢氧化铜[Cu(OH)2]、氨水(NH3·H2O)等。
从名称上看它们最后一个字都是“酸”,从结构上看都含有氢元素。
我们曾学过氨水能使无色酚酞溶液变红色;也学过稀醋酸、碳酸都能使紫色石蕊溶液变红色。哪么,有哪些物质能使无色酚酞溶液和紫色石蕊溶液变颜色呢?
1.概念:
能跟酸或碱的溶液起作用而显示不同的颜色的物质叫做酸碱指示剂。
一、酸碱指示剂
滴入紫色
石蕊溶液后 滴入无色
酚酞溶液后
食醋
石灰水
盐酸
氢氧化钠溶液
食醋和盐酸是酸溶液。
石灰水和氢氧化钠溶液是碱溶液。
石蕊试纸的使用方法:
将石蕊试纸放在表面皿上,用玻璃棒蘸取试样溶液沾在石蕊试纸上,然后观察试纸颜色的变化。
指示剂注意事项:
1.酸碱指示剂遇酸,碱变色是化学变化,变色的物质是 指示剂,而不是酸或碱.
2.不溶于水的酸或碱不能使指示剂变色,如氢氧化铜.
3.只要在酸碱溶液中显示不同的颜色,就可作酸碱指示剂.
4.某溶液中滴入无色酚酞中不变色,该溶液不一定是酸性溶液,也可能是中性溶液,如氯化钠溶液.
5.简记方法:酸 蕊红酚蓝 碱 蕊无酚红
误区警示:
1.碱溶液一定显碱性,碱性溶液不一定是碱溶液,如NaOH溶液和Na2CO3溶液
2.酸溶液一定显酸性,酸性溶液不一定是酸溶液,如盐酸溶液和CuSO4溶液
自制酸碱指示剂
⑴取几种植物的花瓣或果实(如牵牛花、月季花、紫卷心菜、胡萝卜等),分别在研钵中捣烂,加入酒精(乙醇与水的体积比为1∶1)浸泡;
⑵用纱布将浸泡出的汁液过滤或挤出,得到指示剂;
⑶试验指示剂在上述4种溶液中的颜色变化。
指示剂
(溶液) 在不同溶液中的颜色变化
食醋 石灰水 盐酸 氢氧化钠溶液
讨论:上述实验结果,哪些不可以作酸碱指示剂?
讨论:上述实验结果,哪些可以作酸碱指示剂?
金盈菊花瓣汁,因为在酸、碱溶液中没有变色。
紫色菊花瓣汁,三角梅花瓣汁、紫色包菜叶汁。
自制酸碱指示剂
指示剂
(溶液) 在不同溶液中的颜色变化
食醋 石灰水 盐酸 氢氧化钠溶液
紫色菊花瓣汁 红色 绿色 红色 绿色
金盈菊花瓣汁 黄色 黄色 黄色 黄色
三角梅花瓣汁 红色 黄色 红色 黄色
紫色包菜叶汁 红色 绿色 红色 绿色
巩固练习:
1.盐酸是酸溶液,它使紫色石蕊溶液变______,
遇无色酚酞溶液_______。
2.氢氧化钠溶液是碱溶液,它使石蕊溶液变____,使酚酞溶液变______。
红色
仍无色
蓝色
红色
3.紫色石蕊溶液滴入碱溶液(如石灰水)变_____,
将紫色石蕊溶液滴入酸溶液(如稀硫酸)变______。
4.无色酚酞溶液滴入碱溶液(如石灰水)变____,
将无色酚酞溶液滴入酸溶液(如稀硫酸)显_____。
蓝色
红色
红色
无色
注意:是指示剂在变色,不是酸溶液和碱溶液在变色。如说石蕊溶液使盐酸变红色的说法是错误的。
巩固练习:
5.下表是四种花的提取液实验(酒精用于提取花中的色素)
⑴上表中能做酸碱指示剂的花汁是____________ ;
⑵将厨房中的少量白醋滴入大红花的花汁中,可以看到的现象是_________;
⑶若将紫罗兰提取液滴入氯化钠溶液中,则可看到的现象是____________。
大红花、紫罗兰
橙色
紫色
酒精中 酸溶液中 碱溶液中
大红花 粉红色 橙色 绿色
紫罗兰 紫色 红色 蓝色
万寿菊 黄色 黄色 黄色
巩固练习:
6.能使紫色石蕊溶液变蓝的溶液,它能使无色酚酞溶液 ( )
A.变红色 B.变蓝色 C.呈无色 D.变紫色
A
7.下列物质的水溶液能使紫色石蕊溶液变红色的是 ( )
A.NaCl B.NH3 C.HCl D.NaOH
C
盐类、中性
变成氨水
后是碱类
盐酸是酸类
是碱类
巩固练习:
8.化学兴趣学习小组的同学采集了三种植物的花瓣,将它们分别放在研钵中研磨,加入酒精充分浸泡后过滤,得到了三种溶液。将三种溶液分别滴加到下列液体中,得到以下信息:
试回答: ⑴如果用所制得的溶液检验花盆中土壤的酸碱性,你会建议选择__________花的酒精溶液来作酸碱指示剂;在上述三种酒精溶液中,酒精属于_________。(填“溶质”或“溶剂”)
⑵如果得知花盆中的土壤显酸性,某种花卉适合微碱性条件下生长,你会建议选择上表中的__________来进行改良。
玫瑰
溶剂
石灰水
花的种类 所制成溶液的颜色 有关试剂呈现的颜色
白醋 蒸馏水 石灰水
玫瑰 粉红色 红色 粉红色 绿色
黄菊 黄色 黄色 黄色 黄色
雏菊 无色 无色 无色 黄色
1.常见的酸:盐酸(HCl)、硫酸(H2SO4)、硝酸(HNO3)、磷酸(H3PO4)、碳酸(H2CO3)、醋酸(CH3COOH,简写为HAc)等。
从名称上看它们最后一个字都是“酸”,
从结构上看都含有氢元素。
二、常见的酸
【实验 】
(1)观察盐酸、硫酸的颜色、状态;
(2)分别打开盛有盐酸、硫酸的试剂瓶的瓶盖,观察现象并闻气味。
1.常见的酸
浓盐酸(HCl)HCl气体的水溶液
无色液体
瓶口有白雾,有挥发性
有强烈的刺激性气味、有酸味
浓盐酸
颜色状态
打开瓶盖后的现象
气味
浓硫酸:
无色、粘稠、油状的液体
无明显现象,无挥发性
无刺激性气味
浓硫酸
颜色状态
打开瓶盖
气味
2.酸的物理性质
HCl
有刺激性气味
瓶口冒白雾
有
无
有
密封
H2SO4
无气味
无
有
有
密封
不易挥发
浓盐酸 浓硫酸
溶质
气味
打开试剂瓶
挥发性
吸水性
腐蚀性
保存方法
3 .浓盐酸的特性
① 浓盐酸有强挥发性,为物理性质
② HCl气体极易溶于水(1∶500), 质量分数〈38%
1.为何制备H2、CO2不用浓盐酸?
2.为何制备的CO2气体不能使Ca(OH)2变浑浊?
思考:
制得的气体不纯,有HCl杂质气体
CO2中的杂质气体HCl和Ca(OH)2反应成易溶
于水的CaCl2,而不是不溶于水的CaCO3.
思考:
3.浓HCl瓶塞打开,质量如何变化?质量分数如何变化?
4.不饱和溶液变为饱和溶液可采用蒸发溶剂的方式,盐酸也可以吗?
溶质HCl挥发,溶质,溶液质量都减少,
质量分数减少
不可以,溶质HCl易挥发,加热溶质挥发
速度大于溶剂蒸发速度
4 .浓硫酸的特性
(1)吸水性
为物理性质
(2)腐蚀性(脱水性)
为化学性质
(3)溶于水放热,为物理性质
(4)强氧化性
为化学性质
用途:可作气体干燥剂
常期暴露于空气中:溶质质量分数减小
浓硫酸能将有机物中的氢和氧元素按水的组成比脱去
加热时,浓硫酸能与大多数金属反应,
但都没有氢气生成。
4 .浓硫酸的特性
(1)吸水性
(2)脱水性
(3)溶于水放热
(4)强氧化性
用途:可作气体干燥剂
常期暴露于空气中:溶质质量分数减小
浓硫酸能将有机物中的氢和
氧元素按水的组成比脱去
加热时,浓硫酸能与大多数金属反应,
但都没有氢气生成。
浓硫酸脱水性
5.浓硫酸的稀释
将浓硫酸沿烧杯壁缓慢地注入盛有水的烧杯里,
发热或烫
浓硫酸溶于水放热
属于物理变化
用玻璃棒不断搅动,并用手接触烧杯外壁。
“酸入水”
“不断搅”
稀释口诀:
酸入水、沿杯壁
缓慢注、不断搅
手的感觉
分 析
1.你知道稀释浓硫酸时为什么不能将水倒进
浓硫酸里,而是要将浓硫酸沿着器壁慢慢注
入水中,而且还不断搅拌吗?
应立即用大量水冲洗,然后涂上3%~5%的碳
酸氢钠溶液。
2.如果不慎将浓硫酸沾到皮肤或衣服上,应如何处理?
浓硫酸溶于水放出大量热,溶于水暴沸,不断搅拌,是为了降低温度
思考:
6、酸的用途
在实验室和化工生产中常用的酸还
有硝酸HNO3,醋酸CH3COOH等.
另外,生活中常见的许多物质中也
含有酸.
两种酸 酸的用途
盐 酸
HCl 重要的化工产品;用于金属表面除锈、制造药物(如盐酸麻黄素、氯化锌)等;人体胃液中有盐酸,可帮助消化。
硫 酸
H2SO4 重要的化工原料。用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等。
浓硫酸有吸水性,在实验室中常用它做干燥剂。
1.盐酸与硫酸的比较
巩固练习:
浓硫酸 浓盐酸
溶质的化学式 HCl H2SO4
颜色 无色 无色
状态 水状 油状
气味 刺激性气味 无味
密度(与水比较) 大于水 大于水
打开瓶口的现象 瓶口有白雾生成 无现象
其它 挥发性 吸水性,腐蚀性
巩固练习:
2.按下图所示的装置打开分液漏斗的活塞,让水滴入锥形瓶中,可以看到锥形瓶中出现______、的现象,同时在U型管中_____________。这个事实告诉我们:为了防止发生事故。在稀释浓硫酸时,一定要将浓硫酸沿着器壁慢慢注入水中,并不断搅动。
1.某学生在化学晚会上表演如下下魔术:用毛笔蘸取一种无色液体在一张白纸上书写了“化学魔术”四个字,然后再喷上一种无色液体,白纸上立即出现了红色的“化学魔术”四个字。该学生先后所用的无色液体可能是 ( )
A.紫色石蕊溶液和盐酸 B.氢氧化钠溶液和盐酸
C.无色酚酞溶液和盐酸 D.无色酚酞溶液和氢氧化钠溶液
D
沸腾
液面乙高甲低
课外小实验:
将两朵红色或紫色的鲜花分别插入白醋的稀溶液和石灰水中,注意每天观察鲜花并更换溶液。几天后鲜花有什么变化?
课后作业:
完成导学75-79
同课章节目录
