解读中考科学要求,找准初高化学衔接(课件 43张ppt)
文档属性
| 名称 | 解读中考科学要求,找准初高化学衔接(课件 43张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 24.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2020-03-13 00:00:00 | ||
图片预览











文档简介
(共43张PPT)
解读中考科学要求,找准初高化学衔接
2017温州中考
试卷结构 内容 比例
内 容 分 布 生命科学 约25%
物质科学 约70%
地球和宇宙 约5%
2017年科学33小题,涉及化学10小题
科学总分180分,化学48分
2016年科学33小题,涉及化学12小题
科学总分180分,化学52分
2015年科学34小题,涉及化学11小题
科学总分180分,化学54分
2015.3.氚是氢的一种同位素,氚原子含有1个质子和2个中子。下列示意图能正确表示氚原子结构的是( )
2016.7.如图为某原子的结构示意图,该原子的原子核中有( )
A.6个质子和8个中子
B.8个质子和6个中子
C.6个质子和8个电子
D.8个质子和6个电子
2017.2.5月9日,相关机构发布
等四种元素的中文名称。元素的核电荷数为118,相对原子质量为294,则
原子核外电子数为( )21*cnjy*com
A.118 B.176 C.294 D.412
说出原子的构成,原子核的构成
2016.17(2)氧化汞(HgO)中汞元素的化合价为 ▲ 。
2015.11.在研究空气成分的历史上,许多科学家做了大量的研究。下列是普利斯特利在研究中收集到的各种气体及当时的名称,这些气体中氮元素化合价为零的是( )
A.“亚硝蒸气”(NO2) B.“亚硝空气”(NO)
C.“减缩的亚硝空气”(N2O) D.“燃素化空气”(N2)
2017.8.构成人体骨骼和牙齿的无机盐称为骨盐,其中含有氟化钙(CaF2)。氟化钙中氟(F)元素的化合价为( )
A.?2 B.?1 C.+1 D.+2
根据化学式推断元素的化合价(知道一些常见元素的化合价)
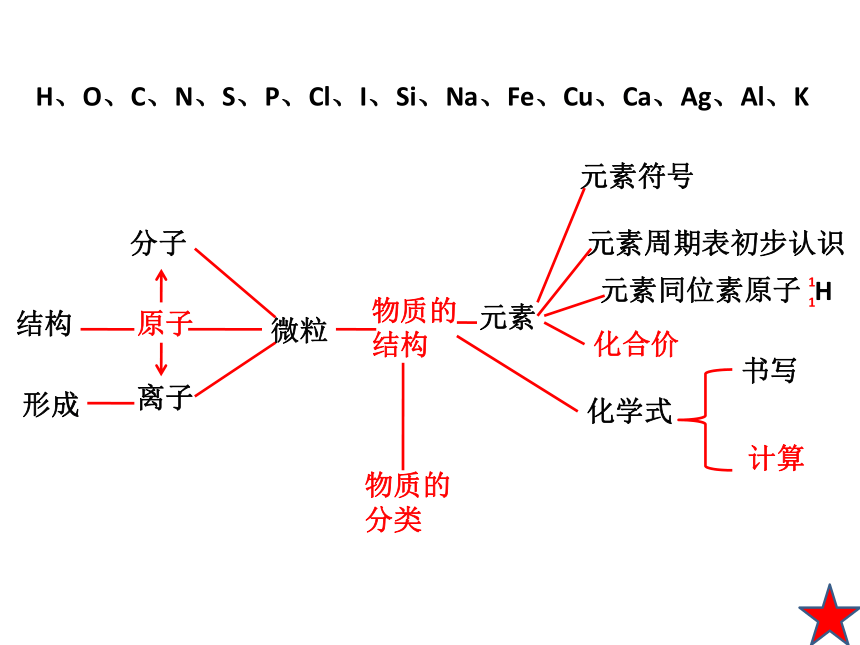
分子
微粒
原子
离子
结构
形成
元素
元素符号
元素周期表初步认识
化合价
化学式
书写
计算
元素同位素原子 H
1
1
H、O、C、N、S、P、Cl、I、Si、Na、Fe、Cu、Ca、Ag、Al、K
物质的结构
物质的分类
常见的带电的原子团有:
离子的名称 离子的符号 离子所带电荷
氢氧根离子 OH_ _1
硫酸根离子 SO42_ _2
硝酸根离子 NO3_ _1
碳酸根离子 CO32_ _2
碳酸氢根离子 HCO3_ _1
铵根离子 NH4+ +1
金属元素 元素
符号 常见的化合价 非金属
元素 元素符号 常见的
化合价
钾 K +1 氢 H +1
钠 Na +1 氟 F -1
银 Ag +1 氧 O -2
钙 Ca +2 氯 Cl -1、+5、+7
镁 Mg +2 溴 Br -1、+5、+7
钡 Ba +2 碘 I -1、+5、+7
锌 Zn +2 氮 N -3、+5
铝 Al +3 磷 P -3、+5
铜 Cu +1、+2 硫 S -2、+4、+6
铁 Fe +2、+3 碳 C -4、+2、+4
锰 Mn +2、+4、+6、+7 硅 Si -4、+4
常见元素的化合价
电离的离子构成
酸:电离时产生的阳离子只有氢离子.
HCl = H+ + Cl-
H2SO4 = 2H+ + SO42-
HNO3 = H+ + NO3-
盐酸:
硫酸:
硝酸:
电离
方程式
原子
( + )
( - )
( + )
( )
原子核
核外电子
质子
中子
2015.6.钛(Ti)是一种广泛应用于航空、航天等领域的重要金属
。工业上制钛的化学方程式为:
高温
TiCl4 + 2Mg Ti + 2MgCl2 ,该反应属于( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
2016.8.实验室中各种化学药品需要合理保存,否则容易变质。
硝酸通常存放在棕色试剂瓶中,其原因是硝酸在光照下会发生如
下反应:4HNO3====(光)4NO2+2H2O+O2↑,该反应属于( )
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
2014.3.1774年,科学家拉瓦锡加热氧化汞产生气体,后来该气体被命名为“氧气”。该反应的化学方程式为2HgO=Hg+O2↑,则该反应的类型属于( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
辨认具体化学反应的基本类型
0.74
2015、20 (2)查阅资料发现:反应生成的红色固体除了铜以外还可能含有氧化亚铜(Cu2O),氧化亚铜可以与硫酸发生如下反应: Cu2O+H2SO4 △ Cu+CuSO4+X,该反应中X的化学式为 ▲ 。0.81
2NH3+3O2 2HNO2+2X。
硝化细菌
2017.(3)水体中氮元素含量过高是河道水污染的主要原因之一。人造水草中的硝化细菌能将污水中的含氮化合物最终转化为无污染物质,该过程涉及到的化学反应之一是 : 则X的化学式为 ▲ 。
应用质量守恒定律定律推理化学式
实验一 实验二 实验三
反应前稀盐酸+烧杯质量(克) 150 150 150
反应前固体样品质量(克) 4 8 12
反应后烧杯内物质+烧杯质量(克) m 155.8 158.7
(第32题图)
电子天平
2017.32.实验室有一变质的氢氧化钠样品(样品中只含碳酸钠杂质,且成分均匀),为测量样品中Na2CO3的质量分数,小明进行了如下实验。21·cn·jy·com
①取质量、大小相同的3个烧杯,分别加入一定质量分数的稀
盐酸100克;
②向上述3个烧杯中分别加入3份质量不同的样品;
③充分反应后,再用电子天平称量烧杯及烧杯内物质的总质量(假设产生的气体完全逸出)。实验数据记录如下:
已知实验中发生的化学反应: NaOH+HCl = NaCl+H2O
Na2CO3+2HCl =2NaCl+H2O+CO2↑(1)分析表中数据,写出判断实验二中的样品已完全反应的理由: ▲ 。
(2)表中的m值为 ▲ 。
(3)根据实验二的数据计算样品中Na2CO3的质量分数。
考查:考查化学方程式计算。
化学反应
化学反应基本类型
燃烧及灭火
质量守恒定律
化学方程式及计算
能量变化
氧化还原反应
催化剂
化学反应应用
(酸与碱反应)
放出热量
吸收热量
化学能与内能转化
化学能转化为电能
催化剂:在化学反应里能改变其他物质的化学反应速率,而本身质量和化学性质在化学反应前后都没有发生变化的物质。
催化剂的特点:
一变:化学反应速率变
二不变:质量不变、化学性质不变
化学反应的速度影响因素
氢氧化钠与盐酸反应示意图
酚酞
氢氧化钠溶液
盐酸
2015.31(3)腌制咸鸭蛋需要合适溶质质量分数的食盐水。
现有10千克溶质质量分数为25%的食盐水,若将
其稀释到20%,需加水多少千克?
难度值:0.6
2017.29(2)乙同学抽到的是B组中的一个实验:
配制50克10%的氯化钠溶液。为完成该实验,
他应称取固体氯化钠 ▲ 克。
2016.29.实验室用如下(图甲)方法制取氢氧化铜固体。
(1)步骤 ①需配制200克溶质质量分数为4%的NaOH溶液,
需NaOH固体 克。
应用溶质质量分数公式进行简单计算
2015.22.运用酸、碱、盐的性质可以解决工业生产中的许多问题。
(2)某工厂向含有AgNO3、Cu(NO3)2的废水中加入一定量的锌粉(Zn)以回收金属,充分反应后,得到的金属组成可能有哪几种情况? ▲ 。
难度值:0.32
2016.15.为了验证“Fe、Cu、Ag三种金属的活动性由强到弱”,小明设计了如图所示的实验。其中可以达到实验目的的组合是( )【来源:21·世纪·教育·网】
A.①② B.①③ C.②④ D.③④
2017.7.在柠檬中插入两种不同的金属可以制得水果电池。相同条
件下,水果电池的电压与两种金属的活动性差异大小有关。下列柠
檬电池的两种金属,活动性差异最大的是( )
铝
锌
铁
锌
铜
银
A B C D
铝
银
比较金属的活动性顺序
2017.29(3)丙同学抽到的是B组中另一个实验:验证
稀硫酸和氢氧化钠溶液的酸碱性。用到的试剂有:稀
硫酸、氢氧化钠溶液、紫色石蕊试液。实验结束后,
他将实验后的溶液全部倒入废液缸,混合溶液呈蓝色
,则混合溶液中除石蕊外还含有的溶质为 ▲ (写化学式)。
选项 性质 用途
A 氢氧化钙呈碱性 改良酸性土壤
B 浓硫酸具有脱水性 干燥氧气
C 稀盐酸能与某些金属氧化物反应 除铁锈
D 氢氢化钠能与某此非金属氧化物反应 吸收二氧化硫
2016.11.下列物质的性质与用途的对应关系错误的是( )
2015.22.运用酸、碱、盐的性质可以解决工业生产中的许多问题。
(1)工业上常选用 ▲ 来除去铁锈。(写出一种具体物质)
说出常见酸碱的性质和用途
2015.31.温州产盐历史悠久,盐产品在日常生活、工业生产中有广泛用途。
(1)用下图方法可进行粗盐提纯,其中操作②的名称为 ▲ 。
粗盐
泥沙
滤液
精盐
③蒸发
悬浊液
①溶解
②
2016.29.(2)请从图乙中选取步骤②过滤时需
要用到的器材 。(可多选)
2017.29.某校举行科学实验操作考查,由学生抽签确定考查的实验内容,要求根据提供的实验器材完成相关实验。
(1)A组实验有:①过滤含泥沙的食盐水;②蒸发氯化钠溶液获得晶体;③用实验室方法制取一瓶二氧化碳。甲同学抽到的是A组中的一个实验,需要如下器材:则他抽到的实验是 ▲ (选填序号)。
说明粗盐提纯的过程,过滤操作要点。
2017.27.在用氯酸钾和二氧化锰的混合物制取氧气实验后,为了进一步探究二氧化锰的用量对氯酸钾分解速度的影响,小明用如图装置,以及实验室提供的实验所需药品和器材进行实验。老师对实验的建议:①每组实验氯酸钾用量可取4克,二氧化锰质量不宜超过2克。②实验应设计4组。j-(1)结合老师建议,补充完整实验步骤①之后的其它步骤。①检查装置的气密性;
……
(2)实验结束后,小明回收了二氧化锰。如果要证明二氧化锰是氯酸钾分解的催化剂,还需验证该二氧化锰的 ▲ 保持不变。
【来
氧气制取—化学反应速度影响因素研究
常见物质
物质分离
水(溶液)
金属
空气
组成
物质分散系
沉淀、过滤、
结晶、蒸馏
合金
空气氧气体积分数测定
氧气
二氧化碳
配置(质量分数)
物质性质
酸、碱、盐、有机物
物质间的转化
氧、碳循环
自然界中的碳循环
自然界中氧、碳循环主要途径
物质的分散系
乳浊液:液体小液滴分散在水中(牛奶)
溶液:物质以分子或者离子形式分
散在水中(高锰酸钾)
悬浊液:固体小颗粒分散
在水中(钡餐、血液)
均一、稳定
粗盐提纯
水的净化-蒸馏
常见气体的制取
酸
碱
盐
HCl、硫酸
氢氧化钠、氢氧化钙
氯化钠、碳酸钙、碳酸钠
酸
指示剂
金属
金属氧化物
碱
盐
指示剂
非金属
氧化物
盐
碱
酸
个性到共性到特性
有机物的特性
(1)大部分有机物熔点较低,受热易分解,易挥发,不易导电,易燃烧(生成二氧化碳和水,不完全燃烧生成炭黑)等。
(2)绝大多数有机物难溶于水,易溶于汽油、酒精、苯等有机溶剂
乙炔C2H2
丁烷(C4H10)
甲烷CH4
1、糖类元素组成:由C、H、O三种组成
2、蛋白质元素组成:C、H、O、N、S、P
3、脂肪:元素组成:C、H、O
金属
金属材料
金属性质
物理性质
化学性质
金属防锈
盐
酸
氧气
铜与硝酸银溶液的反应
铁与硫酸铜溶液的反应
金属与其化合物转化
非金属与其化合物转化
金属冶炼
化合物间转化
物质转化
金属
单质
金属
氧化物
碱
氧气
水
非金属
单质
非金属
氧化物
酸
氧气
水
中考要求:说明金属、金属氧化物、碱之间的转化关系
中考要求:说明非金属、非金属氧化物、酸之间的转化关系
金属
单质
金属
氧化物
碱
盐
氧气
水
酸
非金属
单质
非金属
氧化物
酸
盐
氧气
水
碱
盐
盐+水
盐+盐
盐+酸
盐+碱
盐+H2
盐
+
金
属
4横+4斜+2折
10种反应生成盐
初中科学课程结构
科学、技术、社会、环境
物质科学 地球与空间科学
生命科学
科学探究
初中化学知识结构
氢离子、氢氧根离子、氯离子、硫酸根、碳酸根
化学式 CO2 H2O H2O2 CH4 CO
分子模型 ? ? ?
原子个数比 ? ?
1:2
2:1
2:2
1:4
1:1
化合价的本质是什么?
含义:各种元素在相互化合时,原子之间都有固定的化合数目,用化合价表示这种性质。
氧化反应:物质跟氧的反应。
还原反应:含氧化合物被夺取氧的反应
2KClO3===2KCl+3O2 ↑
CaCO3+2HCl===CaCl2+H2O+CO2↑
案例:研究氢氧化钙的性质. 问题:为什么氯化铁试管中现象不明显?
试剂滴加顺序不一样,实验现象不一样?
稀盐酸滴加到碳酸钠溶液中,碳酸钠溶液滴加到稀盐酸中。
案例:向硫酸铜和盐酸的混合溶液中,逐渐加入
氢氧化钠溶液,请画出产生沉淀的质量与所滴
入氢氧化钠溶液的质量(X)关系图,并说明
各段变化的理由。
反应先后问题
雨雪等在形成和降落过程中,吸收并溶解了空气中的二氧化硫,氮氧化物等物质,形成了pH低于5.6的酸性降水,称为酸雨。酸雨中主要的有害物质是硫酸和硝酸。
原子 种类 核电 荷数 质子数 中子数 电子数 相对原子质量
1 1
氧 8 8
12 23
12 12
17 18
13 27
26 30
氢 1 0 1
8 8 16
钠 11 11 11
镁 12 12 24
氯 17 17 35
铝 13 14 13
铁 26 26 56
相对原子质量数 = 质子数 + 中子数
THANKS
谢谢聆听,敬请指教!
中考考纲未要求的化学知识点:
1、物质分离方法的结晶(冷却热饱和溶液)
2、物质分离方法中的蒸馏法
3、微观粒子的大小、质量
4、同位素及应用
5、元素在人体、大海、地壳的分布
6、有机合成材料
7、材料的利用与发展
解读中考科学要求,找准初高化学衔接
2017温州中考
试卷结构 内容 比例
内 容 分 布 生命科学 约25%
物质科学 约70%
地球和宇宙 约5%
2017年科学33小题,涉及化学10小题
科学总分180分,化学48分
2016年科学33小题,涉及化学12小题
科学总分180分,化学52分
2015年科学34小题,涉及化学11小题
科学总分180分,化学54分
2015.3.氚是氢的一种同位素,氚原子含有1个质子和2个中子。下列示意图能正确表示氚原子结构的是( )
2016.7.如图为某原子的结构示意图,该原子的原子核中有( )
A.6个质子和8个中子
B.8个质子和6个中子
C.6个质子和8个电子
D.8个质子和6个电子
2017.2.5月9日,相关机构发布
等四种元素的中文名称。元素的核电荷数为118,相对原子质量为294,则
原子核外电子数为( )21*cnjy*com
A.118 B.176 C.294 D.412
说出原子的构成,原子核的构成
2016.17(2)氧化汞(HgO)中汞元素的化合价为 ▲ 。
2015.11.在研究空气成分的历史上,许多科学家做了大量的研究。下列是普利斯特利在研究中收集到的各种气体及当时的名称,这些气体中氮元素化合价为零的是( )
A.“亚硝蒸气”(NO2) B.“亚硝空气”(NO)
C.“减缩的亚硝空气”(N2O) D.“燃素化空气”(N2)
2017.8.构成人体骨骼和牙齿的无机盐称为骨盐,其中含有氟化钙(CaF2)。氟化钙中氟(F)元素的化合价为( )
A.?2 B.?1 C.+1 D.+2
根据化学式推断元素的化合价(知道一些常见元素的化合价)
分子
微粒
原子
离子
结构
形成
元素
元素符号
元素周期表初步认识
化合价
化学式
书写
计算
元素同位素原子 H
1
1
H、O、C、N、S、P、Cl、I、Si、Na、Fe、Cu、Ca、Ag、Al、K
物质的结构
物质的分类
常见的带电的原子团有:
离子的名称 离子的符号 离子所带电荷
氢氧根离子 OH_ _1
硫酸根离子 SO42_ _2
硝酸根离子 NO3_ _1
碳酸根离子 CO32_ _2
碳酸氢根离子 HCO3_ _1
铵根离子 NH4+ +1
金属元素 元素
符号 常见的化合价 非金属
元素 元素符号 常见的
化合价
钾 K +1 氢 H +1
钠 Na +1 氟 F -1
银 Ag +1 氧 O -2
钙 Ca +2 氯 Cl -1、+5、+7
镁 Mg +2 溴 Br -1、+5、+7
钡 Ba +2 碘 I -1、+5、+7
锌 Zn +2 氮 N -3、+5
铝 Al +3 磷 P -3、+5
铜 Cu +1、+2 硫 S -2、+4、+6
铁 Fe +2、+3 碳 C -4、+2、+4
锰 Mn +2、+4、+6、+7 硅 Si -4、+4
常见元素的化合价
电离的离子构成
酸:电离时产生的阳离子只有氢离子.
HCl = H+ + Cl-
H2SO4 = 2H+ + SO42-
HNO3 = H+ + NO3-
盐酸:
硫酸:
硝酸:
电离
方程式
原子
( + )
( - )
( + )
( )
原子核
核外电子
质子
中子
2015.6.钛(Ti)是一种广泛应用于航空、航天等领域的重要金属
。工业上制钛的化学方程式为:
高温
TiCl4 + 2Mg Ti + 2MgCl2 ,该反应属于( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
2016.8.实验室中各种化学药品需要合理保存,否则容易变质。
硝酸通常存放在棕色试剂瓶中,其原因是硝酸在光照下会发生如
下反应:4HNO3====(光)4NO2+2H2O+O2↑,该反应属于( )
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
2014.3.1774年,科学家拉瓦锡加热氧化汞产生气体,后来该气体被命名为“氧气”。该反应的化学方程式为2HgO=Hg+O2↑,则该反应的类型属于( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
辨认具体化学反应的基本类型
0.74
2015、20 (2)查阅资料发现:反应生成的红色固体除了铜以外还可能含有氧化亚铜(Cu2O),氧化亚铜可以与硫酸发生如下反应: Cu2O+H2SO4 △ Cu+CuSO4+X,该反应中X的化学式为 ▲ 。0.81
2NH3+3O2 2HNO2+2X。
硝化细菌
2017.(3)水体中氮元素含量过高是河道水污染的主要原因之一。人造水草中的硝化细菌能将污水中的含氮化合物最终转化为无污染物质,该过程涉及到的化学反应之一是 : 则X的化学式为 ▲ 。
应用质量守恒定律定律推理化学式
实验一 实验二 实验三
反应前稀盐酸+烧杯质量(克) 150 150 150
反应前固体样品质量(克) 4 8 12
反应后烧杯内物质+烧杯质量(克) m 155.8 158.7
(第32题图)
电子天平
2017.32.实验室有一变质的氢氧化钠样品(样品中只含碳酸钠杂质,且成分均匀),为测量样品中Na2CO3的质量分数,小明进行了如下实验。21·cn·jy·com
①取质量、大小相同的3个烧杯,分别加入一定质量分数的稀
盐酸100克;
②向上述3个烧杯中分别加入3份质量不同的样品;
③充分反应后,再用电子天平称量烧杯及烧杯内物质的总质量(假设产生的气体完全逸出)。实验数据记录如下:
已知实验中发生的化学反应: NaOH+HCl = NaCl+H2O
Na2CO3+2HCl =2NaCl+H2O+CO2↑(1)分析表中数据,写出判断实验二中的样品已完全反应的理由: ▲ 。
(2)表中的m值为 ▲ 。
(3)根据实验二的数据计算样品中Na2CO3的质量分数。
考查:考查化学方程式计算。
化学反应
化学反应基本类型
燃烧及灭火
质量守恒定律
化学方程式及计算
能量变化
氧化还原反应
催化剂
化学反应应用
(酸与碱反应)
放出热量
吸收热量
化学能与内能转化
化学能转化为电能
催化剂:在化学反应里能改变其他物质的化学反应速率,而本身质量和化学性质在化学反应前后都没有发生变化的物质。
催化剂的特点:
一变:化学反应速率变
二不变:质量不变、化学性质不变
化学反应的速度影响因素
氢氧化钠与盐酸反应示意图
酚酞
氢氧化钠溶液
盐酸
2015.31(3)腌制咸鸭蛋需要合适溶质质量分数的食盐水。
现有10千克溶质质量分数为25%的食盐水,若将
其稀释到20%,需加水多少千克?
难度值:0.6
2017.29(2)乙同学抽到的是B组中的一个实验:
配制50克10%的氯化钠溶液。为完成该实验,
他应称取固体氯化钠 ▲ 克。
2016.29.实验室用如下(图甲)方法制取氢氧化铜固体。
(1)步骤 ①需配制200克溶质质量分数为4%的NaOH溶液,
需NaOH固体 克。
应用溶质质量分数公式进行简单计算
2015.22.运用酸、碱、盐的性质可以解决工业生产中的许多问题。
(2)某工厂向含有AgNO3、Cu(NO3)2的废水中加入一定量的锌粉(Zn)以回收金属,充分反应后,得到的金属组成可能有哪几种情况? ▲ 。
难度值:0.32
2016.15.为了验证“Fe、Cu、Ag三种金属的活动性由强到弱”,小明设计了如图所示的实验。其中可以达到实验目的的组合是( )【来源:21·世纪·教育·网】
A.①② B.①③ C.②④ D.③④
2017.7.在柠檬中插入两种不同的金属可以制得水果电池。相同条
件下,水果电池的电压与两种金属的活动性差异大小有关。下列柠
檬电池的两种金属,活动性差异最大的是( )
铝
锌
铁
锌
铜
银
A B C D
铝
银
比较金属的活动性顺序
2017.29(3)丙同学抽到的是B组中另一个实验:验证
稀硫酸和氢氧化钠溶液的酸碱性。用到的试剂有:稀
硫酸、氢氧化钠溶液、紫色石蕊试液。实验结束后,
他将实验后的溶液全部倒入废液缸,混合溶液呈蓝色
,则混合溶液中除石蕊外还含有的溶质为 ▲ (写化学式)。
选项 性质 用途
A 氢氧化钙呈碱性 改良酸性土壤
B 浓硫酸具有脱水性 干燥氧气
C 稀盐酸能与某些金属氧化物反应 除铁锈
D 氢氢化钠能与某此非金属氧化物反应 吸收二氧化硫
2016.11.下列物质的性质与用途的对应关系错误的是( )
2015.22.运用酸、碱、盐的性质可以解决工业生产中的许多问题。
(1)工业上常选用 ▲ 来除去铁锈。(写出一种具体物质)
说出常见酸碱的性质和用途
2015.31.温州产盐历史悠久,盐产品在日常生活、工业生产中有广泛用途。
(1)用下图方法可进行粗盐提纯,其中操作②的名称为 ▲ 。
粗盐
泥沙
滤液
精盐
③蒸发
悬浊液
①溶解
②
2016.29.(2)请从图乙中选取步骤②过滤时需
要用到的器材 。(可多选)
2017.29.某校举行科学实验操作考查,由学生抽签确定考查的实验内容,要求根据提供的实验器材完成相关实验。
(1)A组实验有:①过滤含泥沙的食盐水;②蒸发氯化钠溶液获得晶体;③用实验室方法制取一瓶二氧化碳。甲同学抽到的是A组中的一个实验,需要如下器材:则他抽到的实验是 ▲ (选填序号)。
说明粗盐提纯的过程,过滤操作要点。
2017.27.在用氯酸钾和二氧化锰的混合物制取氧气实验后,为了进一步探究二氧化锰的用量对氯酸钾分解速度的影响,小明用如图装置,以及实验室提供的实验所需药品和器材进行实验。老师对实验的建议:①每组实验氯酸钾用量可取4克,二氧化锰质量不宜超过2克。②实验应设计4组。j-(1)结合老师建议,补充完整实验步骤①之后的其它步骤。①检查装置的气密性;
……
(2)实验结束后,小明回收了二氧化锰。如果要证明二氧化锰是氯酸钾分解的催化剂,还需验证该二氧化锰的 ▲ 保持不变。
【来
氧气制取—化学反应速度影响因素研究
常见物质
物质分离
水(溶液)
金属
空气
组成
物质分散系
沉淀、过滤、
结晶、蒸馏
合金
空气氧气体积分数测定
氧气
二氧化碳
配置(质量分数)
物质性质
酸、碱、盐、有机物
物质间的转化
氧、碳循环
自然界中的碳循环
自然界中氧、碳循环主要途径
物质的分散系
乳浊液:液体小液滴分散在水中(牛奶)
溶液:物质以分子或者离子形式分
散在水中(高锰酸钾)
悬浊液:固体小颗粒分散
在水中(钡餐、血液)
均一、稳定
粗盐提纯
水的净化-蒸馏
常见气体的制取
酸
碱
盐
HCl、硫酸
氢氧化钠、氢氧化钙
氯化钠、碳酸钙、碳酸钠
酸
指示剂
金属
金属氧化物
碱
盐
指示剂
非金属
氧化物
盐
碱
酸
个性到共性到特性
有机物的特性
(1)大部分有机物熔点较低,受热易分解,易挥发,不易导电,易燃烧(生成二氧化碳和水,不完全燃烧生成炭黑)等。
(2)绝大多数有机物难溶于水,易溶于汽油、酒精、苯等有机溶剂
乙炔C2H2
丁烷(C4H10)
甲烷CH4
1、糖类元素组成:由C、H、O三种组成
2、蛋白质元素组成:C、H、O、N、S、P
3、脂肪:元素组成:C、H、O
金属
金属材料
金属性质
物理性质
化学性质
金属防锈
盐
酸
氧气
铜与硝酸银溶液的反应
铁与硫酸铜溶液的反应
金属与其化合物转化
非金属与其化合物转化
金属冶炼
化合物间转化
物质转化
金属
单质
金属
氧化物
碱
氧气
水
非金属
单质
非金属
氧化物
酸
氧气
水
中考要求:说明金属、金属氧化物、碱之间的转化关系
中考要求:说明非金属、非金属氧化物、酸之间的转化关系
金属
单质
金属
氧化物
碱
盐
氧气
水
酸
非金属
单质
非金属
氧化物
酸
盐
氧气
水
碱
盐
盐+水
盐+盐
盐+酸
盐+碱
盐+H2
盐
+
金
属
4横+4斜+2折
10种反应生成盐
初中科学课程结构
科学、技术、社会、环境
物质科学 地球与空间科学
生命科学
科学探究
初中化学知识结构
氢离子、氢氧根离子、氯离子、硫酸根、碳酸根
化学式 CO2 H2O H2O2 CH4 CO
分子模型 ? ? ?
原子个数比 ? ?
1:2
2:1
2:2
1:4
1:1
化合价的本质是什么?
含义:各种元素在相互化合时,原子之间都有固定的化合数目,用化合价表示这种性质。
氧化反应:物质跟氧的反应。
还原反应:含氧化合物被夺取氧的反应
2KClO3===2KCl+3O2 ↑
CaCO3+2HCl===CaCl2+H2O+CO2↑
案例:研究氢氧化钙的性质. 问题:为什么氯化铁试管中现象不明显?
试剂滴加顺序不一样,实验现象不一样?
稀盐酸滴加到碳酸钠溶液中,碳酸钠溶液滴加到稀盐酸中。
案例:向硫酸铜和盐酸的混合溶液中,逐渐加入
氢氧化钠溶液,请画出产生沉淀的质量与所滴
入氢氧化钠溶液的质量(X)关系图,并说明
各段变化的理由。
反应先后问题
雨雪等在形成和降落过程中,吸收并溶解了空气中的二氧化硫,氮氧化物等物质,形成了pH低于5.6的酸性降水,称为酸雨。酸雨中主要的有害物质是硫酸和硝酸。
原子 种类 核电 荷数 质子数 中子数 电子数 相对原子质量
1 1
氧 8 8
12 23
12 12
17 18
13 27
26 30
氢 1 0 1
8 8 16
钠 11 11 11
镁 12 12 24
氯 17 17 35
铝 13 14 13
铁 26 26 56
相对原子质量数 = 质子数 + 中子数
THANKS
谢谢聆听,敬请指教!
中考考纲未要求的化学知识点:
1、物质分离方法的结晶(冷却热饱和溶液)
2、物质分离方法中的蒸馏法
3、微观粒子的大小、质量
4、同位素及应用
5、元素在人体、大海、地壳的分布
6、有机合成材料
7、材料的利用与发展
同课章节目录
