课题2 二氧化碳制取的研究 课件(20张PPT)
文档属性
| 名称 | 课题2 二氧化碳制取的研究 课件(20张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 8.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-17 00:00:00 | ||
图片预览






文档简介
(共20张PPT)
欢迎进入化学课堂
课题2二氧化碳制取的研究
展示
生成
检测
互动
预 习
展示
生成
检测
互动
预 习
预 习
展 示
互 动
检 测
学习目标
生 成
1.探究实验室制取二氧化碳的原理;
2.设计实验室中制取二氧化碳的发生装置,
3.掌握二氧化碳的收集方法和验满及验证方法。
4.了解实验室制取气体的一般思路和基本依据。
学习目标
实验室制取气体的思路
药品及反应原理
实验装置
收集方法
检验
步骤
预 习
互 动
展示
生成
检测
预 习
互 动
展示
生成
检测
实验室制取气体应该考虑因素
实验是否易于操作
原料是否易得
产生气体速度是否适中
生成的气体是否易于收集
反应条件是否易于达到
预 习
生成
检测
第一站 药品及反应原理的探究
议一议
你知道生成二氧化碳的反应有哪些?
这些反应是否适合实验室制取二氧化碳
为什么?
互 动
展示
预 习
生成
检测
互 动
展示
做一做
1、碳酸钠粉末和稀盐酸反应
2、大理石块和稀盐酸反应
3、大理石块和稀硫酸反应
注意事项:
1、粉末只用一药匙,大石理2-5粒
(反应容器是试管,装药顺序先固后)
2、分别倒入1/5试管的稀盐酸或稀硫酸
3、观察的重点是比较三个反应中产生气泡的快慢
预 习
互 动
展示
生成
检测
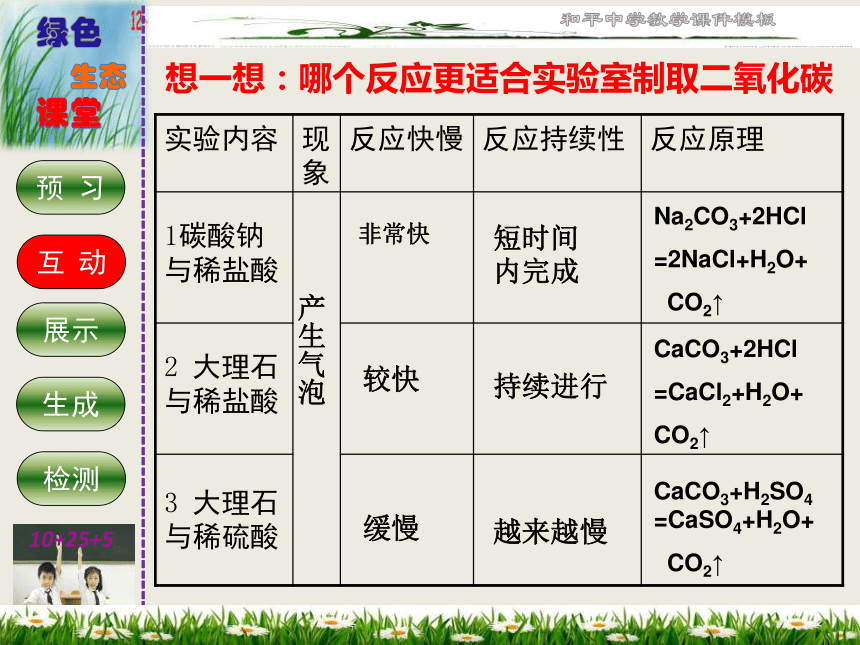
想一想:哪个反应更适合实验室制取二氧化碳
实验内容 现象 反应快慢 反应持续性 反应原理
1碳酸钠与稀盐酸
2 大理石与稀盐酸
3 大理石与稀硫酸
产生气泡
非常快
缓慢
较快
越来越慢
Na2CO3+2HCl
=2NaCl+H2O+
CO2↑
持续进行
CaCO3+H2SO4=CaSO4+H2O+
CO2↑
短时间内完成
CaCO3+2HCl
=CaCl2+H2O+
CO2↑
预 习
生成
检测
第二站 二氧化碳发生装置的设计
结合实验药品及其原理,仿照实验室制取氧气的装置,利用讲台上的仪器设计组装一套实验室制取二氧化碳的发生装置。
展示
互 动
预 习
生成
检测
互 动
展示
第三站 收集方法的选择
【查阅资料】:常温下,二氧化碳是无色无味的气体,易溶于水,密度比空气大。在一定条件下,二氧化碳会变成液体或固体。固态二氧化碳叫做“干冰”干冰升华时吸收大量的热。
结合资料,同学们讨论应如何收集二氧化
碳气体?
预 习
生成
检测
互 动
展示
问题思考:实验室制取二氧化碳的操作步骤如何?
验(满)
查
装
收
放
第四站 实验步骤总结
预 习
生成
检测
互 动
展示
第五站 气体的验证及其验满
你知道如何检验二氧化碳气体吗?
把收集到的气体通入到澄清石灰水中,如果石灰水变浑浊,则证明是二氧化碳。
你知道如何检验二氧化碳气体是否收集满吗?
把燃着的木条放在集气瓶口,如果木条火焰熄灭,证明二氧化碳已经收集满
预 习
生成
检测
展示
互 动
试一试
请同学们观察老师演示实验室制取二氧化碳的过程
预 习
生成
检测
互 动
展示
讨 论
1、实验室制取气体的一般思路和方法?
2、确定气体发生装置时应考虑哪些因素?
3、确定气体收集装置时应考虑哪些因素?
结合教材和这节课的探究过程,讨论完成下列问题:
预 习
互 动
展示
生成
检测
本课小结 理一理
一、实验室制取气体的一般思路和方法:
1、选择适当的反应,包括反应物和反应条件
2、选择合适的实验装置,(发生和收集)
3、验证所制得的气体
二、气体发生装置的选择依据和收集装置的依据
1、气体发生装置的选择依据:
2、气体发生装置的选择依据:
反应物的状态及条件
气体的密度及其溶解性
预 习
互 动
展示
生成
检测
当堂检测
小试牛刀:
1、甲烷的实验室制法是:用无水醋酸钠和碱石灰两种固态药品,经研磨均匀混合后装入反应装置中,加热产生甲烷气体。甲烷是一种无色、无味,比空气轻,极难溶于水的气体。
(1)本实验中反应物的状态为——反应条件为——
(2)请你画出本实验的气体发生装置。此实验的气体发生装置与什么气体的发生装置相同
(3)甲烷气体是否难溶于水,密度是否比空气大。利用此性质应用什么方法来收集甲烷
作 业
预习125页实验活动2:
二氧化碳的实验室制取与性质
下节课我们到化学实验室自己动手制取并收集二氧化碳
预 习
互 动
展示
生成
检测
你都掌握了吗?
课下进一步整理、完善本节内容
预 习
互 动
展示
生成
检测
预 习
互 动
展示
生成
检测
牛刀小试:
根据化学方程式
4
P+ 5O
2
2P
2
O
5
回答下列问题:
点燃
其中P的相对原子质量是31,
O的相对原子质量是16
计算生产852吨五氧化二磷需要磷和氧气共多少吨?你能知道分别需要多少吨吗?
欢迎进入化学课堂
课题2二氧化碳制取的研究
展示
生成
检测
互动
预 习
展示
生成
检测
互动
预 习
预 习
展 示
互 动
检 测
学习目标
生 成
1.探究实验室制取二氧化碳的原理;
2.设计实验室中制取二氧化碳的发生装置,
3.掌握二氧化碳的收集方法和验满及验证方法。
4.了解实验室制取气体的一般思路和基本依据。
学习目标
实验室制取气体的思路
药品及反应原理
实验装置
收集方法
检验
步骤
预 习
互 动
展示
生成
检测
预 习
互 动
展示
生成
检测
实验室制取气体应该考虑因素
实验是否易于操作
原料是否易得
产生气体速度是否适中
生成的气体是否易于收集
反应条件是否易于达到
预 习
生成
检测
第一站 药品及反应原理的探究
议一议
你知道生成二氧化碳的反应有哪些?
这些反应是否适合实验室制取二氧化碳
为什么?
互 动
展示
预 习
生成
检测
互 动
展示
做一做
1、碳酸钠粉末和稀盐酸反应
2、大理石块和稀盐酸反应
3、大理石块和稀硫酸反应
注意事项:
1、粉末只用一药匙,大石理2-5粒
(反应容器是试管,装药顺序先固后)
2、分别倒入1/5试管的稀盐酸或稀硫酸
3、观察的重点是比较三个反应中产生气泡的快慢
预 习
互 动
展示
生成
检测
想一想:哪个反应更适合实验室制取二氧化碳
实验内容 现象 反应快慢 反应持续性 反应原理
1碳酸钠与稀盐酸
2 大理石与稀盐酸
3 大理石与稀硫酸
产生气泡
非常快
缓慢
较快
越来越慢
Na2CO3+2HCl
=2NaCl+H2O+
CO2↑
持续进行
CaCO3+H2SO4=CaSO4+H2O+
CO2↑
短时间内完成
CaCO3+2HCl
=CaCl2+H2O+
CO2↑
预 习
生成
检测
第二站 二氧化碳发生装置的设计
结合实验药品及其原理,仿照实验室制取氧气的装置,利用讲台上的仪器设计组装一套实验室制取二氧化碳的发生装置。
展示
互 动
预 习
生成
检测
互 动
展示
第三站 收集方法的选择
【查阅资料】:常温下,二氧化碳是无色无味的气体,易溶于水,密度比空气大。在一定条件下,二氧化碳会变成液体或固体。固态二氧化碳叫做“干冰”干冰升华时吸收大量的热。
结合资料,同学们讨论应如何收集二氧化
碳气体?
预 习
生成
检测
互 动
展示
问题思考:实验室制取二氧化碳的操作步骤如何?
验(满)
查
装
收
放
第四站 实验步骤总结
预 习
生成
检测
互 动
展示
第五站 气体的验证及其验满
你知道如何检验二氧化碳气体吗?
把收集到的气体通入到澄清石灰水中,如果石灰水变浑浊,则证明是二氧化碳。
你知道如何检验二氧化碳气体是否收集满吗?
把燃着的木条放在集气瓶口,如果木条火焰熄灭,证明二氧化碳已经收集满
预 习
生成
检测
展示
互 动
试一试
请同学们观察老师演示实验室制取二氧化碳的过程
预 习
生成
检测
互 动
展示
讨 论
1、实验室制取气体的一般思路和方法?
2、确定气体发生装置时应考虑哪些因素?
3、确定气体收集装置时应考虑哪些因素?
结合教材和这节课的探究过程,讨论完成下列问题:
预 习
互 动
展示
生成
检测
本课小结 理一理
一、实验室制取气体的一般思路和方法:
1、选择适当的反应,包括反应物和反应条件
2、选择合适的实验装置,(发生和收集)
3、验证所制得的气体
二、气体发生装置的选择依据和收集装置的依据
1、气体发生装置的选择依据:
2、气体发生装置的选择依据:
反应物的状态及条件
气体的密度及其溶解性
预 习
互 动
展示
生成
检测
当堂检测
小试牛刀:
1、甲烷的实验室制法是:用无水醋酸钠和碱石灰两种固态药品,经研磨均匀混合后装入反应装置中,加热产生甲烷气体。甲烷是一种无色、无味,比空气轻,极难溶于水的气体。
(1)本实验中反应物的状态为——反应条件为——
(2)请你画出本实验的气体发生装置。此实验的气体发生装置与什么气体的发生装置相同
(3)甲烷气体是否难溶于水,密度是否比空气大。利用此性质应用什么方法来收集甲烷
作 业
预习125页实验活动2:
二氧化碳的实验室制取与性质
下节课我们到化学实验室自己动手制取并收集二氧化碳
预 习
互 动
展示
生成
检测
你都掌握了吗?
课下进一步整理、完善本节内容
预 习
互 动
展示
生成
检测
预 习
互 动
展示
生成
检测
牛刀小试:
根据化学方程式
4
P+ 5O
2
2P
2
O
5
回答下列问题:
点燃
其中P的相对原子质量是31,
O的相对原子质量是16
计算生产852吨五氧化二磷需要磷和氧气共多少吨?你能知道分别需要多少吨吗?
同课章节目录
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的构成
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题1 质量守恒定律
- 课题2 如何正确书写化学方程式
- 课题3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动3 燃烧的条件
- 旧版目录
- 第五单元 物质组成的表示
- 课题2 燃料和热量
- 课题3 使用燃料对环境的影响
