第一单元 金属和金属材料复习 第1课时 课件(17张PPT)
文档属性
| 名称 | 第一单元 金属和金属材料复习 第1课时 课件(17张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 603.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-18 00:00:00 | ||
图片预览





文档简介
(共17张PPT)
人教五?四学制2011课标版
复习 第1课时
金属的化学性质(高频考点)
1、金属材料
2、金属矿物及其冶炼(铁的冶炼)
1、金属的化学性质
2、置换反应
3、金属活动性顺序
常见的金属材料
共性:
1、金属材料
特性
铁合金:
概念:
有金属光泽、导电性、导热性和延展性
颜色:大多数金属为_____色,
但铜为_____色,金为___色
状态:常温下大多数金属为固体,但汞为_____。
纯金属
银白
紫红
黄
液体
合金
特性:
在金属中加热熔合某些_____或_____,
制得的具有_____特征的物质。
合金属于_____物。
金属
非金属
金属
混合
强度和硬度一般比它们的纯
金属更高,抗腐蚀性更好
生铁和钢(含碳量不同)
常见的金属材料
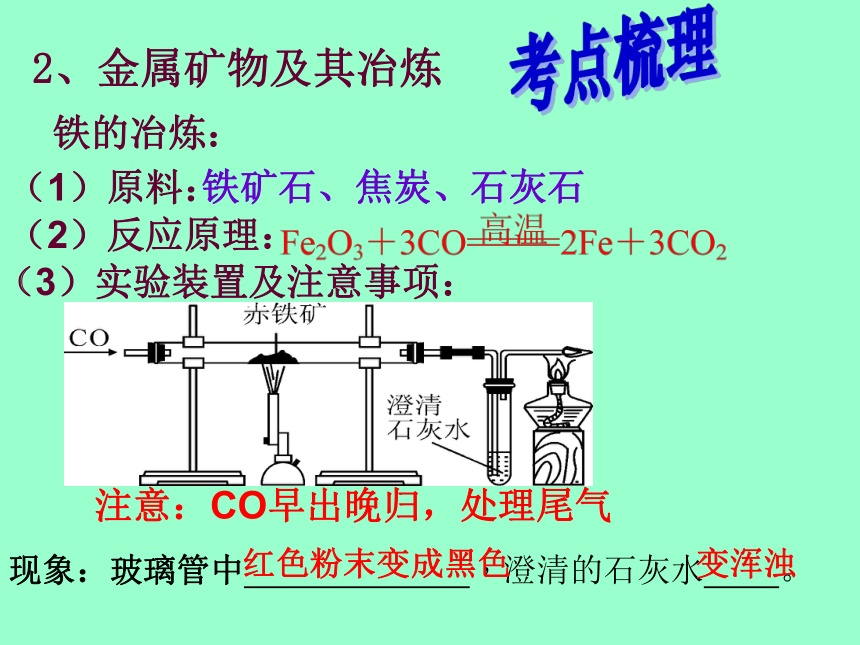
2、金属矿物及其冶炼
铁的冶炼:
(1)原料:
(2)反应原理:
(3)实验装置及注意事项:
注意:CO早出晚归,处理尾气
铁矿石、焦炭、石灰石
现象:玻璃管中 ,澄清的石灰水 。
红色粉末变成黑色
变浑浊
1.(2016·乐山)汽车是现代生活中重要的交通工具。请 回答下列问题:
(1)汽车电路中的导线一般为铜芯线,这是利用了金属铜的延展性和________性。
(2)下列制造汽车所用到的材料中,属于合金的是________。(填序号)
①钢铁 ②合成橡胶 ③羊毛织物 ④铝合金 ⑤塑料
导电
①④
2.(2016·北京)铜能被加工成厚度仅为7 μm的超薄铜
箔,说明铜具有良好的( )
A.导电性 B.延展性 C.导热性 D.抗腐
B
3.(2015·宜宾)下列有关金属材料的说法正确的是( ) A.硬铝片比纯铝片硬度小 B.钢的性能优良,是很纯的铁
C.沙漠地区的铁制品锈蚀较快
D.为防止钢铁生锈,可在其表面涂油
D
4.(2015?重庆)如右图所示的炼铁高炉中发生了许多化学反应,其中就涉及碳及其化合物的相互转化。请回答下列问题。
(1)空气通过进风口与原料中的焦炭充分反应,其化学方程式为 。
(2)生成铁的主要反应为Fe2O3+3CO 2Fe+3CO2,该反应中发生氧化反应的物质是 (填序号)。
A.Fe2O3 B.CO C.Fe D.CO2
(3)高炉气体的主要成分为N2、CO、CO2,如果将高炉气体通入足量的NaOH溶液中,发生反应的化学方程式为
。
C+O2 CO2
B
2NaOH+CO2==Na2CO3+H2O
金属的化学性质(高频考点)
(1)金属+氧气→
金属氧化物
2Mg+O2 2MgO
3Fe+2O2 Fe3O4
4Al+3O2 2Al2O3
2Cu+O2 2CuO
(2)金属+酸→
盐+ H2↑
Zn+2HCl====ZnCl2+H2↑
Zn+H2SO4====ZnSO4+H2↑
Fe+2HCl====FeCl2+H2↑
Fe+H2SO4====FeSO4+H2↑
(3)金属+盐→
新盐+ 新金属
Fe+CuSO4====FeSO4+Cu
Cu+2AgNO3====Cu(NO3)2+2Ag
1、金属的化学性质
反应发生的条件:
盐必须可溶,且在金属活动性
顺序中金属要排在盐中金属的前面
2.置换反应:
(1)定义:
(2)特点:
置换反应前后元素化合价一定改变
由一种单质与一种化合物反应,
生成另一种单质和另一种化合物的反应。
金属活动性顺序的应用:
3.金属活动性顺序:
由强逐渐减弱
①判断金属的活动性强弱:
金属的位置越靠前,它的活动性越强。
②判断金属与酸是否发生反应:
排在氢前面的金属能置换出盐酸、稀硫酸中的氢。
位于前面的金属能把位于后面金属从它们的盐溶液里置换出来。
③判断金属与盐溶液是否发生反应:
1、(2016·广安)常见金属X与硝酸银溶液反应的化学方程式为X+3AgNO3===3Ag+X(NO3)3,有关该反应说法错误的是( )
A.该反应是置换反应 B.X可能是铁
C.金属活动性X>Ag D.X表面有固体析出
B
2、(2015·广安)将相同状态的铁和镁分别与相同质量分数的稀盐酸反应,产生氢气的质量与反应时间的关系如图所示,下列说法正确的是( )
A.反应的铁和镁的质量相同
B.甲是铁,乙是镁
C.铁和镁完全反应所消耗的稀盐酸质量相同
D.反应后溶液的质量均减少
C
4、(2016·山西)在学习金属的化学性质时,老师给大家演示了如图所示的实验,下列说法正确的是( )
A.铜片表面始终没有明显变化
B.一段时间后溶液由无色变为浅绿色
C.反应后溶液中一定有硝酸铜,
可能有硝酸银
D.通过实验现象推测银和硫酸铜溶液
也可以反应
C
3、(2015·连云港)现有X、Y、Z三种金属,已知:①X和稀硫酸不反应 ②Z+H2SO4(稀)====ZSO4+H2↑ ③X+2YNO3====2Y+X(NO3)2 这三种金属的活动性顺序正确的是( )
A.X>Y>Z B.Z>X>Y C.Y>Z>X D.Z>Y>X
B
6.【同类变式】将一定量的铁粉和锌粉的混合物加入Cu(NO3)2溶液中,充分反应后过滤,向滤渣中加入稀盐酸,有气泡冒出。根据实验现象分析判断下列说法中,正确的是( )
A.滤液一定是无色的????????B.滤液中可能有Cu2+
C.滤渣中一定有Cu和Fe ??D.滤渣一定有Cu和Zn
C
5.(2016·乐山)某汽修厂清洗汽车零件后的废液中常含有一定量的AgNO3和Cu(NO3)2。向AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤液中加入稀盐酸,没有白色沉淀产生。下列正确的是( )
A.滤渣中一定没有Fe
B.滤液中一定有Fe(NO3)2和Cu(NO3)2
C.滤渣中一定有Ag,可能有Cu
D.滤液中一定有Fe(NO3)2,可能有AgNO3
C
金属与盐溶液混合时,反应的规律
(1)向几种盐的混合溶液中加入一种金属时,最不活泼的金属最先被置换出来。
(2)向一种盐溶液中加入几种金属时,最活泼的金属最先反应。
钢铁的锈蚀与防护
(高频考点)
1、铁生锈的条件:
3、防冶钢铁锈蚀的方法:
2、铁锈的主要成分:
4、保护金属资源的途径:
(1)防止金属的腐蚀
(2)回收利用废旧金属
(3)合理有效地开采矿物质
(4)寻找金属的代用品
(1)保持铁制品的洁净、干燥
(2)覆盖保护层(涂油、刷漆、镀别的金属等)
(3)改变金属的组成和结构(制成合金等)
铁与_____和_____同时接触
Fe2O3
氧气
水
5、回收废旧金属的意义
节约金属资源和能源、减少对环境的污染
1.(2016·漳州)下列情况中,铁钉容易生锈的是( )
A.在干燥的空气中 B.浸没在蒸馏水中
C.部分浸入食盐水中 D.浸没在植物油中
2.(2015·随州)一天,小明的爸爸在清理祖传宝物时发现:金手镯光彩夺目,完好无损,圆铜镜表面有少量铜锈,而铁弓则锈迹斑斑。请你帮忙解开他心中的疑问
(1)同是金属物件受损程度不同,说明金、铜、铁三种金属的活动性由强到弱的顺序是 。
(2)铜锈的主要成分是碱式碳酸铜[Cu2(OH)2CO3],铜生锈除了与氧气和水有关外,还与空气中的 有关。
(3)为了防止铁制品锈蚀,你的建议是(写一条即可)。
C
铁>铜>金(或Fe>Cu>Au)
CO2(或二氧化碳)
保持铁制品表面洁净和干燥
3.(2012·佛山)铁在潮湿的空气里会生锈蚀,要证明氧气一定参加了反应则必须要做的实验是( )
A.①② B.①③ C.②③ D.①②③
A
4、【变式备选】日常生活中的一些铁制品经常会被锈蚀。下列做法中不能起防锈作用的是( )
①在铁制品表面镀锌 ②在铁制品表面涂油
③保留铁件表面的铁锈作保护层 ④在铁器表面刷油漆
⑤自行车脏了用清水冲洗 ⑥用废酸液冲洗铁制污水管道⑦切完咸菜后,尽快将菜刀洗净擦干
A.②⑤ B.③⑤⑥ C.①③⑦ D.②⑥⑦
B
金属的化学性质(高频考点)
1、金属材料
2、金属矿物及其冶炼(铁的冶炼)
1、金属的化学性质
2、置换反应
3、金属活动性顺序
常见的金属材料
课堂小结与回顾
课后练习与提升:达标检测
人教五?四学制2011课标版
复习 第1课时
金属的化学性质(高频考点)
1、金属材料
2、金属矿物及其冶炼(铁的冶炼)
1、金属的化学性质
2、置换反应
3、金属活动性顺序
常见的金属材料
共性:
1、金属材料
特性
铁合金:
概念:
有金属光泽、导电性、导热性和延展性
颜色:大多数金属为_____色,
但铜为_____色,金为___色
状态:常温下大多数金属为固体,但汞为_____。
纯金属
银白
紫红
黄
液体
合金
特性:
在金属中加热熔合某些_____或_____,
制得的具有_____特征的物质。
合金属于_____物。
金属
非金属
金属
混合
强度和硬度一般比它们的纯
金属更高,抗腐蚀性更好
生铁和钢(含碳量不同)
常见的金属材料
2、金属矿物及其冶炼
铁的冶炼:
(1)原料:
(2)反应原理:
(3)实验装置及注意事项:
注意:CO早出晚归,处理尾气
铁矿石、焦炭、石灰石
现象:玻璃管中 ,澄清的石灰水 。
红色粉末变成黑色
变浑浊
1.(2016·乐山)汽车是现代生活中重要的交通工具。请 回答下列问题:
(1)汽车电路中的导线一般为铜芯线,这是利用了金属铜的延展性和________性。
(2)下列制造汽车所用到的材料中,属于合金的是________。(填序号)
①钢铁 ②合成橡胶 ③羊毛织物 ④铝合金 ⑤塑料
导电
①④
2.(2016·北京)铜能被加工成厚度仅为7 μm的超薄铜
箔,说明铜具有良好的( )
A.导电性 B.延展性 C.导热性 D.抗腐
B
3.(2015·宜宾)下列有关金属材料的说法正确的是( ) A.硬铝片比纯铝片硬度小 B.钢的性能优良,是很纯的铁
C.沙漠地区的铁制品锈蚀较快
D.为防止钢铁生锈,可在其表面涂油
D
4.(2015?重庆)如右图所示的炼铁高炉中发生了许多化学反应,其中就涉及碳及其化合物的相互转化。请回答下列问题。
(1)空气通过进风口与原料中的焦炭充分反应,其化学方程式为 。
(2)生成铁的主要反应为Fe2O3+3CO 2Fe+3CO2,该反应中发生氧化反应的物质是 (填序号)。
A.Fe2O3 B.CO C.Fe D.CO2
(3)高炉气体的主要成分为N2、CO、CO2,如果将高炉气体通入足量的NaOH溶液中,发生反应的化学方程式为
。
C+O2 CO2
B
2NaOH+CO2==Na2CO3+H2O
金属的化学性质(高频考点)
(1)金属+氧气→
金属氧化物
2Mg+O2 2MgO
3Fe+2O2 Fe3O4
4Al+3O2 2Al2O3
2Cu+O2 2CuO
(2)金属+酸→
盐+ H2↑
Zn+2HCl====ZnCl2+H2↑
Zn+H2SO4====ZnSO4+H2↑
Fe+2HCl====FeCl2+H2↑
Fe+H2SO4====FeSO4+H2↑
(3)金属+盐→
新盐+ 新金属
Fe+CuSO4====FeSO4+Cu
Cu+2AgNO3====Cu(NO3)2+2Ag
1、金属的化学性质
反应发生的条件:
盐必须可溶,且在金属活动性
顺序中金属要排在盐中金属的前面
2.置换反应:
(1)定义:
(2)特点:
置换反应前后元素化合价一定改变
由一种单质与一种化合物反应,
生成另一种单质和另一种化合物的反应。
金属活动性顺序的应用:
3.金属活动性顺序:
由强逐渐减弱
①判断金属的活动性强弱:
金属的位置越靠前,它的活动性越强。
②判断金属与酸是否发生反应:
排在氢前面的金属能置换出盐酸、稀硫酸中的氢。
位于前面的金属能把位于后面金属从它们的盐溶液里置换出来。
③判断金属与盐溶液是否发生反应:
1、(2016·广安)常见金属X与硝酸银溶液反应的化学方程式为X+3AgNO3===3Ag+X(NO3)3,有关该反应说法错误的是( )
A.该反应是置换反应 B.X可能是铁
C.金属活动性X>Ag D.X表面有固体析出
B
2、(2015·广安)将相同状态的铁和镁分别与相同质量分数的稀盐酸反应,产生氢气的质量与反应时间的关系如图所示,下列说法正确的是( )
A.反应的铁和镁的质量相同
B.甲是铁,乙是镁
C.铁和镁完全反应所消耗的稀盐酸质量相同
D.反应后溶液的质量均减少
C
4、(2016·山西)在学习金属的化学性质时,老师给大家演示了如图所示的实验,下列说法正确的是( )
A.铜片表面始终没有明显变化
B.一段时间后溶液由无色变为浅绿色
C.反应后溶液中一定有硝酸铜,
可能有硝酸银
D.通过实验现象推测银和硫酸铜溶液
也可以反应
C
3、(2015·连云港)现有X、Y、Z三种金属,已知:①X和稀硫酸不反应 ②Z+H2SO4(稀)====ZSO4+H2↑ ③X+2YNO3====2Y+X(NO3)2 这三种金属的活动性顺序正确的是( )
A.X>Y>Z B.Z>X>Y C.Y>Z>X D.Z>Y>X
B
6.【同类变式】将一定量的铁粉和锌粉的混合物加入Cu(NO3)2溶液中,充分反应后过滤,向滤渣中加入稀盐酸,有气泡冒出。根据实验现象分析判断下列说法中,正确的是( )
A.滤液一定是无色的????????B.滤液中可能有Cu2+
C.滤渣中一定有Cu和Fe ??D.滤渣一定有Cu和Zn
C
5.(2016·乐山)某汽修厂清洗汽车零件后的废液中常含有一定量的AgNO3和Cu(NO3)2。向AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤液中加入稀盐酸,没有白色沉淀产生。下列正确的是( )
A.滤渣中一定没有Fe
B.滤液中一定有Fe(NO3)2和Cu(NO3)2
C.滤渣中一定有Ag,可能有Cu
D.滤液中一定有Fe(NO3)2,可能有AgNO3
C
金属与盐溶液混合时,反应的规律
(1)向几种盐的混合溶液中加入一种金属时,最不活泼的金属最先被置换出来。
(2)向一种盐溶液中加入几种金属时,最活泼的金属最先反应。
钢铁的锈蚀与防护
(高频考点)
1、铁生锈的条件:
3、防冶钢铁锈蚀的方法:
2、铁锈的主要成分:
4、保护金属资源的途径:
(1)防止金属的腐蚀
(2)回收利用废旧金属
(3)合理有效地开采矿物质
(4)寻找金属的代用品
(1)保持铁制品的洁净、干燥
(2)覆盖保护层(涂油、刷漆、镀别的金属等)
(3)改变金属的组成和结构(制成合金等)
铁与_____和_____同时接触
Fe2O3
氧气
水
5、回收废旧金属的意义
节约金属资源和能源、减少对环境的污染
1.(2016·漳州)下列情况中,铁钉容易生锈的是( )
A.在干燥的空气中 B.浸没在蒸馏水中
C.部分浸入食盐水中 D.浸没在植物油中
2.(2015·随州)一天,小明的爸爸在清理祖传宝物时发现:金手镯光彩夺目,完好无损,圆铜镜表面有少量铜锈,而铁弓则锈迹斑斑。请你帮忙解开他心中的疑问
(1)同是金属物件受损程度不同,说明金、铜、铁三种金属的活动性由强到弱的顺序是 。
(2)铜锈的主要成分是碱式碳酸铜[Cu2(OH)2CO3],铜生锈除了与氧气和水有关外,还与空气中的 有关。
(3)为了防止铁制品锈蚀,你的建议是(写一条即可)。
C
铁>铜>金(或Fe>Cu>Au)
CO2(或二氧化碳)
保持铁制品表面洁净和干燥
3.(2012·佛山)铁在潮湿的空气里会生锈蚀,要证明氧气一定参加了反应则必须要做的实验是( )
A.①② B.①③ C.②③ D.①②③
A
4、【变式备选】日常生活中的一些铁制品经常会被锈蚀。下列做法中不能起防锈作用的是( )
①在铁制品表面镀锌 ②在铁制品表面涂油
③保留铁件表面的铁锈作保护层 ④在铁器表面刷油漆
⑤自行车脏了用清水冲洗 ⑥用废酸液冲洗铁制污水管道⑦切完咸菜后,尽快将菜刀洗净擦干
A.②⑤ B.③⑤⑥ C.①③⑦ D.②⑥⑦
B
金属的化学性质(高频考点)
1、金属材料
2、金属矿物及其冶炼(铁的冶炼)
1、金属的化学性质
2、置换反应
3、金属活动性顺序
常见的金属材料
课堂小结与回顾
课后练习与提升:达标检测
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
