人教版初中化学九年级下专题训练,同步练习,复习补习资料:专题10.1.3 常见的碱(第3课时)
文档属性
| 名称 | 人教版初中化学九年级下专题训练,同步练习,复习补习资料:专题10.1.3 常见的碱(第3课时) |

|
|
| 格式 | zip | ||
| 文件大小 | 600.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-21 00:00:00 | ||
图片预览




文档简介
第十单元 酸和碱
课题1 常见的酸和碱
知识
一、几种常见的碱
1.氢氧化钠
(1)物理性质
氢氧化钠是 色的固体, 溶于水,溶解时会 大量的热。在空气中容易吸收水分,表面潮湿并逐渐溶解,这种现象叫做 ,它属于 。
(2)保存
氢氧化钠具有吸水性,可做气体 ,因能与空气中的 反应而变质。氢氧化钠应_______保存。
(3)安全使用
氢氧化钠的俗名是_____________、_____________、_____________。有强烈的腐蚀性。如果不慎沾到皮肤上,采取的措施是_________________________________________________________。
(4)用途
氢氧化钠是一种重要的化工原料,用于制取_________,石油、造纸、纺织和印染等工业。还能制作炉具清洁剂,用来去除油污,其原理是________________________________。
2.氢氧化钙
(1)俗名是_____________、_____________,是一种_______________状固体。具有_________性,使用时要小心。
(2)溶解性
①__________溶于水,溶解度随温度的升高而___________。
②氢氧化钙的水溶液叫做_____________,含有较多未溶解的熟石灰时叫做__________________________。
(3)制备
由_____________和水反应得到,反应方程式为_______________________________________。
(4)用途
用作建筑材料;涂刷树木,能防止树木_________,并防止害虫____________;还能与_____________配制成具有杀菌作用的波尔多液;还可以用来改良_________性土壤。
3.其他常见的碱
常见的碱还有氢氧化钾、氨水、氢氧化铁、氢氧化铜、氢氧化镁等。
二、碱的化学性质
1.与酸碱指示剂反应
碱溶液能使指示剂变色:使紫色石蕊溶液变__________,使无色酚酞溶液变___________。 注意:难溶于水的碱不能使酸碱指示剂变色,如氢氧化铜、氢氧化铁、氢氧化镁等。
2.与部分非金属氧化物反应
(1)与二氧化碳的反应
①氢氧化钠:_____________________________________________(用化学方程式表示)。
②氢氧化钙:_____________________________________________。
(2)与二氧化硫的反应
①氢氧化钠:_____________________________________________。
②氢氧化钙:_____________________________________________。
(3)与三氧化硫的反应
①氢氧化钠:_____________________________________________。
②氢氧化钙:_____________________________________________。
三、溶液的导电性
1.导电性实验
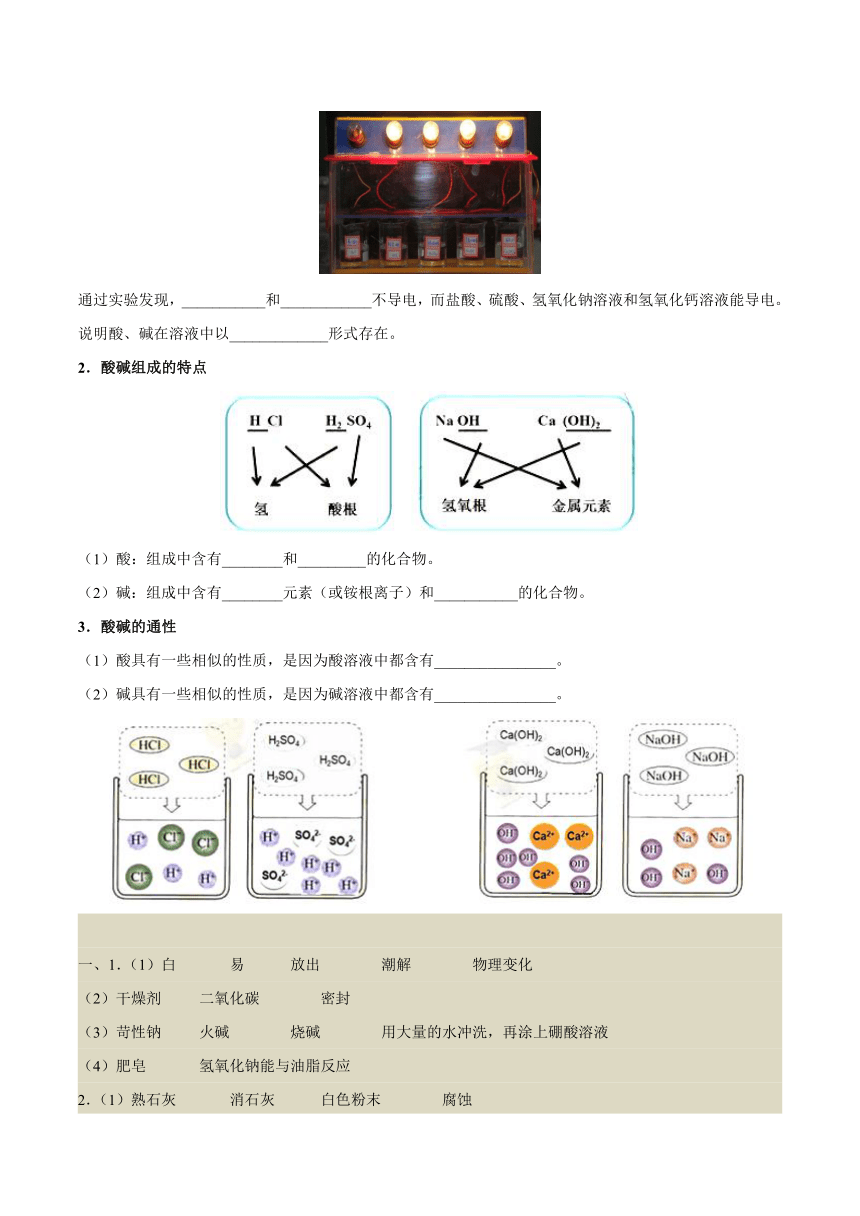
通过实验发现,___________和____________不导电,而盐酸、硫酸、氢氧化钠溶液和氢氧化钙溶液能导电。说明酸、碱在溶液中以_____________形式存在。
2.酸碱组成的特点
(1)酸:组成中含有________和_________的化合物。
(2)碱:组成中含有________元素(或铵根离子)和___________的化合物。
3.酸碱的通性
(1)酸具有一些相似的性质,是因为酸溶液中都含有________________。
(2)碱具有一些相似的性质,是因为碱溶液中都含有________________。
一、1.(1)白 易 放出 潮解 物理变化
(2)干燥剂 二氧化碳 密封
(3)苛性钠 火碱 烧碱 用大量的水冲洗,再涂上硼酸溶液
(4)肥皂 氢氧化钠能与油脂反应
2.(1)熟石灰 消石灰 白色粉末 腐蚀
(2)①微 减小
②石灰水 石灰乳或石灰浆
(3)生石灰 CaO+H2OCa(OH)2
(4)冻伤 生卵 硫酸铜 酸
二、1.蓝色 红色
2.(1)①2NaOH+CO2Na2CO3+H2O
②Ca(OH)2+CO2CaCO3↓+H2O
(2)①2NaOH+SO2Na2SO3+H2O
②Ca(OH)2+SO2CaSO3↓+H2O
(3)①2NaOH+SO3Na2SO4+H2O
②Ca(OH)2+SO3CaSO4↓+H2O
三、1.蒸馏水 乙醇 离子
2.(1)氢 酸根
(2)金属 氢氧根
3.(1)H+或氢离子
(2)OH-或氢氧根
重点
一、干燥剂和干燥器的选择
1.干燥剂的选择
根据被干燥气体的性质选择,不能让干燥剂与被干燥的气体反应。
干燥剂
可干燥的气体
不能干燥的气体
碱性
生石灰、固体氢氧化钠、碱石灰
碱性气体:NH3;中性气体:H2、O2、CO、CH4、N2等
酸性气体:H2S、CO2、SO2、HCl等
酸性
浓硫酸
酸性气体:CO2、SO2、HCl等;中性气体:H2、O2、CO、CH4、N2等
碱性气体:NH3;还原性气体:H2S等(浓硫酸具有强氧化性)
中性
无水氯化钙(CaCl2)
绝大多数气体
NH3(无水CaCl2与NH3反应生成CaCl2·8NH3)
二、氢氧化钠和氢氧化钙部分变质
1.氢氧化钠部分变质的证明方法 ①取样,(如果是固体,就需要加适量水,使固体完全溶解),加过量的氯化钙(或硝酸钙)溶液,如果有白色沉淀产生,说明有碳酸钠存在: Na2CO3+CaCl22NaCl+CaCO3↓或Na2CO3+Ca(NO3)22NaNO3+CaCO3↓ ②过滤,向滤液中滴加酚酞溶液,如果滤液变红,说明有氢氧化钠存在,氢氧化钠部分变质。
2.氢氧化钙固体部分变质的证明方法 ①取样,加入过量的稀盐酸,如果有气泡产生,说明有碳酸钙存在: CaCO3+2HClCaCl2+H2O+CO2↑ ②另取少量固体,加适量水使固体完全溶解,向上层清液中加入酚酞试液,若溶液变红色,说明有氢氧化钙存在,氢氧化钙部分变质。
三、氢氧化钠固体的称量方法
称量氢氧化钠固体时要放在玻璃皿中,不能放在纸上,防止氢氧化钠固体潮解后沾到纸片上;也不能用托盘直接测量,防止氢氧化钠固体潮解后腐蚀天平的托盘。
错误操作:
正确操作:
典例1 下列生活中的做法错误的是
A.用生石灰作食品干燥剂
B.用汽油或加了洗涤剂的水来除去衣服上的油污
C.浓硫酸作干燥剂时,气体要长进短出
D.实验室制取干燥的二氧化碳,用碱石灰作干燥剂
【解析】A、石灰水与水反应生成氢氧化钙固体,可作食品干燥剂,正确;B、汽油对油污有溶解作用,洗涤剂对油污有乳化作用,都能去除油污,正确;C、浓硫酸作干燥剂时,气体需通入浓硫酸中进行干燥,导管要长进短出,正确;D、碱石灰能与二氧化碳反应,不能用来干燥二氧化碳,错误。故选D。
【答案】D
典例2 下列溶液在空气中敞口放置后,溶液质量因发生化学反应而增大的是
A.浓氨水 B.浓硫酸
C.浓盐酸 D.烧碱溶液
【解析】A、浓氨水易挥发,所以敞口放置溶液的质量减少,不符合题意;B、浓硫酸具有吸水性,溶液质量增加,不符合题意;C、浓盐酸挥发使溶液的质量减少,但属于物理变化,不符合题意;D、烧碱溶液吸收二氧化碳反应生成碳酸钠,得到碳酸钠溶液,溶液质量增加,符合题意。故选D。
【答案】D
典例3 具备基本的化学实验技能是进行科学探究活动的基础和保证。下列实验操作正确的是
A.点燃酒精灯 B.
C. D.
【解析】A、点燃酒精灯时要用火柴点燃,不能用酒精灯引燃,容易发生火灾,错误;B、选用量筒时要选择比所量取液体量大,且最接近的,所以用10 mL量筒量取9.5 mL液体,错误;C、氢氧化钠具有腐蚀性,必须放在玻璃器皿中称量,错误;D、稀释浓硫酸时将浓硫酸沿着容器壁慢慢倒入水中,并用玻璃棒不断搅拌,并且标签朝手心(向上),正确。故选D。
【答案】D
基础训练
1.下列不是NaOH俗称的是
A.烧碱 B.火碱 C.纯碱 D.苛性钠
2.危险品要在包装标签上印有警示性标志。氢氧化钠应选用的标志是
??
3.酸和碱的组成中一定含有的元素是
A.氧元素
B.氢元素
C.氮元素
D.金属元素
4.熟石灰在日常生活中和工农业生产中有广泛的用途,下列关于熟石灰的用途中,说法不正确的是
A.作建筑材料
B.改良酸性土壤
C.制农药波尔多液
D.治疗胃酸过多
5.用如图所示装置进行实验,下列各组物质中,能使 U 型管内 a 端液面上升的是
A.硝酸铵和水 B.生石灰和水
C.镁条和稀盐酸 D.氢氧化钠和水
6.物质的用途与性质密切相关。下列说法不正确是
A.铜用于制导线,是由于铜有良好的导电性
B.氮气的化学性质比较稳定,可充入食品包装袋中防腐
C.氢氧化钠用于除去油污,是由于氢氧化钠能溶解油脂
D.人体胃液中含有盐酸,可帮助消化食物
7.下列物质的用途中,主要利用其物理性质的是
A.用生石灰做干燥剂
B.用氢气制造燃料电池
C.用铜丝制作导线
D.用稀盐酸除去水垢
8.下列有关熟石灰的说法错误的是
A.熟石灰又称为消石灰
B.熟石灰由生石灰与水反应制得
C.熟石灰的溶解度随温度升高而增大
D.熟石灰可以用来改良酸性土壤
能力提升
9.下列各组物质的名称或俗称和化学式表示的是同一种物质的是
A.熟石灰、消石灰、CaO
B.铁锈、氢氧化铁、Fe(OH)3
C.生石灰、消石灰、Ca(OH)2
D.烧碱、火碱、NaOH
10.实验室长期保存下列药品的方法中,不正确的是
A.氢氧化钠密封保存在试剂瓶中
B.硝酸银溶液密封保存在棕色试剂瓶中
C.浓盐酸密封保存在试剂瓶中
D.少量氨水保存在烧杯中
11.消石灰的主要成分是Ca(OH)2,是一种常用的廉价消毒剂。下列关于消石灰的说法不正确的是
A.消石灰的水溶液显碱性,滴加酚酞时溶液变蓝色
B.Ca(OH)2的化学式量是74
C.消石灰需要密封保存
D.由生石灰和水反应制得消石灰的反应是一个放热反应
12.在化学实验或日常生活中都应该强化安全意识。下列做法符合安全要求的是
A.氢氧化钠不慎沾到皮肤上,立即用硫酸冲洗
B.在一氧化碳还原氧化铁的实验中,将尾气直接排放
C.使用酒精灯时,直接向燃着的酒精灯内添加酒精
D.家中天然气泄漏时,立即关闭阀门并打开门窗通风
13.如图所示装置有多种用途,其中不正确的是
选项
广口瓶内盛放的药品
用途
A
浓硫酸
干燥氧气
B
水
收集氧气
C
氢氧化钠溶液
除去H2中混有的CO2气体
D
石灰水
检验CO2气体
真题练习
14.[2019·广州]下列物质属于碱的是
A.H2O B.NaHCO3 C.Ca(OH)2 D.H3BO3
15.[2019·重庆B]氢氧化钠溶液和氨水都能使酚酞溶液变红,其原因是二者的溶液中均含有一种相同的粒子是
A.H+ B.OH- C.H2O D.H
16.[2019·郴州]下列关于氢氧化钠的说法中错误的是
A.俗名苛性钠、火碱或烧碱
B.易溶于水,溶于水时吸收大量的热
C.氢氧化钠固体露置在空气中容易变质
D.是重要的化工原料,广泛用于肥皂、纺织、印刷等工业
17.[2019·泰州]下列对实验意外事故的处理方法错误的是
A.若不慎将稀硫酸溅入眼睛,要先用手揉眼睛,再立即用水冲洗
B.若不慎将烧碱溶液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液
C.若不慎将燃着的酒精灯碰倒,洒出的酒精在桌面上燃烧,应立刻用湿抹布扑盖
D.若不慎将少量浓硫酸沾到皮肤上,应立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液
18.[2019·聊城]某化学学习小组的同学对一瓶敞口放置氢氧化钙固体的化学成分产生了兴趣,他们根据自己所学知识进行如下探究:
【提出问题】该瓶药品的化学成分是什么?
【查阅资料】(1)氢氧化钙能与空气中的二氧化碳反应而变质。
(2)氢氧化钙的溶解度曲线如图:
【猜想假设】猜想一:Ca(OH)2
猜想二:____________________
猜想三:CaCO3
【实验验证】
实验操作
实验现象
实验结论
(1)取1 g样品放入盛有50 g水的烧杯中,充分搅拌后,静置
烧杯底部有较多固体未溶解
样品中含有CaCO3
(2)取实验(1)中上层清液少许于试管中,再向试管中滴加2~3滴无色酚酞试液
__________________________________
样品中含有Ca(OH)2
【得出结论】甲同学认为猜想二正确。
【反思交流】
(1)乙同学认为甲同学的结论不合理,他认为猜想_____也可能正确,原因是__________________________________________________________________。
(2)丙同学认为要想验证猜想二正确,还需做如下实验:取实验(1)中未溶解固体于试管中,向试管中滴加适量稀盐酸,如有___________________,则猜想二正确。
【拓展提升】要想验证反应后物质的成分,除需验证有生成物以外,还应考虑反应物是否________________。
参考答案
基础训练
1.【答案】C
【解析】氢氧化钠俗称烧碱、火碱、苛性钠,纯碱是碳酸钠的俗称。故选C。
2.【答案】A
3.【答案】B
【解析】酸是由氢离子和酸根离子构成的;碱是由金属离子和氢氧根离子构成的。故酸和碱中均含有氢元素。故选B。
4.【答案】D
【解析】A、主要成分是氢氧化钙的石灰浆可作建筑材料;B、氢氧化钙可以与酸发生反应,可用于改良酸性土壤;C、氢氧化钙和硫酸铜的混合制农药波尔多液;D、氢氧化钙的腐蚀性较强,不能用于治疗胃酸过多。故选D。
5.【答案】A
【解析】U 型管内 a 端液面上升,说明集气瓶内气体减少或温度降低,使瓶内气体压强变小。A、硝酸铵溶于水,溶液温度降低,符合题意;B、生石灰和水反应生成氢氧化钙,放出大量热,不符合题意;C、镁条和稀盐酸反应生成氢气,并且放出大量热,不符合题意;D、氢氧化钠和水溶于水放出大量热,不符合题意。故选A。
6.【答案】C
【解析】A、铜具有良好的导电性,故可以做导线,正确;B、氮气的化学性质比较稳定,可充入食品包装袋中隔绝氧气,起到防腐作用,正确;C、氢氧化钠用于除去油污,是由于氢氧化钠能与油脂发生反应,错误;D、人体胃液中含有盐酸,可帮助消化食物,正确。故选C。
7.【答案】C
【解析】物理性质是指物质不需要经过化学变化就直接表现出来的性质。化学性质是指物质经过化学变化表现出来的性质。A、用生石灰做干燥剂,生石灰与水发生了化学反应,属于化学性质;B、用氢气制造燃料电池,发生了化学反应,利用了氢气的还原性,属于化学性质;C、用铜丝制作导线,导电性属于物理性质;D、用稀盐酸除去水垢,稀盐酸与水垢发生了化学反应,利用了盐酸的酸性,属于化学性质。
8.【答案】C
【解析】A、氢氧化钙俗称熟石灰、消石灰,正确;B、生石灰与水反应生成熟石灰,正确;C、熟石灰的溶解度随温度的升高而减小,错误;D、氢氧化钙具有碱性,常用于改良酸性土壤,正确。故选C。
能力提升
9.【答案】D
10.【答案】D
【解析】A、因为氢氧化钠能吸收水分潮解,能与二氧化碳反应而变质,故应密封保存,叙述正确;B、硝酸银见光易分解,故保存在棕色瓶中,叙述正确;C、浓盐酸有挥发性,故要密封保存,叙述正确;D、氨水有挥发性,故要密封保存,叙述错误。故选D。
11.【答案】A
【解析】A、消石灰即氢氧化钙,其水溶液俗称石灰水,显碱性,滴加酚酞时溶液变红色,错误;B、化学式量=(相对原子质量×原子个数)之和,Ca(OH)2的化学式量是74,正确;C、消石灰易与空气中的二氧化碳反应而变质,需要密封保存,错误;D、由生石灰和水反应制得消石灰时会放出大量的热,正确。故选A。
12.【答案】D
【解析】A、H2SO4具有强的腐蚀性,能灼伤皮肤,不慎将NaOH沾到皮肤上,应该立即用大量的水冲洗,然后再涂上稀硼酸溶液,故A错误;B、一氧化碳有毒,若一氧化碳逸出会污染空气,应设计尾气吸收或处理装置,故B错误;C、使用酒精灯时,直接向燃着的酒精灯内添加酒精,容易引起酒精燃烧,故C错误;D、天然气泄漏时,立即关闭阀门使天然气不再泄漏,打开门窗通风使泄漏的天然气浓度降低,防止爆炸,故D正确。故选D。
13.【答案】B
【解析】A、用浓硫酸干燥氧气时,气体由长管进入,故A正确;B、用排水法收集氧气,瓶内盛满水,气体应该从短管进,利用气体的压力将水从长管压出,故B错误;C、氢气不与氢氧化钠溶液反应,而二氧化碳能与氢氧化钠溶液反应,所以可以除去氢气中混有的二氧化碳气体,故C正确;D、检验二氧化碳气体时,用澄清的石灰水,气体由长管进入,故D正确。故选B。
点睛:“多功能瓶”在实验中有很多用途:当用它净化或检验气体时,必须根据气体性质选择合适的实验试剂,气体由长管进入。此外可以用它来收集气体:若用排空气法收集气体,密度比空气大的气体由长管进入,比空气小的由短管进入;采用排水法收集,则需先将瓶子装满水,然后气体由短管进入;此外,气体净化原则:不减少被净化的气体,不能引进新的杂质。气体干燥原则:干燥剂只能吸收气体中的水分,不能与被干燥的气体发生反应。
真题练习
14.【答案】C
15.【答案】B
【解析】溶液的化学性质是由溶质溶于水产生的微粒决定的。氢氧化钠溶液和氨水都能使酚酞溶液变红,其原因是二者溶于水,发生电离,产生的阴离子都是氢氧根离子,溶液的相似的化学性质就是氢氧根离子的性质。故选B。
16.【答案】B
【解析】A、氢氧化钠的俗称有苛性钠、火碱或烧碱,正确;B、氢氧化钠易溶于水,溶于水的过程中放出热量,错误;C、氢氧化钠易与空气中的二氧化碳反应而变质,正确;D、氢氧化钠是是重要的化工原料,广泛用于肥皂、纺织、印刷等工业,正确。故选B。
17.【答案】A
【解析】A、若不慎将稀硫酸溅入眼睛,不要用手揉眼睛,应立即用大量的水冲洗,错误;B、若不慎将烧碱溶液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液,硼酸属于弱酸,可以中和碱,正确;C、若不慎将燃着的酒精灯碰倒,洒出的酒精在桌面上燃烧,应立刻用湿抹布扑盖,这是常用的有效方法,正确;D、若不慎将少量浓硫酸沾到皮肤上,应立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液,碳酸氢钠溶液呈碱性,与硫酸反应生成硫酸钠、水和二氧化碳,正确。故选A。
18.【答案】【猜想假设】?Ca(OH)2和CaCO3
【实验验证】溶液由无色变成红色
【反思交流】(1)一 氢氧化钙微溶于水,未溶解固体可能只含氢氧化钙
(2)气泡产生
【拓展提升】有剩余
【拓展提升】根据上述探究可知,要想验证反应后物质的成分,除需验证有生成物以外,还应考虑反应物是否有剩余。
课题1 常见的酸和碱
知识
一、几种常见的碱
1.氢氧化钠
(1)物理性质
氢氧化钠是 色的固体, 溶于水,溶解时会 大量的热。在空气中容易吸收水分,表面潮湿并逐渐溶解,这种现象叫做 ,它属于 。
(2)保存
氢氧化钠具有吸水性,可做气体 ,因能与空气中的 反应而变质。氢氧化钠应_______保存。
(3)安全使用
氢氧化钠的俗名是_____________、_____________、_____________。有强烈的腐蚀性。如果不慎沾到皮肤上,采取的措施是_________________________________________________________。
(4)用途
氢氧化钠是一种重要的化工原料,用于制取_________,石油、造纸、纺织和印染等工业。还能制作炉具清洁剂,用来去除油污,其原理是________________________________。
2.氢氧化钙
(1)俗名是_____________、_____________,是一种_______________状固体。具有_________性,使用时要小心。
(2)溶解性
①__________溶于水,溶解度随温度的升高而___________。
②氢氧化钙的水溶液叫做_____________,含有较多未溶解的熟石灰时叫做__________________________。
(3)制备
由_____________和水反应得到,反应方程式为_______________________________________。
(4)用途
用作建筑材料;涂刷树木,能防止树木_________,并防止害虫____________;还能与_____________配制成具有杀菌作用的波尔多液;还可以用来改良_________性土壤。
3.其他常见的碱
常见的碱还有氢氧化钾、氨水、氢氧化铁、氢氧化铜、氢氧化镁等。
二、碱的化学性质
1.与酸碱指示剂反应
碱溶液能使指示剂变色:使紫色石蕊溶液变__________,使无色酚酞溶液变___________。 注意:难溶于水的碱不能使酸碱指示剂变色,如氢氧化铜、氢氧化铁、氢氧化镁等。
2.与部分非金属氧化物反应
(1)与二氧化碳的反应
①氢氧化钠:_____________________________________________(用化学方程式表示)。
②氢氧化钙:_____________________________________________。
(2)与二氧化硫的反应
①氢氧化钠:_____________________________________________。
②氢氧化钙:_____________________________________________。
(3)与三氧化硫的反应
①氢氧化钠:_____________________________________________。
②氢氧化钙:_____________________________________________。
三、溶液的导电性
1.导电性实验
通过实验发现,___________和____________不导电,而盐酸、硫酸、氢氧化钠溶液和氢氧化钙溶液能导电。说明酸、碱在溶液中以_____________形式存在。
2.酸碱组成的特点
(1)酸:组成中含有________和_________的化合物。
(2)碱:组成中含有________元素(或铵根离子)和___________的化合物。
3.酸碱的通性
(1)酸具有一些相似的性质,是因为酸溶液中都含有________________。
(2)碱具有一些相似的性质,是因为碱溶液中都含有________________。
一、1.(1)白 易 放出 潮解 物理变化
(2)干燥剂 二氧化碳 密封
(3)苛性钠 火碱 烧碱 用大量的水冲洗,再涂上硼酸溶液
(4)肥皂 氢氧化钠能与油脂反应
2.(1)熟石灰 消石灰 白色粉末 腐蚀
(2)①微 减小
②石灰水 石灰乳或石灰浆
(3)生石灰 CaO+H2OCa(OH)2
(4)冻伤 生卵 硫酸铜 酸
二、1.蓝色 红色
2.(1)①2NaOH+CO2Na2CO3+H2O
②Ca(OH)2+CO2CaCO3↓+H2O
(2)①2NaOH+SO2Na2SO3+H2O
②Ca(OH)2+SO2CaSO3↓+H2O
(3)①2NaOH+SO3Na2SO4+H2O
②Ca(OH)2+SO3CaSO4↓+H2O
三、1.蒸馏水 乙醇 离子
2.(1)氢 酸根
(2)金属 氢氧根
3.(1)H+或氢离子
(2)OH-或氢氧根
重点
一、干燥剂和干燥器的选择
1.干燥剂的选择
根据被干燥气体的性质选择,不能让干燥剂与被干燥的气体反应。
干燥剂
可干燥的气体
不能干燥的气体
碱性
生石灰、固体氢氧化钠、碱石灰
碱性气体:NH3;中性气体:H2、O2、CO、CH4、N2等
酸性气体:H2S、CO2、SO2、HCl等
酸性
浓硫酸
酸性气体:CO2、SO2、HCl等;中性气体:H2、O2、CO、CH4、N2等
碱性气体:NH3;还原性气体:H2S等(浓硫酸具有强氧化性)
中性
无水氯化钙(CaCl2)
绝大多数气体
NH3(无水CaCl2与NH3反应生成CaCl2·8NH3)
二、氢氧化钠和氢氧化钙部分变质
1.氢氧化钠部分变质的证明方法 ①取样,(如果是固体,就需要加适量水,使固体完全溶解),加过量的氯化钙(或硝酸钙)溶液,如果有白色沉淀产生,说明有碳酸钠存在: Na2CO3+CaCl22NaCl+CaCO3↓或Na2CO3+Ca(NO3)22NaNO3+CaCO3↓ ②过滤,向滤液中滴加酚酞溶液,如果滤液变红,说明有氢氧化钠存在,氢氧化钠部分变质。
2.氢氧化钙固体部分变质的证明方法 ①取样,加入过量的稀盐酸,如果有气泡产生,说明有碳酸钙存在: CaCO3+2HClCaCl2+H2O+CO2↑ ②另取少量固体,加适量水使固体完全溶解,向上层清液中加入酚酞试液,若溶液变红色,说明有氢氧化钙存在,氢氧化钙部分变质。
三、氢氧化钠固体的称量方法
称量氢氧化钠固体时要放在玻璃皿中,不能放在纸上,防止氢氧化钠固体潮解后沾到纸片上;也不能用托盘直接测量,防止氢氧化钠固体潮解后腐蚀天平的托盘。
错误操作:
正确操作:
典例1 下列生活中的做法错误的是
A.用生石灰作食品干燥剂
B.用汽油或加了洗涤剂的水来除去衣服上的油污
C.浓硫酸作干燥剂时,气体要长进短出
D.实验室制取干燥的二氧化碳,用碱石灰作干燥剂
【解析】A、石灰水与水反应生成氢氧化钙固体,可作食品干燥剂,正确;B、汽油对油污有溶解作用,洗涤剂对油污有乳化作用,都能去除油污,正确;C、浓硫酸作干燥剂时,气体需通入浓硫酸中进行干燥,导管要长进短出,正确;D、碱石灰能与二氧化碳反应,不能用来干燥二氧化碳,错误。故选D。
【答案】D
典例2 下列溶液在空气中敞口放置后,溶液质量因发生化学反应而增大的是
A.浓氨水 B.浓硫酸
C.浓盐酸 D.烧碱溶液
【解析】A、浓氨水易挥发,所以敞口放置溶液的质量减少,不符合题意;B、浓硫酸具有吸水性,溶液质量增加,不符合题意;C、浓盐酸挥发使溶液的质量减少,但属于物理变化,不符合题意;D、烧碱溶液吸收二氧化碳反应生成碳酸钠,得到碳酸钠溶液,溶液质量增加,符合题意。故选D。
【答案】D
典例3 具备基本的化学实验技能是进行科学探究活动的基础和保证。下列实验操作正确的是
A.点燃酒精灯 B.
C. D.
【解析】A、点燃酒精灯时要用火柴点燃,不能用酒精灯引燃,容易发生火灾,错误;B、选用量筒时要选择比所量取液体量大,且最接近的,所以用10 mL量筒量取9.5 mL液体,错误;C、氢氧化钠具有腐蚀性,必须放在玻璃器皿中称量,错误;D、稀释浓硫酸时将浓硫酸沿着容器壁慢慢倒入水中,并用玻璃棒不断搅拌,并且标签朝手心(向上),正确。故选D。
【答案】D
基础训练
1.下列不是NaOH俗称的是
A.烧碱 B.火碱 C.纯碱 D.苛性钠
2.危险品要在包装标签上印有警示性标志。氢氧化钠应选用的标志是
??
3.酸和碱的组成中一定含有的元素是
A.氧元素
B.氢元素
C.氮元素
D.金属元素
4.熟石灰在日常生活中和工农业生产中有广泛的用途,下列关于熟石灰的用途中,说法不正确的是
A.作建筑材料
B.改良酸性土壤
C.制农药波尔多液
D.治疗胃酸过多
5.用如图所示装置进行实验,下列各组物质中,能使 U 型管内 a 端液面上升的是
A.硝酸铵和水 B.生石灰和水
C.镁条和稀盐酸 D.氢氧化钠和水
6.物质的用途与性质密切相关。下列说法不正确是
A.铜用于制导线,是由于铜有良好的导电性
B.氮气的化学性质比较稳定,可充入食品包装袋中防腐
C.氢氧化钠用于除去油污,是由于氢氧化钠能溶解油脂
D.人体胃液中含有盐酸,可帮助消化食物
7.下列物质的用途中,主要利用其物理性质的是
A.用生石灰做干燥剂
B.用氢气制造燃料电池
C.用铜丝制作导线
D.用稀盐酸除去水垢
8.下列有关熟石灰的说法错误的是
A.熟石灰又称为消石灰
B.熟石灰由生石灰与水反应制得
C.熟石灰的溶解度随温度升高而增大
D.熟石灰可以用来改良酸性土壤
能力提升
9.下列各组物质的名称或俗称和化学式表示的是同一种物质的是
A.熟石灰、消石灰、CaO
B.铁锈、氢氧化铁、Fe(OH)3
C.生石灰、消石灰、Ca(OH)2
D.烧碱、火碱、NaOH
10.实验室长期保存下列药品的方法中,不正确的是
A.氢氧化钠密封保存在试剂瓶中
B.硝酸银溶液密封保存在棕色试剂瓶中
C.浓盐酸密封保存在试剂瓶中
D.少量氨水保存在烧杯中
11.消石灰的主要成分是Ca(OH)2,是一种常用的廉价消毒剂。下列关于消石灰的说法不正确的是
A.消石灰的水溶液显碱性,滴加酚酞时溶液变蓝色
B.Ca(OH)2的化学式量是74
C.消石灰需要密封保存
D.由生石灰和水反应制得消石灰的反应是一个放热反应
12.在化学实验或日常生活中都应该强化安全意识。下列做法符合安全要求的是
A.氢氧化钠不慎沾到皮肤上,立即用硫酸冲洗
B.在一氧化碳还原氧化铁的实验中,将尾气直接排放
C.使用酒精灯时,直接向燃着的酒精灯内添加酒精
D.家中天然气泄漏时,立即关闭阀门并打开门窗通风
13.如图所示装置有多种用途,其中不正确的是
选项
广口瓶内盛放的药品
用途
A
浓硫酸
干燥氧气
B
水
收集氧气
C
氢氧化钠溶液
除去H2中混有的CO2气体
D
石灰水
检验CO2气体
真题练习
14.[2019·广州]下列物质属于碱的是
A.H2O B.NaHCO3 C.Ca(OH)2 D.H3BO3
15.[2019·重庆B]氢氧化钠溶液和氨水都能使酚酞溶液变红,其原因是二者的溶液中均含有一种相同的粒子是
A.H+ B.OH- C.H2O D.H
16.[2019·郴州]下列关于氢氧化钠的说法中错误的是
A.俗名苛性钠、火碱或烧碱
B.易溶于水,溶于水时吸收大量的热
C.氢氧化钠固体露置在空气中容易变质
D.是重要的化工原料,广泛用于肥皂、纺织、印刷等工业
17.[2019·泰州]下列对实验意外事故的处理方法错误的是
A.若不慎将稀硫酸溅入眼睛,要先用手揉眼睛,再立即用水冲洗
B.若不慎将烧碱溶液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液
C.若不慎将燃着的酒精灯碰倒,洒出的酒精在桌面上燃烧,应立刻用湿抹布扑盖
D.若不慎将少量浓硫酸沾到皮肤上,应立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液
18.[2019·聊城]某化学学习小组的同学对一瓶敞口放置氢氧化钙固体的化学成分产生了兴趣,他们根据自己所学知识进行如下探究:
【提出问题】该瓶药品的化学成分是什么?
【查阅资料】(1)氢氧化钙能与空气中的二氧化碳反应而变质。
(2)氢氧化钙的溶解度曲线如图:
【猜想假设】猜想一:Ca(OH)2
猜想二:____________________
猜想三:CaCO3
【实验验证】
实验操作
实验现象
实验结论
(1)取1 g样品放入盛有50 g水的烧杯中,充分搅拌后,静置
烧杯底部有较多固体未溶解
样品中含有CaCO3
(2)取实验(1)中上层清液少许于试管中,再向试管中滴加2~3滴无色酚酞试液
__________________________________
样品中含有Ca(OH)2
【得出结论】甲同学认为猜想二正确。
【反思交流】
(1)乙同学认为甲同学的结论不合理,他认为猜想_____也可能正确,原因是__________________________________________________________________。
(2)丙同学认为要想验证猜想二正确,还需做如下实验:取实验(1)中未溶解固体于试管中,向试管中滴加适量稀盐酸,如有___________________,则猜想二正确。
【拓展提升】要想验证反应后物质的成分,除需验证有生成物以外,还应考虑反应物是否________________。
参考答案
基础训练
1.【答案】C
【解析】氢氧化钠俗称烧碱、火碱、苛性钠,纯碱是碳酸钠的俗称。故选C。
2.【答案】A
3.【答案】B
【解析】酸是由氢离子和酸根离子构成的;碱是由金属离子和氢氧根离子构成的。故酸和碱中均含有氢元素。故选B。
4.【答案】D
【解析】A、主要成分是氢氧化钙的石灰浆可作建筑材料;B、氢氧化钙可以与酸发生反应,可用于改良酸性土壤;C、氢氧化钙和硫酸铜的混合制农药波尔多液;D、氢氧化钙的腐蚀性较强,不能用于治疗胃酸过多。故选D。
5.【答案】A
【解析】U 型管内 a 端液面上升,说明集气瓶内气体减少或温度降低,使瓶内气体压强变小。A、硝酸铵溶于水,溶液温度降低,符合题意;B、生石灰和水反应生成氢氧化钙,放出大量热,不符合题意;C、镁条和稀盐酸反应生成氢气,并且放出大量热,不符合题意;D、氢氧化钠和水溶于水放出大量热,不符合题意。故选A。
6.【答案】C
【解析】A、铜具有良好的导电性,故可以做导线,正确;B、氮气的化学性质比较稳定,可充入食品包装袋中隔绝氧气,起到防腐作用,正确;C、氢氧化钠用于除去油污,是由于氢氧化钠能与油脂发生反应,错误;D、人体胃液中含有盐酸,可帮助消化食物,正确。故选C。
7.【答案】C
【解析】物理性质是指物质不需要经过化学变化就直接表现出来的性质。化学性质是指物质经过化学变化表现出来的性质。A、用生石灰做干燥剂,生石灰与水发生了化学反应,属于化学性质;B、用氢气制造燃料电池,发生了化学反应,利用了氢气的还原性,属于化学性质;C、用铜丝制作导线,导电性属于物理性质;D、用稀盐酸除去水垢,稀盐酸与水垢发生了化学反应,利用了盐酸的酸性,属于化学性质。
8.【答案】C
【解析】A、氢氧化钙俗称熟石灰、消石灰,正确;B、生石灰与水反应生成熟石灰,正确;C、熟石灰的溶解度随温度的升高而减小,错误;D、氢氧化钙具有碱性,常用于改良酸性土壤,正确。故选C。
能力提升
9.【答案】D
10.【答案】D
【解析】A、因为氢氧化钠能吸收水分潮解,能与二氧化碳反应而变质,故应密封保存,叙述正确;B、硝酸银见光易分解,故保存在棕色瓶中,叙述正确;C、浓盐酸有挥发性,故要密封保存,叙述正确;D、氨水有挥发性,故要密封保存,叙述错误。故选D。
11.【答案】A
【解析】A、消石灰即氢氧化钙,其水溶液俗称石灰水,显碱性,滴加酚酞时溶液变红色,错误;B、化学式量=(相对原子质量×原子个数)之和,Ca(OH)2的化学式量是74,正确;C、消石灰易与空气中的二氧化碳反应而变质,需要密封保存,错误;D、由生石灰和水反应制得消石灰时会放出大量的热,正确。故选A。
12.【答案】D
【解析】A、H2SO4具有强的腐蚀性,能灼伤皮肤,不慎将NaOH沾到皮肤上,应该立即用大量的水冲洗,然后再涂上稀硼酸溶液,故A错误;B、一氧化碳有毒,若一氧化碳逸出会污染空气,应设计尾气吸收或处理装置,故B错误;C、使用酒精灯时,直接向燃着的酒精灯内添加酒精,容易引起酒精燃烧,故C错误;D、天然气泄漏时,立即关闭阀门使天然气不再泄漏,打开门窗通风使泄漏的天然气浓度降低,防止爆炸,故D正确。故选D。
13.【答案】B
【解析】A、用浓硫酸干燥氧气时,气体由长管进入,故A正确;B、用排水法收集氧气,瓶内盛满水,气体应该从短管进,利用气体的压力将水从长管压出,故B错误;C、氢气不与氢氧化钠溶液反应,而二氧化碳能与氢氧化钠溶液反应,所以可以除去氢气中混有的二氧化碳气体,故C正确;D、检验二氧化碳气体时,用澄清的石灰水,气体由长管进入,故D正确。故选B。
点睛:“多功能瓶”在实验中有很多用途:当用它净化或检验气体时,必须根据气体性质选择合适的实验试剂,气体由长管进入。此外可以用它来收集气体:若用排空气法收集气体,密度比空气大的气体由长管进入,比空气小的由短管进入;采用排水法收集,则需先将瓶子装满水,然后气体由短管进入;此外,气体净化原则:不减少被净化的气体,不能引进新的杂质。气体干燥原则:干燥剂只能吸收气体中的水分,不能与被干燥的气体发生反应。
真题练习
14.【答案】C
15.【答案】B
【解析】溶液的化学性质是由溶质溶于水产生的微粒决定的。氢氧化钠溶液和氨水都能使酚酞溶液变红,其原因是二者溶于水,发生电离,产生的阴离子都是氢氧根离子,溶液的相似的化学性质就是氢氧根离子的性质。故选B。
16.【答案】B
【解析】A、氢氧化钠的俗称有苛性钠、火碱或烧碱,正确;B、氢氧化钠易溶于水,溶于水的过程中放出热量,错误;C、氢氧化钠易与空气中的二氧化碳反应而变质,正确;D、氢氧化钠是是重要的化工原料,广泛用于肥皂、纺织、印刷等工业,正确。故选B。
17.【答案】A
【解析】A、若不慎将稀硫酸溅入眼睛,不要用手揉眼睛,应立即用大量的水冲洗,错误;B、若不慎将烧碱溶液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液,硼酸属于弱酸,可以中和碱,正确;C、若不慎将燃着的酒精灯碰倒,洒出的酒精在桌面上燃烧,应立刻用湿抹布扑盖,这是常用的有效方法,正确;D、若不慎将少量浓硫酸沾到皮肤上,应立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液,碳酸氢钠溶液呈碱性,与硫酸反应生成硫酸钠、水和二氧化碳,正确。故选A。
18.【答案】【猜想假设】?Ca(OH)2和CaCO3
【实验验证】溶液由无色变成红色
【反思交流】(1)一 氢氧化钙微溶于水,未溶解固体可能只含氢氧化钙
(2)气泡产生
【拓展提升】有剩余
【拓展提升】根据上述探究可知,要想验证反应后物质的成分,除需验证有生成物以外,还应考虑反应物是否有剩余。
同课章节目录
