人教版初中化学九年级下专题训练,同步练习,复习补习资料:专题10.2.1 中和反应(第1课时)
文档属性
| 名称 | 人教版初中化学九年级下专题训练,同步练习,复习补习资料:专题10.2.1 中和反应(第1课时) |
|
|
| 格式 | zip | ||
| 文件大小 | 728.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-21 00:00:00 | ||
图片预览





文档简介
第十单元 酸和碱
课题2 酸和碱的中和反应
知识
一、中和反应
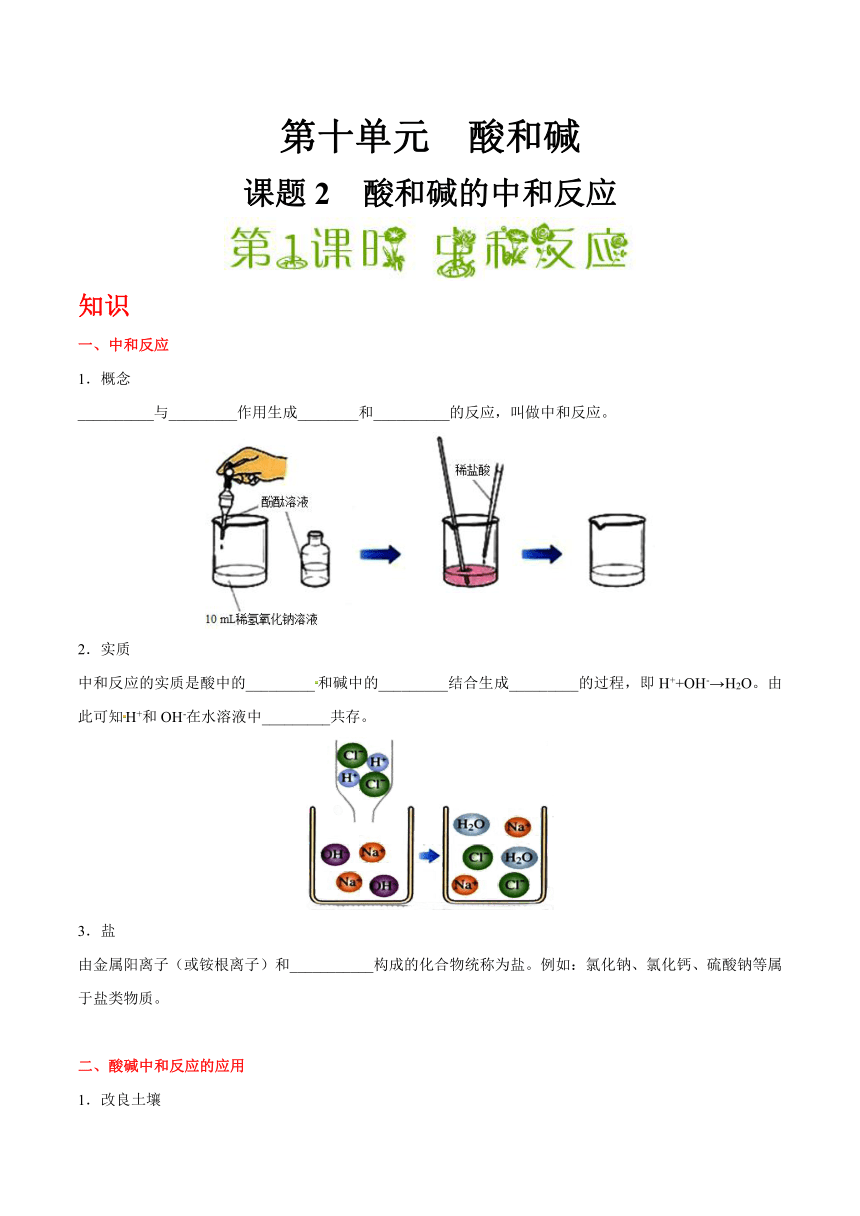
1.概念
__________与_________作用生成________和__________的反应,叫做中和反应。
2.实质
中和反应的实质是酸中的_________和碱中的_________结合生成_________的过程,即H++OH-→H2O。由此可知H+和OH-在水溶液中_________共存。
3.盐
由金属阳离子(或铵根离子)和___________构成的化合物统称为盐。例如:氯化钠、氯化钙、硫酸钠等属于盐类物质。
二、酸碱中和反应的应用 1.改良土壤
农作物一般适宜在中性或接近中性土壤中生长,如果土壤酸性或碱性太强都不利于农作物的生长。若某地区土壤显酸性,可将适量的_____________加入土壤中,以中和酸性物质。
2.处理工厂废水
(1)一般用_____________中和硫酸厂的废水。
(2)若工厂的废水显碱性,则可用____________中和。
3.用于医药
(1)人的胃液中含有适量的____________,可以帮助消化。但是胃酸过多,反而造成消化不良,可以服用含氢氧化铝的药物中和胃酸过多。
(2)被黄蜂蛰了(黄蜂毒液显________性)可以涂抹食醋减轻痛痒;被蚊虫叮咬(分泌________)后涂抹碱性物质,如肥皂水、牙膏等物质可以减轻痛痒。
一、1.酸 碱 盐 水
2.H+ OH- 水 不能
3.酸根离子
二、1.熟石灰
2.(1)熟石灰
(2)硫酸
3.(1)盐酸
(2)碱 蚁酸
重点
一、酸、碱、盐类物质的比较
名称
构成粒子
水溶液中解离出的离子
特点
举例
酸
分子
H+和酸根离子
阳离子全部是H+
HCl、H2SO4
碱
离子或分子
OH-和金属离子(或铵根离子)
阴离子全部是OH-
NaOH、Ca(OH)2、Ba(OH)2
盐
离子
金属离子(或铵根离子)和酸根离子
除金属离子(或铵根离子)和酸根离子外,可能还含有其他离子
NaCl、K2SO4、
NaHSO4、CuSO4
二、中和反应
1.中和反应不是基本反应类型,它特指酸和碱作用生成盐和水的反应。
2.中和反应生成盐和水,但生成盐和水的反应不一定是中和反应,如Fe2O3+3H2SO4Fe2(SO4)3+3H2O、2NaOH+CO2Na2CO3+H2O。
典例1 郴州市万华岩是一处规模宏大至今仍在发育的地下河溶洞,属于我国南方典型的喀斯特岩溶地貌,溶洞中的钟乳石、石笋、石柱的主要成分是CaCO3。CaCO3属于
A.酸 B.碱 C.盐 D.氧化物
【解析】酸能电离出氢离子;碱能电离出氢氧根离子;由两种元素组成,其中一种元素是氧元素的化合物,叫做氧化物;盐是由金属离子和酸根离子构成的化合物。CaCO3是由钙离子和碳酸根离子构成,属于盐。故选C。
【答案】C
典例2 下列实际应用中,与中和反应原理无关的是
A.用浓硫酸干燥氧气
B.用熟石灰改良酸性土壤
C.用肥皂水涂在被蚊虫叮咬的皮肤上止痒
D.用氢氧化钠溶液洗涤石油产品中残留的硫酸
【解析】A、浓硫酸具有吸水性,可以干燥氧气,与中和反应的原理无关,符合题意;B、用熟石灰改良酸性土壤,是用氢氧化钙与酸反应,生成盐和水,故与中和反应的原理有关,不符合题意;C、用肥皂水涂在被蚊虫叮咬的皮肤上止痒是利用了肥皂水的碱性与蚁酸反应,故与中和反应的原理有关,不符合题意;D、用氢氧化钠溶液洗涤石油产品中残留的硫酸是利用氢氧化钠与硫酸反应生成硫酸钠和水,与中和反应的原理有关,不符合题意。故选A。
【答案】A
基础训练
1.某氧化物不仅可作干燥剂,还能与酸反应,用于改良酸性土壤,该氧化物是
A.CaO B.CO2
C.H2O D.CuO
2.槟榔芋皮上含有一种碱性的物质——皂角素,皮肤沾上它会奇痒难忍。你认为以下物质适合用来涂抹止痒的是
A.食盐水 B.肥皂水
C.硫酸溶液 D.食醋
3.一辆运输浓盐酸的车辆发生事故,导致酸液在闹市泄漏,经喷水和撒石灰处理后,排除了险情。下列对喷水和撒石灰这一做法的叙述,错误的是
A.喷水可以减少浓盐酸挥发
B.喷水可以降低盐酸酸性
C.撒石灰是为了消除盐酸污染
D.喷水是为了尽快把盐酸冲进下水道
4.物质X可发生下列所示的两个反应:①X+酸→盐+H2O,②X+非金属氧化物→盐+H2O。则X可能是
A.CaO
B.H2SO4
C.NaOH
D.CO2
5.分类是学习化学的方法之一,下列物质是按单质、盐、混合物的顺序排列的是
A.氧气、碳酸钙、空气
B.氢气、硫酸钠、水
C.甲烷、食盐、冰水
D.金刚石、熟石灰、石油
6.下列化学方程式符合题意且书写正确的是
A.正常的雨水略呈酸性的原因:CO2 + H2OH2CO3
B.生活中用天然气作燃料:C2H5OH + 3O22CO2 + 3H2O
C.胃舒平(含氢氧化铝)治疗胃酸过多症:Al(OH)3 + HClAlCl3 + H2O
D.用大理石和盐酸制取二氧化碳:CaCO3 + 2HClCaCl2 + H2O + CO2
7.下列生活中的做法错误的是
A.用食醋去除水壶中的水垢
B.钢铁表面采用涂油、刷漆、镀铬等方法都能防止钢铁生锈
C.用火碱来除去衣服上的油污
D.蚊虫叮咬后,用肥皂水涂抹患处以减轻痛痒
8.根据如图实验判断下列说法错误的是
A.浓盐酸有挥发性
B.分子在不断运动
C.B烧杯溶液的颜色会改变
D.实验后B烧杯内溶液颜色为无色,说明二者恰好完全反应
能力提升
9.以下应用与中和反应原理无关的是
A.用含碳酸氢钠和有机酸的发酵粉焙制糕点
B.服用含氢氧化镁的药物治疗胃酸过多
C.用硫酸溶液处理印染厂废水中残留的氢氧化钠
D.在蚊虫叮咬处涂抹稀氨水可以减轻蚊虫分泌的蚁酸造成的痛痒
10.在总结化学知识时,以下归纳或判断正确的是
A.有水生成的放热反应一定是中和反应
B.由一种元素组成的物质一定是单质
C.能分解产生氧气的物质一定含有氧元素
D.能与碱反应生成盐和水的物质一定是酸
11.取2%的NaOH溶液20 g和2%的HCl溶液20 g,使其充分反应,所得到的溶液能使紫色石蕊试液显
A.红色 B.蓝色
C.无色 D.紫色
12.中和反应是放热反应吗?三位同学为探究此问题进行了下列实验:
(1)甲同学取10 mL?10%的NaOH溶液于试管中,逐滴加入10%的稀硫酸,随着硫酸的加入,烧杯中溶液温度与加入硫酸体积之间的变化关系如甲图所示。本实验选用10%的NaOH溶液而不选用NaOH固体的原因是__________________________________________________________________________。
(2)乙同学按乙图装置进行实验,其中的澄清饱和石灰水的作用是_______________________________________________________________________________。
(3)丙同学按丙图实验,可以根据______________________________________的现象也能证明中和反应是放热的。
真题练习
13.[2019·南京]下列物质所对应的用途不正确的是
A.大理石——用作建筑材料
B.钛合金——制造人造骨
C.氢氧化钠——治疗胃酸过多
D.熟石灰——改良酸性土壤
14.[2019·宿迁]下列说法正确的是
A.稀盐酸、稀硫酸化学性质相似,是因为其溶液中都含有H+
B.生成盐和水的反应一定是中和反应
C.将硝酸铵固体溶于水溶液温度会升高
D.目前计入空气污染指数的有害气体包括:SO2、NO2、CO2、CO等
15.[2019·淄博]如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论正确的是
A.反应后溶液的pH大于7
B.反应前的溶液均可导电,反应后的溶液不导电
C.反应后溶液中存在的粒子只有Na+和Cl-
D.反应前后所有元素的化合价均无变化
16.[2019·鄂州]某实验小组的同学用氢氧化钠溶液和盐酸做中和反应的实验,当他们向盛有氢氧化钠溶液的烧杯中滴加一定量的稀盐酸后,发现忘记了滴加指示剂。他们停止滴加稀盐酸,对烧杯内溶液中的溶质成分进行探究。
(1)写出该中和反应的化学方程式:______________________________________________。
(2)探究烧杯内溶液中溶质的成分。
【猜想】
猜想一:可能是NaCl和NaOH;
猜想二:可能只有NaCl;
猜想三:_________________________________________。
【进行实验】
实验步骤
实验操作
实验现象
结论
①
取少量烧杯内的溶液于试管中,滴入几滴酚酞溶液,振荡
____________
猜想一不成立
②
取少量烧杯内的溶液于试管中,滴加碳酸钠溶液
____________
猜想三成立
参考答案
基础训练
1.【答案】A
【解析】不仅可作干燥剂,还能与酸反应,用于改良酸性土壤,应属于碱性氧化物,该氧化物是CaO。二氧化碳、水、氧化铜不能做干燥剂,且氧化铜与酸反应生成的铜离子属于重金属离子,污染土壤。故选A。
2.【答案】D
【解析】皂角素显碱性,利用中和反应原理,应该选用酸性物质。A、食盐水,显中性,错误;B、肥皂水,显碱性,错误;C、硫酸溶液,显酸性,但有很强的腐蚀性,错误;D、食醋(含有醋酸)显酸性,腐蚀性不强,正确。故选D。
3.【答案】D
4.【答案】C
【解析】A、CaO与非金属氧化物反应生成盐,但不会生成水,故A错误;B、H2SO4和酸、非金属氧化物均不反应,故B错误;C、可溶性的碱既能与非金属氧化物反应,又能与酸反应,故C正确;D、CO2和酸、非金属氧化物均不反应,故D错误。故选C。
5.【答案】A
【解析】按单质、盐、混合物的顺序排列的是氧气、碳酸钙、空气。B、水是纯净物;C、冰水是纯净物;D、熟石灰是碱。故选A。
6.【答案】A
【解析】A、二氧化碳溶于水生成的碳酸具有酸性,故正常雨水呈酸性的原因是CO2+H2OH2CO3,正确;B、天然气的主要成分为甲烷,错误;C、胃舒平主要成分氢氧化铝能与盐酸发生中和反应,且氢氧化铝没有腐蚀性,故常用来治疗胃酸过多症,反应方程式未配平,正确的化学方程式为Al(OH)3 + 3HClAlCl3 + 3H2O,错误;D、用大理石和盐酸制取二氧化碳,化学方程式中要标注气体符号,准确的化学方程式为CaCO3+2HClCaCl2+H2O+CO2↑,错误。故选A。
7.【答案】C
8.【答案】D
【解析】A、一段时间后B烧杯中的酚酞溶液颜色变为无色,而两者没有直接接触,说明浓盐酸有挥发性,故选项说法正确;B、一段时间后B烧杯中的酚酞溶液颜色变为无色,而两者没有直接接触,说明分子是在不断的运动的,故选项说法正确;C、浓盐酸中挥发出来的氯化氢气体,与氢氧化钠反应生成氯化钠和水,溶液的碱性减弱,至恰好完全反应,溶液由红色变为无色,故选项说法正确;D、浓盐酸中挥发出来的氯化氢气体,与氢氧化钠反应生成氯化钠和水,烧杯B中氯化氢有剩余也是无色,故选项说法错误。故选D。
能力提升
9.【答案】A
【解析】A、用含碳酸氢钠和有机酸的发酵粉焙制糕点,该反应是盐与酸的反应,不属于中和反应,符合题意;B、胃酸的主要成分是盐酸,氢氧化镁和盐酸反应生成氯化镁和水,该反应是酸与碱的反应,属于中和反应,不符合题意;C、用硫酸溶液处理印染厂废水中残留的NaOH,氢氧化钠溶液与硫酸反应生成硫酸钠和水,该反应是酸与碱反应生成盐和水的反应,属于中和反应,不符合题意;D、在蚊虫叮咬处涂抹稀氨水可以减轻蚊虫分泌出的蚁酸造成的痛痒,稀氨水属于碱,与蚁酸反应生成盐和水,该反应是酸与碱反应生成盐和水的反应,属于中和反应,不符合题意。故选B。
10.【答案】C
【解析】A、氢气燃烧放热,产物是水,错误;B、由一种元素组成的纯净物一定是单质,但是由一种元素组成的物质不一定是单质,比如氧气和臭氧的混合物,错误;C、根据质量守恒定律,能分解产生氧气的物质一定含有氧元素,正确;D、能与碱反应生成盐和水的物质不一定是酸,二氧化碳能和氢氧化钙反应生成碳酸钙和水,但是二氧化碳是氧化物,错误。故选C。
11.【答案】A
12.【答案】(1)氢氧化钠固体溶于水放热,会对实验造成干扰
(2)饱和石灰水变浑浊,说明氢氧化钠与硫酸反应能放出热量
(3)浸入烧杯内水中的导管口有气泡冒出
【解析】(1)氢氧化钠固体溶于水放热,会对实验造成干扰,不能探究中和反应本身是否放热。(2)氢氧化钙的溶解度随温度的升高而减小,饱和溶液升温时,会因溶解度减小析出固体而变浑浊。饱和石灰水变浑浊,说明氢氧化钠与硫酸反应能放出热量。(3)中和反应放热能使广口瓶内气体受热膨胀而逸出,浸入烧杯水中的导管口有气泡冒出。
真题练习
13.【答案】C
【解析】A、大理石坚硬、美观、耐磨,常用作建筑材料,正确;B、钛合金与人体具有很好的相容性,常用来制造人造骨,正确;C、氢氧化钠属于强碱,不可治疗胃酸过多,错误;D、熟石灰属于碱,能与碱中和,并且价格便宜,常用来改良酸性土壤,正确。故选C。
14.【答案】A
【解析】A、稀盐酸、稀硫酸化学性质相似,是因为其溶液中都含有H+,该选项说法正确;B、生成盐和水的反应不一定是中和反应,例如二氧化碳和氢氧化钠反应生成碳酸钠和水,不属于中和反应,该选项说法不正确;C、将硝酸铵固体溶于水时,吸热,导致溶液温度降低,该选项说法不正确;D、目前计入空气污染指数的有害气体不包括二氧化碳,该选项说法不正确。故选A。
15.【答案】D
16.【答案】(1)NaOH + HClNaCl + H2O
(2)【猜想】可能是NaCl和HCl
【进行实验】①溶液不变色
②有气泡产生
【解析】(1)氢氧化钠溶液和盐酸中和反应生成氯化钠和水,根据质量守恒定律和观察法配平反应的化学方程式,该中和反应的化学方程式为NaOH + HClNaCl + H2O。(2)烧杯内溶液中溶质的成分有三种可能:一是加入的盐酸不足,则氢氧化钠有剩余,故溶质为剩余的氢氧化钠和生成的氯化钠;二是加入的盐酸恰好完全反应,则烧杯内溶液中溶质为反应生成的氯化钠;三是加入的盐酸过量,则烧杯内溶液中溶质为反应生成的氯化钠和过量盐酸中的氯化氢。故猜想三:可能是NaCl和HCl。【进行实验】①猜想一不成立,则溶液可能呈酸性或中性,不能使酚酞试液变色;②猜想三成立,说明溶液中含有盐酸,加入碳酸钠溶液,有气泡产生。
课题2 酸和碱的中和反应
知识
一、中和反应
1.概念
__________与_________作用生成________和__________的反应,叫做中和反应。
2.实质
中和反应的实质是酸中的_________和碱中的_________结合生成_________的过程,即H++OH-→H2O。由此可知H+和OH-在水溶液中_________共存。
3.盐
由金属阳离子(或铵根离子)和___________构成的化合物统称为盐。例如:氯化钠、氯化钙、硫酸钠等属于盐类物质。
二、酸碱中和反应的应用 1.改良土壤
农作物一般适宜在中性或接近中性土壤中生长,如果土壤酸性或碱性太强都不利于农作物的生长。若某地区土壤显酸性,可将适量的_____________加入土壤中,以中和酸性物质。
2.处理工厂废水
(1)一般用_____________中和硫酸厂的废水。
(2)若工厂的废水显碱性,则可用____________中和。
3.用于医药
(1)人的胃液中含有适量的____________,可以帮助消化。但是胃酸过多,反而造成消化不良,可以服用含氢氧化铝的药物中和胃酸过多。
(2)被黄蜂蛰了(黄蜂毒液显________性)可以涂抹食醋减轻痛痒;被蚊虫叮咬(分泌________)后涂抹碱性物质,如肥皂水、牙膏等物质可以减轻痛痒。
一、1.酸 碱 盐 水
2.H+ OH- 水 不能
3.酸根离子
二、1.熟石灰
2.(1)熟石灰
(2)硫酸
3.(1)盐酸
(2)碱 蚁酸
重点
一、酸、碱、盐类物质的比较
名称
构成粒子
水溶液中解离出的离子
特点
举例
酸
分子
H+和酸根离子
阳离子全部是H+
HCl、H2SO4
碱
离子或分子
OH-和金属离子(或铵根离子)
阴离子全部是OH-
NaOH、Ca(OH)2、Ba(OH)2
盐
离子
金属离子(或铵根离子)和酸根离子
除金属离子(或铵根离子)和酸根离子外,可能还含有其他离子
NaCl、K2SO4、
NaHSO4、CuSO4
二、中和反应
1.中和反应不是基本反应类型,它特指酸和碱作用生成盐和水的反应。
2.中和反应生成盐和水,但生成盐和水的反应不一定是中和反应,如Fe2O3+3H2SO4Fe2(SO4)3+3H2O、2NaOH+CO2Na2CO3+H2O。
典例1 郴州市万华岩是一处规模宏大至今仍在发育的地下河溶洞,属于我国南方典型的喀斯特岩溶地貌,溶洞中的钟乳石、石笋、石柱的主要成分是CaCO3。CaCO3属于
A.酸 B.碱 C.盐 D.氧化物
【解析】酸能电离出氢离子;碱能电离出氢氧根离子;由两种元素组成,其中一种元素是氧元素的化合物,叫做氧化物;盐是由金属离子和酸根离子构成的化合物。CaCO3是由钙离子和碳酸根离子构成,属于盐。故选C。
【答案】C
典例2 下列实际应用中,与中和反应原理无关的是
A.用浓硫酸干燥氧气
B.用熟石灰改良酸性土壤
C.用肥皂水涂在被蚊虫叮咬的皮肤上止痒
D.用氢氧化钠溶液洗涤石油产品中残留的硫酸
【解析】A、浓硫酸具有吸水性,可以干燥氧气,与中和反应的原理无关,符合题意;B、用熟石灰改良酸性土壤,是用氢氧化钙与酸反应,生成盐和水,故与中和反应的原理有关,不符合题意;C、用肥皂水涂在被蚊虫叮咬的皮肤上止痒是利用了肥皂水的碱性与蚁酸反应,故与中和反应的原理有关,不符合题意;D、用氢氧化钠溶液洗涤石油产品中残留的硫酸是利用氢氧化钠与硫酸反应生成硫酸钠和水,与中和反应的原理有关,不符合题意。故选A。
【答案】A
基础训练
1.某氧化物不仅可作干燥剂,还能与酸反应,用于改良酸性土壤,该氧化物是
A.CaO B.CO2
C.H2O D.CuO
2.槟榔芋皮上含有一种碱性的物质——皂角素,皮肤沾上它会奇痒难忍。你认为以下物质适合用来涂抹止痒的是
A.食盐水 B.肥皂水
C.硫酸溶液 D.食醋
3.一辆运输浓盐酸的车辆发生事故,导致酸液在闹市泄漏,经喷水和撒石灰处理后,排除了险情。下列对喷水和撒石灰这一做法的叙述,错误的是
A.喷水可以减少浓盐酸挥发
B.喷水可以降低盐酸酸性
C.撒石灰是为了消除盐酸污染
D.喷水是为了尽快把盐酸冲进下水道
4.物质X可发生下列所示的两个反应:①X+酸→盐+H2O,②X+非金属氧化物→盐+H2O。则X可能是
A.CaO
B.H2SO4
C.NaOH
D.CO2
5.分类是学习化学的方法之一,下列物质是按单质、盐、混合物的顺序排列的是
A.氧气、碳酸钙、空气
B.氢气、硫酸钠、水
C.甲烷、食盐、冰水
D.金刚石、熟石灰、石油
6.下列化学方程式符合题意且书写正确的是
A.正常的雨水略呈酸性的原因:CO2 + H2OH2CO3
B.生活中用天然气作燃料:C2H5OH + 3O22CO2 + 3H2O
C.胃舒平(含氢氧化铝)治疗胃酸过多症:Al(OH)3 + HClAlCl3 + H2O
D.用大理石和盐酸制取二氧化碳:CaCO3 + 2HClCaCl2 + H2O + CO2
7.下列生活中的做法错误的是
A.用食醋去除水壶中的水垢
B.钢铁表面采用涂油、刷漆、镀铬等方法都能防止钢铁生锈
C.用火碱来除去衣服上的油污
D.蚊虫叮咬后,用肥皂水涂抹患处以减轻痛痒
8.根据如图实验判断下列说法错误的是
A.浓盐酸有挥发性
B.分子在不断运动
C.B烧杯溶液的颜色会改变
D.实验后B烧杯内溶液颜色为无色,说明二者恰好完全反应
能力提升
9.以下应用与中和反应原理无关的是
A.用含碳酸氢钠和有机酸的发酵粉焙制糕点
B.服用含氢氧化镁的药物治疗胃酸过多
C.用硫酸溶液处理印染厂废水中残留的氢氧化钠
D.在蚊虫叮咬处涂抹稀氨水可以减轻蚊虫分泌的蚁酸造成的痛痒
10.在总结化学知识时,以下归纳或判断正确的是
A.有水生成的放热反应一定是中和反应
B.由一种元素组成的物质一定是单质
C.能分解产生氧气的物质一定含有氧元素
D.能与碱反应生成盐和水的物质一定是酸
11.取2%的NaOH溶液20 g和2%的HCl溶液20 g,使其充分反应,所得到的溶液能使紫色石蕊试液显
A.红色 B.蓝色
C.无色 D.紫色
12.中和反应是放热反应吗?三位同学为探究此问题进行了下列实验:
(1)甲同学取10 mL?10%的NaOH溶液于试管中,逐滴加入10%的稀硫酸,随着硫酸的加入,烧杯中溶液温度与加入硫酸体积之间的变化关系如甲图所示。本实验选用10%的NaOH溶液而不选用NaOH固体的原因是__________________________________________________________________________。
(2)乙同学按乙图装置进行实验,其中的澄清饱和石灰水的作用是_______________________________________________________________________________。
(3)丙同学按丙图实验,可以根据______________________________________的现象也能证明中和反应是放热的。
真题练习
13.[2019·南京]下列物质所对应的用途不正确的是
A.大理石——用作建筑材料
B.钛合金——制造人造骨
C.氢氧化钠——治疗胃酸过多
D.熟石灰——改良酸性土壤
14.[2019·宿迁]下列说法正确的是
A.稀盐酸、稀硫酸化学性质相似,是因为其溶液中都含有H+
B.生成盐和水的反应一定是中和反应
C.将硝酸铵固体溶于水溶液温度会升高
D.目前计入空气污染指数的有害气体包括:SO2、NO2、CO2、CO等
15.[2019·淄博]如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论正确的是
A.反应后溶液的pH大于7
B.反应前的溶液均可导电,反应后的溶液不导电
C.反应后溶液中存在的粒子只有Na+和Cl-
D.反应前后所有元素的化合价均无变化
16.[2019·鄂州]某实验小组的同学用氢氧化钠溶液和盐酸做中和反应的实验,当他们向盛有氢氧化钠溶液的烧杯中滴加一定量的稀盐酸后,发现忘记了滴加指示剂。他们停止滴加稀盐酸,对烧杯内溶液中的溶质成分进行探究。
(1)写出该中和反应的化学方程式:______________________________________________。
(2)探究烧杯内溶液中溶质的成分。
【猜想】
猜想一:可能是NaCl和NaOH;
猜想二:可能只有NaCl;
猜想三:_________________________________________。
【进行实验】
实验步骤
实验操作
实验现象
结论
①
取少量烧杯内的溶液于试管中,滴入几滴酚酞溶液,振荡
____________
猜想一不成立
②
取少量烧杯内的溶液于试管中,滴加碳酸钠溶液
____________
猜想三成立
参考答案
基础训练
1.【答案】A
【解析】不仅可作干燥剂,还能与酸反应,用于改良酸性土壤,应属于碱性氧化物,该氧化物是CaO。二氧化碳、水、氧化铜不能做干燥剂,且氧化铜与酸反应生成的铜离子属于重金属离子,污染土壤。故选A。
2.【答案】D
【解析】皂角素显碱性,利用中和反应原理,应该选用酸性物质。A、食盐水,显中性,错误;B、肥皂水,显碱性,错误;C、硫酸溶液,显酸性,但有很强的腐蚀性,错误;D、食醋(含有醋酸)显酸性,腐蚀性不强,正确。故选D。
3.【答案】D
4.【答案】C
【解析】A、CaO与非金属氧化物反应生成盐,但不会生成水,故A错误;B、H2SO4和酸、非金属氧化物均不反应,故B错误;C、可溶性的碱既能与非金属氧化物反应,又能与酸反应,故C正确;D、CO2和酸、非金属氧化物均不反应,故D错误。故选C。
5.【答案】A
【解析】按单质、盐、混合物的顺序排列的是氧气、碳酸钙、空气。B、水是纯净物;C、冰水是纯净物;D、熟石灰是碱。故选A。
6.【答案】A
【解析】A、二氧化碳溶于水生成的碳酸具有酸性,故正常雨水呈酸性的原因是CO2+H2OH2CO3,正确;B、天然气的主要成分为甲烷,错误;C、胃舒平主要成分氢氧化铝能与盐酸发生中和反应,且氢氧化铝没有腐蚀性,故常用来治疗胃酸过多症,反应方程式未配平,正确的化学方程式为Al(OH)3 + 3HClAlCl3 + 3H2O,错误;D、用大理石和盐酸制取二氧化碳,化学方程式中要标注气体符号,准确的化学方程式为CaCO3+2HClCaCl2+H2O+CO2↑,错误。故选A。
7.【答案】C
8.【答案】D
【解析】A、一段时间后B烧杯中的酚酞溶液颜色变为无色,而两者没有直接接触,说明浓盐酸有挥发性,故选项说法正确;B、一段时间后B烧杯中的酚酞溶液颜色变为无色,而两者没有直接接触,说明分子是在不断的运动的,故选项说法正确;C、浓盐酸中挥发出来的氯化氢气体,与氢氧化钠反应生成氯化钠和水,溶液的碱性减弱,至恰好完全反应,溶液由红色变为无色,故选项说法正确;D、浓盐酸中挥发出来的氯化氢气体,与氢氧化钠反应生成氯化钠和水,烧杯B中氯化氢有剩余也是无色,故选项说法错误。故选D。
能力提升
9.【答案】A
【解析】A、用含碳酸氢钠和有机酸的发酵粉焙制糕点,该反应是盐与酸的反应,不属于中和反应,符合题意;B、胃酸的主要成分是盐酸,氢氧化镁和盐酸反应生成氯化镁和水,该反应是酸与碱的反应,属于中和反应,不符合题意;C、用硫酸溶液处理印染厂废水中残留的NaOH,氢氧化钠溶液与硫酸反应生成硫酸钠和水,该反应是酸与碱反应生成盐和水的反应,属于中和反应,不符合题意;D、在蚊虫叮咬处涂抹稀氨水可以减轻蚊虫分泌出的蚁酸造成的痛痒,稀氨水属于碱,与蚁酸反应生成盐和水,该反应是酸与碱反应生成盐和水的反应,属于中和反应,不符合题意。故选B。
10.【答案】C
【解析】A、氢气燃烧放热,产物是水,错误;B、由一种元素组成的纯净物一定是单质,但是由一种元素组成的物质不一定是单质,比如氧气和臭氧的混合物,错误;C、根据质量守恒定律,能分解产生氧气的物质一定含有氧元素,正确;D、能与碱反应生成盐和水的物质不一定是酸,二氧化碳能和氢氧化钙反应生成碳酸钙和水,但是二氧化碳是氧化物,错误。故选C。
11.【答案】A
12.【答案】(1)氢氧化钠固体溶于水放热,会对实验造成干扰
(2)饱和石灰水变浑浊,说明氢氧化钠与硫酸反应能放出热量
(3)浸入烧杯内水中的导管口有气泡冒出
【解析】(1)氢氧化钠固体溶于水放热,会对实验造成干扰,不能探究中和反应本身是否放热。(2)氢氧化钙的溶解度随温度的升高而减小,饱和溶液升温时,会因溶解度减小析出固体而变浑浊。饱和石灰水变浑浊,说明氢氧化钠与硫酸反应能放出热量。(3)中和反应放热能使广口瓶内气体受热膨胀而逸出,浸入烧杯水中的导管口有气泡冒出。
真题练习
13.【答案】C
【解析】A、大理石坚硬、美观、耐磨,常用作建筑材料,正确;B、钛合金与人体具有很好的相容性,常用来制造人造骨,正确;C、氢氧化钠属于强碱,不可治疗胃酸过多,错误;D、熟石灰属于碱,能与碱中和,并且价格便宜,常用来改良酸性土壤,正确。故选C。
14.【答案】A
【解析】A、稀盐酸、稀硫酸化学性质相似,是因为其溶液中都含有H+,该选项说法正确;B、生成盐和水的反应不一定是中和反应,例如二氧化碳和氢氧化钠反应生成碳酸钠和水,不属于中和反应,该选项说法不正确;C、将硝酸铵固体溶于水时,吸热,导致溶液温度降低,该选项说法不正确;D、目前计入空气污染指数的有害气体不包括二氧化碳,该选项说法不正确。故选A。
15.【答案】D
16.【答案】(1)NaOH + HClNaCl + H2O
(2)【猜想】可能是NaCl和HCl
【进行实验】①溶液不变色
②有气泡产生
【解析】(1)氢氧化钠溶液和盐酸中和反应生成氯化钠和水,根据质量守恒定律和观察法配平反应的化学方程式,该中和反应的化学方程式为NaOH + HClNaCl + H2O。(2)烧杯内溶液中溶质的成分有三种可能:一是加入的盐酸不足,则氢氧化钠有剩余,故溶质为剩余的氢氧化钠和生成的氯化钠;二是加入的盐酸恰好完全反应,则烧杯内溶液中溶质为反应生成的氯化钠;三是加入的盐酸过量,则烧杯内溶液中溶质为反应生成的氯化钠和过量盐酸中的氯化氢。故猜想三:可能是NaCl和HCl。【进行实验】①猜想一不成立,则溶液可能呈酸性或中性,不能使酚酞试液变色;②猜想三成立,说明溶液中含有盐酸,加入碳酸钠溶液,有气泡产生。
同课章节目录
