课题2 酸和碱的中和反应课件(26张PPT)
文档属性
| 名称 | 课题2 酸和碱的中和反应课件(26张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 4.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-23 00:00:00 | ||
图片预览







文档简介
(共26张PPT)
实验活动课
CO2的制取与性质的改进实验
牡丹江市田家炳实验中学
酸和碱能发生什么反应
第十单元之
酸与碱能发生怎样的反应?
酸与碱能否发生反应?
学习酸碱反应的价值何在?
学以致用:酸碱反应的应用
设计完成实验:验证酸碱能否发生反应
从宏-微-符三重表征认识酸碱反应
学习目标
学习任务
任务一
酸与碱能否发生反应?
氢氧化铜+稀硫酸
氢氧化钡溶液+稀硫酸
氢氧化钠溶液+稀盐酸
NaOH溶液和稀盐酸混合
假设1:没反应
假设2:反应,但无明显现象
VS
温馨提示:
可以借助酸碱指示剂的显色作用
盐酸和氢氧化钠混合,
会发生什么呢?
1、提出问题:
2、猜想与假设:
猜想1酸和碱之间能发生反应
猜想2酸和碱之间不能发生反应
3、设计实验方案
4、进行实验探究
5、分析结果,得出结论
酸和碱之间是否会发生反应?
你的方案
方案一
方案二
。。。
。。。
操作 现象 结论
(1)滴入氢氧化钠溶液,若没有立即变红,说明过量
(2)滴入石蕊溶液,若变红,说明过量;
(3)加入镁条,若有气泡冒出,说明过量。
。。。。。。
思考:什么时候溶液呈中性?
思考:如何判断盐酸是否过量?
酸与碱反应是否都没有现象呢?
实验一:向Ba(OH)2溶液中,滴加适量稀硫酸,
观察现象。
实验二:向Cu(OH)2溶液中,滴加适量稀硫酸,
观察现象。
中和反应
酸和碱作用生成盐和水的反应。
你能写出几个反应?
氢氧化钾
氢氧化钠
氢氧化钡
稀硫酸
稀盐酸
稀硝酸
HCl == H+ + Cl-
NaOH == Na+ + OH-
酸与碱反应实质:
H+ + OH- == H2O
VS
含酸废水
熟石灰
(碱性废水可用酸中和,酸性废水可用碱中和)
二、中和反应在实际中的应用
改变土壤的酸碱性
VS
酸性土壤
熟石灰
VS
碱性土壤
松针土
H2SO4+ Ca(OH)2 = CaSO4 + 2H2O
能否用NaOH?
碱性太强,氢氧化钠极易溶于水,
斯达舒说明书
[药品名称] 维U颠茄铝胶囊
[性状] 本品为胶囊剂,内容物为白色或类白色粉末,气味臭,味微苦
[主要成分] 每粒含氢氧化铝[Al(OH)3 ]140毫克、维生素U50毫克;辅料为:淀粉,硬脂酸镁
[药理作用] 中和胃酸过多、抗溃疡、镇痛、抗炎
[功能与主治] 用于慢性胃炎胃酸和多酸胃痛。行气止痛,收敛生肌,促进溃疡愈合。用于胃胀闷疼痛,嗳气泛酸,恶心呕吐,气滞引起的胃腕疼痛。
用于医药
Al(OH)3 + 3HCl === AlCl3 + 3H2O
腌制过程中生成了碱
吃起来有涩味
蘸少量的食醋
涩味消失
发生了什么反应?
发生了中和反应
发生了中和反应
练习:
判断:下列化合物中,哪些是酸,哪些是碱,哪些是盐?
KOH、HCl、CaCl2、HNO3、SO2、BaSO4、CuO、Ca(OH)2、H2SO4、Na2CO3、NH3 · H2O、CaCO3
回答:
酸: HCl、 HNO3、 H2SO4
碱: KOH 、Ca(OH)2、 NH3 · H2O
盐:CaCl2、BaSO4、Na2CO3、CaCO3
氧化物:SO2 、CuO
课堂练习一
1.下列物质属于盐的是( )
A. CuO B. Cu(OH)2 C. CuSO4 D. HCl
C
课堂练习二
2.下列反应中属于中和反应的是( )
A、2NaOH + CO2 = Na2CO3 + H2O
B、CuO + 2HCl = CuCl2 + H2O
C、Ca(OH)2+ H2SO4 = CaSO4 + 2H2O
D、CaCO3 + 2HCl = CaCl2+CO2↑+H2O
B
下列反应,属于中和反应的是( )
A Zn +2HCl == ZnCl2 + H2↑
B CuO + 2HCl == CuCl2 + H2O
C Cu(OH)2 + H2SO4 == CuSO4 + 2H2O
D CO2 + 2NaOH == Na2CO3 + H2O
课堂练习三
C
课堂练习四
下列反应,要借助酸碱指示剂,才能判断二者发生反应的是( )
A、大理石和稀盐酸
B、石灰水和稀盐酸
C、铁锈与稀盐酸
D、镁和稀硫酸
B
实验活动课
CO2的制取与性质的改进实验
牡丹江市田家炳实验中学
酸和碱能发生什么反应
第十单元之
酸与碱能发生怎样的反应?
酸与碱能否发生反应?
学习酸碱反应的价值何在?
学以致用:酸碱反应的应用
设计完成实验:验证酸碱能否发生反应
从宏-微-符三重表征认识酸碱反应
学习目标
学习任务
任务一
酸与碱能否发生反应?
氢氧化铜+稀硫酸
氢氧化钡溶液+稀硫酸
氢氧化钠溶液+稀盐酸
NaOH溶液和稀盐酸混合
假设1:没反应
假设2:反应,但无明显现象
VS
温馨提示:
可以借助酸碱指示剂的显色作用
盐酸和氢氧化钠混合,
会发生什么呢?
1、提出问题:
2、猜想与假设:
猜想1酸和碱之间能发生反应
猜想2酸和碱之间不能发生反应
3、设计实验方案
4、进行实验探究
5、分析结果,得出结论
酸和碱之间是否会发生反应?
你的方案
方案一
方案二
。。。
。。。
操作 现象 结论
(1)滴入氢氧化钠溶液,若没有立即变红,说明过量
(2)滴入石蕊溶液,若变红,说明过量;
(3)加入镁条,若有气泡冒出,说明过量。
。。。。。。
思考:什么时候溶液呈中性?
思考:如何判断盐酸是否过量?
酸与碱反应是否都没有现象呢?
实验一:向Ba(OH)2溶液中,滴加适量稀硫酸,
观察现象。
实验二:向Cu(OH)2溶液中,滴加适量稀硫酸,
观察现象。
中和反应
酸和碱作用生成盐和水的反应。
你能写出几个反应?
氢氧化钾
氢氧化钠
氢氧化钡
稀硫酸
稀盐酸
稀硝酸
HCl == H+ + Cl-
NaOH == Na+ + OH-
酸与碱反应实质:
H+ + OH- == H2O
VS
含酸废水
熟石灰
(碱性废水可用酸中和,酸性废水可用碱中和)
二、中和反应在实际中的应用
改变土壤的酸碱性
VS
酸性土壤
熟石灰
VS
碱性土壤
松针土
H2SO4+ Ca(OH)2 = CaSO4 + 2H2O
能否用NaOH?
碱性太强,氢氧化钠极易溶于水,
斯达舒说明书
[药品名称] 维U颠茄铝胶囊
[性状] 本品为胶囊剂,内容物为白色或类白色粉末,气味臭,味微苦
[主要成分] 每粒含氢氧化铝[Al(OH)3 ]140毫克、维生素U50毫克;辅料为:淀粉,硬脂酸镁
[药理作用] 中和胃酸过多、抗溃疡、镇痛、抗炎
[功能与主治] 用于慢性胃炎胃酸和多酸胃痛。行气止痛,收敛生肌,促进溃疡愈合。用于胃胀闷疼痛,嗳气泛酸,恶心呕吐,气滞引起的胃腕疼痛。
用于医药
Al(OH)3 + 3HCl === AlCl3 + 3H2O
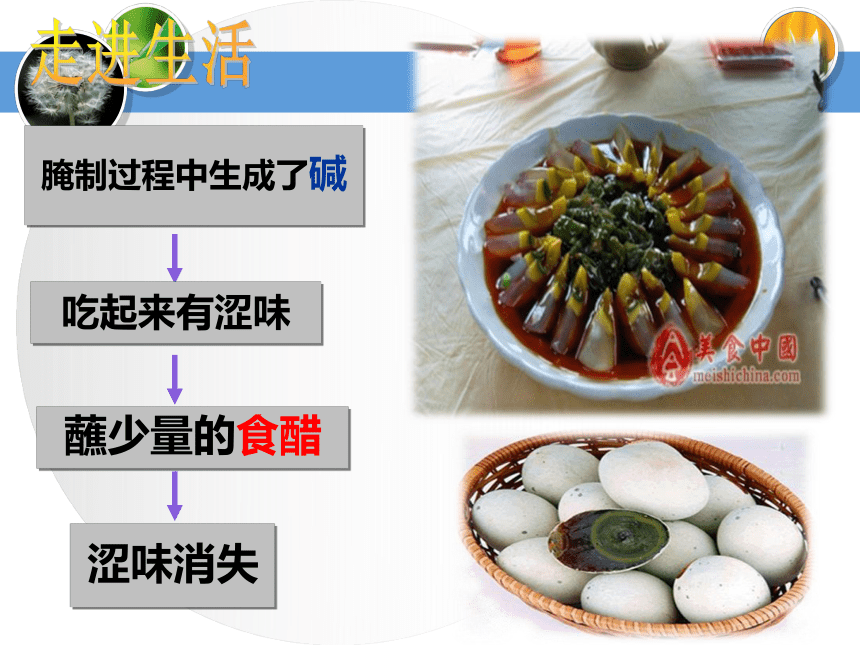
腌制过程中生成了碱
吃起来有涩味
蘸少量的食醋
涩味消失
发生了什么反应?
发生了中和反应
发生了中和反应
练习:
判断:下列化合物中,哪些是酸,哪些是碱,哪些是盐?
KOH、HCl、CaCl2、HNO3、SO2、BaSO4、CuO、Ca(OH)2、H2SO4、Na2CO3、NH3 · H2O、CaCO3
回答:
酸: HCl、 HNO3、 H2SO4
碱: KOH 、Ca(OH)2、 NH3 · H2O
盐:CaCl2、BaSO4、Na2CO3、CaCO3
氧化物:SO2 、CuO
课堂练习一
1.下列物质属于盐的是( )
A. CuO B. Cu(OH)2 C. CuSO4 D. HCl
C
课堂练习二
2.下列反应中属于中和反应的是( )
A、2NaOH + CO2 = Na2CO3 + H2O
B、CuO + 2HCl = CuCl2 + H2O
C、Ca(OH)2+ H2SO4 = CaSO4 + 2H2O
D、CaCO3 + 2HCl = CaCl2+CO2↑+H2O
B
下列反应,属于中和反应的是( )
A Zn +2HCl == ZnCl2 + H2↑
B CuO + 2HCl == CuCl2 + H2O
C Cu(OH)2 + H2SO4 == CuSO4 + 2H2O
D CO2 + 2NaOH == Na2CO3 + H2O
课堂练习三
C
课堂练习四
下列反应,要借助酸碱指示剂,才能判断二者发生反应的是( )
A、大理石和稀盐酸
B、石灰水和稀盐酸
C、铁锈与稀盐酸
D、镁和稀硫酸
B
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
