2019-2020学年鲁科版选修5 第2章第3节 醛和酮 糖类课件(共28张PPT)
文档属性
| 名称 | 2019-2020学年鲁科版选修5 第2章第3节 醛和酮 糖类课件(共28张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-25 00:00:00 | ||
图片预览







文档简介
(共28张PPT)
第3节 醛和酮 糖类
糖 类
探究点一 单 糖
探究点二 双 糖
探究点三 多 糖
1.熟知葡萄糖的结构和性质,学会葡萄糖的检验方法。
2.知道常见的二糖(麦芽糖、蔗糖)、多糖(淀粉、纤维素)的性质及它们之间的相互
关系,学会淀粉的检验方法。
学习重难点:
葡萄糖的结构和性质。
1 mol低聚糖水解后能产生 2~10mol 单糖,若水解生成 2 mol单糖,则称为双糖,重要的双糖有麦芽糖、乳糖和蔗糖等。
糖类是由C、H、O三种元素组成的一类有机化合物,其组成大多可以用通式Cn(H2O)m表示,过去曾称其为碳水化合物。
1.糖类组成:
2.根据糖类能否水解以及水解后的产物,糖类可分为
凡是不能水解的糖称为单糖,如葡萄糖、果糖、核糖及脱氧核糖等。
(1)单糖:
(2)双糖:
1 mol 多糖水解后能产生很多摩尔单糖,如淀粉、纤维素等。
(3)多糖:
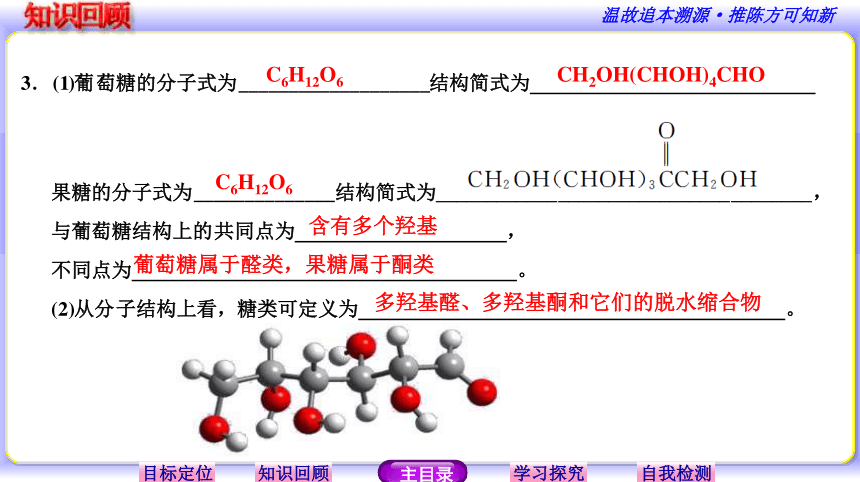
CH2OH(CHOH)4CHO
C6H12O6
C6H12O6
含有多个羟基
葡萄糖属于醛类,果糖属于酮类
多羟基醛、多羟基酮和它们的脱水缩合物
单 糖
1.葡萄糖是一种六碳醛糖,分子中还含有多个羟基,能发生酯化反应、银镜反应、能与新制Cu(OH)2悬浊液反应。
(1)在一支洁净试管中配制 2 mL银氨溶液,加入1 mL 10%葡萄糖溶液,振荡并在水浴中加热。观察到的实验现象是试管内壁有银镜生成,
C6H12O6
—OH
同分异构体
无色
易
(1)葡萄糖的结构和性质
(2)葡萄糖与果糖互为同分异构体。
与Na反应放出H2体现了葡萄糖的氧化性,
葡萄糖把银氨溶液还原成单质银,体现了葡萄糖的还原性
与酸发生酯化反应是取代反应,为非氧化还原反应
与H2发生加成反应体现了它的氧化性
B
该题由葡萄糖的结构和组成入手,结合其性质即可进行解答。由CH2OH(CHOH)4CHO知,1 mol葡萄糖发生银镜反应生成2 mol银,反应后变为葡萄糖酸铵;1 mol葡萄糖完全酯化需5 mol乙酸,质量为300 g;葡萄糖燃烧的化学方程式是C6H12O6+6O2 6CO2+6H2O,1 mol葡萄糖燃烧需标准状况下氧气的体积为
6 mol×22.4 L·mol-1=134.4 L。
葡萄糖酸铵
2
CH2OH(CHOH)4COONH4
300
134.4
双 糖
1.蔗糖溶液、麦芽糖溶液还原性实验探究
(1)在盛有新制Cu(OH)2悬浊液的两支试管中,一支试管中加入蔗糖溶液,另一支试管中加入麦芽糖溶液,分别加热。实验中的现象是___________________________
_____________________________________.
加蔗糖溶液的试管无明显现象,
蔗糖分子中无醛基;麦芽糖分子中有醛基,具有还原性。
加入麦芽糖的试管有砖红色沉淀生成。
(2)由上述实验得出的结论
2.蔗糖水解及其产物性质实验探究
(1)在一支试管中加入20%蔗糖溶液5 mL,加入稀硫酸,水浴加热;然后用NaOH溶液中和呈弱碱性;再加入新制的Cu(OH)2加热,观察到的实验现象是 ,实验结论是 。
(2)蔗糖和麦芽糖都可以水解,写出其水解方程式:
有砖红色沉淀生成
蔗糖水解产物中有还原性糖
(1)蔗糖和麦芽糖的分子式都是C12H22O11,互为同分异构体,都能水解生成两分子的单糖,水解产物中都有葡萄糖生成。蔗糖分子中不含醛基,是非还原性糖,麦芽糖分子中含有醛基,具有还原性。
(2)鉴别蔗糖和麦芽糖的方法是向其溶液中分别加入银氨溶液,水浴加热,能发生银镜反应的是麦芽糖,不能发生银镜反应的是蔗糖(也可用新制的氢氧化铜悬浊液鉴别)。
能发生银镜反应,说明有机物结构中含有醛基;能发生水解反应的有卤代烃、酯及低聚糖或多糖等。甲酸甲酯中有—CHO和
—COO—,能发生银镜反应,也能发生水解反应;蔗糖能发生水解反应,但无—CHO;葡萄糖能发生银镜反应,但不能水解;麦芽糖能发生银镜反应,也能发生水解反应。
理解感悟 (1)能发生银镜反应的物质,其分子结构中必含有—CHO,但不一定属于醛类。目前已学过的能发生银镜反应的物质:醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等。
(2)能发生水解反应的物质主要有卤代烃、酯、蔗糖、麦芽糖、淀粉、纤维素等。卤代烃在碱性条件下水解,酯在酸性或碱性条件下均能水解,其中碱性条件下水解趋于完全,蔗糖、麦芽糖在稀硫酸作催化剂条件下能水解。此外可溶性的酚盐、羧酸盐等也可发生水解,使溶液呈碱性。
例如:CH3COONa+H2O?? CH3COOH+NaOH。
A
多 糖
2.淀粉是无 、无 的粉末状物质, 溶于冷水,在热水中 。
1.淀粉和纤维素属于多糖,分子式均为 ,每个葡萄糖单元仍有三个羟基,其分子式也可写成 ,由于n值不同,它们 同分异构体,它们都属于 化合物。
(2)淀粉水解的化学方程式为
葡萄糖酿酒的反应为
(C6H10O5)n
[C6H7O2(OH)3]n
不是
天然高分子
不
嗅
味
淀粉颗粒会膨胀破裂(或形成胶状淀粉糊)
(1)淀粉遇碘(I2)显蓝色。
(2)纤维素含有羟基,可以与硝酸、醋酸等发生酯化反应,生成重要的化工原料硝酸纤维素和醋酸纤维素。
3.纤维素是白色、无嗅、无味的具有纤维状结构的物质。一般不溶于水和有机溶剂。
(1)纤维素与淀粉一样,没有还原性,但在强酸中的水解产物具有还原性。
用银氨溶液和碘水来检验淀粉在水溶液中是否发生了水解及水解是否已进行完全,实验步骤如下:
(1)实验现象及结论:
(2)实验中加入NaOH溶液的作用是银镜反应或与新制Cu(OH)2悬浊液反应必须在碱性条件下进行,因此必须先加入NaOH溶液中和催化剂稀硫酸。
淀粉尚未水解
淀粉部分水解
淀粉完全水解
现象A 现象B 结论
1 未出现银镜 溶液变蓝色
2 出现银镜 溶液变蓝色
3 出现银镜 溶液不变蓝色
18%
稀硫酸
NaOH溶液
不可以,银镜反应必须在碱性条件下进行
理解感悟 验证淀粉的水解产物时,首先要加入NaOH溶液调至碱性,再进行实验。要验证混合液中是否还有淀粉应直接取水解后的混合液加碘水,而不能在加入NaOH溶液后再加碘水,因为碘水与NaOH溶液反应。
糖类相互转化关系如下图所示:
1
2
3
4
5
6
含有C、H、O三种元素的有机物不一定是糖类
并不是所有的糖类都可以写成Cn(H2O)m的形式
有甜味的物质不一定是糖类
D
1
2
3
4
5
6
蔗糖是非还原性糖,其溶液能发生银镜反应,说明它有部分发生了水解。
D
1
2
3
4
5
6
B
1
2
3
4
5
6
B
检验葡萄糖可利用其分子结构中含有醛基,将其与新制的Cu(OH)2悬浊液混合后共热,看是否有砖红色沉淀生成来判定,当然也可借助银镜反应来检验葡萄糖。
1
2
3
4
5
6
用米酿酒,米中含有大量淀粉,在微生物的作用下,首先将淀粉水解为麦芽糖,然后再水解为葡萄糖,从而产生甜味。
B
1
2
3
4
5
6
淀粉和纤维素都可以用(C6H10O5)n表示,都是天然高分子化合物,但二者的 n 值不同,二者不属于同分异构体,都是混合物,淀粉和纤维素水解的最终产物都是葡萄糖。
D
本讲内容结束
请完成课时作业
第3节 醛和酮 糖类
糖 类
探究点一 单 糖
探究点二 双 糖
探究点三 多 糖
1.熟知葡萄糖的结构和性质,学会葡萄糖的检验方法。
2.知道常见的二糖(麦芽糖、蔗糖)、多糖(淀粉、纤维素)的性质及它们之间的相互
关系,学会淀粉的检验方法。
学习重难点:
葡萄糖的结构和性质。
1 mol低聚糖水解后能产生 2~10mol 单糖,若水解生成 2 mol单糖,则称为双糖,重要的双糖有麦芽糖、乳糖和蔗糖等。
糖类是由C、H、O三种元素组成的一类有机化合物,其组成大多可以用通式Cn(H2O)m表示,过去曾称其为碳水化合物。
1.糖类组成:
2.根据糖类能否水解以及水解后的产物,糖类可分为
凡是不能水解的糖称为单糖,如葡萄糖、果糖、核糖及脱氧核糖等。
(1)单糖:
(2)双糖:
1 mol 多糖水解后能产生很多摩尔单糖,如淀粉、纤维素等。
(3)多糖:
CH2OH(CHOH)4CHO
C6H12O6
C6H12O6
含有多个羟基
葡萄糖属于醛类,果糖属于酮类
多羟基醛、多羟基酮和它们的脱水缩合物
单 糖
1.葡萄糖是一种六碳醛糖,分子中还含有多个羟基,能发生酯化反应、银镜反应、能与新制Cu(OH)2悬浊液反应。
(1)在一支洁净试管中配制 2 mL银氨溶液,加入1 mL 10%葡萄糖溶液,振荡并在水浴中加热。观察到的实验现象是试管内壁有银镜生成,
C6H12O6
—OH
同分异构体
无色
易
(1)葡萄糖的结构和性质
(2)葡萄糖与果糖互为同分异构体。
与Na反应放出H2体现了葡萄糖的氧化性,
葡萄糖把银氨溶液还原成单质银,体现了葡萄糖的还原性
与酸发生酯化反应是取代反应,为非氧化还原反应
与H2发生加成反应体现了它的氧化性
B
该题由葡萄糖的结构和组成入手,结合其性质即可进行解答。由CH2OH(CHOH)4CHO知,1 mol葡萄糖发生银镜反应生成2 mol银,反应后变为葡萄糖酸铵;1 mol葡萄糖完全酯化需5 mol乙酸,质量为300 g;葡萄糖燃烧的化学方程式是C6H12O6+6O2 6CO2+6H2O,1 mol葡萄糖燃烧需标准状况下氧气的体积为
6 mol×22.4 L·mol-1=134.4 L。
葡萄糖酸铵
2
CH2OH(CHOH)4COONH4
300
134.4
双 糖
1.蔗糖溶液、麦芽糖溶液还原性实验探究
(1)在盛有新制Cu(OH)2悬浊液的两支试管中,一支试管中加入蔗糖溶液,另一支试管中加入麦芽糖溶液,分别加热。实验中的现象是___________________________
_____________________________________.
加蔗糖溶液的试管无明显现象,
蔗糖分子中无醛基;麦芽糖分子中有醛基,具有还原性。
加入麦芽糖的试管有砖红色沉淀生成。
(2)由上述实验得出的结论
2.蔗糖水解及其产物性质实验探究
(1)在一支试管中加入20%蔗糖溶液5 mL,加入稀硫酸,水浴加热;然后用NaOH溶液中和呈弱碱性;再加入新制的Cu(OH)2加热,观察到的实验现象是 ,实验结论是 。
(2)蔗糖和麦芽糖都可以水解,写出其水解方程式:
有砖红色沉淀生成
蔗糖水解产物中有还原性糖
(1)蔗糖和麦芽糖的分子式都是C12H22O11,互为同分异构体,都能水解生成两分子的单糖,水解产物中都有葡萄糖生成。蔗糖分子中不含醛基,是非还原性糖,麦芽糖分子中含有醛基,具有还原性。
(2)鉴别蔗糖和麦芽糖的方法是向其溶液中分别加入银氨溶液,水浴加热,能发生银镜反应的是麦芽糖,不能发生银镜反应的是蔗糖(也可用新制的氢氧化铜悬浊液鉴别)。
能发生银镜反应,说明有机物结构中含有醛基;能发生水解反应的有卤代烃、酯及低聚糖或多糖等。甲酸甲酯中有—CHO和
—COO—,能发生银镜反应,也能发生水解反应;蔗糖能发生水解反应,但无—CHO;葡萄糖能发生银镜反应,但不能水解;麦芽糖能发生银镜反应,也能发生水解反应。
理解感悟 (1)能发生银镜反应的物质,其分子结构中必含有—CHO,但不一定属于醛类。目前已学过的能发生银镜反应的物质:醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等。
(2)能发生水解反应的物质主要有卤代烃、酯、蔗糖、麦芽糖、淀粉、纤维素等。卤代烃在碱性条件下水解,酯在酸性或碱性条件下均能水解,其中碱性条件下水解趋于完全,蔗糖、麦芽糖在稀硫酸作催化剂条件下能水解。此外可溶性的酚盐、羧酸盐等也可发生水解,使溶液呈碱性。
例如:CH3COONa+H2O?? CH3COOH+NaOH。
A
多 糖
2.淀粉是无 、无 的粉末状物质, 溶于冷水,在热水中 。
1.淀粉和纤维素属于多糖,分子式均为 ,每个葡萄糖单元仍有三个羟基,其分子式也可写成 ,由于n值不同,它们 同分异构体,它们都属于 化合物。
(2)淀粉水解的化学方程式为
葡萄糖酿酒的反应为
(C6H10O5)n
[C6H7O2(OH)3]n
不是
天然高分子
不
嗅
味
淀粉颗粒会膨胀破裂(或形成胶状淀粉糊)
(1)淀粉遇碘(I2)显蓝色。
(2)纤维素含有羟基,可以与硝酸、醋酸等发生酯化反应,生成重要的化工原料硝酸纤维素和醋酸纤维素。
3.纤维素是白色、无嗅、无味的具有纤维状结构的物质。一般不溶于水和有机溶剂。
(1)纤维素与淀粉一样,没有还原性,但在强酸中的水解产物具有还原性。
用银氨溶液和碘水来检验淀粉在水溶液中是否发生了水解及水解是否已进行完全,实验步骤如下:
(1)实验现象及结论:
(2)实验中加入NaOH溶液的作用是银镜反应或与新制Cu(OH)2悬浊液反应必须在碱性条件下进行,因此必须先加入NaOH溶液中和催化剂稀硫酸。
淀粉尚未水解
淀粉部分水解
淀粉完全水解
现象A 现象B 结论
1 未出现银镜 溶液变蓝色
2 出现银镜 溶液变蓝色
3 出现银镜 溶液不变蓝色
18%
稀硫酸
NaOH溶液
不可以,银镜反应必须在碱性条件下进行
理解感悟 验证淀粉的水解产物时,首先要加入NaOH溶液调至碱性,再进行实验。要验证混合液中是否还有淀粉应直接取水解后的混合液加碘水,而不能在加入NaOH溶液后再加碘水,因为碘水与NaOH溶液反应。
糖类相互转化关系如下图所示:
1
2
3
4
5
6
含有C、H、O三种元素的有机物不一定是糖类
并不是所有的糖类都可以写成Cn(H2O)m的形式
有甜味的物质不一定是糖类
D
1
2
3
4
5
6
蔗糖是非还原性糖,其溶液能发生银镜反应,说明它有部分发生了水解。
D
1
2
3
4
5
6
B
1
2
3
4
5
6
B
检验葡萄糖可利用其分子结构中含有醛基,将其与新制的Cu(OH)2悬浊液混合后共热,看是否有砖红色沉淀生成来判定,当然也可借助银镜反应来检验葡萄糖。
1
2
3
4
5
6
用米酿酒,米中含有大量淀粉,在微生物的作用下,首先将淀粉水解为麦芽糖,然后再水解为葡萄糖,从而产生甜味。
B
1
2
3
4
5
6
淀粉和纤维素都可以用(C6H10O5)n表示,都是天然高分子化合物,但二者的 n 值不同,二者不属于同分异构体,都是混合物,淀粉和纤维素水解的最终产物都是葡萄糖。
D
本讲内容结束
请完成课时作业
