课题1 生活中常见的盐 - -复分解反应 课件(40张PPT)
文档属性
| 名称 | 课题1 生活中常见的盐 - -复分解反应 课件(40张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-27 00:00:00 | ||
图片预览








文档简介
(共40张PPT)
如何证明氢氧化钠溶液是否变质?
复分解反应
课题1 生活中常见的盐(三)
第十一单元
以上化学反应的特点
1、反应物、生成物都是两种 化合物
2、互相交换成分
3、各元素的化合价不变
A
+
C
=
B
A
B
D
C
D
+
酸、碱、盐、氧化物
由两种化合物互相交换成分生成另外两种化合物的反应叫做复分解反应。
︸
内结合、外结合 双交换、价不变
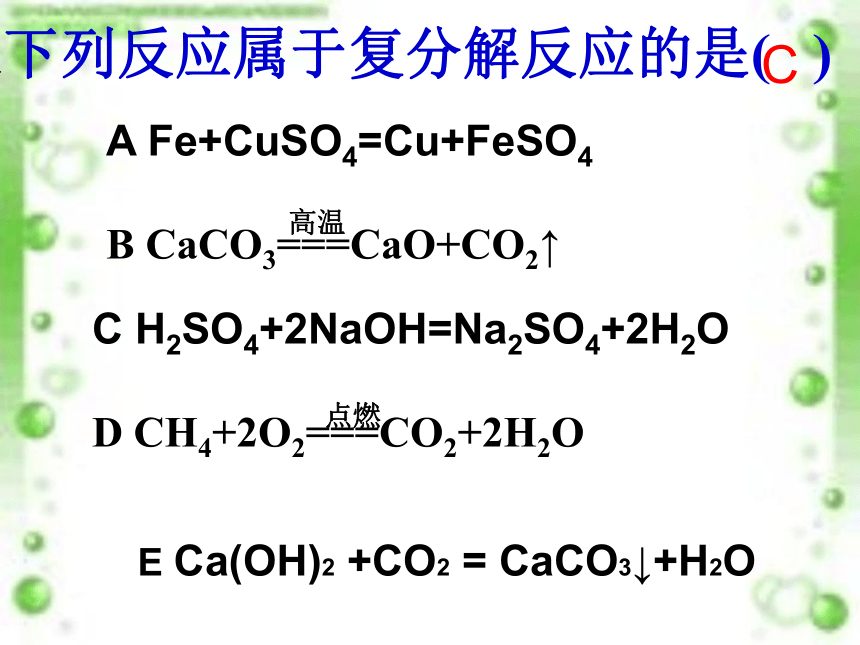
.下列反应属于复分解反应的是( )
C H2SO4+2NaOH=Na2SO4+2H2O
D CH4+2O2===CO2+2H2O
A Fe+CuSO4=Cu+FeSO4
B CaCO3===CaO+CO2↑
点燃
高温
E Ca(OH)2 +CO2 = CaCO3↓+H2O
C
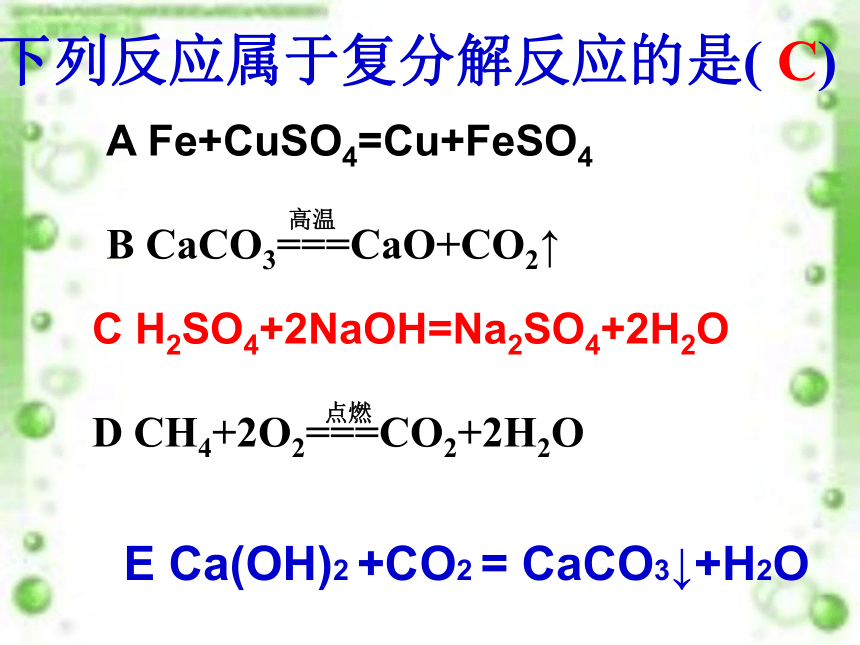
.下列反应属于复分解反应的是( C)
C H2SO4+2NaOH=Na2SO4+2H2O
D CH4+2O2===CO2+2H2O
A Fe+CuSO4=Cu+FeSO4
B CaCO3===CaO+CO2↑
点燃
高温
E Ca(OH)2 +CO2 = CaCO3↓+H2O
有蓝色沉淀生成
有白色沉淀生成
CuSO4+2NaOH=
Cu(OH)2↓+Na2SO4
CuSO4+BaCl2=
BaSO4↓+CuCl2
CuSO4溶液+NaOH溶液 CuSO4溶+BaCl2溶液
现象
化学
方程式
除了有沉淀生成的反应外
还有哪些反应属于
复分解反应呢?
复分解反应发生的条件
或有气体(↑)
或有水(H2O)
有沉淀(↓)
具备三者之一,复分解反应就能发生
生成物中
溶、挥
溶、挥
溶、挥
溶
溶、挥
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
不
微
溶
溶
溶
溶
溶
溶
溶
不
不
不
微
不
不
不
—
一
—
不
微
不
不
不
不
不
不
不
—
微
碱
铵盐
钾盐
钠盐
硝酸盐
盐酸盐
硫酸盐
碳酸盐
水
酸
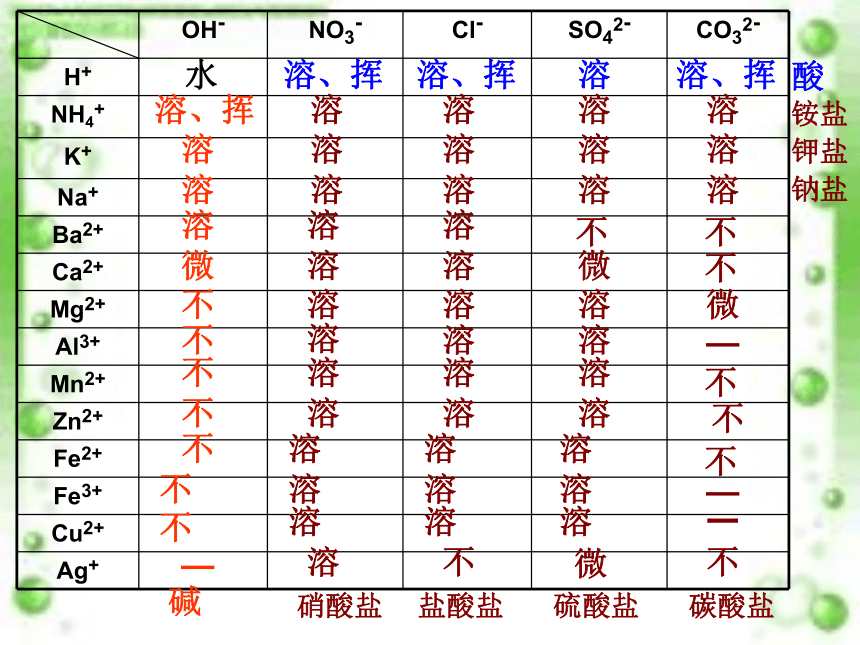
OH- NO3- Cl- SO42- CO32-
H+
NH4+
K+
Na+
Ba2+
Ca2+
Mg2+
Al3+
Mn2+
Zn2+
Fe2+
Fe3+
Cu2+
Ag+
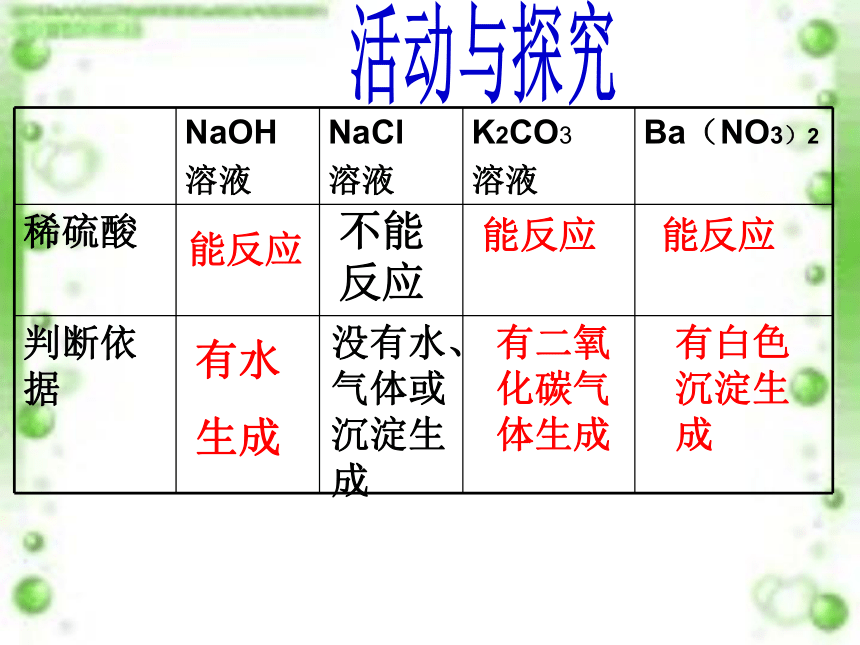
能反应
不能反应
能反应
能反应
有水
生成
没有水、气体或沉淀生成
有二氧化碳气体生成
有白色沉淀生成
NaOH
溶液 NaCl
溶液 K2CO3
溶液 Ba(NO3)2
稀硫酸
判断依据
设计实验证明你的判断。
(利用桌上的仪器和药品实验探究)
气
水
微
红
无
水
操作 现象 结论
先在氢氧化钠溶液中滴加酚酞溶液,然后逐滴滴入适量的稀盐酸 溶液颜色由 色变成 色 证明稀盐酸和氢氧化钠发生了反应
复分解反应条件的探究
Ba2+
SO42-
Cl-
Cl-
Na+
Na+
BaSO4
氯化钡与硫酸钠反应
结论:
有沉淀生成时,复分解反应能够发生
实质:
旁观者:
Cl-和Na+
复分解反应条件的探究
Na+
Na+
CO32-
Cl-
H+
Cl-
H+
H2O
碳酸钠和盐酸反应
结论:
有______生成时,复分解反应能够发生
CO2
实质:
旁观者:
Cl-和Na+
气体
K+
OH-
H+
NO3-
H2O
KOH和稀HNO3反应
复分解反应条件的探究
结论:
有______生成时,复分解反应能够发生
实质:
旁观者:
NO3-和K+
水
6.想一想:化学方程式是否正确?
NaCl+KNO3=KCl+NaNO3
NaCl+KNO3 ——
NaCl+KNO3 ——
NaCl+KNO3 ——
NaCl+KNO3 ——
NaCl+KNO3 ——
NaCl+KNO3 ——
NaCl+KNO3——
总结:复分解反应的实质是:
1、有水生成:
2、有气体生成:
3、有沉淀生成:
H+ + OH- → H2O
H+ + CO32-
( H+ + HCO3- )
co2
溶液中离子的浓度减小
判断下列物质之间能否发生化学反应,如果能写出方程式,不能说明理由
1、碳酸钠溶液和硝酸钡溶液
2、硝酸银溶液与氯化钠溶液
3、硝酸和氯化钠溶液
4、碳酸钠溶液和硫酸
5、氢氧化钠溶液和氯化钙溶液
判断下列物质之间能否发生化学反应,如果能写出方程式,不能说明理由
1、碳酸钠溶液和硝酸钡溶液
2、硝酸银溶液与氯化钠溶液
3、硝酸和氯化钠溶液(X)
4、碳酸钠溶液和硫酸
5、氢氧化钠溶液和氯化钙溶液(X)
我
学
爱
化#39
关键是看几种物质之间能否发生反应
复分解反应的应用
1、下列物质能在水溶液中大量共存的是( )
A CuSO4和NaOH
B Ba(NO3)2和Na2SO4
C Na2CO3和HCl
D CaCl2和KNO3
D
#31. 幻灯片 31
2、下列各组离子能在同一种无色溶液中大量共存的是( )
A.H+、CO32-
B.H+、 OH-
C.Cu2+、 OH-
D.Ca2+、NO3-
D
幻灯片 31
3、下列物质中,一般不能发生复分解反应的是( )
A、硝酸钾
B、氢氧化钠
C、碳酸钠
D、盐酸
A
幻灯片 31
二. 鉴别物质
请用化学方法区分
盐酸、和石灰水二种溶液。
鉴别方法
幻灯片 31
盐酸 石灰水
紫色石蕊 红色 蓝色
Na2CO3溶液 放出气体 产生白色沉淀
三 除去溶液中混有的少量杂质
选用何种试剂除去NaNO3溶液中混有的少量Ba(NO3)2杂质
幻灯片 31
复分解反应类型
1、酸+金属氧化物→盐 + 水
2、酸 + 碱 → 盐 + 水
Fe2O3 + 6HCl =2FeCl3+ 3H2O
NaOH + HCl = NaCl +H2O
3、盐+酸→新盐+新酸
CaCO3+2HCl=CaCl2+ CO2 ↑ +HO
4、盐+碱→新盐+新碱
5、盐+盐→新盐+新盐
CuCl2+2NaOH=Cu(OH)2↓+2NaCl
BaCl2+Na2SO4=BaSO4↓+2NaCl
盐的化学性质
盐+金属——新金属+新盐
盐+酸——新酸+新盐
盐+碱——新碱+新盐
盐+盐——新盐+新盐
H+
OH-
CO32-
HCO3-
NH4+
Ba2+
Ca2+
SO42-
Mg2+
Cu2+
Al3+
Fe3+
Ag+
Cl-
如何证明氢氧化钠溶液是否变质?
复分解反应
课题1 生活中常见的盐(三)
第十一单元
以上化学反应的特点
1、反应物、生成物都是两种 化合物
2、互相交换成分
3、各元素的化合价不变
A
+
C
=
B
A
B
D
C
D
+
酸、碱、盐、氧化物
由两种化合物互相交换成分生成另外两种化合物的反应叫做复分解反应。
︸
内结合、外结合 双交换、价不变
.下列反应属于复分解反应的是( )
C H2SO4+2NaOH=Na2SO4+2H2O
D CH4+2O2===CO2+2H2O
A Fe+CuSO4=Cu+FeSO4
B CaCO3===CaO+CO2↑
点燃
高温
E Ca(OH)2 +CO2 = CaCO3↓+H2O
C
.下列反应属于复分解反应的是( C)
C H2SO4+2NaOH=Na2SO4+2H2O
D CH4+2O2===CO2+2H2O
A Fe+CuSO4=Cu+FeSO4
B CaCO3===CaO+CO2↑
点燃
高温
E Ca(OH)2 +CO2 = CaCO3↓+H2O
有蓝色沉淀生成
有白色沉淀生成
CuSO4+2NaOH=
Cu(OH)2↓+Na2SO4
CuSO4+BaCl2=
BaSO4↓+CuCl2
CuSO4溶液+NaOH溶液 CuSO4溶+BaCl2溶液
现象
化学
方程式
除了有沉淀生成的反应外
还有哪些反应属于
复分解反应呢?
复分解反应发生的条件
或有气体(↑)
或有水(H2O)
有沉淀(↓)
具备三者之一,复分解反应就能发生
生成物中
溶、挥
溶、挥
溶、挥
溶
溶、挥
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
不
微
溶
溶
溶
溶
溶
溶
溶
不
不
不
微
不
不
不
—
一
—
不
微
不
不
不
不
不
不
不
—
微
碱
铵盐
钾盐
钠盐
硝酸盐
盐酸盐
硫酸盐
碳酸盐
水
酸
OH- NO3- Cl- SO42- CO32-
H+
NH4+
K+
Na+
Ba2+
Ca2+
Mg2+
Al3+
Mn2+
Zn2+
Fe2+
Fe3+
Cu2+
Ag+
能反应
不能反应
能反应
能反应
有水
生成
没有水、气体或沉淀生成
有二氧化碳气体生成
有白色沉淀生成
NaOH
溶液 NaCl
溶液 K2CO3
溶液 Ba(NO3)2
稀硫酸
判断依据
设计实验证明你的判断。
(利用桌上的仪器和药品实验探究)
气
水
微
红
无
水
操作 现象 结论
先在氢氧化钠溶液中滴加酚酞溶液,然后逐滴滴入适量的稀盐酸 溶液颜色由 色变成 色 证明稀盐酸和氢氧化钠发生了反应
复分解反应条件的探究
Ba2+
SO42-
Cl-
Cl-
Na+
Na+
BaSO4
氯化钡与硫酸钠反应
结论:
有沉淀生成时,复分解反应能够发生
实质:
旁观者:
Cl-和Na+
复分解反应条件的探究
Na+
Na+
CO32-
Cl-
H+
Cl-
H+
H2O
碳酸钠和盐酸反应
结论:
有______生成时,复分解反应能够发生
CO2
实质:
旁观者:
Cl-和Na+
气体
K+
OH-
H+
NO3-
H2O
KOH和稀HNO3反应
复分解反应条件的探究
结论:
有______生成时,复分解反应能够发生
实质:
旁观者:
NO3-和K+
水
6.想一想:化学方程式是否正确?
NaCl+KNO3=KCl+NaNO3
NaCl+KNO3 ——
NaCl+KNO3 ——
NaCl+KNO3 ——
NaCl+KNO3 ——
NaCl+KNO3 ——
NaCl+KNO3 ——
NaCl+KNO3——
总结:复分解反应的实质是:
1、有水生成:
2、有气体生成:
3、有沉淀生成:
H+ + OH- → H2O
H+ + CO32-
( H+ + HCO3- )
co2
溶液中离子的浓度减小
判断下列物质之间能否发生化学反应,如果能写出方程式,不能说明理由
1、碳酸钠溶液和硝酸钡溶液
2、硝酸银溶液与氯化钠溶液
3、硝酸和氯化钠溶液
4、碳酸钠溶液和硫酸
5、氢氧化钠溶液和氯化钙溶液
判断下列物质之间能否发生化学反应,如果能写出方程式,不能说明理由
1、碳酸钠溶液和硝酸钡溶液
2、硝酸银溶液与氯化钠溶液
3、硝酸和氯化钠溶液(X)
4、碳酸钠溶液和硫酸
5、氢氧化钠溶液和氯化钙溶液(X)
我
学
爱
化#39
关键是看几种物质之间能否发生反应
复分解反应的应用
1、下列物质能在水溶液中大量共存的是( )
A CuSO4和NaOH
B Ba(NO3)2和Na2SO4
C Na2CO3和HCl
D CaCl2和KNO3
D
#31. 幻灯片 31
2、下列各组离子能在同一种无色溶液中大量共存的是( )
A.H+、CO32-
B.H+、 OH-
C.Cu2+、 OH-
D.Ca2+、NO3-
D
幻灯片 31
3、下列物质中,一般不能发生复分解反应的是( )
A、硝酸钾
B、氢氧化钠
C、碳酸钠
D、盐酸
A
幻灯片 31
二. 鉴别物质
请用化学方法区分
盐酸、和石灰水二种溶液。
鉴别方法
幻灯片 31
盐酸 石灰水
紫色石蕊 红色 蓝色
Na2CO3溶液 放出气体 产生白色沉淀
三 除去溶液中混有的少量杂质
选用何种试剂除去NaNO3溶液中混有的少量Ba(NO3)2杂质
幻灯片 31
复分解反应类型
1、酸+金属氧化物→盐 + 水
2、酸 + 碱 → 盐 + 水
Fe2O3 + 6HCl =2FeCl3+ 3H2O
NaOH + HCl = NaCl +H2O
3、盐+酸→新盐+新酸
CaCO3+2HCl=CaCl2+ CO2 ↑ +HO
4、盐+碱→新盐+新碱
5、盐+盐→新盐+新盐
CuCl2+2NaOH=Cu(OH)2↓+2NaCl
BaCl2+Na2SO4=BaSO4↓+2NaCl
盐的化学性质
盐+金属——新金属+新盐
盐+酸——新酸+新盐
盐+碱——新碱+新盐
盐+盐——新盐+新盐
H+
OH-
CO32-
HCO3-
NH4+
Ba2+
Ca2+
SO42-
Mg2+
Cu2+
Al3+
Fe3+
Ag+
Cl-
同课章节目录
