人教版初中化学九年级下册第九单元《溶液》检测题(含答案)
文档属性
| 名称 | 人教版初中化学九年级下册第九单元《溶液》检测题(含答案) |  | |
| 格式 | zip | ||
| 文件大小 | 122.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-28 10:30:43 | ||
图片预览


文档简介
本卷由系统自动生成,请仔细校对后使用,答案仅供参考。
《溶液》检测题
一、单选题
1.KNO3和NaCl的溶解度表及溶解度曲线如下,下列说法错误的是( )
A.t1介于20℃-40℃之间
B.50℃时,溶液的溶质质量分数:KNO3>NaCl
C.当KNO3中混有少量NaCl时,可用降温结晶的方法提纯
D.60℃时,30g KNO3加入50g水,充分溶解,再降温到20℃,会析出晶体14.2g
2.下列关于溶液的说法中,正确的是
A.溶液都是均一、稳定的纯净物
B.饱和溶液的浓度一定大于不饱和溶液的浓度
C.温度高低和溶剂的种类不会影响物质的溶解性
D.配制一定溶质质量分数的溶液需要经过计算、称量(量取)、溶解
3.40℃时,KCl的溶解度为40g。40℃时,将50g KCl固体加入盛有100g水的烧杯中,充分溶解得到溶液。下列说法正确的是
A.得到的是饱和溶液
B.溶液的质量是150g
C.溶液中溶质质量分数的计算式为
D.若再向烧杯中加入一定量水,此时溶液中溶质的质量分数一定减小
4.下列实验现象描述正确的是( )
A.点燃一氧化碳气体时,发出蓝色火焰
B.硫在空气中燃烧,发出蓝紫色火焰,生成无色无味的气体
C.细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
D.将硝酸铵固体溶于水,溶液的温度升高
5.下列鉴别两种不同物质的方法中错误的是
待鉴别的物质 鉴别的方法
A 羊毛与涤纶 燃烧,闻气味
B 烧碱与硝酸铵 加水,测量液体的温度变化
C 铝与铝合金 相互刻划
D 氯化铵与硫酸铵 加熟石灰,研磨
A.A B.B C.C D.D
6.夏天打开碳酸饮料瓶盖,有大量二氧化碳气体逸出。关于打开瓶盖前后的变化,下列说法错误的是
A.二氧化碳的溶解度减小
B.剩余溶液仍为二氧化碳的饱和溶液
C.瓶内二氧化碳的溶质质量分数减小
D.二氧化碳从化合态变为游离态
7.下列过程吸收热量的是
A.氢氧化钠固体溶丁水 B.硝酸铵固体溶于水
C.把水加入生石灰中 D.氢氧化钠溶液与稀硫酸反应
8.实验室配制50g溶质质量分数为6%的氯化钠溶液,下列做法正确的是( )
A.用托盘天平称取5g氯化钠
B.用50mL量筒量取所需水的体积
C.溶解氯化钠时,使用的玻璃仪器有量筒、玻璃棒
D.将配制好的溶液装入广口瓶中,塞好瓶塞并贴上标签
9.将少量下列物质与水混合,能形成溶液的是( )
A.面粉 B.食盐 C.淀粉 D.花生油
10.将少量下列物质分别放入水中,充分搅拌,不能形成溶液的是( )
A.蔗糖 B.酒精 C.白醋 D.泥土
11.请选择下列物质的溶解性:硝酸亚铁
A.易溶 B.微溶 C.难溶 D.不溶
二、实验题
12.水是一种重要的资源。请回答:
(1)保持水的化学性质的最小粒子是_____(填名称)。
(2)下列做法中,有利于保护水资源的是_____(填字母),
A使用节水型马桶 B生活污水任意排放
C合理使用农药和化肥 D工业废水处理达标后排放
(3)75%的酒精溶液可用于消毒,其溶剂是_____。
(4)下列各组白色固体能用水区分的是_____(填字母)。
A氯化银、硫酸钡 B生石灰、石灰石
C淀粉、白糖 D氧化钠、硝酸铵
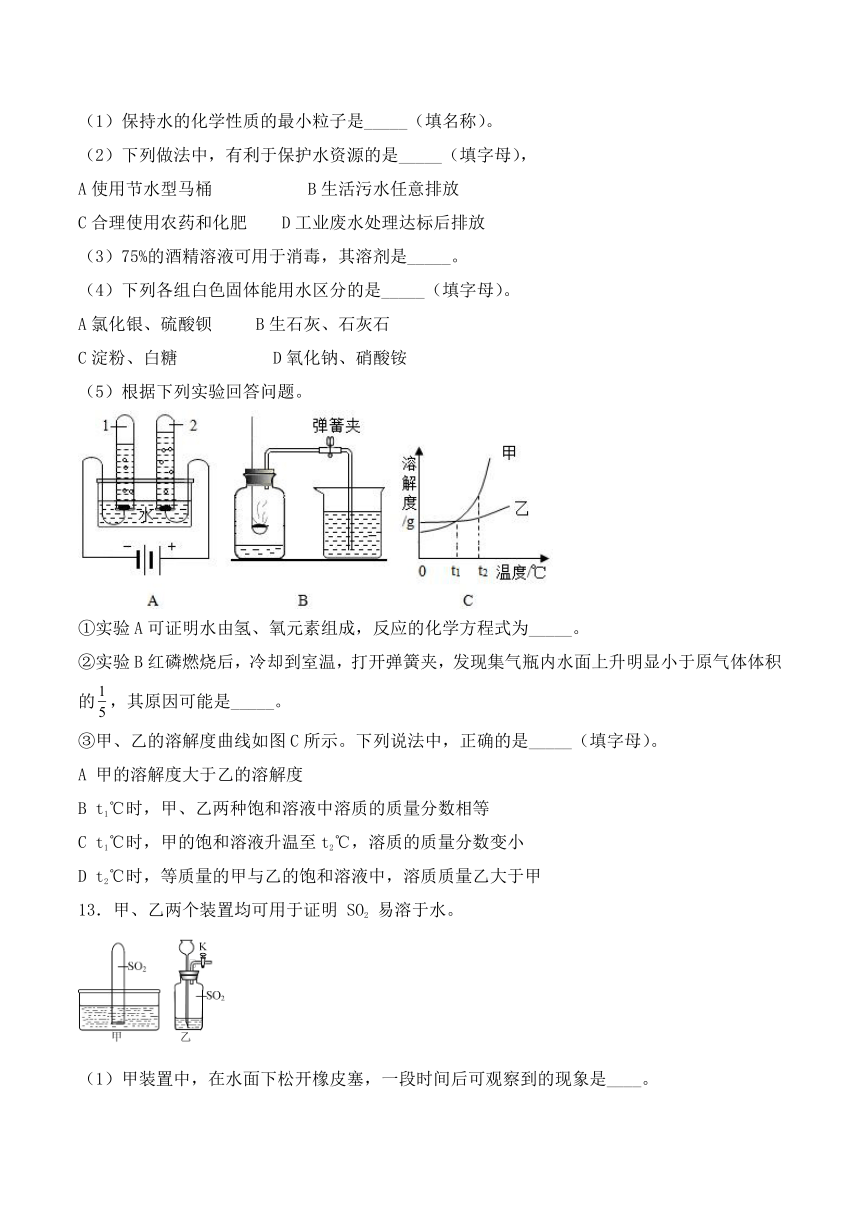
(5)根据下列实验回答问题。
①实验A可证明水由氢、氧元素组成,反应的化学方程式为_____。
②实验B红磷燃烧后,冷却到室温,打开弹簧夹,发现集气瓶内水面上升明显小于原气体体积的,其原因可能是_____。
③甲、乙的溶解度曲线如图C所示。下列说法中,正确的是_____(填字母)。
A 甲的溶解度大于乙的溶解度
B t1℃时,甲、乙两种饱和溶液中溶质的质量分数相等
C t1℃时,甲的饱和溶液升温至t2℃,溶质的质量分数变小
D t2℃时,等质量的甲与乙的饱和溶液中,溶质质量乙大于甲
13.甲、乙两个装置均可用于证明 SO2 易溶于水。
(1)甲装置中,在水面下松开橡皮塞,一段时间后可观察到的现象是____。
(2)按乙装置组装仪器,该装置气密性检查方法是:关闭活塞K,_________,若观察到____________,则装置不漏气。收集一瓶 SO2,打开活塞 K,向长颈漏斗加水至如图位置,关闭活塞 K,一段时间后可观察到的现象是_________。
三、推断题
14.同学们到实验室去进行“探究金属的性质”实验。将锌粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。请你填空。
(1)若将所得滤渣放入稀盐酸中,有气泡产生,则
①滤液里一定含有_____(填写化学式,下同),可能含有_____;
②滤渣中一定含有_____,可能含有_____。
(2)若反应后所得滤液呈无色,则滤渣中一定含有_____(填写化学式)。
(3)反应后所得滤液的溶质质量分数_____(选填“大于”、“等于”或“小于”)原硝酸银溶液的溶质质量分数。
15.A、B、C、D、E、F是初中化学常见的物质,A在常温下是一种无色液体,D俗称为酒精,F是大理石的主要成分。它们之间的转化关系如图所示:
请回答:
(1)F的化学式为_____ 。
(2) 反应①的化学反应类型是_____反应。
(3) 写出反应②化学方程式:_____。
16.我国化工专家侯德榜创立了“侯氏制碱法”,促进了世界制碱技术的发展。其流程简图和部分物质的溶解度曲线如下:
已知:①母液中有一种铵态氮肥
②
请回答下列问题:
(1)操作a的名称是_____。
(2)结合图2分析,图1反应1中NaHCO3作为晶体析出的原因是_____,从图2中还能获得的一条信息是_____。
(3)图1中得到的母液中一定含有的阳离子是_____ (填离子符号), 流程中可以循环使用的物质是_____。
(4)从图2可以看出温度高于60°C,NaHCO3 的溶解度曲线“消失”了,其原因可能是_____。
四、计算题
17.17.化学小组的同学为了测定某铜矿中碱式碳酸铜[化学式为Cu2(OH)2CO3,相对分子质量为222]的质量分数,称取该铜矿样品30g,加入132.2g稀盐酸时恰好完全反应,所得固液混合物的质量为157.8g。反应的化学方程式如下:
Cu2(OH)2CO33+4HCl=2CuCl2+3H2O+CO2↑
请你计算:
(1)铜矿样品中碱式碳酸铜的质量是多少克?其质量分数是多少?
(2)反应后所得溶液中溶质质量分数是多少?(假设铜矿中的杂质不与稀盐酸反应,也不溶于水.)
18.学习了酸和碱的知识后,阿达力同学知道了白醋的主要成分是醋酸(CH3COOH)。为了测定白醋中醋酸的质量分数,他在30 g白醋中滴加5.6%的氢氧化钾溶液,反应完全共用去氢氧化钾溶液100 g(其他成分不参加反应)。(化学反应方程式为:CH3COOH+KOH=== CH3COOK+H2O)
请计算:(1)氢氧化钾溶液中溶质的质量为________g;
(2)白醋中醋酸的质量分数为________?
19.某市售过氧乙酸(化学式为C2H4O3),其标签上的部分文字说明如下。请回答:
(1)该溶液中溶质的成分有(写化学式)_____、_____。
(2)过氧乙酸受热时容易_____。
(3)过氧乙酸中碳、氢、氧三种元素的质量比为_____(最简整数比)。
(4)一瓶过 氧乙酸溶液中含有过氧化氢溶质_____克。
参考答案
1.B 2.D 3.A 4.A 5.D 6.D 7.B 8.B 9.B 10.D
11.A.易溶
12.水分子 ACD 水 BCD 2H2O2H2↑+O2↑ 装置漏气或红磷的量不足 B
13.水槽内的水倒流在试管内形成了一段水柱 向长颈漏斗中加入液体 长颈漏斗中液面不再下降 在漏斗下口冒出气泡
14.Zn(NO3)2 Fe(NO3)2 Ag、Fe Zn Ag、Fe 小于
15.CaCO3 分解 C2H5OH+3O22CO2+3H2O
16.过滤 此温度下碳酸氢钠的溶解度较小 氯化铵的溶解度受温度的影响较大 Na+、NH4+ CO2 温度高于60℃时,碳酸氢钠开始分解
17.(1)22.2g;74%;(2) 18%
18.5.6 20%
19.C2H4O3 H2O2 分解 6:1:12 12.5
答案第1页,总2页
《溶液》检测题
一、单选题
1.KNO3和NaCl的溶解度表及溶解度曲线如下,下列说法错误的是( )
A.t1介于20℃-40℃之间
B.50℃时,溶液的溶质质量分数:KNO3>NaCl
C.当KNO3中混有少量NaCl时,可用降温结晶的方法提纯
D.60℃时,30g KNO3加入50g水,充分溶解,再降温到20℃,会析出晶体14.2g
2.下列关于溶液的说法中,正确的是
A.溶液都是均一、稳定的纯净物
B.饱和溶液的浓度一定大于不饱和溶液的浓度
C.温度高低和溶剂的种类不会影响物质的溶解性
D.配制一定溶质质量分数的溶液需要经过计算、称量(量取)、溶解
3.40℃时,KCl的溶解度为40g。40℃时,将50g KCl固体加入盛有100g水的烧杯中,充分溶解得到溶液。下列说法正确的是
A.得到的是饱和溶液
B.溶液的质量是150g
C.溶液中溶质质量分数的计算式为
D.若再向烧杯中加入一定量水,此时溶液中溶质的质量分数一定减小
4.下列实验现象描述正确的是( )
A.点燃一氧化碳气体时,发出蓝色火焰
B.硫在空气中燃烧,发出蓝紫色火焰,生成无色无味的气体
C.细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
D.将硝酸铵固体溶于水,溶液的温度升高
5.下列鉴别两种不同物质的方法中错误的是
待鉴别的物质 鉴别的方法
A 羊毛与涤纶 燃烧,闻气味
B 烧碱与硝酸铵 加水,测量液体的温度变化
C 铝与铝合金 相互刻划
D 氯化铵与硫酸铵 加熟石灰,研磨
A.A B.B C.C D.D
6.夏天打开碳酸饮料瓶盖,有大量二氧化碳气体逸出。关于打开瓶盖前后的变化,下列说法错误的是
A.二氧化碳的溶解度减小
B.剩余溶液仍为二氧化碳的饱和溶液
C.瓶内二氧化碳的溶质质量分数减小
D.二氧化碳从化合态变为游离态
7.下列过程吸收热量的是
A.氢氧化钠固体溶丁水 B.硝酸铵固体溶于水
C.把水加入生石灰中 D.氢氧化钠溶液与稀硫酸反应
8.实验室配制50g溶质质量分数为6%的氯化钠溶液,下列做法正确的是( )
A.用托盘天平称取5g氯化钠
B.用50mL量筒量取所需水的体积
C.溶解氯化钠时,使用的玻璃仪器有量筒、玻璃棒
D.将配制好的溶液装入广口瓶中,塞好瓶塞并贴上标签
9.将少量下列物质与水混合,能形成溶液的是( )
A.面粉 B.食盐 C.淀粉 D.花生油
10.将少量下列物质分别放入水中,充分搅拌,不能形成溶液的是( )
A.蔗糖 B.酒精 C.白醋 D.泥土
11.请选择下列物质的溶解性:硝酸亚铁
A.易溶 B.微溶 C.难溶 D.不溶
二、实验题
12.水是一种重要的资源。请回答:
(1)保持水的化学性质的最小粒子是_____(填名称)。
(2)下列做法中,有利于保护水资源的是_____(填字母),
A使用节水型马桶 B生活污水任意排放
C合理使用农药和化肥 D工业废水处理达标后排放
(3)75%的酒精溶液可用于消毒,其溶剂是_____。
(4)下列各组白色固体能用水区分的是_____(填字母)。
A氯化银、硫酸钡 B生石灰、石灰石
C淀粉、白糖 D氧化钠、硝酸铵
(5)根据下列实验回答问题。
①实验A可证明水由氢、氧元素组成,反应的化学方程式为_____。
②实验B红磷燃烧后,冷却到室温,打开弹簧夹,发现集气瓶内水面上升明显小于原气体体积的,其原因可能是_____。
③甲、乙的溶解度曲线如图C所示。下列说法中,正确的是_____(填字母)。
A 甲的溶解度大于乙的溶解度
B t1℃时,甲、乙两种饱和溶液中溶质的质量分数相等
C t1℃时,甲的饱和溶液升温至t2℃,溶质的质量分数变小
D t2℃时,等质量的甲与乙的饱和溶液中,溶质质量乙大于甲
13.甲、乙两个装置均可用于证明 SO2 易溶于水。
(1)甲装置中,在水面下松开橡皮塞,一段时间后可观察到的现象是____。
(2)按乙装置组装仪器,该装置气密性检查方法是:关闭活塞K,_________,若观察到____________,则装置不漏气。收集一瓶 SO2,打开活塞 K,向长颈漏斗加水至如图位置,关闭活塞 K,一段时间后可观察到的现象是_________。
三、推断题
14.同学们到实验室去进行“探究金属的性质”实验。将锌粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。请你填空。
(1)若将所得滤渣放入稀盐酸中,有气泡产生,则
①滤液里一定含有_____(填写化学式,下同),可能含有_____;
②滤渣中一定含有_____,可能含有_____。
(2)若反应后所得滤液呈无色,则滤渣中一定含有_____(填写化学式)。
(3)反应后所得滤液的溶质质量分数_____(选填“大于”、“等于”或“小于”)原硝酸银溶液的溶质质量分数。
15.A、B、C、D、E、F是初中化学常见的物质,A在常温下是一种无色液体,D俗称为酒精,F是大理石的主要成分。它们之间的转化关系如图所示:
请回答:
(1)F的化学式为_____ 。
(2) 反应①的化学反应类型是_____反应。
(3) 写出反应②化学方程式:_____。
16.我国化工专家侯德榜创立了“侯氏制碱法”,促进了世界制碱技术的发展。其流程简图和部分物质的溶解度曲线如下:
已知:①母液中有一种铵态氮肥
②
请回答下列问题:
(1)操作a的名称是_____。
(2)结合图2分析,图1反应1中NaHCO3作为晶体析出的原因是_____,从图2中还能获得的一条信息是_____。
(3)图1中得到的母液中一定含有的阳离子是_____ (填离子符号), 流程中可以循环使用的物质是_____。
(4)从图2可以看出温度高于60°C,NaHCO3 的溶解度曲线“消失”了,其原因可能是_____。
四、计算题
17.17.化学小组的同学为了测定某铜矿中碱式碳酸铜[化学式为Cu2(OH)2CO3,相对分子质量为222]的质量分数,称取该铜矿样品30g,加入132.2g稀盐酸时恰好完全反应,所得固液混合物的质量为157.8g。反应的化学方程式如下:
Cu2(OH)2CO33+4HCl=2CuCl2+3H2O+CO2↑
请你计算:
(1)铜矿样品中碱式碳酸铜的质量是多少克?其质量分数是多少?
(2)反应后所得溶液中溶质质量分数是多少?(假设铜矿中的杂质不与稀盐酸反应,也不溶于水.)
18.学习了酸和碱的知识后,阿达力同学知道了白醋的主要成分是醋酸(CH3COOH)。为了测定白醋中醋酸的质量分数,他在30 g白醋中滴加5.6%的氢氧化钾溶液,反应完全共用去氢氧化钾溶液100 g(其他成分不参加反应)。(化学反应方程式为:CH3COOH+KOH=== CH3COOK+H2O)
请计算:(1)氢氧化钾溶液中溶质的质量为________g;
(2)白醋中醋酸的质量分数为________?
19.某市售过氧乙酸(化学式为C2H4O3),其标签上的部分文字说明如下。请回答:
(1)该溶液中溶质的成分有(写化学式)_____、_____。
(2)过氧乙酸受热时容易_____。
(3)过氧乙酸中碳、氢、氧三种元素的质量比为_____(最简整数比)。
(4)一瓶过 氧乙酸溶液中含有过氧化氢溶质_____克。
参考答案
1.B 2.D 3.A 4.A 5.D 6.D 7.B 8.B 9.B 10.D
11.A.易溶
12.水分子 ACD 水 BCD 2H2O2H2↑+O2↑ 装置漏气或红磷的量不足 B
13.水槽内的水倒流在试管内形成了一段水柱 向长颈漏斗中加入液体 长颈漏斗中液面不再下降 在漏斗下口冒出气泡
14.Zn(NO3)2 Fe(NO3)2 Ag、Fe Zn Ag、Fe 小于
15.CaCO3 分解 C2H5OH+3O22CO2+3H2O
16.过滤 此温度下碳酸氢钠的溶解度较小 氯化铵的溶解度受温度的影响较大 Na+、NH4+ CO2 温度高于60℃时,碳酸氢钠开始分解
17.(1)22.2g;74%;(2) 18%
18.5.6 20%
19.C2H4O3 H2O2 分解 6:1:12 12.5
答案第1页,总2页
同课章节目录
