人教版化学必修2第四章第二节《资源综合利用 环境保护》课件(共63张PPT)
文档属性
| 名称 | 人教版化学必修2第四章第二节《资源综合利用 环境保护》课件(共63张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 4.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-27 00:00:00 | ||
图片预览








文档简介
(共63张PPT)
第二节 化学与资源综合利用、环境保护
三废:
废气、废水、废渣
煤、石油和天然气仍然是人类使用的主要能源,也是三种重要的化石燃料
优点: 提供能量、化工原料
缺点: 不可再生、环境污染
我国是最早用煤的国家,距今7200年的辽宁新乐遗址里,就有用煤的古物。
试扫其煤以为墨,黑光如漆,松墨也.
——宋· 沈括《梦溪笔谈》
我国最早发现、开采和利用石油及天然气,要从3000多年前周代算起,《易经》中有“上火下泽”、“泽中有火”等记载,说明可燃的天然气在地表湖沼水面上逸出气苗。
1900多年前,班固的《汉书.地理志》记载:“商奴,有洧水,可蘸”,是说在陕西延安一带的洧水(即清涧河)水面上有像油一样的东西可燃烧。
石油在古代曾被称为石漆、石脂水、猛火油、火油、石脑油、石烛等等。 北宋科学家沈括在《梦溪笔谈》中首先使用了“石油”的名称,指出“石油至多,生于地中无穷”,并预言“此物后必大行于世”。
沈括出身于仕宦之家,幼年随父宦游各地。嘉祐八年(1063年),进士及第,授扬州司理参军。宋神宗时参与熙宁变法,受王安石器重,历任太子中允、检正中书刑房、提举司天监、史馆检讨、三司使等职。元丰三年(1080年),出知延州,兼任鄜延路经略安抚使,驻守边境,抵御西夏,后因永乐城之战牵连被贬。晚年移居润州(今江苏镇江),隐居梦溪园。绍圣二年(1095年),因病辞世,享年六十五岁。
沈括一生致志于科学研究,在众多学科领域都有很深的造诣和卓越的成就,被誉为“中国整部科学史中最卓越的人物”。其代表作《梦溪笔谈》,内容丰富,集前代科学成就之大成,在世界文化史上有着重要的地位,被称为“中国科学史上的里程碑”。
《梦溪笔谈》,北宋科学家、政治家沈括(1031—1095)撰,是一部涉及古代中国自然科学、工艺技术及社会历史现象的综合性笔记体著作。该书在国际亦受重视,英国科学史家李约瑟评价为“中国科学史上的里程碑”。
据现可见的最古本元大德刻本,《梦溪笔谈》一共分30卷,其中《笔谈》26卷,《补笔谈》3卷,《续笔谈》1卷。全书有十七目,凡609条。内容涉及天文、数学、物理、化学、生物等各个门类学科,其价值非凡。
思考:为什么我国会是世界上最早使用
煤、石油、天然气的国家?
我的观点:1、文字;
2、文化。
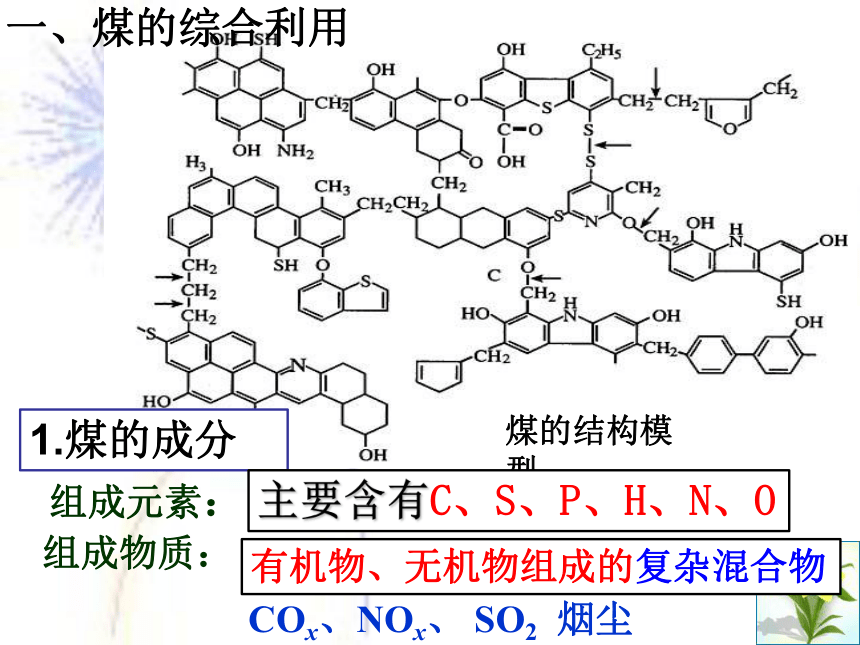
煤的结构模型
组成元素:
组成物质:
一、煤的综合利用
1.煤的成分
主要含有C、S、P、H、N、O
有机物、无机物组成的复杂混合物
COx、NOx、 SO2 烟尘
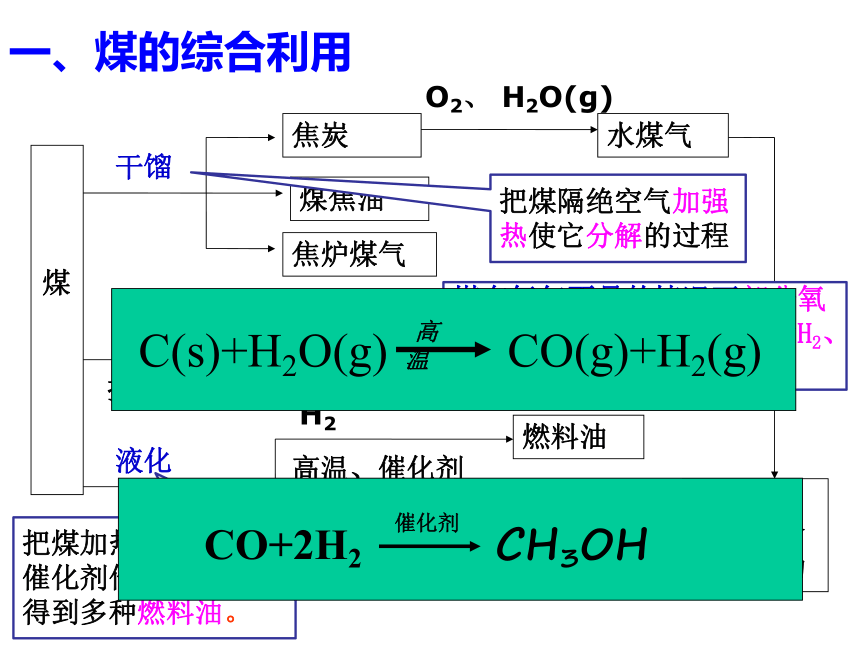
煤
焦炭
煤焦油
焦炉煤气
可燃气体
燃料油
水煤气
液态烃、甲醇等含氧有机物
水煤气
干馏
气化
控制燃烧
液化
H2
高温、催化剂
H2O(g)
高温
O2、 H2O(g)
把煤隔绝空气加强热使它分解的过程
煤在氧气不足的情况下部分氧化,使煤中的有机物转化为H2、CH4、CO 等气体物质
把煤加热裂解,并在催化剂作用下加氢,得到多种燃料油。
一、煤的综合利用
C(s)+H2O(g) CO(g)+H2(g)
高温
CO+2H2 CH3OH
催化剂
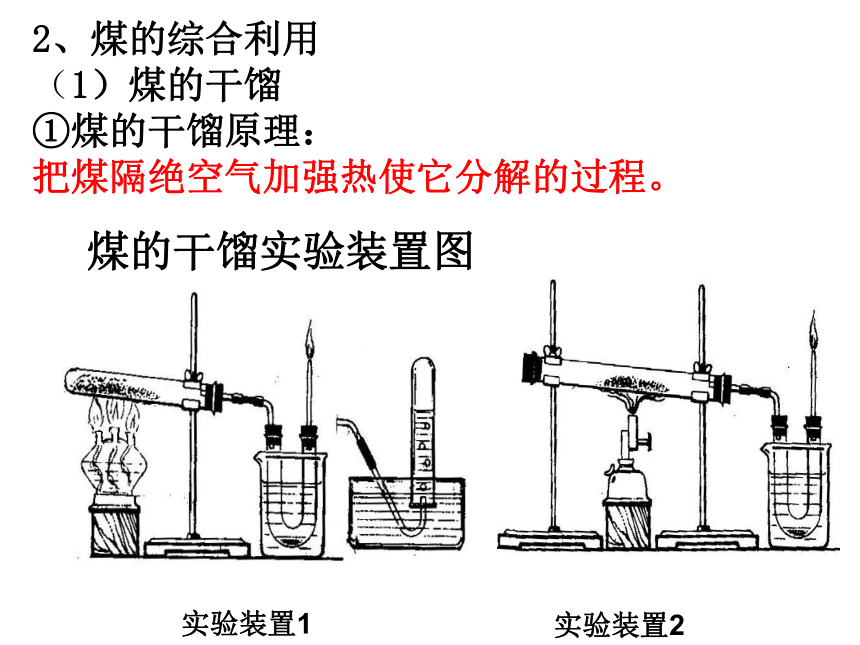
煤的干馏实验装置图
实验装置1
实验装置2
2、煤的综合利用
(1)煤的干馏
①煤的干馏原理:
把煤隔绝空气加强热使它分解的过程。
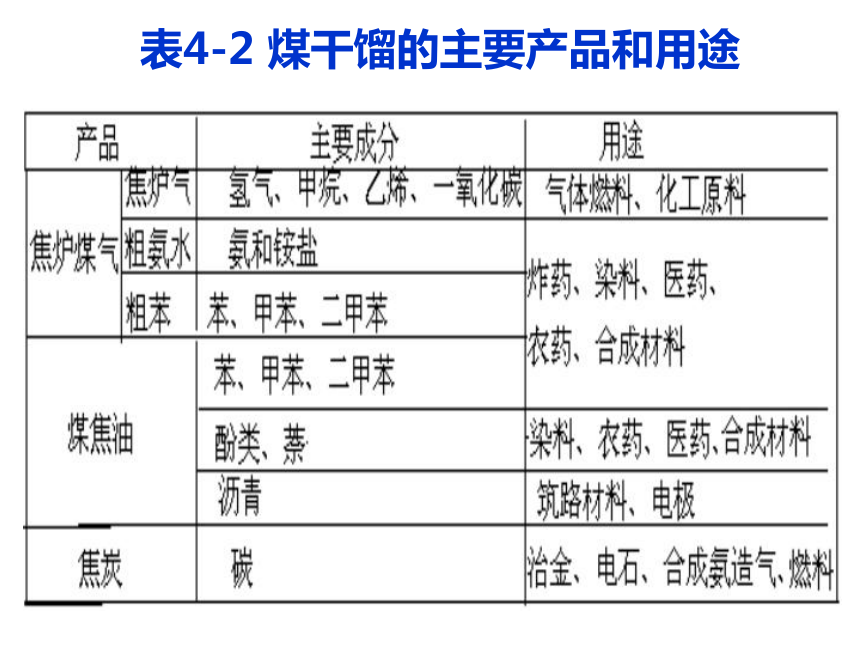
表4-2 煤干馏的主要产品和用途
二、石油的综合利用
(1)形成:古代动植物遗体经过非常复杂的变化而形成的
(2)组成元素:C、H还含有少量的 O、N、S 等元素
(3)化学成分:烷烃、环烷烃、芳香烃等,大部分是液态烃,在液态烃里溶有气态烃和固体烃
(4)物理性质:黑色或深棕色粘稠状液体,有特殊气味,密度小于水,不溶于水,没有固定的熔点和沸点
1、石油的存在和组成
石油是混合物,无固定的沸点。如何分离?
石油分馏示意图
(1)石油的分馏:
2、石油和石油的炼制
石油常压分馏
石油气(C1~C4) 低于20℃
汽油(C5~C12) 20-200℃
煤油(C12~C16) 175-275℃
柴油(C15~C18) 250-400℃
重油(C20)以上
润滑油(C16~C20) 高于350℃
25%
75%
二、石油的综合利用
蒸 馏 烧 瓶
冷 凝 管
尾接管
锥 形 瓶
温度计
酒 精 灯
铁架台
冷凝水出口
冷凝水进口
铁圈、石棉网
蒸馏
碎瓷片
比较蒸馏、分馏、干馏
蒸馏 分馏 干馏
操作过程
原理
目的
加热和冷凝 加热和冷凝 隔绝空气
加强热
物理
变化 物理
变化 复杂的物理变化和化学变化
分离 精炼 加工煤
目的:提高汽油等轻质油的产量和质量;
裂化原理:在催化剂下,把分子量大, 沸点高的烃断裂为分子量小、沸点低的烃(汽油等)的过程。
类型:热裂化(500℃)和催化裂化
C16H34
催化剂
加热、 加压
C8H18
辛烷
+ C8H16
辛烯
故裂化汽油中含有不饱和烃。
原料: 重油或石蜡
2、石油和石油的炼制
(2)石油的裂化
目的:为了获得更多的短链的不饱和气态烃(主要是乙烯)
衡量石油化工发展水平的重要标志
原理:采用比裂化更高的温度(700℃--1000℃),把具有长链的分子烃断裂成乙烯、丙烯等气态短链烃
2、石油和石油的炼制
(2)石油的裂解--深度的裂化
丁烷 丁烯
乙烯 乙烷
甲烷 丙烯
C4H8
2C2H4
催化剂
加热、 加压
乙烯
C4H10
CH4 + C3H6
催化剂
加热、 加压
C8H18
C4H10 + C4H8
催化剂
加热、 加压
C4H10
C2H4 + C2H6
催化剂
加热、 加压
石油分馏产品及用途示意图
(4)石油的催化重整:
在加热和催化剂的作用下,可以通过结构的重新调整,使链状烃转化为环状烃,如苯、甲苯
2、石油和石油的炼制
目的:
为了提高轻质油(汽油)的质量
三.天然气的组成及其综合利用
天然气的主要成分是甲烷。
我国的天然气资源很丰富,但分布很不均匀,为了改善我国东部的能源结构,制定了什么计划?
综合利用:
A、燃料:清洁能源
B、化工原料:合成氨、生产甲醇、合成两碳或多碳有机物
可燃冰是天然气(甲烷等)的水合物,它易燃烧,外形似冰,被称为“可燃冰”。“可燃冰”储量较大,可燃冰将成为最理想替代能源。
千年的希望——可燃冰
四、三大合成材料:
塑料、合成橡胶和合成纤维
——加成聚合反应(即加聚反应)
方法:将双键改为单键,将原来连在不饱和碳原子上的其它原子(或原子团)写在链节的上方或下方。
nCH2=CH2
[ CH2—CH2 ]n
(单体)
(链节)
nCH2=CHCH3
催化剂
[ CH2—CH ]n
CH3
丙烯
聚丙烯
(n 为聚合度)
聚合反应:由相对分子质量小的化合物分子互相结合成相对分子质量大的高分子的反应。
此反应属于乙烯的加成反应,所以这种聚合反应又叫加成聚合反应,简称加聚反应。
三大合成材料:
塑料、合成橡胶、合成纤维
综合利用的意义:物尽其用、保护资源,
创造出更多产品
加聚反应
聚丙烯:
单体:
CH2=CHCH3
聚苯乙烯
单体:
CH2=CH
C6H5
聚苯乙烯泡沫
聚甲基丙烯酸甲酯
(有机玻璃)
单体:
CH2=C
CH3
COOCH3
聚四氟乙烯
单体:
CF2=CF2
酚醛塑料
单体:
苯酚、甲醛
酚醛塑料
P98资料卡:聚酯纤维
2、缩聚反应:
单体之间相互形成高分子化合物的同时,还生成小分子化合物(如H2O、NH3、HX等)的聚合反应
聚乙烯颗粒
思考:如何处理高分子材料带来的环境污染?
白色污染
1.由于合成材料的广泛应用和发展,一些塑料制品带来的环境污染就是“白色污染”。
2.白色污染的危害;
3.白色污染的治理:
(1)废弃塑料的再利用(如直接作为材料、制作单体和燃料油、制作气体等);
(2)制造易降解材料;
(3)超市塑料袋有偿使用。
回收利用废旧合成材料主要有三种途径:一是通过熔融再生重新作成多种有用的材料;二是采用热裂解或化学处理的方法使其分解,用于制备多种化工原料;三是将废旧合成材料作为燃料使用。
练习
石油加工的主要目的是( )
将石油按其成分的沸点不同加以分离
将石油按饱和与不饱和烃加以分离
得到碳原子数多的烃类
将石油中烷烃、环烷烃和芳香烃分开
A
石油加工的主要目的是( )
将石油按其成分的沸点不同加以分离
将石油按饱和与不饱和烃加以分离
得到碳原子数多的烃类
将石油中烷烃、环烷烃和芳香烃分开
用重油制取丙烯的方法是( )
A.减压分馏 B.干馏 C.裂化 D.裂解
D
用重油制取丙烯的方法是( )
A.减压分馏 B.干馏 C.裂化 D.裂解
石油裂解的目的是( )
提高轻质液体燃料的产量
主要提高汽油的产量
获得短链不饱和烃
改善汽油的质量
C
石油裂解的目的是( )
提高轻质液体燃料的产量
主要提高汽油的产量
获得短链不饱和烃
改善汽油的质量
第二课时
二、环境保护与绿色化学
环境问题的含义
保护环境工作者当前的任务:
(1)对环境情况的检测
(2)三废的治理
(3)寻找源头治理环境的生产工艺
要较好地完成这些任务,都离不开化学知识。
生态环境破坏
环境污染
废气(化学燃料燃烧及工厂废气)
废水(工业废水、生活废水等)
废渣(工业垃圾、生活垃圾等)
传统的化学工业给环境带来的污染已十分严重,目前世界每年产生的有害废物达3亿吨~4亿吨,给环境造成危害,并威胁着人类的生存。有识之士提出了绿色化学的号召,并立即得到了全世界的积极响应。绿色化学的核心就是要利用化学原理从源头减少和消除污染。
人类保护伞的洞——臭氧层被破坏
空中死神——酸雨
全球变暖——温室效应
光化学烟雾
无形杀手——居室污染
环境污染的类别:
1、大气污染:来自工业废气,汽车尾气,生活废气(硫与氮的氧化物,碳氧化物,氮氢化物,卤素化合物,放射性)
臭氧层损耗与“臭氧洞”在大气层的平流层内离地面20~30km的地方是臭氧的集中层带,臭氧层是地球最好的保护伞,它吸收了来自太阳的大部分紫外线。臭氧(O3)是氧元素的同素异形体,它的化学性质十分活泼,很容易跟其他物质发生化学反应。实际上,在臭氧层内臭氧的形成是众多物质参与,一系列化学反应达到化学平衡的结果。臭氧在遇到H,OH,NO,Cl,Br时,就会被催化,加速分解为O2。氯氟烃之所以被认为是破坏臭氧层的物质,就是因为它们在太阳辐射下分解出Cl原子和Br原子。人类过多地使用氯氟烃类化学物质(用CFCs表示)是臭氧层被破坏的主要原因。
酸雨是指PH≤5.6的酸性降水,其主要成分是硫酸和硝酸,属于严重的大气污染现象,会区域性或随风漂移形成对土壤肥力、森林、水生动植物和建筑物等的大范围危害。酸雨主要是由化石燃料的燃烧、金属矿物的冶炼、生产和使用硫酸、硝酸的工厂等排放的硫氧化物和氮氧化物所造成的。
温室效应是指透射阳光的密闭空间由于与外界缺乏热交换而形成的保温效应,就是太阳短波辐射可以透过大气射入地面,而地面增暖后放出的长波辐射却被大气中的二氧化碳等物质所吸收,从而产生大气变暖的效应。引起温室效应的气体,如C02、甲烷、各种氟氯烃、臭氧和水蒸气等,称为温室气。尤其是CO2,其对温室效应的贡献超过了其他人为温室气体,成为对温室效应贡献最大的人为温室气体,其中,化石燃料所排放的CO2占温室气体总排放量的56.6%。
光化学烟雾是汽车、工厂等污染源排入大气的碳氢化合物(HC)和氮氧化物(NOx)等一次污染物在阳光(紫外光)作用下发生光化学反应生成二次污染物,后与一次污染物混合所形成的有害浅蓝色烟雾。光化学烟雾对大气的污染造成很多不良影响,对动植物有影响,甚至对建筑材料也有影响,并且大大降低能见度影响出行。
居室污染是指来自建筑装潢材料产生的甲醛、苯、氨、氡、TVOC;室内家用电器电磁波以及辐射;煤、液化气、天然气等的燃烧;煎炒烘烤等高温烹调加工过程中产生的烟雾;烟草的燃烧;家宠身上的病毒、细菌等污染物破坏家庭日常生活环境,影响人们健康的现象。
2、水污染:来自工业废水、生活废水(无
机物, 重金属盐类,营养物有机物, 洗
涤剂, 石油)
·水体富营养化(N、P、K、S的化合物)
·(生活污水、农田排水、化肥、合成洗涤剂、工业废水引起藻类、浮游生物暴发性繁殖—— 赤潮、水华)
水华是淡水中的一种自然生态现象,是由于水的富营养
化引起藻类 (如蓝藻 、绿藻、硅藻等)的迅猛生长,
水一般呈蓝色或绿色。
淡水中“水华”造成的最大危害是:饮用水源受到威胁,
藻毒素通过食物链影响人类的健康,蓝藻“水华”的次
生代谢产物MCRST能损害肝脏,具有促癌效应,直接威胁
人类的健康和生存。
赤潮是由于海水中浮游藻类、原生动物或细菌异常增殖或
聚集而引起海水变色的现象。实际上,赤潮并不一定都是
红色的,它可因引发赤潮的生物种类和数量不同而呈现出
不同颜色。
返回
水!
1998摩洛哥干旱羊上树
屡次经受干旱考验的摩洛哥山羊学会了在没有草吃的时候爬上树吃树叶。
重金属污染:
如 汞、镉、铅、铬、砷
猫自杀事件——水俣病(汞污染)
骨骼畸形变脆——骨痛病(镉污染)
智力发展隐性杀手——铅污染
3、土壤污染
来自工业垃圾、生活垃圾、废水、化肥、农药残留(Cl,P,S)、放射物质残留
4、噪声污染
5、辐射污染
6、食品污染:
2月02日:国际湿地日
3月22日:世界水日
4月22日:地球日
5月31日:世界无烟日
6月05日:世界环境日
6月17日:世界防治荒漠化和干旱日
7月11日:世界人口日
9月16日:国际保护臭氧层日
10月4日:世界动物日
10月16日:世界粮食日
12月29日:国际生物多样性日
世
界
环
境
日
把保护生态环境看成自己的神圣使命,正成为世界上越来越多人的共识。请看 ---
太阳能汽车
绿色化学
绿色化学的核心内容之二:5R原则
Reduction——“减量”
Reuse——“重复使用”
Recycling——“回收”
Regeneration——“再生”
Rejection ——“拒用”
原子经济性反应
高选择性反应
反应物
无毒无害原料
可再生资源
反应过程
安全的生产工艺
提高能源的利用率
应用无毒无害的溶剂
应用无毒无害的催化剂
产物
环境友好产品
(安全、能降
解、可再利用)
绿色化学应用于科学研究
1
2
3
4
5
6
7
利用化学方法可以控制硫和氮氧化物,进而控制
酸雨等危害。例如:针对我国以煤炭为主、酸雨类型
属于硫酸型的特点,主要采取燃料预脱煤、炉内脱硫
和烟囱排气除硫等措施,用CaCO3、CaO、Ca(OH)2、
NH3、水等吸收脱硫。
CaO+SO2====CaSO3
2CaSO3+O2====2CaSO4
SO2+2NH3+H2O====(NH4)2SO3
800 ℃
800 ℃
再如,机动车辆的尾气排放也同样需要控制,
其中的氮氧化物还是光化学污染的主要成因,
它比硫氧化物的消除难度大,一般采用CH4、H2、
NH3等在Pt、Pd等催化作用下是氮氧化物还原,
转化为N2、CO2、H2O等无害气体。
CH4+4NO2======4NO+CO2+2H2O
CH4+4NO======2N2+CO2+2H2O
Pt
400~500 ℃
Pt
400~500℃
原子利用率是指被利用的原子的质量比上总原子的质量
公式为原子利用率=(预期产物的总质量/生成物的总质量)×100%
原子利用率=25.4%
原子利用率=100%
绿色化学对于化学反应提出了“原子经济性”(原子节约)的新
概念及要求。理想的原子经济性反应是原料分子中的原子全部转
变成所需产物,不产生副产物,实现零排放。下列几种生产乙苯
的方法中,原子经济性最好的是(反应均在一定条件下进行)
( )
A
+C2H5Cl→
+HCl
B
+C2H5OH→
+H2O
C
+CH2=CH2→
→
D
+HBr
→
+H2→
C
某工厂利用铜屑制硝酸铜。你认为可以用哪些
方法?哪种最好?
利用铜屑制硝酸铜可以采用以下三种方法:
铜与浓硝酸反应;
铜与稀硝酸反应;
铜与氧气反应后,再与硝酸反应。
从原子经济性的角度考虑,从最大限度地减少废
物的排放的角度考虑,采用铜与氧气反应后,再
与硝酸反应的方法是最好的。
汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气
的污染源。治理的方法之一是在汽车的排气管上装一个
“催化转换器”(用铂、钯合金作催化剂)。它的特点
是使CO与NO反应,生成可参与大气生态环境循环的无毒
气体,并促使烃类充分燃烧及SO2的转化。
(1)写出一氧化碳与一氧化氮反应的化学方程式 :
2CO+2NO
2CO2+N2
(2)“催化转换器”的缺点是在一定程度上提高空气的
酸度,其原因是( )
SO2转化为SO3,产生硫酸酸雾
(3)控制城市空气污染源的方法可以有 (多选扣分)
a 开发氢能源 b 使用电动车
c 植树造林 d 戴上呼吸面具
ab
第二节 化学与资源综合利用、环境保护
三废:
废气、废水、废渣
煤、石油和天然气仍然是人类使用的主要能源,也是三种重要的化石燃料
优点: 提供能量、化工原料
缺点: 不可再生、环境污染
我国是最早用煤的国家,距今7200年的辽宁新乐遗址里,就有用煤的古物。
试扫其煤以为墨,黑光如漆,松墨也.
——宋· 沈括《梦溪笔谈》
我国最早发现、开采和利用石油及天然气,要从3000多年前周代算起,《易经》中有“上火下泽”、“泽中有火”等记载,说明可燃的天然气在地表湖沼水面上逸出气苗。
1900多年前,班固的《汉书.地理志》记载:“商奴,有洧水,可蘸”,是说在陕西延安一带的洧水(即清涧河)水面上有像油一样的东西可燃烧。
石油在古代曾被称为石漆、石脂水、猛火油、火油、石脑油、石烛等等。 北宋科学家沈括在《梦溪笔谈》中首先使用了“石油”的名称,指出“石油至多,生于地中无穷”,并预言“此物后必大行于世”。
沈括出身于仕宦之家,幼年随父宦游各地。嘉祐八年(1063年),进士及第,授扬州司理参军。宋神宗时参与熙宁变法,受王安石器重,历任太子中允、检正中书刑房、提举司天监、史馆检讨、三司使等职。元丰三年(1080年),出知延州,兼任鄜延路经略安抚使,驻守边境,抵御西夏,后因永乐城之战牵连被贬。晚年移居润州(今江苏镇江),隐居梦溪园。绍圣二年(1095年),因病辞世,享年六十五岁。
沈括一生致志于科学研究,在众多学科领域都有很深的造诣和卓越的成就,被誉为“中国整部科学史中最卓越的人物”。其代表作《梦溪笔谈》,内容丰富,集前代科学成就之大成,在世界文化史上有着重要的地位,被称为“中国科学史上的里程碑”。
《梦溪笔谈》,北宋科学家、政治家沈括(1031—1095)撰,是一部涉及古代中国自然科学、工艺技术及社会历史现象的综合性笔记体著作。该书在国际亦受重视,英国科学史家李约瑟评价为“中国科学史上的里程碑”。
据现可见的最古本元大德刻本,《梦溪笔谈》一共分30卷,其中《笔谈》26卷,《补笔谈》3卷,《续笔谈》1卷。全书有十七目,凡609条。内容涉及天文、数学、物理、化学、生物等各个门类学科,其价值非凡。
思考:为什么我国会是世界上最早使用
煤、石油、天然气的国家?
我的观点:1、文字;
2、文化。
煤的结构模型
组成元素:
组成物质:
一、煤的综合利用
1.煤的成分
主要含有C、S、P、H、N、O
有机物、无机物组成的复杂混合物
COx、NOx、 SO2 烟尘
煤
焦炭
煤焦油
焦炉煤气
可燃气体
燃料油
水煤气
液态烃、甲醇等含氧有机物
水煤气
干馏
气化
控制燃烧
液化
H2
高温、催化剂
H2O(g)
高温
O2、 H2O(g)
把煤隔绝空气加强热使它分解的过程
煤在氧气不足的情况下部分氧化,使煤中的有机物转化为H2、CH4、CO 等气体物质
把煤加热裂解,并在催化剂作用下加氢,得到多种燃料油。
一、煤的综合利用
C(s)+H2O(g) CO(g)+H2(g)
高温
CO+2H2 CH3OH
催化剂
煤的干馏实验装置图
实验装置1
实验装置2
2、煤的综合利用
(1)煤的干馏
①煤的干馏原理:
把煤隔绝空气加强热使它分解的过程。
表4-2 煤干馏的主要产品和用途
二、石油的综合利用
(1)形成:古代动植物遗体经过非常复杂的变化而形成的
(2)组成元素:C、H还含有少量的 O、N、S 等元素
(3)化学成分:烷烃、环烷烃、芳香烃等,大部分是液态烃,在液态烃里溶有气态烃和固体烃
(4)物理性质:黑色或深棕色粘稠状液体,有特殊气味,密度小于水,不溶于水,没有固定的熔点和沸点
1、石油的存在和组成
石油是混合物,无固定的沸点。如何分离?
石油分馏示意图
(1)石油的分馏:
2、石油和石油的炼制
石油常压分馏
石油气(C1~C4) 低于20℃
汽油(C5~C12) 20-200℃
煤油(C12~C16) 175-275℃
柴油(C15~C18) 250-400℃
重油(C20)以上
润滑油(C16~C20) 高于350℃
25%
75%
二、石油的综合利用
蒸 馏 烧 瓶
冷 凝 管
尾接管
锥 形 瓶
温度计
酒 精 灯
铁架台
冷凝水出口
冷凝水进口
铁圈、石棉网
蒸馏
碎瓷片
比较蒸馏、分馏、干馏
蒸馏 分馏 干馏
操作过程
原理
目的
加热和冷凝 加热和冷凝 隔绝空气
加强热
物理
变化 物理
变化 复杂的物理变化和化学变化
分离 精炼 加工煤
目的:提高汽油等轻质油的产量和质量;
裂化原理:在催化剂下,把分子量大, 沸点高的烃断裂为分子量小、沸点低的烃(汽油等)的过程。
类型:热裂化(500℃)和催化裂化
C16H34
催化剂
加热、 加压
C8H18
辛烷
+ C8H16
辛烯
故裂化汽油中含有不饱和烃。
原料: 重油或石蜡
2、石油和石油的炼制
(2)石油的裂化
目的:为了获得更多的短链的不饱和气态烃(主要是乙烯)
衡量石油化工发展水平的重要标志
原理:采用比裂化更高的温度(700℃--1000℃),把具有长链的分子烃断裂成乙烯、丙烯等气态短链烃
2、石油和石油的炼制
(2)石油的裂解--深度的裂化
丁烷 丁烯
乙烯 乙烷
甲烷 丙烯
C4H8
2C2H4
催化剂
加热、 加压
乙烯
C4H10
CH4 + C3H6
催化剂
加热、 加压
C8H18
C4H10 + C4H8
催化剂
加热、 加压
C4H10
C2H4 + C2H6
催化剂
加热、 加压
石油分馏产品及用途示意图
(4)石油的催化重整:
在加热和催化剂的作用下,可以通过结构的重新调整,使链状烃转化为环状烃,如苯、甲苯
2、石油和石油的炼制
目的:
为了提高轻质油(汽油)的质量
三.天然气的组成及其综合利用
天然气的主要成分是甲烷。
我国的天然气资源很丰富,但分布很不均匀,为了改善我国东部的能源结构,制定了什么计划?
综合利用:
A、燃料:清洁能源
B、化工原料:合成氨、生产甲醇、合成两碳或多碳有机物
可燃冰是天然气(甲烷等)的水合物,它易燃烧,外形似冰,被称为“可燃冰”。“可燃冰”储量较大,可燃冰将成为最理想替代能源。
千年的希望——可燃冰
四、三大合成材料:
塑料、合成橡胶和合成纤维
——加成聚合反应(即加聚反应)
方法:将双键改为单键,将原来连在不饱和碳原子上的其它原子(或原子团)写在链节的上方或下方。
nCH2=CH2
[ CH2—CH2 ]n
(单体)
(链节)
nCH2=CHCH3
催化剂
[ CH2—CH ]n
CH3
丙烯
聚丙烯
(n 为聚合度)
聚合反应:由相对分子质量小的化合物分子互相结合成相对分子质量大的高分子的反应。
此反应属于乙烯的加成反应,所以这种聚合反应又叫加成聚合反应,简称加聚反应。
三大合成材料:
塑料、合成橡胶、合成纤维
综合利用的意义:物尽其用、保护资源,
创造出更多产品
加聚反应
聚丙烯:
单体:
CH2=CHCH3
聚苯乙烯
单体:
CH2=CH
C6H5
聚苯乙烯泡沫
聚甲基丙烯酸甲酯
(有机玻璃)
单体:
CH2=C
CH3
COOCH3
聚四氟乙烯
单体:
CF2=CF2
酚醛塑料
单体:
苯酚、甲醛
酚醛塑料
P98资料卡:聚酯纤维
2、缩聚反应:
单体之间相互形成高分子化合物的同时,还生成小分子化合物(如H2O、NH3、HX等)的聚合反应
聚乙烯颗粒
思考:如何处理高分子材料带来的环境污染?
白色污染
1.由于合成材料的广泛应用和发展,一些塑料制品带来的环境污染就是“白色污染”。
2.白色污染的危害;
3.白色污染的治理:
(1)废弃塑料的再利用(如直接作为材料、制作单体和燃料油、制作气体等);
(2)制造易降解材料;
(3)超市塑料袋有偿使用。
回收利用废旧合成材料主要有三种途径:一是通过熔融再生重新作成多种有用的材料;二是采用热裂解或化学处理的方法使其分解,用于制备多种化工原料;三是将废旧合成材料作为燃料使用。
练习
石油加工的主要目的是( )
将石油按其成分的沸点不同加以分离
将石油按饱和与不饱和烃加以分离
得到碳原子数多的烃类
将石油中烷烃、环烷烃和芳香烃分开
A
石油加工的主要目的是( )
将石油按其成分的沸点不同加以分离
将石油按饱和与不饱和烃加以分离
得到碳原子数多的烃类
将石油中烷烃、环烷烃和芳香烃分开
用重油制取丙烯的方法是( )
A.减压分馏 B.干馏 C.裂化 D.裂解
D
用重油制取丙烯的方法是( )
A.减压分馏 B.干馏 C.裂化 D.裂解
石油裂解的目的是( )
提高轻质液体燃料的产量
主要提高汽油的产量
获得短链不饱和烃
改善汽油的质量
C
石油裂解的目的是( )
提高轻质液体燃料的产量
主要提高汽油的产量
获得短链不饱和烃
改善汽油的质量
第二课时
二、环境保护与绿色化学
环境问题的含义
保护环境工作者当前的任务:
(1)对环境情况的检测
(2)三废的治理
(3)寻找源头治理环境的生产工艺
要较好地完成这些任务,都离不开化学知识。
生态环境破坏
环境污染
废气(化学燃料燃烧及工厂废气)
废水(工业废水、生活废水等)
废渣(工业垃圾、生活垃圾等)
传统的化学工业给环境带来的污染已十分严重,目前世界每年产生的有害废物达3亿吨~4亿吨,给环境造成危害,并威胁着人类的生存。有识之士提出了绿色化学的号召,并立即得到了全世界的积极响应。绿色化学的核心就是要利用化学原理从源头减少和消除污染。
人类保护伞的洞——臭氧层被破坏
空中死神——酸雨
全球变暖——温室效应
光化学烟雾
无形杀手——居室污染
环境污染的类别:
1、大气污染:来自工业废气,汽车尾气,生活废气(硫与氮的氧化物,碳氧化物,氮氢化物,卤素化合物,放射性)
臭氧层损耗与“臭氧洞”在大气层的平流层内离地面20~30km的地方是臭氧的集中层带,臭氧层是地球最好的保护伞,它吸收了来自太阳的大部分紫外线。臭氧(O3)是氧元素的同素异形体,它的化学性质十分活泼,很容易跟其他物质发生化学反应。实际上,在臭氧层内臭氧的形成是众多物质参与,一系列化学反应达到化学平衡的结果。臭氧在遇到H,OH,NO,Cl,Br时,就会被催化,加速分解为O2。氯氟烃之所以被认为是破坏臭氧层的物质,就是因为它们在太阳辐射下分解出Cl原子和Br原子。人类过多地使用氯氟烃类化学物质(用CFCs表示)是臭氧层被破坏的主要原因。
酸雨是指PH≤5.6的酸性降水,其主要成分是硫酸和硝酸,属于严重的大气污染现象,会区域性或随风漂移形成对土壤肥力、森林、水生动植物和建筑物等的大范围危害。酸雨主要是由化石燃料的燃烧、金属矿物的冶炼、生产和使用硫酸、硝酸的工厂等排放的硫氧化物和氮氧化物所造成的。
温室效应是指透射阳光的密闭空间由于与外界缺乏热交换而形成的保温效应,就是太阳短波辐射可以透过大气射入地面,而地面增暖后放出的长波辐射却被大气中的二氧化碳等物质所吸收,从而产生大气变暖的效应。引起温室效应的气体,如C02、甲烷、各种氟氯烃、臭氧和水蒸气等,称为温室气。尤其是CO2,其对温室效应的贡献超过了其他人为温室气体,成为对温室效应贡献最大的人为温室气体,其中,化石燃料所排放的CO2占温室气体总排放量的56.6%。
光化学烟雾是汽车、工厂等污染源排入大气的碳氢化合物(HC)和氮氧化物(NOx)等一次污染物在阳光(紫外光)作用下发生光化学反应生成二次污染物,后与一次污染物混合所形成的有害浅蓝色烟雾。光化学烟雾对大气的污染造成很多不良影响,对动植物有影响,甚至对建筑材料也有影响,并且大大降低能见度影响出行。
居室污染是指来自建筑装潢材料产生的甲醛、苯、氨、氡、TVOC;室内家用电器电磁波以及辐射;煤、液化气、天然气等的燃烧;煎炒烘烤等高温烹调加工过程中产生的烟雾;烟草的燃烧;家宠身上的病毒、细菌等污染物破坏家庭日常生活环境,影响人们健康的现象。
2、水污染:来自工业废水、生活废水(无
机物, 重金属盐类,营养物有机物, 洗
涤剂, 石油)
·水体富营养化(N、P、K、S的化合物)
·(生活污水、农田排水、化肥、合成洗涤剂、工业废水引起藻类、浮游生物暴发性繁殖—— 赤潮、水华)
水华是淡水中的一种自然生态现象,是由于水的富营养
化引起藻类 (如蓝藻 、绿藻、硅藻等)的迅猛生长,
水一般呈蓝色或绿色。
淡水中“水华”造成的最大危害是:饮用水源受到威胁,
藻毒素通过食物链影响人类的健康,蓝藻“水华”的次
生代谢产物MCRST能损害肝脏,具有促癌效应,直接威胁
人类的健康和生存。
赤潮是由于海水中浮游藻类、原生动物或细菌异常增殖或
聚集而引起海水变色的现象。实际上,赤潮并不一定都是
红色的,它可因引发赤潮的生物种类和数量不同而呈现出
不同颜色。
返回
水!
1998摩洛哥干旱羊上树
屡次经受干旱考验的摩洛哥山羊学会了在没有草吃的时候爬上树吃树叶。
重金属污染:
如 汞、镉、铅、铬、砷
猫自杀事件——水俣病(汞污染)
骨骼畸形变脆——骨痛病(镉污染)
智力发展隐性杀手——铅污染
3、土壤污染
来自工业垃圾、生活垃圾、废水、化肥、农药残留(Cl,P,S)、放射物质残留
4、噪声污染
5、辐射污染
6、食品污染:
2月02日:国际湿地日
3月22日:世界水日
4月22日:地球日
5月31日:世界无烟日
6月05日:世界环境日
6月17日:世界防治荒漠化和干旱日
7月11日:世界人口日
9月16日:国际保护臭氧层日
10月4日:世界动物日
10月16日:世界粮食日
12月29日:国际生物多样性日
世
界
环
境
日
把保护生态环境看成自己的神圣使命,正成为世界上越来越多人的共识。请看 ---
太阳能汽车
绿色化学
绿色化学的核心内容之二:5R原则
Reduction——“减量”
Reuse——“重复使用”
Recycling——“回收”
Regeneration——“再生”
Rejection ——“拒用”
原子经济性反应
高选择性反应
反应物
无毒无害原料
可再生资源
反应过程
安全的生产工艺
提高能源的利用率
应用无毒无害的溶剂
应用无毒无害的催化剂
产物
环境友好产品
(安全、能降
解、可再利用)
绿色化学应用于科学研究
1
2
3
4
5
6
7
利用化学方法可以控制硫和氮氧化物,进而控制
酸雨等危害。例如:针对我国以煤炭为主、酸雨类型
属于硫酸型的特点,主要采取燃料预脱煤、炉内脱硫
和烟囱排气除硫等措施,用CaCO3、CaO、Ca(OH)2、
NH3、水等吸收脱硫。
CaO+SO2====CaSO3
2CaSO3+O2====2CaSO4
SO2+2NH3+H2O====(NH4)2SO3
800 ℃
800 ℃
再如,机动车辆的尾气排放也同样需要控制,
其中的氮氧化物还是光化学污染的主要成因,
它比硫氧化物的消除难度大,一般采用CH4、H2、
NH3等在Pt、Pd等催化作用下是氮氧化物还原,
转化为N2、CO2、H2O等无害气体。
CH4+4NO2======4NO+CO2+2H2O
CH4+4NO======2N2+CO2+2H2O
Pt
400~500 ℃
Pt
400~500℃
原子利用率是指被利用的原子的质量比上总原子的质量
公式为原子利用率=(预期产物的总质量/生成物的总质量)×100%
原子利用率=25.4%
原子利用率=100%
绿色化学对于化学反应提出了“原子经济性”(原子节约)的新
概念及要求。理想的原子经济性反应是原料分子中的原子全部转
变成所需产物,不产生副产物,实现零排放。下列几种生产乙苯
的方法中,原子经济性最好的是(反应均在一定条件下进行)
( )
A
+C2H5Cl→
+HCl
B
+C2H5OH→
+H2O
C
+CH2=CH2→
→
D
+HBr
→
+H2→
C
某工厂利用铜屑制硝酸铜。你认为可以用哪些
方法?哪种最好?
利用铜屑制硝酸铜可以采用以下三种方法:
铜与浓硝酸反应;
铜与稀硝酸反应;
铜与氧气反应后,再与硝酸反应。
从原子经济性的角度考虑,从最大限度地减少废
物的排放的角度考虑,采用铜与氧气反应后,再
与硝酸反应的方法是最好的。
汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气
的污染源。治理的方法之一是在汽车的排气管上装一个
“催化转换器”(用铂、钯合金作催化剂)。它的特点
是使CO与NO反应,生成可参与大气生态环境循环的无毒
气体,并促使烃类充分燃烧及SO2的转化。
(1)写出一氧化碳与一氧化氮反应的化学方程式 :
2CO+2NO
2CO2+N2
(2)“催化转换器”的缺点是在一定程度上提高空气的
酸度,其原因是( )
SO2转化为SO3,产生硫酸酸雾
(3)控制城市空气污染源的方法可以有 (多选扣分)
a 开发氢能源 b 使用电动车
c 植树造林 d 戴上呼吸面具
ab
