第1节物体是由大量分子组成的(共37张PPT)
文档属性
| 名称 | 第1节物体是由大量分子组成的(共37张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 530.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 物理 | ||
| 更新时间 | 2020-03-28 00:00:00 | ||
图片预览










文档简介
(共37张PPT)
物体是由大量
分子组成的
教学目标
1.在物理知识方面的要求:
(1)知道一般分子直径和质量的数量级;
(2)知道阿伏伽德罗常数的含义,记住这个常数的数值和单位;
(3)知道用单分子油膜方法估算分子的直径。
2.培养学生在物理学中的估算能力,会通过阿伏伽德罗常数估算固体和液体分子的质量、分子的体积(或直径)、分子数等微观量。
1,3,5
3.渗透物理学方法的教育。运用理想化方法,建立物质分子是球形体的模型,是为了简化计算,突出主要因素的理想化方法。
二、重点、难点分析
1.重点有两个,其一是使学生理解和学会用单分子油膜法估算分子大小(直径)的方法;其二是运用阿伏伽德罗常数估算微观量(分子的体积、直径、分子数等)的方法。
2.尽管今天科学技术已经达到很高的水平,但是在物理课上还不能给学生展现出分子的真实形状和分子的外观。这给讲授分子的知识带来一定的困难,也更突出了运用估算方法和建立理想模型方法研究固体、液体分子的体积、直径、分子数的重要意义。
三、教具
1.幻灯投影片或课件:水面上单分子油膜的示意图;离子显微镜下看到钨原子分布的图样。
2.演示实验:演示单分子油膜:油酸酒精溶液(1∶200),滴管,直径约20cm圆形水槽,烧杯,画有方格线的透明塑料板。
阅读课文,回答以下问题:
这里所说的分子与化学中所说的分子有何不同?
[答] 化学中讲的分子是:具有物质的化学性质的最小微粒
物理中所说的分子指的是:做热运动时遵从相同规律的微粒,包括组成物质的原子、离子或分子。
一、分子的大小
组成物质的分子是很小的,不但用肉眼不能直接看到它们,就是用光学显微镜也看不到它们。 那怎么才能看到分子呢?
我国科学家用扫描隧道显微镜拍摄的石墨表面原子的排布图,图中的每个亮斑都是一个碳原子.
用扫描隧道显微镜(能有放大几亿倍)
(一)、扫描隧道显微镜
扫描隧道显微镜拍摄的石墨表面原子排布图
分子的大小
放大上亿倍的蛋白质分子结构模型
怎样才能知道分子的大小呢?
?
2.具体做法是:?
把一滴油酸滴到水面上,油酸在水面上散开形成单分子油膜,如果把分子看成球形,单分子油膜的厚度就可认为等于油膜分子的直径.?
1.有一种粗略测定分子大小的方法叫油膜法.
那么如何才能求出单分子油膜层的厚度(即分子直径)呢?
1.先测出油酸滴的体积V:
2.测出水面上漂浮的油膜的表面积S;
3.单分子油膜的厚度等于油滴体积V与油膜面积S的比值:
方法小结:通过测量较大量来研究较小量。
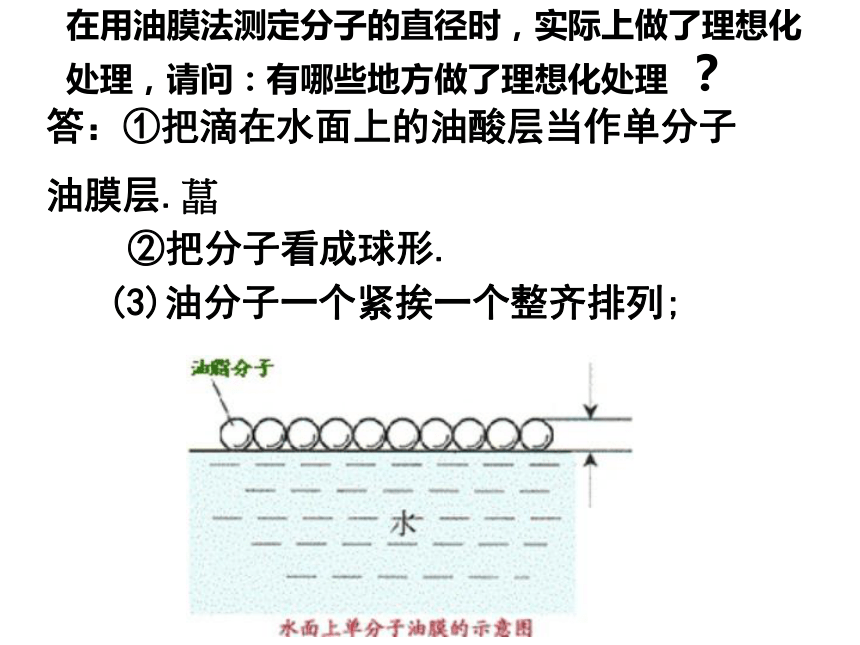
在用油膜法测定分子的直径时,实际上做了理想化处理,请问:有哪些地方做了理想化处理 ?
②把分子看成球形.
答:①把滴在水面上的油酸层当作单分子
油膜层.?
(3)油分子一个紧挨一个整齐排列;
一些数据太大或很小,为了书写方便,习惯上用科学记数法写成10的乘方数,如 3×10-10m。我们把10的乘方数叫做数量级, 1×10-10m和 9×10-10m,数量级都是 10-10m。
一般分子直径的数量级为10-10m(除少数有机物大分子以外)
数量级
例1、将1cm3油酸溶于酒精,制成200cm3的油酸酒精溶液,已知1cm3溶液有50滴,现取1滴油酸酒精溶液滴到水面上,随着酒精溶于水,油酸在水面上形成一单分子薄层,已测出这一薄层的面积为0.2m2,由此可估测油酸分子直径是多少?
1滴油酸酒精的体积为1/50cm3
其中含油酸体积为10-10m3
油酸膜的厚度为5×10-10m
练习1、体积是10-4cm3的油滴滴于水中,若展开成一单分子油膜,则油膜面积的数量级是??( )
A.102cm2???????????? B.104cm2????????????
C.106cm2?????????????D.108cm2
B
固体、液体
小球模型
气体
立方体模型
分子?
①分子模型:在计算固液体分子大小时,作为一个近似的物理模型,可把分子看成是一小球.则:
②对气体可以把分子当作是一个小立方体,这个小立方体的边长可以看作相当于分子间的平均距离.即
(以上两式中d表示分子的直径,V表示固液体分子的体积或气体分子所占的空间体积.)
二、阿伏加德罗常数
1.回忆化学中学过的阿伏加德罗常数.
1 mol的任何物质都含有相同的粒子数,这个数就叫阿伏加德罗常数 。
例2:已知水的摩尔体积是1.8×10-5 m3/mol,每个水分子的直径是4×10-10m ,设想水分子是一个挨一个排列的,求1 mol水中所含的水分子数.?
2. 根据分子的大小,可以计算出阿伏加德罗常数
一个分子的体积:
1 mol水中所含的水分子数:.
=6.0×1023 mol-1
N=
练习2.由油滴实验测得油酸分子的直径为1.12×10-9 m,已知油酸的密度为6.37×102 kg/m3,已知油酸的摩尔质量为282 g/mol,试求阿伏加德罗常数.
解:设想油酸分子一个挨一个排列,1 mol 油酸分子的质量为M,密度为ρ,油酸分子的直径为d,把每个油酸分子当作小球.则其体积为:
1 mol油酸的体积 :
1 mol油酸所含的微粒数,即阿伏加德罗常数为NA .?
∴NA=6×1023 mol-1
应用:
(1)已知物质的摩尔质量M,物体的密度p,阿伏加德罗常数NA,物质的质量 m
则 :分子的质量m分子=M/NA
分子的体积v分子=V摩尔/ NA= ( M /p ) / NA
所含有的分子数N=摩尔数×NA
=(m /M) ×NA
标准状态下,1 mol气体的体积为22.4升。 v升气体含有的分子数N=( v/V摩尔)×NA
注意:上式对气体不适用,求得的分子体积应是气体分子占有的空间
(2)应用阿伏加德罗常数
A、计算物质所含的粒子数
例3.求:1cm3水中含有的分子数(1mol水的质量是0.018kg)
B、计算分子的质量
分子质量的数量级: 10-26--10-27kg
例4.已知:水和氢气的摩尔质量分别是1.8×10-2kg/mol和2×10-3kg/mol,求水分子和氢分子的质量(已知NA=6.0×1023mol-1)
C、计算分子的体积
不适用于求气体分子的体积
但能计算气体分子所占的空间体积
例5.已知:水的摩尔质量是1.8×10-2kg/mol,水的密度是1×103kg/m3,求水分子的体积(已知NA=6.0×1023mol-1)
例6.若已知铁的原子量是56,铁的密度是7.8×103kg/m3,求:
1)质量是1g的铁块中铁原子的数目(取1位有效数字)
2)计算出铁原子的直径是多少米?
例题:
已知空气的摩尔质量是
,则空气中气体分子的平均质量多大?成年人做一次深呼吸,约吸入450cm3的空气,则做一次深呼吸所吸入的空气质量是多少?所吸入的气体分子数量是多少?(按标准状况估算)
解析 :
1.空气分子的平均质量为:
2.成年人做一次深呼吸所吸入的空气质量为:
3.所吸入的分子数为:
随堂练习
1、下列哪一组已知数据中能求出阿伏加德罗常数 。 ( )
A物质分子的质量和体积
B物体的质量和它的摩尔质量
C物体的质量、密度和它的分子体积
D物体的摩尔体积、密度及其分子质量
D
D
2、1克水中含有的水分子个数为( )
A 6.02×1023 B 3.01×1023
C 6.02×1022 D 3.34×1022
3.(2004年浙江高考)若以μ表示水的摩尔质量,υ表示在标准状态下水蒸气的摩尔体积,ρ为表示在标准状态下水蒸气的密度,NA为阿伏加德罗常数,m、Δ分别表示每个水分子的质量和体积,下面是四个关系式
① NA =υρ/m ② ρ =μ/NAΔ
③ m = μ/NA ④Δ= υ/NA
其中
A.①和②都是正确的;B.①和③都是正确的;
C.②和④都是正确的;D.①和④都是正确的。
答案:B
4.已知阿伏加德罗常数为NA,铜的摩尔质量为M,密度为ρ(均为国际单位),则( )
A.1m3铜原子含原子数目为ρNA/M
B.1个铜原子质量是M /NA
C.1个铜原子的体积是M/ρNA
D.1kg铜所含原子的数目是ρNA
ABC
5.只要知道下列哪一组物理量,就可以估算出气体中分子的平均距离 ( )
A.阿伏加德罗常数、该气体的摩尔质量和质量
B.阿伏加德罗常数、该气体的摩尔质量和密度
C.阿伏加德罗常数、该气体的摩尔质量和体积
D.该气体的密度、体积和摩尔质量
B
6.下列数据能求出阿伏加德罗常数的是( )
A.水的密度和水的摩尔质量
B.水的摩尔质量和水分子的体积
C.水分子的体积和水分子的质量
D.水分子的质量和水的摩尔质量
D
7.水的分子量18,水的密度为103kg/m3,阿伏加德罗常数为NA=6.02×1023个/ mol,则:
(1)水的摩尔质量M=__________
18g/mol
(2)水的摩尔体积V=__________
M/ρ=18/1=18g/cm3
(3)一个水分子的质量m0 =_____________
M/ NA =18 / 6.02×1023 =2.99 ×10-26 kg
(4)一个水分子的体积V0 =_____________
V/ NA =2.99 ×10-23 cm3
(5)10g水中含有的分子数目N=___________________
mNA/M=3.344 ×1021
8.估算在标准状态下气体分子间的距离。
解:将每个空气分子所占据的空间设为小立方体,则小立方体的边长为气体分子间的距离。(V摩尔=22.4×10-3 m3)
NA×d3=V摩尔
d= (V摩尔 / NA )1/3
=[22.4×10-3 /( 6.02×1023 )]1/3m
=3.8 ×10-9 m
[小结]
1.一般物体中的分子数目是很大的.
2.一般分子的质量也是很小的.?一般分子质量数量级是10-26Kg
3.阿伏加德罗常数是联系微观世界和宏观世界的桥梁,通过该常数把摩尔质量、摩尔体积跟分子质量、分子大小等微观物理量联系起来了.
一般分子直径的数量级为10-10 m
分子的模型:把分子看成球形或正方体模型。
物体是由大量
分子组成的
教学目标
1.在物理知识方面的要求:
(1)知道一般分子直径和质量的数量级;
(2)知道阿伏伽德罗常数的含义,记住这个常数的数值和单位;
(3)知道用单分子油膜方法估算分子的直径。
2.培养学生在物理学中的估算能力,会通过阿伏伽德罗常数估算固体和液体分子的质量、分子的体积(或直径)、分子数等微观量。
1,3,5
3.渗透物理学方法的教育。运用理想化方法,建立物质分子是球形体的模型,是为了简化计算,突出主要因素的理想化方法。
二、重点、难点分析
1.重点有两个,其一是使学生理解和学会用单分子油膜法估算分子大小(直径)的方法;其二是运用阿伏伽德罗常数估算微观量(分子的体积、直径、分子数等)的方法。
2.尽管今天科学技术已经达到很高的水平,但是在物理课上还不能给学生展现出分子的真实形状和分子的外观。这给讲授分子的知识带来一定的困难,也更突出了运用估算方法和建立理想模型方法研究固体、液体分子的体积、直径、分子数的重要意义。
三、教具
1.幻灯投影片或课件:水面上单分子油膜的示意图;离子显微镜下看到钨原子分布的图样。
2.演示实验:演示单分子油膜:油酸酒精溶液(1∶200),滴管,直径约20cm圆形水槽,烧杯,画有方格线的透明塑料板。
阅读课文,回答以下问题:
这里所说的分子与化学中所说的分子有何不同?
[答] 化学中讲的分子是:具有物质的化学性质的最小微粒
物理中所说的分子指的是:做热运动时遵从相同规律的微粒,包括组成物质的原子、离子或分子。
一、分子的大小
组成物质的分子是很小的,不但用肉眼不能直接看到它们,就是用光学显微镜也看不到它们。 那怎么才能看到分子呢?
我国科学家用扫描隧道显微镜拍摄的石墨表面原子的排布图,图中的每个亮斑都是一个碳原子.
用扫描隧道显微镜(能有放大几亿倍)
(一)、扫描隧道显微镜
扫描隧道显微镜拍摄的石墨表面原子排布图
分子的大小
放大上亿倍的蛋白质分子结构模型
怎样才能知道分子的大小呢?
?
2.具体做法是:?
把一滴油酸滴到水面上,油酸在水面上散开形成单分子油膜,如果把分子看成球形,单分子油膜的厚度就可认为等于油膜分子的直径.?
1.有一种粗略测定分子大小的方法叫油膜法.
那么如何才能求出单分子油膜层的厚度(即分子直径)呢?
1.先测出油酸滴的体积V:
2.测出水面上漂浮的油膜的表面积S;
3.单分子油膜的厚度等于油滴体积V与油膜面积S的比值:
方法小结:通过测量较大量来研究较小量。
在用油膜法测定分子的直径时,实际上做了理想化处理,请问:有哪些地方做了理想化处理 ?
②把分子看成球形.
答:①把滴在水面上的油酸层当作单分子
油膜层.?
(3)油分子一个紧挨一个整齐排列;
一些数据太大或很小,为了书写方便,习惯上用科学记数法写成10的乘方数,如 3×10-10m。我们把10的乘方数叫做数量级, 1×10-10m和 9×10-10m,数量级都是 10-10m。
一般分子直径的数量级为10-10m(除少数有机物大分子以外)
数量级
例1、将1cm3油酸溶于酒精,制成200cm3的油酸酒精溶液,已知1cm3溶液有50滴,现取1滴油酸酒精溶液滴到水面上,随着酒精溶于水,油酸在水面上形成一单分子薄层,已测出这一薄层的面积为0.2m2,由此可估测油酸分子直径是多少?
1滴油酸酒精的体积为1/50cm3
其中含油酸体积为10-10m3
油酸膜的厚度为5×10-10m
练习1、体积是10-4cm3的油滴滴于水中,若展开成一单分子油膜,则油膜面积的数量级是??( )
A.102cm2???????????? B.104cm2????????????
C.106cm2?????????????D.108cm2
B
固体、液体
小球模型
气体
立方体模型
分子?
①分子模型:在计算固液体分子大小时,作为一个近似的物理模型,可把分子看成是一小球.则:
②对气体可以把分子当作是一个小立方体,这个小立方体的边长可以看作相当于分子间的平均距离.即
(以上两式中d表示分子的直径,V表示固液体分子的体积或气体分子所占的空间体积.)
二、阿伏加德罗常数
1.回忆化学中学过的阿伏加德罗常数.
1 mol的任何物质都含有相同的粒子数,这个数就叫阿伏加德罗常数 。
例2:已知水的摩尔体积是1.8×10-5 m3/mol,每个水分子的直径是4×10-10m ,设想水分子是一个挨一个排列的,求1 mol水中所含的水分子数.?
2. 根据分子的大小,可以计算出阿伏加德罗常数
一个分子的体积:
1 mol水中所含的水分子数:.
=6.0×1023 mol-1
N=
练习2.由油滴实验测得油酸分子的直径为1.12×10-9 m,已知油酸的密度为6.37×102 kg/m3,已知油酸的摩尔质量为282 g/mol,试求阿伏加德罗常数.
解:设想油酸分子一个挨一个排列,1 mol 油酸分子的质量为M,密度为ρ,油酸分子的直径为d,把每个油酸分子当作小球.则其体积为:
1 mol油酸的体积 :
1 mol油酸所含的微粒数,即阿伏加德罗常数为NA .?
∴NA=6×1023 mol-1
应用:
(1)已知物质的摩尔质量M,物体的密度p,阿伏加德罗常数NA,物质的质量 m
则 :分子的质量m分子=M/NA
分子的体积v分子=V摩尔/ NA= ( M /p ) / NA
所含有的分子数N=摩尔数×NA
=(m /M) ×NA
标准状态下,1 mol气体的体积为22.4升。 v升气体含有的分子数N=( v/V摩尔)×NA
注意:上式对气体不适用,求得的分子体积应是气体分子占有的空间
(2)应用阿伏加德罗常数
A、计算物质所含的粒子数
例3.求:1cm3水中含有的分子数(1mol水的质量是0.018kg)
B、计算分子的质量
分子质量的数量级: 10-26--10-27kg
例4.已知:水和氢气的摩尔质量分别是1.8×10-2kg/mol和2×10-3kg/mol,求水分子和氢分子的质量(已知NA=6.0×1023mol-1)
C、计算分子的体积
不适用于求气体分子的体积
但能计算气体分子所占的空间体积
例5.已知:水的摩尔质量是1.8×10-2kg/mol,水的密度是1×103kg/m3,求水分子的体积(已知NA=6.0×1023mol-1)
例6.若已知铁的原子量是56,铁的密度是7.8×103kg/m3,求:
1)质量是1g的铁块中铁原子的数目(取1位有效数字)
2)计算出铁原子的直径是多少米?
例题:
已知空气的摩尔质量是
,则空气中气体分子的平均质量多大?成年人做一次深呼吸,约吸入450cm3的空气,则做一次深呼吸所吸入的空气质量是多少?所吸入的气体分子数量是多少?(按标准状况估算)
解析 :
1.空气分子的平均质量为:
2.成年人做一次深呼吸所吸入的空气质量为:
3.所吸入的分子数为:
随堂练习
1、下列哪一组已知数据中能求出阿伏加德罗常数 。 ( )
A物质分子的质量和体积
B物体的质量和它的摩尔质量
C物体的质量、密度和它的分子体积
D物体的摩尔体积、密度及其分子质量
D
D
2、1克水中含有的水分子个数为( )
A 6.02×1023 B 3.01×1023
C 6.02×1022 D 3.34×1022
3.(2004年浙江高考)若以μ表示水的摩尔质量,υ表示在标准状态下水蒸气的摩尔体积,ρ为表示在标准状态下水蒸气的密度,NA为阿伏加德罗常数,m、Δ分别表示每个水分子的质量和体积,下面是四个关系式
① NA =υρ/m ② ρ =μ/NAΔ
③ m = μ/NA ④Δ= υ/NA
其中
A.①和②都是正确的;B.①和③都是正确的;
C.②和④都是正确的;D.①和④都是正确的。
答案:B
4.已知阿伏加德罗常数为NA,铜的摩尔质量为M,密度为ρ(均为国际单位),则( )
A.1m3铜原子含原子数目为ρNA/M
B.1个铜原子质量是M /NA
C.1个铜原子的体积是M/ρNA
D.1kg铜所含原子的数目是ρNA
ABC
5.只要知道下列哪一组物理量,就可以估算出气体中分子的平均距离 ( )
A.阿伏加德罗常数、该气体的摩尔质量和质量
B.阿伏加德罗常数、该气体的摩尔质量和密度
C.阿伏加德罗常数、该气体的摩尔质量和体积
D.该气体的密度、体积和摩尔质量
B
6.下列数据能求出阿伏加德罗常数的是( )
A.水的密度和水的摩尔质量
B.水的摩尔质量和水分子的体积
C.水分子的体积和水分子的质量
D.水分子的质量和水的摩尔质量
D
7.水的分子量18,水的密度为103kg/m3,阿伏加德罗常数为NA=6.02×1023个/ mol,则:
(1)水的摩尔质量M=__________
18g/mol
(2)水的摩尔体积V=__________
M/ρ=18/1=18g/cm3
(3)一个水分子的质量m0 =_____________
M/ NA =18 / 6.02×1023 =2.99 ×10-26 kg
(4)一个水分子的体积V0 =_____________
V/ NA =2.99 ×10-23 cm3
(5)10g水中含有的分子数目N=___________________
mNA/M=3.344 ×1021
8.估算在标准状态下气体分子间的距离。
解:将每个空气分子所占据的空间设为小立方体,则小立方体的边长为气体分子间的距离。(V摩尔=22.4×10-3 m3)
NA×d3=V摩尔
d= (V摩尔 / NA )1/3
=[22.4×10-3 /( 6.02×1023 )]1/3m
=3.8 ×10-9 m
[小结]
1.一般物体中的分子数目是很大的.
2.一般分子的质量也是很小的.?一般分子质量数量级是10-26Kg
3.阿伏加德罗常数是联系微观世界和宏观世界的桥梁,通过该常数把摩尔质量、摩尔体积跟分子质量、分子大小等微观物理量联系起来了.
一般分子直径的数量级为10-10 m
分子的模型:把分子看成球形或正方体模型。
