课题2 二氧化碳制取的研究 课件(23张PPT)
文档属性
| 名称 | 课题2 二氧化碳制取的研究 课件(23张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-29 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
猜猜我!
二氧化碳的用途
化工产品的原料
制碳酸饮料
灭火
气体肥料
人工降雨
制冷剂
Thank
you
课题2:
二氧化碳制取的研究
1.初步学会实验室制取二氧化碳;
学习目标
2.掌握实验室制取气体的一般思路和方法;
3.学会与他人合作制取二氧化碳气体。
实验室制取氧气的知识回顾
药品 KMnO4 H2O2溶液和MnO2
反应原理
发生装置
收集装置
检验方法
验满方法
A
B
C或D
用带火星的木条伸进集气瓶中,木条复燃,则该气体是氧气。
用带火星的木条放在集气瓶口,木条复燃,则氧气已收集满。
2KMnO4 K2MnO4+MnO2+O2↑
2H2O2 2H2O+O2↑
=
=
△
MnO2
活动一:
实验室制取二氧化碳原理的探究
温馨提示:
实验室制取二氧化碳药品选取原则是:
①反应条件是否容易达到;
②产生气体的速率是否合适;
③收集的气体是否纯净;
④装置、操作是否简单;
⑤原料是否易得、价廉。
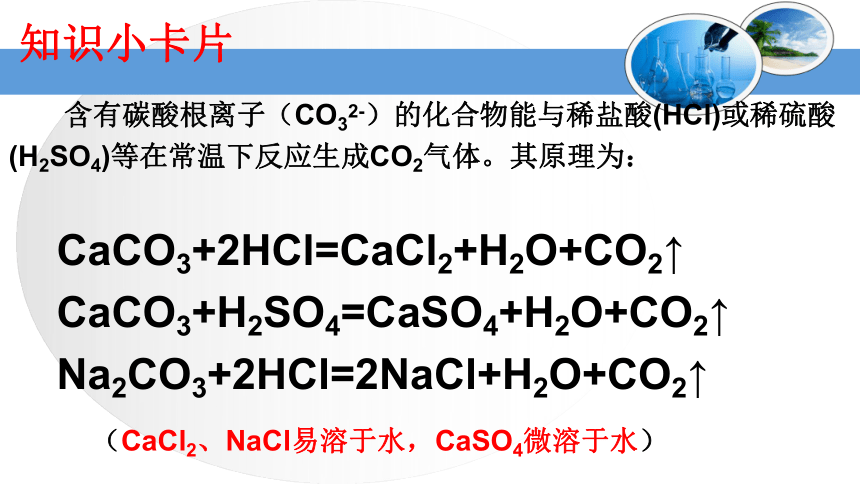
含有碳酸根离子(CO32-)的化合物能与稀盐酸(HCl)或稀硫酸(H2SO4)等在常温下反应生成CO2气体。其原理为:
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+H2SO4=CaSO4+H2O+CO2↑
Na2CO3+2HCl=2NaCl+H2O+CO2↑
(CaCl2、NaCl易溶于水,CaSO4微溶于水)
知识小卡片
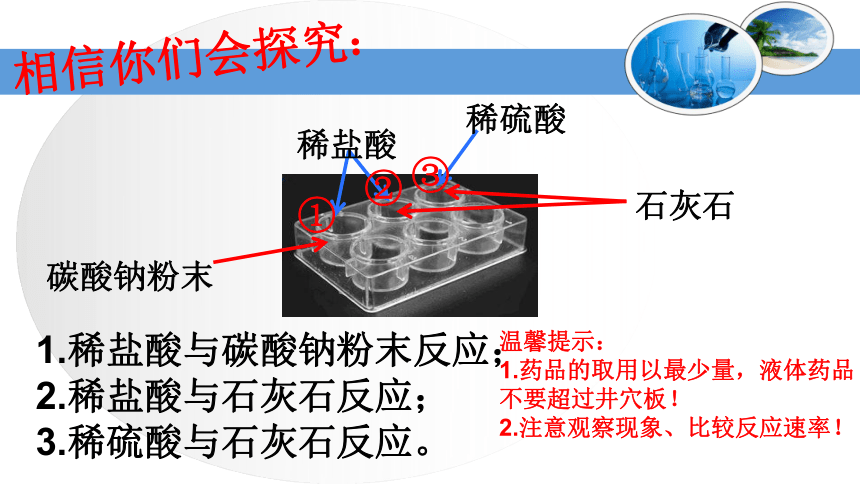
相信你们会探究:
稀盐酸
稀硫酸
碳酸钠粉末
石灰石
1.稀盐酸与碳酸钠粉末反应;
2.稀盐酸与石灰石反应;
3.稀硫酸与石灰石反应。
温馨提示:
1.药品的取用以最少量,液体药品不要超过井穴板!
2.注意观察现象、比较反应速率!
①
②
③
石灰石(或大理石)和稀盐酸
药品:
原理:
实验室制取CO2的反应原理
知识小结
碳酸钙 + 稀盐酸 = 氯化钙 + 水 + 二氧化碳
CaCO3+ 2HCl = CaCl2 + H2O+ CO2
活动二:
实验室制取二氧化碳装置的探究
(向上排空气法)
(向下排空气法)
(排水法)
相信你们会分析:
相信你们会选择:
发生装置 收集装置
制O2
制CO2
反应物状态
反应条件
装置图
气体密度
气体溶解性
2H2O2 === 2H2O +O2↑
MnO2
2KMnO4 === K2MnO4+MnO2+O2 ↑
△
CaCO3+2HCl==CaCl2+H2O+CO2↑
能溶于水且能与水反应
固+液
不需加热
固
加热
固+液
不需加热
比空气略大
不易溶于水
比空气大
不适宜用排水法
发生装置
固体和固体
固体和液体
液体和液体
收集装置
反应物的状态
反应条件(是否需要加热、加催化剂等)
排空气法
排水法
(不易溶于水、不与水发生反应)
密度比空气的大—— 向上排气法
密度比空气的小—— 向下排气法
实验室制取气体装置的确定
知识小结
实验室制取CO2的装置:
我知道啦!
检验方法
澄清石灰水
变浑浊
验满方法
活动三:
实验室制取二氧化碳步骤的探究
相信你们会合作:
利用老师提供的仪器制取一瓶二氧化碳气体,检验并验满二氧化碳气体。
温馨提示:
1.注意操作的规范性;
2.小组之间分工合作看谁完成的最快?
3.注意发现装置的优点。
相信你们会发现:
A B C D E
实验室制取气体的一般思路
药品
反应原理
发生装置
收集装置
检验方法
验满方法
相信你们会归纳:
活动四:
实验室制取气体的一般思路研究
相信你们会分享:
我学到的知识…
我学到的学习方法…
我还想到知道的知识…
1. 化学实验小组用以下仪器组装并制取气体。
小明同学在制取气体时使用的仪器是①③
④⑤⑦⑧,他制取的气体是 ;
化学方程式为 .
O2
2KClO3 2KCl+ 3O2↑
MnO2
△
2KMnO4 K2MnO4 + MnO2+ O2↑
△
或:
铁架台 锥形瓶 试管 酒精灯 集气瓶
① ② ③ ④ ⑤
长颈漏斗 水槽
⑥ ⑦ ⑧ ⑨ ⑩
相信你们会应用:
(1)用以上所给仪器可以组装出多套氧气的发生装置和收集装置。请你组装一套氧气的发生装置和收集装置,写出所选择的仪器编号 .
(2)简要说明你组装的气体发生装置的优点
2. 在实验室里常采用过氧化氢和二氧化锰混合的方法制取氧气。请回答下列问题:
? ① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ ⑩
双孔
单孔
①⑦ ③⑤
①④⑥ ③⑤
①⑦ ③⑧⑨
①④⑥ ③⑧⑨
知识拓展:
鸡蛋壳的主要成分是碳酸钙,与食醋反应会产生二氧化碳。请用所学知识利用生活用品设计一套装置,制取二氧化碳。
谢
谢!
猜猜我!
二氧化碳的用途
化工产品的原料
制碳酸饮料
灭火
气体肥料
人工降雨
制冷剂
Thank
you
课题2:
二氧化碳制取的研究
1.初步学会实验室制取二氧化碳;
学习目标
2.掌握实验室制取气体的一般思路和方法;
3.学会与他人合作制取二氧化碳气体。
实验室制取氧气的知识回顾
药品 KMnO4 H2O2溶液和MnO2
反应原理
发生装置
收集装置
检验方法
验满方法
A
B
C或D
用带火星的木条伸进集气瓶中,木条复燃,则该气体是氧气。
用带火星的木条放在集气瓶口,木条复燃,则氧气已收集满。
2KMnO4 K2MnO4+MnO2+O2↑
2H2O2 2H2O+O2↑
=
=
△
MnO2
活动一:
实验室制取二氧化碳原理的探究
温馨提示:
实验室制取二氧化碳药品选取原则是:
①反应条件是否容易达到;
②产生气体的速率是否合适;
③收集的气体是否纯净;
④装置、操作是否简单;
⑤原料是否易得、价廉。
含有碳酸根离子(CO32-)的化合物能与稀盐酸(HCl)或稀硫酸(H2SO4)等在常温下反应生成CO2气体。其原理为:
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+H2SO4=CaSO4+H2O+CO2↑
Na2CO3+2HCl=2NaCl+H2O+CO2↑
(CaCl2、NaCl易溶于水,CaSO4微溶于水)
知识小卡片
相信你们会探究:
稀盐酸
稀硫酸
碳酸钠粉末
石灰石
1.稀盐酸与碳酸钠粉末反应;
2.稀盐酸与石灰石反应;
3.稀硫酸与石灰石反应。
温馨提示:
1.药品的取用以最少量,液体药品不要超过井穴板!
2.注意观察现象、比较反应速率!
①
②
③
石灰石(或大理石)和稀盐酸
药品:
原理:
实验室制取CO2的反应原理
知识小结
碳酸钙 + 稀盐酸 = 氯化钙 + 水 + 二氧化碳
CaCO3+ 2HCl = CaCl2 + H2O+ CO2
活动二:
实验室制取二氧化碳装置的探究
(向上排空气法)
(向下排空气法)
(排水法)
相信你们会分析:
相信你们会选择:
发生装置 收集装置
制O2
制CO2
反应物状态
反应条件
装置图
气体密度
气体溶解性
2H2O2 === 2H2O +O2↑
MnO2
2KMnO4 === K2MnO4+MnO2+O2 ↑
△
CaCO3+2HCl==CaCl2+H2O+CO2↑
能溶于水且能与水反应
固+液
不需加热
固
加热
固+液
不需加热
比空气略大
不易溶于水
比空气大
不适宜用排水法
发生装置
固体和固体
固体和液体
液体和液体
收集装置
反应物的状态
反应条件(是否需要加热、加催化剂等)
排空气法
排水法
(不易溶于水、不与水发生反应)
密度比空气的大—— 向上排气法
密度比空气的小—— 向下排气法
实验室制取气体装置的确定
知识小结
实验室制取CO2的装置:
我知道啦!
检验方法
澄清石灰水
变浑浊
验满方法
活动三:
实验室制取二氧化碳步骤的探究
相信你们会合作:
利用老师提供的仪器制取一瓶二氧化碳气体,检验并验满二氧化碳气体。
温馨提示:
1.注意操作的规范性;
2.小组之间分工合作看谁完成的最快?
3.注意发现装置的优点。
相信你们会发现:
A B C D E
实验室制取气体的一般思路
药品
反应原理
发生装置
收集装置
检验方法
验满方法
相信你们会归纳:
活动四:
实验室制取气体的一般思路研究
相信你们会分享:
我学到的知识…
我学到的学习方法…
我还想到知道的知识…
1. 化学实验小组用以下仪器组装并制取气体。
小明同学在制取气体时使用的仪器是①③
④⑤⑦⑧,他制取的气体是 ;
化学方程式为 .
O2
2KClO3 2KCl+ 3O2↑
MnO2
△
2KMnO4 K2MnO4 + MnO2+ O2↑
△
或:
铁架台 锥形瓶 试管 酒精灯 集气瓶
① ② ③ ④ ⑤
长颈漏斗 水槽
⑥ ⑦ ⑧ ⑨ ⑩
相信你们会应用:
(1)用以上所给仪器可以组装出多套氧气的发生装置和收集装置。请你组装一套氧气的发生装置和收集装置,写出所选择的仪器编号 .
(2)简要说明你组装的气体发生装置的优点
2. 在实验室里常采用过氧化氢和二氧化锰混合的方法制取氧气。请回答下列问题:
? ① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ ⑩
双孔
单孔
①⑦ ③⑤
①④⑥ ③⑤
①⑦ ③⑧⑨
①④⑥ ③⑧⑨
知识拓展:
鸡蛋壳的主要成分是碳酸钙,与食醋反应会产生二氧化碳。请用所学知识利用生活用品设计一套装置,制取二氧化碳。
谢
谢!
同课章节目录
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的构成
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题1 质量守恒定律
- 课题2 如何正确书写化学方程式
- 课题3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动3 燃烧的条件
- 旧版目录
- 第五单元 物质组成的表示
- 课题2 燃料和热量
- 课题3 使用燃料对环境的影响
