苏教版高二化学选修四化学反应原理 专题2 第三单元 化学平衡的移动(共56张PPT)
文档属性
| 名称 | 苏教版高二化学选修四化学反应原理 专题2 第三单元 化学平衡的移动(共56张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-30 00:00:00 | ||
图片预览










文档简介
(共56张PPT)
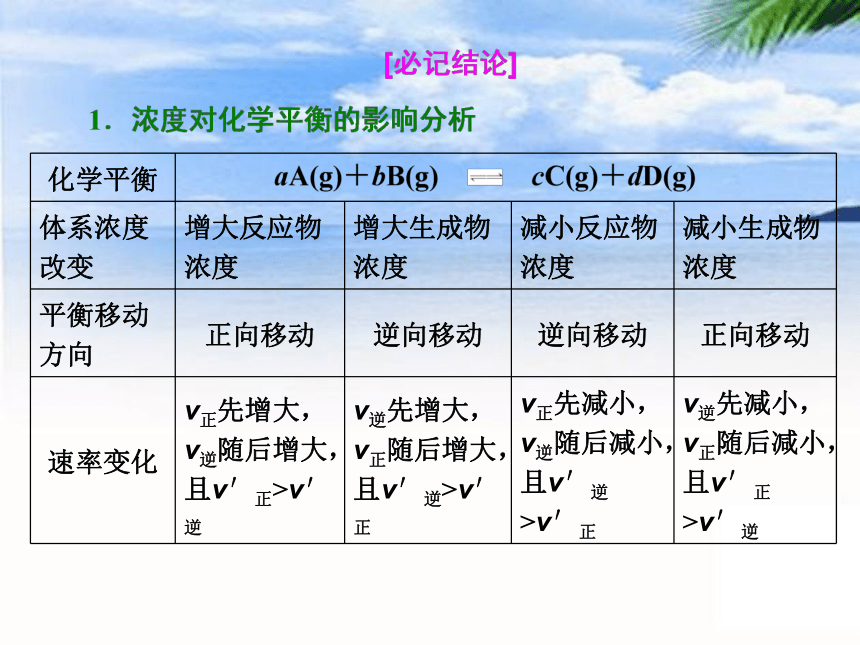
化学平衡
体系浓度改变 增大反应物浓度 增大生成物浓度 减小反应物浓度 减小生成物浓度
平衡移动方向 正向移动 逆向移动 逆向移动 正向移动
速率变化 v正先增大,v逆随后增大,且v′正>v′逆 v逆先增大,v正随后增大,且v′逆>v′正 v正先减小,v逆随后减小,且v′逆>v′正 v逆先减小,v正随后减小,且v′正>v′逆
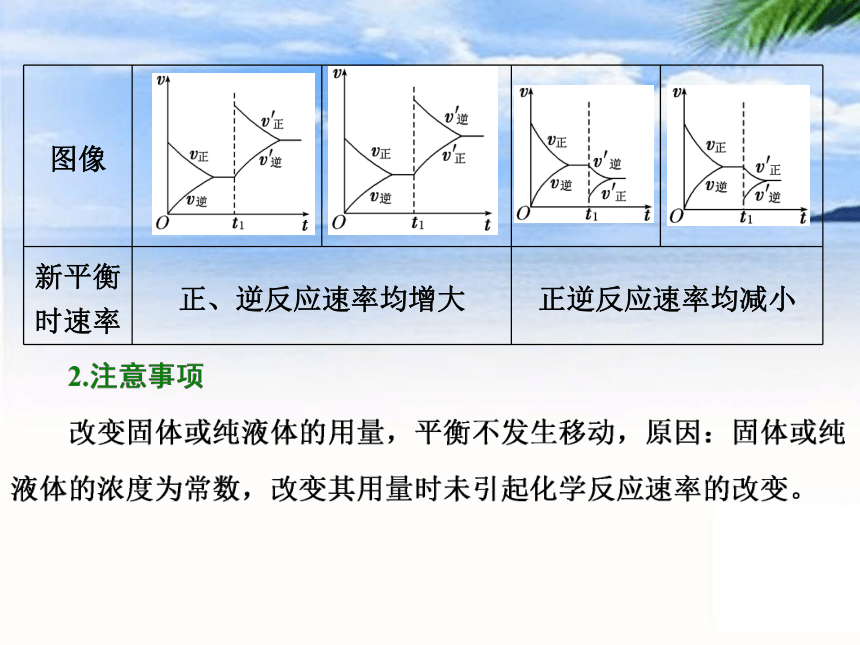
图像
新平衡时速率 正、逆反应速率均增大 正逆反应速率均减小
速率变化 图像 平衡移动方向 新平衡时速率
加压 v(正)、v(逆)同时增大,v′(正)>v′(逆)
正向移动 正、逆反应速率均增大
减压 v(正)、v(逆)同时减小,v′(正)
逆向移动 正、逆反应速率均减小
实验原理
实验
步骤
实验现象 溶液变为 色 溶液不变色 溶液变为 色
实验结论 升高温度,平衡向 方向移动;降低温度,平衡向 方向移动
措施 原因
加入过量的N2 促进平衡 ,提高 的转化率
采用适当的催化剂 反应速率
采用高压 有利于平衡向 移动
采用较高温 同时提高催化剂的活性
将氨液化并及时分离 有利于平衡向 移动
反应速率变化 图像 平衡移动方向 新平衡时速率
升温 v(正)、v(逆)同时增大, v′(正)
移动 正、逆反应速率均增大
降温 v(正)、v(逆)同时减小, v ′(正)
>v′(逆) 正向
移动 正、逆反应速率均减小
化学平衡
体系浓度改变 增大反应物浓度 增大生成物浓度 减小反应物浓度 减小生成物浓度
平衡移动方向 正向移动 逆向移动 逆向移动 正向移动
速率变化 v正先增大,v逆随后增大,且v′正>v′逆 v逆先增大,v正随后增大,且v′逆>v′正 v正先减小,v逆随后减小,且v′逆>v′正 v逆先减小,v正随后减小,且v′正>v′逆
图像
新平衡时速率 正、逆反应速率均增大 正逆反应速率均减小
速率变化 图像 平衡移动方向 新平衡时速率
加压 v(正)、v(逆)同时增大,v′(正)>v′(逆)
正向移动 正、逆反应速率均增大
减压 v(正)、v(逆)同时减小,v′(正)
逆向移动 正、逆反应速率均减小
实验原理
实验
步骤
实验现象 溶液变为 色 溶液不变色 溶液变为 色
实验结论 升高温度,平衡向 方向移动;降低温度,平衡向 方向移动
措施 原因
加入过量的N2 促进平衡 ,提高 的转化率
采用适当的催化剂 反应速率
采用高压 有利于平衡向 移动
采用较高温 同时提高催化剂的活性
将氨液化并及时分离 有利于平衡向 移动
反应速率变化 图像 平衡移动方向 新平衡时速率
升温 v(正)、v(逆)同时增大, v′(正)
降温 v(正)、v(逆)同时减小, v ′(正)
>v′(逆) 正向
移动 正、逆反应速率均减小
