人教版九年级化学 下册 第九单元 课题 1 溶液的形成 课件(共45张PPT)
文档属性
| 名称 | 人教版九年级化学 下册 第九单元 课题 1 溶液的形成 课件(共45张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-31 00:00:00 | ||
图片预览










文档简介
(共45张PPT)
名言欣赏:
对待得失恰似氧化还原,得到会使你的价位降低,而放手却能使你的价位升高。
1、请背诵金属活动顺序表?
2、保护金属资源可以采取哪些措施?
3、常见金属具有哪些物理性质?
温故知新
提出问题
大家喝过咖啡吧?煮咖啡的时候,把咖啡放入杯中,加入适量的水和冰糖,充分溶解,搅匀……
那么,这时的咖啡有什么性质?它是纯净物还是混合物?
课题1 溶液的形成
人教版九年级化学 下册
第九单元 溶 液
目标导航
1.认识溶解现象,知道溶液、溶剂、溶质等概念;
2.知道一些常见的乳化现象;
3.知道溶液是一类重要的物质,在生产和生活中有重要的应用。
自主研学
自主阅读教材,理解教材内容,初步归纳出本节课的知识点,并标注在教材中。
请大家利用5分钟时间:
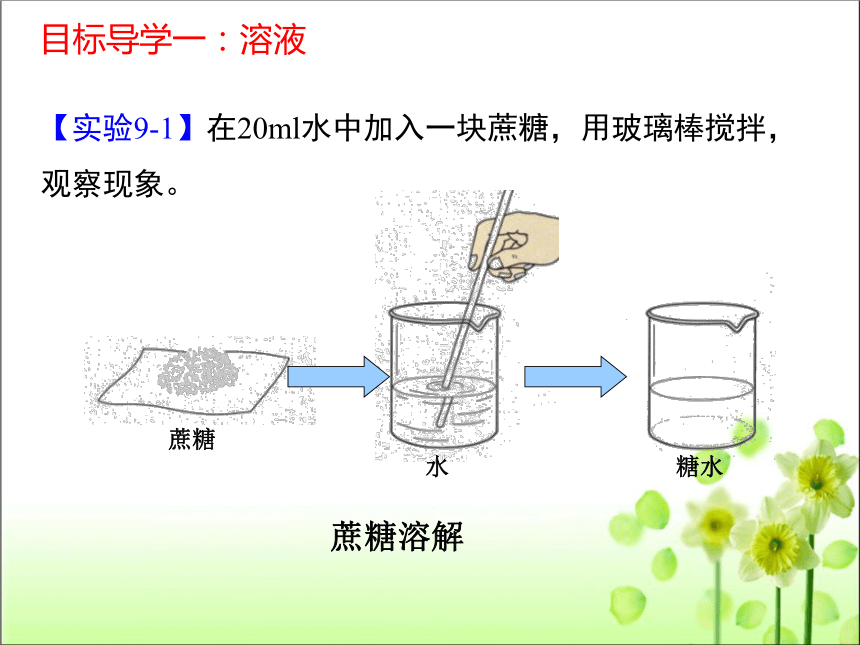
蔗糖溶解
蔗糖
水
糖水
【实验9-1】在20ml水中加入一块蔗糖,用玻璃棒搅拌,观察现象。
目标导学一:溶液
现象
先前液体的味道
搅拌后液体味道
搅拌后的溶液中看不到蔗糖
液体无味
糖水
液体有甜味
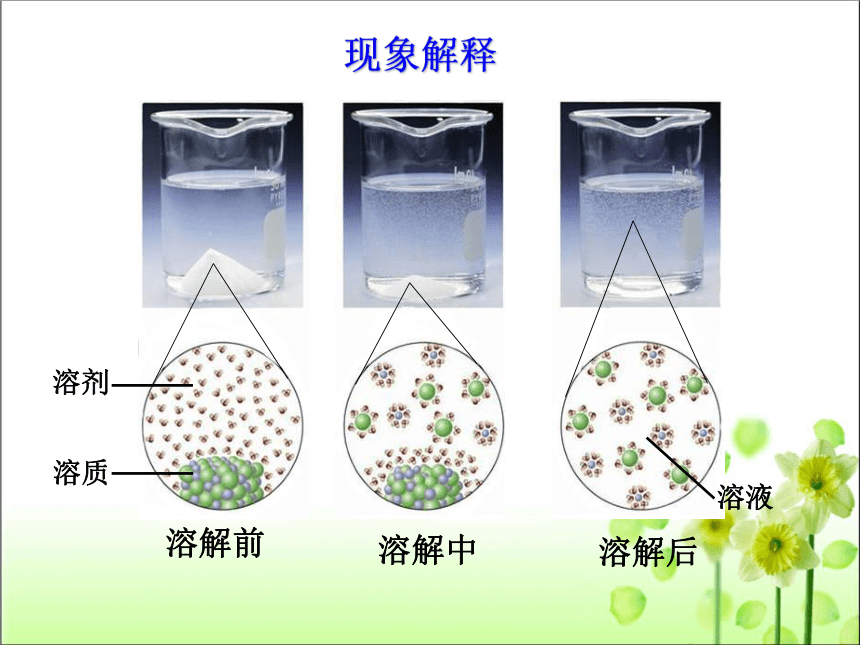
溶解前
溶解中
溶解后
现象解释
溶剂
溶质
溶液
蔗糖与氯化钠两种物质溶解后有什么区别与联系?
区别:蔗糖在水中是以分子形式存在,而氯化钠则是以离子形式存在。
联系:蔗糖和氯化钠溶解后,只要水分不被蒸发,温度不发生变化,蔗糖或氯化钠与水不会分离,取出其中任意一部分进行比较,它们的组成完全相同。
思考
一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物。
2.溶液的特征
1.溶液的定义
均一性、稳定性、透明混合物。
均一性:溶液形成以后,溶液任一部分的组成和性质完全相同(指密度、浓度、性质等)。
透明的混合物:凡是溶液都是透明的混合物。
稳定性:溶液在外界条件(包括温度、压强)不改变的情况下,溶液中的各组成不会发生变化。
透明的混合物,并不是说溶液为无色液体,有的溶液是有颜色的。如硫酸铜溶液为蓝色;氯化亚铁溶液为浅绿色;氯化铁溶液为黄色;高锰酸钾溶液为紫红色。但大多数的溶液为无色液体。
均一、透明、稳定的液体不一定是溶液。
V溶液 V溶质+ V溶剂
m溶液 m溶质+m溶剂
3.溶液的组成
溶液由溶质和溶剂组成。
溶质:被溶解的物质叫溶质。
溶剂:能溶解其它物质的物质叫溶剂。
=
<
溶液的命名:某溶质的某溶剂溶液。如氯化钠的水溶液。
4.溶液、溶质与溶剂之间量的关系
5.溶质和溶剂的确定
E.若有溶液参加的化学反应,反应后的生成物为溶质,水做为溶剂。
B.一般固体或气体溶解于液体中,液体为溶剂。
A.溶质可以是固体、液体和气体。
C.当溶液中有水存在时,不论水量的多少,水都是溶剂。
D.两种液体互溶,溶液中无水存在时,量多的一种叫溶剂,量少的叫溶质。
F.不指明溶剂的溶液,一般指的水溶液。
体系 溶质 溶剂
气 + 液
固 + 液
液 + 液 无水
有水
气体
固体
量少
非水物
液体
液体
量多
水
溶液中溶质和溶剂的确定
1.溶液是无色透明的液体。
2.冰水混合体是溶液。
3.把食盐溶液倒掉一半后,变稀了。
4.在温度不变,水不蒸发的条件下,蔗糖溶液中的蔗糖会从水中分离出来。
5、均一、稳定的液体一定是溶液。
判断:
注意:
1、如果加入的溶质没有完全溶解,那么溶质只是实际溶解的部分。
2、对于任何一种溶液,溶质可以有多种,但溶剂只有一种。
3、当两种物质完全反应后,新生成的物质是溶质,析出的沉淀或逸散的气体不是溶质,如果反应物有剩余,且溶解于水,则剩余物和新生成的物质都是溶质。
想一想
将铁投入一定量的稀硫酸中,直到没有气泡产生,且铁有剩余,所得溶液中溶质为_______溶剂为_______;若铁完全溶解,则溶液中的溶质一定含有_______,可能含有_______
FeSO4
H2SO4
FeSO4
H2O
练习1:烧杯中有100毫升NaCl溶液,请比较A处和B处密度的大小( )
A:?A > ?B B: ?A < ?B
C:?A= ?B D: 不能确定
C
练习2:当水分不蒸发,温度不改变时,KNO3溶液放置一年时间后,KNO3将( )
A:会沉降下来 B:不会分离出来
C:会浮上水面 D:不能确定
B
在硫酸铜溶液、蔗糖溶液、食盐溶液中,溶质是什么?溶剂是什么?
硫酸铜溶液
溶质:硫酸铜
溶剂:水
蔗糖溶液
溶质:蔗糖
溶剂:水
食盐溶液
溶质:食盐
溶剂:水
水能溶解很多物质,是一种最常用的溶剂。
在两支试管中各加入2mL~3mL水,分别加入1~2小粒碘或高锰酸钾;另取两支试管各加入2mL~3mL汽油,再分别加入1~2小粒碘或高锰酸钾。振荡,观察现象。
【实验9-2】 不同的溶质在不同的溶剂中的溶解性
水能溶解所有的物质吗?除了水还有其他的溶剂吗?
溶质 溶剂 现象
碘 水
碘 汽油
高锰酸钾 水
高锰酸钾 汽油
几乎不溶于水
溶解,溶液棕色
溶解,溶液紫色
不溶于汽油
通过上述实验你发现了什么?
相同的溶质在不同的溶剂中溶解性不同
不同的溶质在相同的溶剂中溶解性不同
【实验9-3】 水和乙醇能够互溶吗?
溶剂 溶质 振荡前现象 振荡后现象 静置后现象 结论
水 乙醇
分层
混合均匀
不分层
乙醇与水互溶
注意:乙醇能与水以任意比例互溶
例题 病人在医院接受静脉注射
或滴注时,常用到生理盐水即氯
化钠注射液。如图是某药业公司
生产的氯化钠注射液标签上的部
分文字。请分析标签后回答:
(1)该注射液里的溶质是 ,溶剂是 。
(2)常温下,一瓶合格的氯化钠注射液密封放置一段时间后,是否会出现浑浊?为什么?
氯化钠注射液
[规格] 100ml 0.9g。
[注意]使用前发现溶液中有絮状物、瓶身细微破裂等均不可使用。
[贮藏]密封保存
氯化钠
水
不会,
因为它是溶液,在密封条件下是稳定的。
指出下列溶液中溶质、溶剂各是什么?
溶质 溶剂
(1)硫酸铜溶液
(2)稀硫酸
(3)75%的医用酒精
(4)油脂溶解在汽油里
(5)白磷的二硫化碳溶液
(6)盐酸
(7) CO2溶于水的溶液
CuSO4
水
H2SO4
水
C2H5OH
水
油脂
汽油
白磷
二硫化碳
HCl
水
H2CO3
水
溶液的用途
思考:许多反应在溶液中进行,反应比较快,为什么?
在溶液中反应物接触的更充分,反应的速率快。
现有试管、烧杯、玻璃棒、温度计等仪器和固态NaCl、NH4NO3、NaOH(你还可选用其他仪器和药品),试设计实验方案,探究它们溶解于水时是放出热量还是吸收热量。
1.实验方案:
2.实验简图:
(1)分别向三只烧杯中倒入一定质量的水,然后测出水温
(2)分别将一定量的三种固体放入上述三只烧杯中,搅拌并测出温度
(3)比较前后温度变化
目标导学二:溶解时的吸热或者放热现象
溶解时的吸热或放热现象
水中加入的溶质 NaCl NH4NO3 NaOH
加入溶质前水的温度/℃
溶解现象
加入溶质后水的温度/℃
结论 溶解时
。 溶解时
。 溶解时
。
固体溶解
固体溶解
固体溶解
24
24
24
14
24
56
吸收热量
放出热量
温度不变
活动与探究
衣服和餐具上的油污,用水洗不掉。
为什么在水中加入洗涤剂就能洗掉呢?
目标导学三:乳化现象
探究实验:洗涤剂在清洗油污时起的作用是什么?
分层
分层
振荡时,
不分层
振荡时,
不分层
静置后,
分层
静置后,
不分层
植物油有没有溶解在水中?
没有。这是乳化现象。
乳浊液
1.定义:小液滴分散到液体里形成的混合物。
2.特征:不均一、不稳定
3.乳化现象:洗涤剂有乳化的功能,它能使植物油分散成无数细小的液滴,而不聚集成大的油珠。
用洗发剂洗去头发上的油脂
用洗涤剂洗餐具
用肥皂、洗衣粉洗去衣服上的污渍
乳化原理的应用:
洗衣服(洗衣粉、肥皂);洗头发(洗发露);
洗澡(沐浴露);洗餐具(洗洁精);制农药
1.洗涤剂有什么功能? 它的去污原理是什么?
洗涤剂有乳化功能;洗涤剂的去污原理是:将油污分散成无数小液滴,然后随水流走。(这种现象称为洗涤剂的乳化作用。)
【问题】
2.修汽车的工人,当他的手上沾满油污时,他常用汽油洗去手上的油污。这说明汽油与洗涤剂一样能去油污,那么二者去油污的原理是否相同?若不同,汽油去油污的原理是什么?
汽油去油污的原理是将油污溶解在汽油中,形成溶液,从而除去油污。
一种或几种
物质
另一种物质
分散到
均一稳定的混合物
形成
溶 液
溶剂
被溶解的物质
能溶解其它物质的物质
溶质
固体 液体 气体
水 是 最 常 用 的 溶剂
一、溶液
课堂小结
一种或几种
物质
另一种物质
以小液滴形式分散到
不均一不稳定的混合物
形成
乳浊液
二、溶解时的吸热或放热现象
溶质在溶解的过程中,有的放出热量,有的吸收热量。
乳化剂
乳化现象
三、乳化现象
1、下列液体属于溶液的是___________。(填序号)
①啤酒 ②水 ③泥水 ④澄清石灰水 ⑤盐酸
检测目标
① ④ ⑤
2、某一杯长期放置的食盐水,若上部的密度为a g/cm3,则下部的密度为( )
A、大于a g/cm3
B、等于a g/cm3
C、小于a g/cm3
D、无法判断
B
检测目标
3、下列关于溶液的说法正确的是( )
A.均一、稳定的液体都是溶液
B.溶液是均一、稳定的纯净物
C.溶液是无色透明的液体
D.溶液是均一、稳定的混合物
D
检测目标
4、下列清洗方法中,利用乳化作用的是( )
A.用自来水洗手
B.用汽油清洗油污
C.用清洗剂洗油腻的餐具
D.用盐酸清除铁锈
C
检测目标
5、某同学喝一杯糖开水,第一口与第二口“甜度”相同,这说明溶液是( )
A.混合物 B.澄精的
C.均一的 D.稳定的
C
检测目标
我们已经站在了人生的起跑线上,为了实现心中的远大目标,我们正努力拼搏着。成功属于不畏困难、勇往直前的人。相信自己!
教师寄语
通过本课学习,你收获了什么?
课后作业:
完成教材中的相关练习题。
名言欣赏:
对待得失恰似氧化还原,得到会使你的价位降低,而放手却能使你的价位升高。
1、请背诵金属活动顺序表?
2、保护金属资源可以采取哪些措施?
3、常见金属具有哪些物理性质?
温故知新
提出问题
大家喝过咖啡吧?煮咖啡的时候,把咖啡放入杯中,加入适量的水和冰糖,充分溶解,搅匀……
那么,这时的咖啡有什么性质?它是纯净物还是混合物?
课题1 溶液的形成
人教版九年级化学 下册
第九单元 溶 液
目标导航
1.认识溶解现象,知道溶液、溶剂、溶质等概念;
2.知道一些常见的乳化现象;
3.知道溶液是一类重要的物质,在生产和生活中有重要的应用。
自主研学
自主阅读教材,理解教材内容,初步归纳出本节课的知识点,并标注在教材中。
请大家利用5分钟时间:
蔗糖溶解
蔗糖
水
糖水
【实验9-1】在20ml水中加入一块蔗糖,用玻璃棒搅拌,观察现象。
目标导学一:溶液
现象
先前液体的味道
搅拌后液体味道
搅拌后的溶液中看不到蔗糖
液体无味
糖水
液体有甜味
溶解前
溶解中
溶解后
现象解释
溶剂
溶质
溶液
蔗糖与氯化钠两种物质溶解后有什么区别与联系?
区别:蔗糖在水中是以分子形式存在,而氯化钠则是以离子形式存在。
联系:蔗糖和氯化钠溶解后,只要水分不被蒸发,温度不发生变化,蔗糖或氯化钠与水不会分离,取出其中任意一部分进行比较,它们的组成完全相同。
思考
一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物。
2.溶液的特征
1.溶液的定义
均一性、稳定性、透明混合物。
均一性:溶液形成以后,溶液任一部分的组成和性质完全相同(指密度、浓度、性质等)。
透明的混合物:凡是溶液都是透明的混合物。
稳定性:溶液在外界条件(包括温度、压强)不改变的情况下,溶液中的各组成不会发生变化。
透明的混合物,并不是说溶液为无色液体,有的溶液是有颜色的。如硫酸铜溶液为蓝色;氯化亚铁溶液为浅绿色;氯化铁溶液为黄色;高锰酸钾溶液为紫红色。但大多数的溶液为无色液体。
均一、透明、稳定的液体不一定是溶液。
V溶液 V溶质+ V溶剂
m溶液 m溶质+m溶剂
3.溶液的组成
溶液由溶质和溶剂组成。
溶质:被溶解的物质叫溶质。
溶剂:能溶解其它物质的物质叫溶剂。
=
<
溶液的命名:某溶质的某溶剂溶液。如氯化钠的水溶液。
4.溶液、溶质与溶剂之间量的关系
5.溶质和溶剂的确定
E.若有溶液参加的化学反应,反应后的生成物为溶质,水做为溶剂。
B.一般固体或气体溶解于液体中,液体为溶剂。
A.溶质可以是固体、液体和气体。
C.当溶液中有水存在时,不论水量的多少,水都是溶剂。
D.两种液体互溶,溶液中无水存在时,量多的一种叫溶剂,量少的叫溶质。
F.不指明溶剂的溶液,一般指的水溶液。
体系 溶质 溶剂
气 + 液
固 + 液
液 + 液 无水
有水
气体
固体
量少
非水物
液体
液体
量多
水
溶液中溶质和溶剂的确定
1.溶液是无色透明的液体。
2.冰水混合体是溶液。
3.把食盐溶液倒掉一半后,变稀了。
4.在温度不变,水不蒸发的条件下,蔗糖溶液中的蔗糖会从水中分离出来。
5、均一、稳定的液体一定是溶液。
判断:
注意:
1、如果加入的溶质没有完全溶解,那么溶质只是实际溶解的部分。
2、对于任何一种溶液,溶质可以有多种,但溶剂只有一种。
3、当两种物质完全反应后,新生成的物质是溶质,析出的沉淀或逸散的气体不是溶质,如果反应物有剩余,且溶解于水,则剩余物和新生成的物质都是溶质。
想一想
将铁投入一定量的稀硫酸中,直到没有气泡产生,且铁有剩余,所得溶液中溶质为_______溶剂为_______;若铁完全溶解,则溶液中的溶质一定含有_______,可能含有_______
FeSO4
H2SO4
FeSO4
H2O
练习1:烧杯中有100毫升NaCl溶液,请比较A处和B处密度的大小( )
A:?A > ?B B: ?A < ?B
C:?A= ?B D: 不能确定
C
练习2:当水分不蒸发,温度不改变时,KNO3溶液放置一年时间后,KNO3将( )
A:会沉降下来 B:不会分离出来
C:会浮上水面 D:不能确定
B
在硫酸铜溶液、蔗糖溶液、食盐溶液中,溶质是什么?溶剂是什么?
硫酸铜溶液
溶质:硫酸铜
溶剂:水
蔗糖溶液
溶质:蔗糖
溶剂:水
食盐溶液
溶质:食盐
溶剂:水
水能溶解很多物质,是一种最常用的溶剂。
在两支试管中各加入2mL~3mL水,分别加入1~2小粒碘或高锰酸钾;另取两支试管各加入2mL~3mL汽油,再分别加入1~2小粒碘或高锰酸钾。振荡,观察现象。
【实验9-2】 不同的溶质在不同的溶剂中的溶解性
水能溶解所有的物质吗?除了水还有其他的溶剂吗?
溶质 溶剂 现象
碘 水
碘 汽油
高锰酸钾 水
高锰酸钾 汽油
几乎不溶于水
溶解,溶液棕色
溶解,溶液紫色
不溶于汽油
通过上述实验你发现了什么?
相同的溶质在不同的溶剂中溶解性不同
不同的溶质在相同的溶剂中溶解性不同
【实验9-3】 水和乙醇能够互溶吗?
溶剂 溶质 振荡前现象 振荡后现象 静置后现象 结论
水 乙醇
分层
混合均匀
不分层
乙醇与水互溶
注意:乙醇能与水以任意比例互溶
例题 病人在医院接受静脉注射
或滴注时,常用到生理盐水即氯
化钠注射液。如图是某药业公司
生产的氯化钠注射液标签上的部
分文字。请分析标签后回答:
(1)该注射液里的溶质是 ,溶剂是 。
(2)常温下,一瓶合格的氯化钠注射液密封放置一段时间后,是否会出现浑浊?为什么?
氯化钠注射液
[规格] 100ml 0.9g。
[注意]使用前发现溶液中有絮状物、瓶身细微破裂等均不可使用。
[贮藏]密封保存
氯化钠
水
不会,
因为它是溶液,在密封条件下是稳定的。
指出下列溶液中溶质、溶剂各是什么?
溶质 溶剂
(1)硫酸铜溶液
(2)稀硫酸
(3)75%的医用酒精
(4)油脂溶解在汽油里
(5)白磷的二硫化碳溶液
(6)盐酸
(7) CO2溶于水的溶液
CuSO4
水
H2SO4
水
C2H5OH
水
油脂
汽油
白磷
二硫化碳
HCl
水
H2CO3
水
溶液的用途
思考:许多反应在溶液中进行,反应比较快,为什么?
在溶液中反应物接触的更充分,反应的速率快。
现有试管、烧杯、玻璃棒、温度计等仪器和固态NaCl、NH4NO3、NaOH(你还可选用其他仪器和药品),试设计实验方案,探究它们溶解于水时是放出热量还是吸收热量。
1.实验方案:
2.实验简图:
(1)分别向三只烧杯中倒入一定质量的水,然后测出水温
(2)分别将一定量的三种固体放入上述三只烧杯中,搅拌并测出温度
(3)比较前后温度变化
目标导学二:溶解时的吸热或者放热现象
溶解时的吸热或放热现象
水中加入的溶质 NaCl NH4NO3 NaOH
加入溶质前水的温度/℃
溶解现象
加入溶质后水的温度/℃
结论 溶解时
。 溶解时
。 溶解时
。
固体溶解
固体溶解
固体溶解
24
24
24
14
24
56
吸收热量
放出热量
温度不变
活动与探究
衣服和餐具上的油污,用水洗不掉。
为什么在水中加入洗涤剂就能洗掉呢?
目标导学三:乳化现象
探究实验:洗涤剂在清洗油污时起的作用是什么?
分层
分层
振荡时,
不分层
振荡时,
不分层
静置后,
分层
静置后,
不分层
植物油有没有溶解在水中?
没有。这是乳化现象。
乳浊液
1.定义:小液滴分散到液体里形成的混合物。
2.特征:不均一、不稳定
3.乳化现象:洗涤剂有乳化的功能,它能使植物油分散成无数细小的液滴,而不聚集成大的油珠。
用洗发剂洗去头发上的油脂
用洗涤剂洗餐具
用肥皂、洗衣粉洗去衣服上的污渍
乳化原理的应用:
洗衣服(洗衣粉、肥皂);洗头发(洗发露);
洗澡(沐浴露);洗餐具(洗洁精);制农药
1.洗涤剂有什么功能? 它的去污原理是什么?
洗涤剂有乳化功能;洗涤剂的去污原理是:将油污分散成无数小液滴,然后随水流走。(这种现象称为洗涤剂的乳化作用。)
【问题】
2.修汽车的工人,当他的手上沾满油污时,他常用汽油洗去手上的油污。这说明汽油与洗涤剂一样能去油污,那么二者去油污的原理是否相同?若不同,汽油去油污的原理是什么?
汽油去油污的原理是将油污溶解在汽油中,形成溶液,从而除去油污。
一种或几种
物质
另一种物质
分散到
均一稳定的混合物
形成
溶 液
溶剂
被溶解的物质
能溶解其它物质的物质
溶质
固体 液体 气体
水 是 最 常 用 的 溶剂
一、溶液
课堂小结
一种或几种
物质
另一种物质
以小液滴形式分散到
不均一不稳定的混合物
形成
乳浊液
二、溶解时的吸热或放热现象
溶质在溶解的过程中,有的放出热量,有的吸收热量。
乳化剂
乳化现象
三、乳化现象
1、下列液体属于溶液的是___________。(填序号)
①啤酒 ②水 ③泥水 ④澄清石灰水 ⑤盐酸
检测目标
① ④ ⑤
2、某一杯长期放置的食盐水,若上部的密度为a g/cm3,则下部的密度为( )
A、大于a g/cm3
B、等于a g/cm3
C、小于a g/cm3
D、无法判断
B
检测目标
3、下列关于溶液的说法正确的是( )
A.均一、稳定的液体都是溶液
B.溶液是均一、稳定的纯净物
C.溶液是无色透明的液体
D.溶液是均一、稳定的混合物
D
检测目标
4、下列清洗方法中,利用乳化作用的是( )
A.用自来水洗手
B.用汽油清洗油污
C.用清洗剂洗油腻的餐具
D.用盐酸清除铁锈
C
检测目标
5、某同学喝一杯糖开水,第一口与第二口“甜度”相同,这说明溶液是( )
A.混合物 B.澄精的
C.均一的 D.稳定的
C
检测目标
我们已经站在了人生的起跑线上,为了实现心中的远大目标,我们正努力拼搏着。成功属于不畏困难、勇往直前的人。相信自己!
教师寄语
通过本课学习,你收获了什么?
课后作业:
完成教材中的相关练习题。
同课章节目录
