人教版 高二化学选修五第三章第二节醛(共26张PPT)
文档属性
| 名称 | 人教版 高二化学选修五第三章第二节醛(共26张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-03-30 00:00:00 | ||
图片预览





文档简介
(共26张PPT)
根据醇类催化氧化反应的原理,
完成下列方程式
醇类发生催化氧化的条件是什么?
1.Ag或Cu作催化剂并加热。
2.羟基所连的碳原子上有氢原子。
2CH3CHO+2H2O
第二节 醛
第三章 烃的含氧衍生物
五华县高级中学 曾丽敏
学习目标
1、理解醛的概念、结构特点和分类
2、掌握甲醛、乙醛的物理性质、化学
性质及化学方程式的书写
3、掌握醛类物质的银镜反应和新制氢氧
化铜悬浊液反应的量的关系
自学指导(阅读书56页完成下列问题)
1、概念
醛的定义:________________________
官能团:________
2、常见醛的物理性质
从结构上看,由烃基(或氢原子)跟醛基(— CHO)相连而成的化合物叫醛。
— CHO
HCHO
CH3CHO
无色气态
无色液态
刺激性
气味
刺激性
气味
易溶于水,35%~40%的甲醛水溶液又称
与水、乙醇等
互溶
如何分离提纯乙醛?
一、 醛的物理性质
物质名称 结构简式 颜色状态 气味 溶解性
甲醛
乙醛
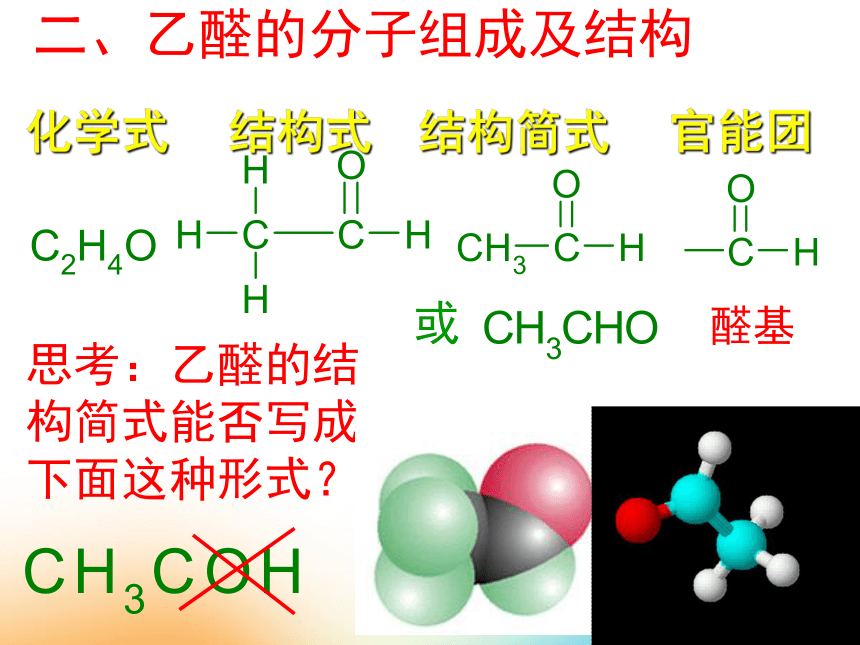
二、乙醛的分子组成及结构
化学式
结构式
结构简式
官能团
思考:乙醛的结构简式能否写成下面这种形式?
或
醛基
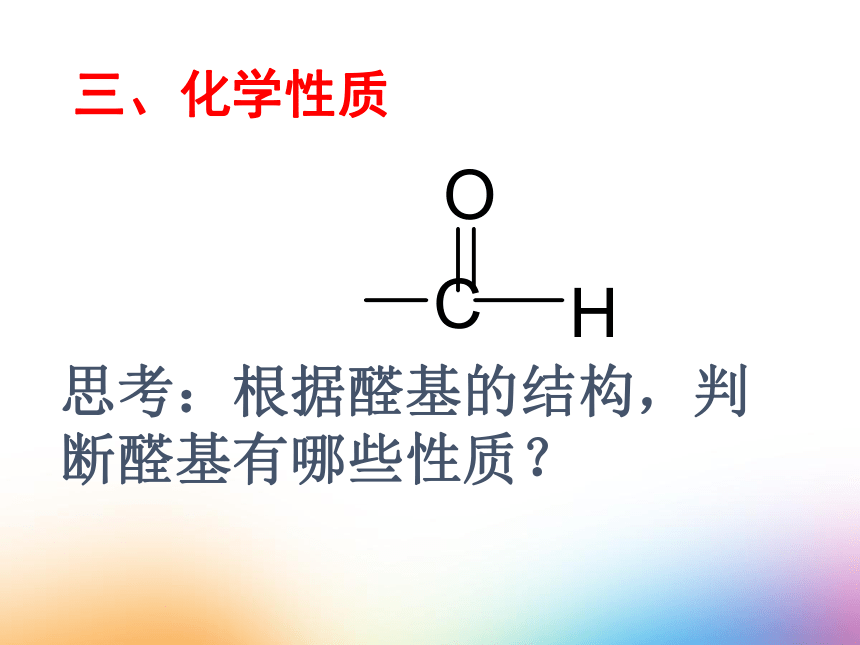
思考:根据醛基的结构,判断醛基有哪些性质?
三、化学性质
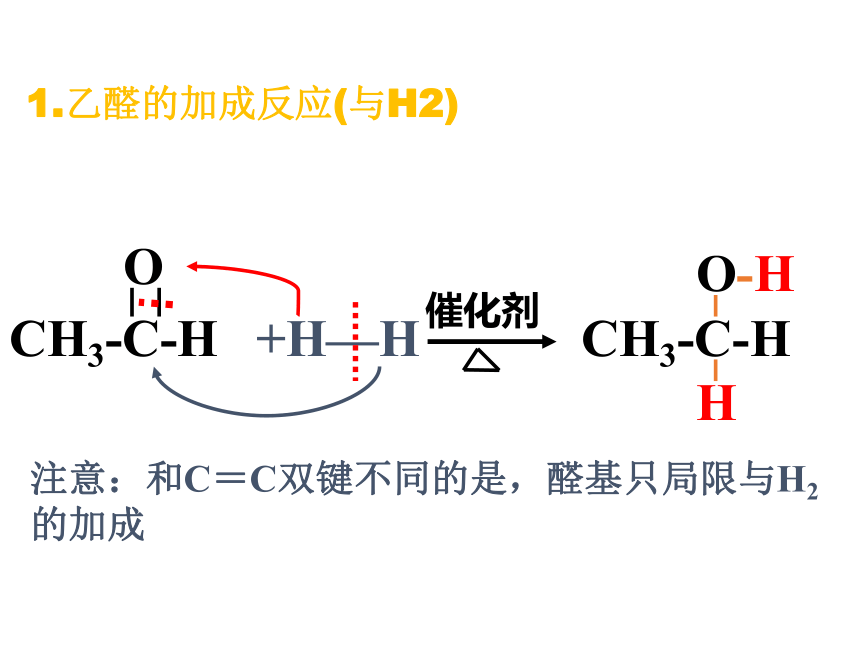
+H—H
注意:和C=C双键不同的是,醛基只局限与H2的加成
1.乙醛的加成反应(与H2)
乙醛
(加H)
乙醇
(去H)
氧化(加O)
乙酸
有机物加O或去H, 发生氧化反应
有机物去O或加H, 发生还原反应
CH3-C_
O
— H
O
①燃烧
②催化氧化
工业制羧酸的主要方法!
2. 氧化反应
2. 氧化反应
1)与银氨溶液
2)与新制Cu(OH)2
③
1)与银氨溶液
现象 :
试管内壁上附上了一层光亮如镜的银
沉淀恰好消失
银氨
溶液
静置加热
银镜
实验成功的关键:
a、洁净的试管。如有油污,得不到光亮的银镜而是黑色沉淀。
b、银氨溶液的配制(现用现制)
且氨水不能过量,否则生成易爆炸的物质
AgNO3 + NH3·H2O = AgOH↓+ NH4NO3
AgOH + 2NH3·H2O = Ag(NH3)2OH + 2H2O
C、温和的水浴加热 且加热时不能振荡
实验后,银镜用HNO3浸泡,再用水洗
银镜反应
a、此反应可用于醛基的检验
说明:a、生成物:一水、二银、三氨、乙酸铵
b、1mol-CHO~2molAg
b、工业上利用此原理制镜和保温瓶胆
应用:
2)与新制Cu(OH)2
4滴~6滴
NaOH溶液
2 ml
CuSO4溶液
新制Cu(OH)2
现象 :
试管内有红色沉淀产生。
实验成功的关键:
a Cu(OH)2必须新制
b NaOH必须过量
C 酒精灯加热煮沸
说明:
1mol醛基 ~1mol Cu2O
应用:
a.检验醛基的存在
b. 医院里,利用这一反应原理检查尿糖是否正常(检查葡萄糖的醛基)
乙醛能使酸性KMnO4溶液和溴水褪色吗?
乙醛使溴水褪色的原因:乙醛被溴水氧化。
能使液溴褪色么?
上的 反应,
在C-H之间插入O
结构分析
结构决定性质
归纳·总结
氧化
加成反应
还原反应
与H2
乙醛
还原(加H)
乙醇
氧化(失H)
氧化(加O)
乙酸
乙醛性质的小结:
1、加成反应
2、氧化反应
⑴燃烧
⑵催化氧化
⑶被弱氧化剂氧化
(银氨溶液、新制的Cu(OH)2)
乙酸
⑷使酸性高锰酸钾溶液、溴水褪色
CO2 + H2O
醛类
醛类物质结构的通式:
饱和一元脂肪醛的分子式的通式:CnH2nO(n≥1)
R—若为烷基则为饱和一元脂肪醛
烃基
1、一定量的某饱和一元醛发生银镜反应,
析出银21.6g,等量的此醛完全燃烧时生成CO2 8.96L,则此醛是( )
A、乙醛 B、丙醛
C、丁醛 D、2-甲基丙醛
2、写出甲醛发生银镜反应,以及与新制Cu(OH)2反应的化学方程式。
即:H2CO3
注意:甲醛分子中相当于含有2个醛基,1mol醛反应最多可生成4molAg或2molCu2O。
3、有机物结构简式为
下列对其性质的判断中,不正确的是( )
A.能被银氨溶液氧化
B.能使KMnO4酸性溶液褪色
C.1mol该有机物只能与1molBr2发生加成反应
D.1mol该有机物只能与1molH2发生加成反应
D
根据醇类催化氧化反应的原理,
完成下列方程式
醇类发生催化氧化的条件是什么?
1.Ag或Cu作催化剂并加热。
2.羟基所连的碳原子上有氢原子。
2CH3CHO+2H2O
第二节 醛
第三章 烃的含氧衍生物
五华县高级中学 曾丽敏
学习目标
1、理解醛的概念、结构特点和分类
2、掌握甲醛、乙醛的物理性质、化学
性质及化学方程式的书写
3、掌握醛类物质的银镜反应和新制氢氧
化铜悬浊液反应的量的关系
自学指导(阅读书56页完成下列问题)
1、概念
醛的定义:________________________
官能团:________
2、常见醛的物理性质
从结构上看,由烃基(或氢原子)跟醛基(— CHO)相连而成的化合物叫醛。
— CHO
HCHO
CH3CHO
无色气态
无色液态
刺激性
气味
刺激性
气味
易溶于水,35%~40%的甲醛水溶液又称
与水、乙醇等
互溶
如何分离提纯乙醛?
一、 醛的物理性质
物质名称 结构简式 颜色状态 气味 溶解性
甲醛
乙醛
二、乙醛的分子组成及结构
化学式
结构式
结构简式
官能团
思考:乙醛的结构简式能否写成下面这种形式?
或
醛基
思考:根据醛基的结构,判断醛基有哪些性质?
三、化学性质
+H—H
注意:和C=C双键不同的是,醛基只局限与H2的加成
1.乙醛的加成反应(与H2)
乙醛
(加H)
乙醇
(去H)
氧化(加O)
乙酸
有机物加O或去H, 发生氧化反应
有机物去O或加H, 发生还原反应
CH3-C_
O
— H
O
①燃烧
②催化氧化
工业制羧酸的主要方法!
2. 氧化反应
2. 氧化反应
1)与银氨溶液
2)与新制Cu(OH)2
③
1)与银氨溶液
现象 :
试管内壁上附上了一层光亮如镜的银
沉淀恰好消失
银氨
溶液
静置加热
银镜
实验成功的关键:
a、洁净的试管。如有油污,得不到光亮的银镜而是黑色沉淀。
b、银氨溶液的配制(现用现制)
且氨水不能过量,否则生成易爆炸的物质
AgNO3 + NH3·H2O = AgOH↓+ NH4NO3
AgOH + 2NH3·H2O = Ag(NH3)2OH + 2H2O
C、温和的水浴加热 且加热时不能振荡
实验后,银镜用HNO3浸泡,再用水洗
银镜反应
a、此反应可用于醛基的检验
说明:a、生成物:一水、二银、三氨、乙酸铵
b、1mol-CHO~2molAg
b、工业上利用此原理制镜和保温瓶胆
应用:
2)与新制Cu(OH)2
4滴~6滴
NaOH溶液
2 ml
CuSO4溶液
新制Cu(OH)2
现象 :
试管内有红色沉淀产生。
实验成功的关键:
a Cu(OH)2必须新制
b NaOH必须过量
C 酒精灯加热煮沸
说明:
1mol醛基 ~1mol Cu2O
应用:
a.检验醛基的存在
b. 医院里,利用这一反应原理检查尿糖是否正常(检查葡萄糖的醛基)
乙醛能使酸性KMnO4溶液和溴水褪色吗?
乙醛使溴水褪色的原因:乙醛被溴水氧化。
能使液溴褪色么?
上的 反应,
在C-H之间插入O
结构分析
结构决定性质
归纳·总结
氧化
加成反应
还原反应
与H2
乙醛
还原(加H)
乙醇
氧化(失H)
氧化(加O)
乙酸
乙醛性质的小结:
1、加成反应
2、氧化反应
⑴燃烧
⑵催化氧化
⑶被弱氧化剂氧化
(银氨溶液、新制的Cu(OH)2)
乙酸
⑷使酸性高锰酸钾溶液、溴水褪色
CO2 + H2O
醛类
醛类物质结构的通式:
饱和一元脂肪醛的分子式的通式:CnH2nO(n≥1)
R—若为烷基则为饱和一元脂肪醛
烃基
1、一定量的某饱和一元醛发生银镜反应,
析出银21.6g,等量的此醛完全燃烧时生成CO2 8.96L,则此醛是( )
A、乙醛 B、丙醛
C、丁醛 D、2-甲基丙醛
2、写出甲醛发生银镜反应,以及与新制Cu(OH)2反应的化学方程式。
即:H2CO3
注意:甲醛分子中相当于含有2个醛基,1mol醛反应最多可生成4molAg或2molCu2O。
3、有机物结构简式为
下列对其性质的判断中,不正确的是( )
A.能被银氨溶液氧化
B.能使KMnO4酸性溶液褪色
C.1mol该有机物只能与1molBr2发生加成反应
D.1mol该有机物只能与1molH2发生加成反应
D
