人教版九年级化学 10.2 酸和碱的中和反应 同步练习 有答案
文档属性
| 名称 | 人教版九年级化学 10.2 酸和碱的中和反应 同步练习 有答案 |

|
|
| 格式 | zip | ||
| 文件大小 | 52.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-04-02 00:00:00 | ||
图片预览


文档简介
10.2 酸和碱的中和反应
一 选择题
1.一些国家正在使用碳酸水浇灌某些植物,这样做不能起到的作用是( )
A.改良碱性土壤 B.促进植物的光合作用
C.改良酸性土壤 D.提高农作物产量
2.下列关于中和反应的说法,正确的是( )
A.纯碱和稀盐酸混合后发生中和反应
B.有盐和水生成的反应一定是中和反应
C.工厂废水中含有的硫酸可以用熟石灰中和
D.中和反应的发生必须借助酸碱指示剂进行判断
3.下列物质溶于水后,所得溶液的pH< 7的是( )
A. Ca(OH)2 B. NaOH C. SO3 D. CaO
4.质量相等,质量分数相等的氢氧化钠溶液和稀盐酸相互混合所得溶液的pH是( )
A.等于7 B.大于7 C.小于7 D.无法判断?
5.下图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论正确的是( )
A.反应后溶液的pH大于7
B.反应前的溶液均可导电,反应后的溶液不导电
C.反应后溶液中存在的粒子只有Na+和Cl―
D.反应前后所有元素的化合价均无变化
6.下列反应,要借助酸碱指示剂才能判断二者是否发生反应的是( )
A. 大理石和稀盐酸 B. 石灰水和稀盐酸 C. 铁锈和稀硫酸 D. 镁和稀硫酸
7.下列说法中正确的( )
A. 碱类物质一定能使酚酞试液变红
B. 有盐和水生成的反应不一定是中和反应
C. 酸雨就是指呈酸性的雨水
D. pH=0的溶液既不显酸性,也不显碱性,呈中性
8.某同学实验时记录的实验现象,其中正确的是( )
A.向滴有酚酞的氢氧化钠溶液中滴加盐酸,溶液由无色逐渐变成红色
B.红磷在空气中燃烧,发出红色的火焰,产生大量白色烟雾
C.大理石上滴加稀盐酸,大理石表面有气泡冒出
D.硫酸铜溶液中滴加氢氧化钠溶液,产生白色沉淀
9.pH是水质监测的重要指标之一,下列水样酸性最强的是( )
A. pH=1.3的工业废水 B. pH=4.5的雨水
C. pH=7.0的蒸馏水 D. pH=7.3的矿泉水
10.生活中一些物质的pH如下表所示,其中显碱性的是( )
A.柠檬 B.糖水 C.牙膏 D.牛奶
二 非选择题
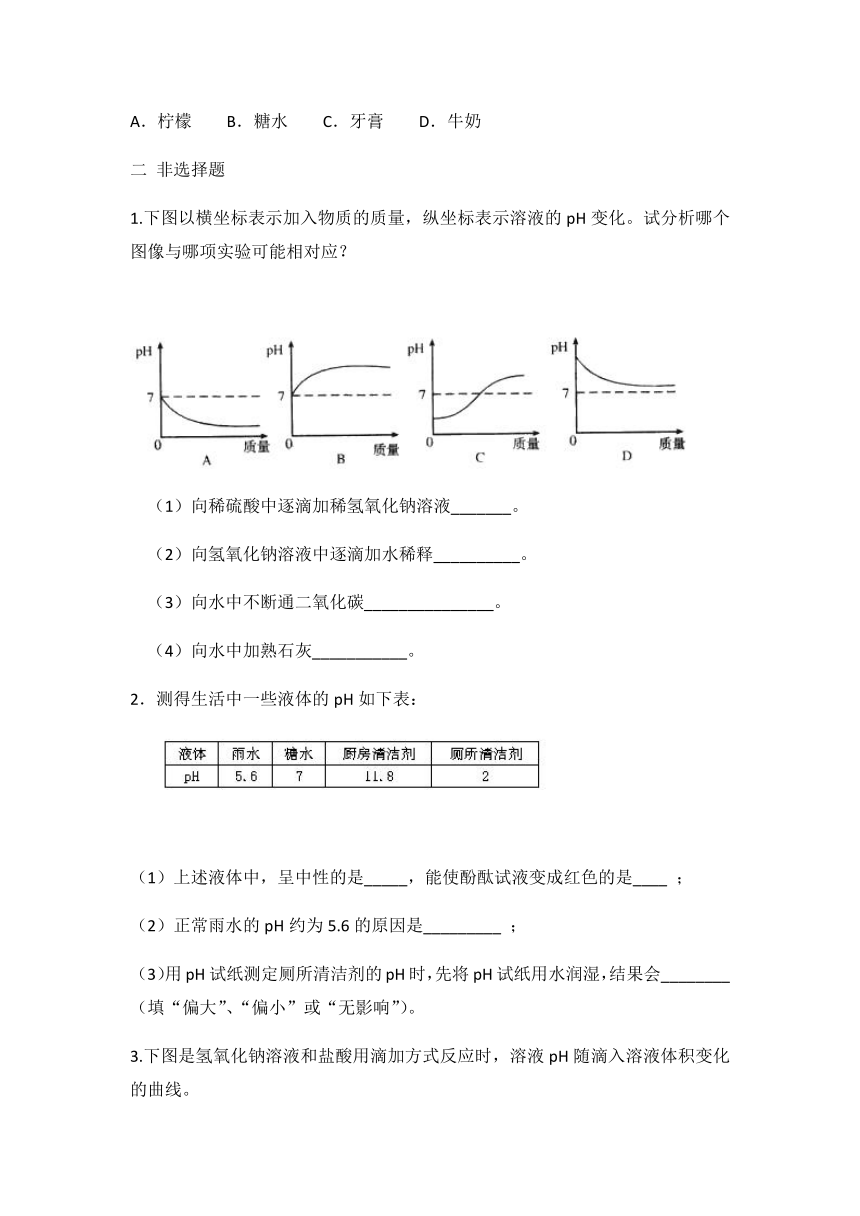
1.下图以横坐标表示加入物质的质量,纵坐标表示溶液的pH变化。试分析哪个图像与哪项实验可能相对应?
(1)向稀硫酸中逐滴加稀氢氧化钠溶液_______。
(2)向氢氧化钠溶液中逐滴加水稀释__________。
(3)向水中不断通二氧化碳_______________。
(4)向水中加熟石灰___________。
2.测得生活中一些液体的pH如下表:
(1)上述液体中,呈中性的是_____,能使酚酞试液变成红色的是____ ;
(2)正常雨水的pH约为5.6的原因是_________ ;
(3)用pH试纸测定厕所清洁剂的pH时,先将pH试纸用水润湿,结果会________ (填“偏大”、“偏小”或“无影响”)。
3.下图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。
(1)氢氧化钠和盐酸恰好完全反应时,溶液的pH_____ 7(填“大于”或“小于”或“等于”)。
(2)根据曲线判断,该反应是将______(填“氢氧化钠溶液”或“盐酸”,下同)滴入_________中,理由是________。
(3)当滴入溶液的体积为5mL时,所得溶液中的溶质为_____写化学式),若在此溶液中滴入石蕊试液,溶液显_____________色。
4.氢氧化钠与硫酸的反应无明显现象,某化学兴趣小组为证明氢氧化钠与硫酸发生了化学反应,进行了如下的实验探究。
【实验探究】小倩在试管中加入约2mL稀氢氧化钠溶液,滴入2滴酚酞溶液,振荡,
溶液变为红色。然后向该试管中倒入稀硫酸,观察到溶液由红色变为无
色,证明氢氧化钠与硫酸发生了反应,该反应的化学方程式为_______ 。
【改进实验】小娜使用与小倩相同的试剂,通过改进上述实验中某一步的操作方法,不但证明氢氧化钠与硫酸发生了反应,还能验证二者恰好完全反应。小娜改进的实验操作中关键的一点是___________ 。
【反思评价】小霞提出也可以使用紫色石蕊溶液代替无色酚酞溶液进行上述实验。你认为___________ (填“酚酞溶液”或“石蕊溶液”)更适合用于验证二者恰好完全反应,你的理由是__________。
【拓展延伸】不是所有的碱与硫酸反应都无明显现象,例如______ (填一种碱)与硫酸反应就有明显的实验现象。
5.实验室欲测定一瓶标签破损的H2SO4的溶质质量分数。现取10g该稀硫酸样品,将5%的NaOH溶液逐渐滴加到样品中,边加边搅拌,随着氢氧化钠溶液的不断加人,溶液的PH的变化如图所示。请回答:
(1)a点溶液中含有的离子有 。
(2)当PH=7时,消耗的氢氧化钠溶液中的氢氧化钠的质量为_____ g。
(3)计算稀硫酸的溶质质量分数。
参考答案
一 选择题
CCCCD BBCAC
二 非选择题
1.(1)C (2)D (3)A (4)B
2(1)糖水 厨房清洁剂 (2)水中溶解了二氧化碳生成碳酸(或二氧化碳与水反应生成碳酸)(3)偏大.
3.(1)= (2)氢氧化钠溶液 盐酸 随着滴入溶液的增加,溶液的pH增大(3)NaCl HCl 红
4.(1)= (2)氢氧化钠溶液 盐酸 随着滴入溶液的增加,溶液的pH增大(3)NaCl HCl 红
5.(1)Na+ 、H+ 、SO42-
(2)16g×5%=0.8g
(3)解:设10g稀硫酸样品中含有H2SO4的质量为x
H2SO4 + 2NaOH=Na2SO4 + 2H2O
98 80
x 0.8g
98:80=x:0.8g x=0.98g
稀硫酸的溶质质量分数:0.98g/10g×100%=9.8%
同课章节目录
