鲁教版化学九年级下册第八单元《海水中的化学》测试题(含答案)
文档属性
| 名称 | 鲁教版化学九年级下册第八单元《海水中的化学》测试题(含答案) |
|
|
| 格式 | zip | ||
| 文件大小 | 279.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-04-02 00:00:00 | ||
图片预览





文档简介
第八单元《海水中的化学》测试题
一、单选题(每小题只有一个正确答案)
1.现有20℃时200g硝酸钾饱和溶液,以下操作中,溶质与溶剂的质量比发生变化的是( )
A.温度不变蒸发掉20g水 B.温度不变加入10g硝酸钾
C.温度不变加入20g水 D.升温到40℃
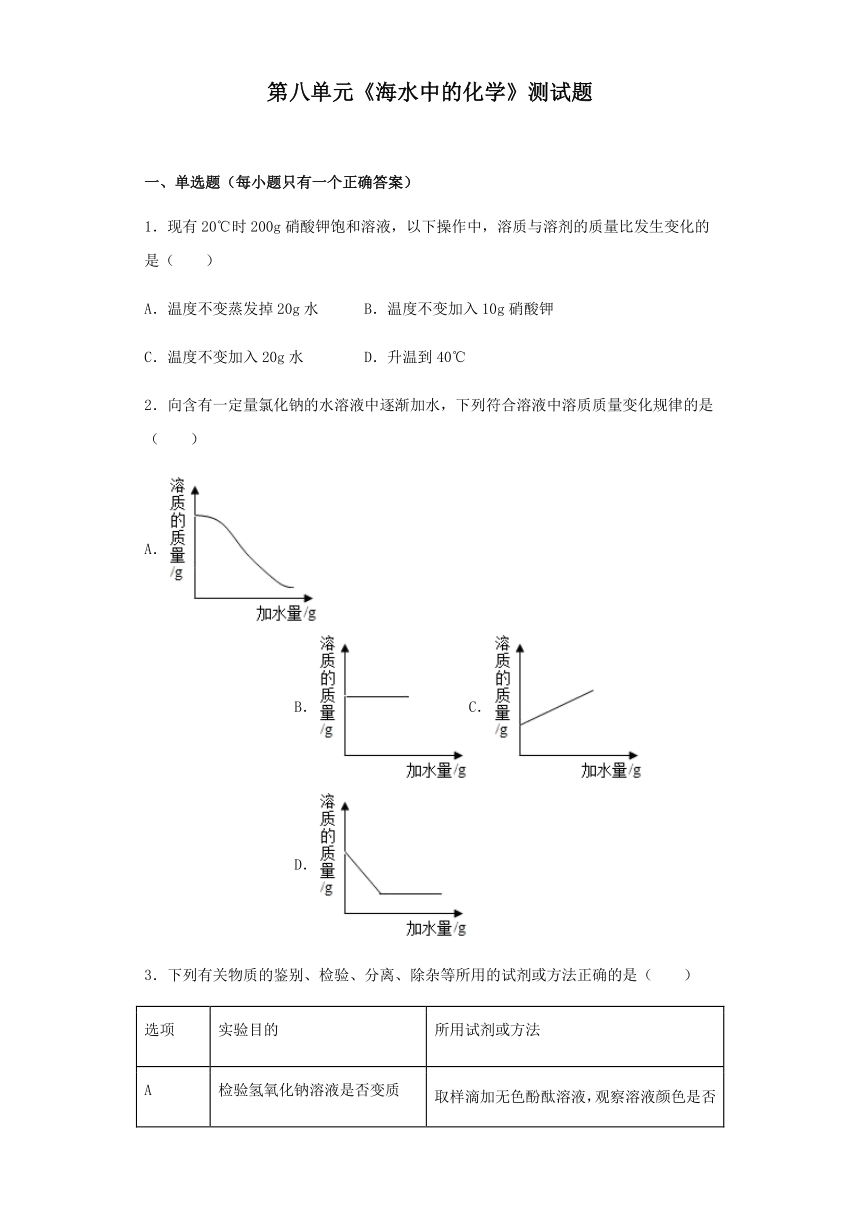
2.向含有一定量氯化钠的水溶液中逐渐加水,下列符合溶液中溶质质量变化规律的是( )
A. B.C. D.
3.下列有关物质的鉴别、检验、分离、除杂等所用的试剂或方法正确的是( )
选项 实验目的 所用试剂或方法
A 检验氢氧化钠溶液是否变质 取样滴加无色酚酞溶液,观察溶液颜色是否变红
B 除去氯化钠溶液中的硫酸铜 加入适量氢氧化钠溶液,过滤
C 除去硫酸钠溶液中的碳酸钠 加入适量稀硫酸溶液
D 鉴别硫酸钠溶液和硝酸银溶液 取样分别滴加氯化钡溶液,观察现象
A.A B.B C.C D.D
4.下列说法正确的是( )
A.大理石可用作补钙剂 B.正常雨水的pH约为7
C.餐具上的油污可用洗涤剂清洗 D.碱性的洗发液不会损伤头发
5.下列各组物质的俗称、化学式,用途不一致的是( )
A.生石灰 CaO 做干燥剂 B.纯碱 NaOH 治疗胃酸过多
C.小苏打 NaHCO3发酵粉主要成分之一 D.干冰 CO2人工降雨
6.下列实验现象描述正确的是( )
A.磷在空气中燃烧产生大量的白雾
B.镁条在空气中燃烧生成氧化镁
C.硫在空气中燃烧发出蓝紫色火焰,生成有刺激性气味的气体
D.铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
7.根据化学知识和生活经验判断,下列说法不正确的是
A.氧气能支持燃烧,具有助燃性 B.“真金不怕火来炼”是因为金的熔点很高
C.玻璃、聚酯塑料都是透明材料 D.进入菜窖要先检验窖内CO2浓度是否有害
8.甲、乙物质的溶解度曲线如图,下列叙述正确的是 ( )
A.甲、乙两种物质都属于微溶性物质
B.t1℃时,甲、乙溶液恒温蒸发等质量的水时,甲、乙析出固体质量相等
C.甲中含有少量乙时,可用蒸发结晶的方法得到乙
D.t2℃时,分别取100g甲、乙物质的饱和溶液,将其降温至t1℃时,所得溶液质量甲小于乙
9.利用溶解度曲线,可以获得许多有关物质溶解度的信息。下图是a、b两物质的溶解度曲线。有关叙述正确的是
A.a的溶解度大于b的溶解度
B.当a物质中混有少量b物质时,可以用蒸发结晶的方法除去b
C.10℃时,取相同质量的a、b两物质分别配成饱和溶液所需水的质量是a大于b
D.将t℃时a、b的饱和溶液升温至40℃,其溶液中溶质的质量分数为a大于b
10.分析下面实验内容和结论,正确的一组是( )
实验内容
实验结论
A
带有火星的木条置于氧气瓶中,木条复燃
氧气有可燃性
B
二氧化碳气体通入紫色石蕊试液中,石蕊试液变红色
二氧化碳有酸性
C
稀盐酸滴入氢氧化钠溶液中,未观察到明显现象
二者没有发生化学变化
D
氯化钙溶液滴入某溶液中,出现白色沉淀
溶液中可能含有CO32-
A.A B.B C.C D.D
11.小苏打(NaHCO3)是焙制糕点所用的发酵粉的主要成分之一,NaHCO3属于
A.酸 B.碱 C.盐 D.有机物
12.把60℃的饱和硝酸钾溶液降温到20℃,下列说法中正确的是
①溶液的质量不变 ②溶质的质量不变 ③溶剂的质量不变 ④仍是饱和状态
A.①和② B.③和④ C.①和③ D.②和④
13.下列各组离子在水中能大量共存的是
A.K+、Ca2+、NO3 、CO32- B.H+、Na+、HCO3- 、SO42-
C.Ba2+、Cu2+、Cl-、NO3- D.Na+、NH4+、Cl-、OH-
14.下列关于甲、乙两种物质溶解度曲线的说法中正确的是
A.甲的溶解度大于乙的溶解度
B.t1℃时,50g甲的饱和溶液中有15g甲
C.t2℃时乙的不饱和溶液降温至t1℃变为饱和溶液
D.甲中含有少量乙时,可以采用冷却热饱和溶液的方法除去乙
15.甲、乙、丙有如图所示的转化关系(部分物质和反应条件已略去),下列各组物质按照甲、乙、丙的顺序符合要求的是
A.Cu、CuO、CuSO4 B.H2O2、H2O、O2
C.KOH、K2CO3、KNO3 D.CaCO3 、Ca( OH)2、CaO
二、填空题
16.2018年5月6日晚,泉城济南筹备了近一年的“明湖灯光秀”首次公演,奇光异彩、如梦如幻的场景让济南备受关注。“明湖秀”作为泉城夜宴的精华,以大明湖为载体,讲述了泉城济南从历史走向未来的动人篇章。某化学兴趣小组的同学也为研究济南大明湖的水质状况,进行了系列探究实验。
(1)小明同学从大明湖中取水样过滤,用滴管取3滴过滤后的滤液滴在洁净的玻璃片上,置于酒精灯上小心加热,水分消失后,观察到玻璃片上有少许固体残留物,其原因是______,说明大明湖湖水属于_________(选填“混合物”或“纯净物”)。
(2)小刚同学通过电解水实验探究水的组成。电解水时,与直流电源的负极相连的电极附近得到气体是______,通过实验可以得出水是由______组成的。请写出电解水的化学方程式_______。
(3)2018年3月22日是第二十六届“世界水日”,联合国确定2018年“世界水日”宣传主题是“Nature for water(借自然之力,护绿水青山)。保护环境,人人有责。下列做法中,你认为与保护环境不相符的是_______(填编号)。
①生活污水直接排入大明湖 ②工业废水处理达标后排放
③向湖水中随意丢弃废电池 ④提倡使用无磷洗衣粉
(4)同学们又探究了温度对物质溶解性的影响(溶解度曲线如图所示),试回答下列问题:
①时,M物质饱和溶液的溶质质量分数_____N物质饱和溶液的溶质质量分数(填“大于”“小于”“等于”之一)。
②时,将40g物质N投入到100g水中,得到物质N的_____(填“饱和”或“不饱和”)溶液;此时溶液的溶质质量分数是_________(结果精确到0.1%)。
③将时等质量M、N两物质的饱和溶液分别降温至,对此时所得溶液的叙述中,正确的是_________________(填序号)。
A 溶质质量:M<N B 溶剂质量:M>N
C 溶质质量分数:M>N D 溶液质量:M=N
17.硝酸钾固体与氯化钾固体的溶解度曲线如下图所示,回答下列问题:
(1)℃时,两种物质中溶解度较大的是_____。
(2)℃时,两种物质的等质量饱和溶液降温至℃,析出固体质量较多的是_____的溶液。
(3)℃时,将50g水加入盛有25g氯化钾的烧杯中,充分溶解后,所得溶液为_____(填“饱和”或“不饱和”)溶液,该溶液中所含的大量离子,其符号是_____。
(4)欲配制溶质质量分数为20%的硝酸钾溶液,应满足的温度范围:_____。
18.我国海岸线曲折,海洋资源十分丰富。
(1)如图所示,从海水中获得淡水的方法是_____,你认为该技术的优点是_____。
(2)从海水中提取金属镁,可按如图所示流程进行:
①写出步骤Ⅱ发生反应的化学方程式_____;
②根据流程图,下列说法正确的是_____(选填字母序号)。
A、步骤Ⅰ通过一步反应即可实现
B、步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁
C、步骤Ⅲ发生了中和反应
D、步骤Ⅴ中化学能转化为电能
(3)我国著名化学家侯德榜发明的“联合制碱法”主要工艺流程示意图如下:
①为了除去粗盐水中可溶性杂质,可加入下列物质,利用过滤等操作进行除杂,则加入下列三种物质的先后顺序为_____。
a.稍过量的Na2CO3溶液 b.适量的盐酸 c.稍过量的Ba(OH)2溶液
②流程一,氨化溶液后,溶液的pH_____7(选填“>”、“<”或“=”),从而有利于吸收气体A,流程一反应的化学方程式为_____。
19.若粗盐中含有Na2SO4、MgCl2、CaCl2三种杂质,加入正确的除杂试剂后,得到的沉淀中盐的化学式为________ ,过滤后滤液中溶质有 _____种,若加入过量稀盐酸,则造成所得精盐的质量_______(填偏大、偏小、不变)。
20.现有两瓶失去标签的溶液,溶质分别可能是硝酸钠、硝酸铜、硫酸钠、硫酸、碳酸钾中的一种,检验步骤如下:
(1)分别取少量混用,无明显现象,溶液无色透明,经测定混合溶液显酸性。由此可推断这两瓶溶液中的溶质一定不是________;(填化学式,多填、少填、错填均不得分,下同)
(2)向上述混合溶液中加入Ba(NO3)2溶液,产生白色沉淀。则这两瓶溶液的溶质至少是________________中的一种;反应的化学方程式为________________________ (任意一个即可);
试推断这两瓶溶液的溶质可能的组合有__________种(填数字),请写出其中含阴离子种类最少的一种组合________________________。
三、推断题
21.甲、乙、丙、丁、戊分别是Na2SO4、Ba(NO3)2、HNO3、BaCl2、NaOH五种溶液中的一种,现利用X溶液鉴别它们,试根据下图关系回答问题:
X溶液中溶质的化学式为___________;生成气体Y的化学方程式为___________________;
溶液丙与溶液丁反应时的化学方程式为___________________。
22.化合物A、B、C都含三种元素,其中两种元素的质量比均为1:2.它们之间有如图所示的关系,在图示的三个化学反应中(“→”表示转化关系):一个反应有沉淀生成,另一个反应有气体生产,还有一个反应既有沉淀又有水生成.请回答下列问题:
(1)写出A的化学式 ;
(2)写出B→C反应的化学方程式 .
四、实验题
23.欲测定某溶液中溶质成分.已知该溶液中的溶质可能是H2SO4、HCl、NaOH、BaCl2
中一种或二种,现设计以下实验进行探究.(提示:氯化钡溶液呈中性)
①取少量溶液于试管中滴入2滴紫色石蕊,石蕊变红,溶液中一定不存在 .
②为了进一步测定成分,重新取少量溶液于烧杯中,逐滴加入10.0%的Na2CO3溶液,测得滴加溶液的质量与产生沉淀的关系(图1)和滴加溶液的质量与烧杯中溶液的pH关系(图2).
Ⅰ.根据图1,推断该溶液中的溶质是 .用化学方程式解释一定不存在物质的原因是 .
Ⅱ.滴入Na2CO3溶液的过程中依次观察到的现象是 .
Ⅲ.图2中d点时,溶液中溶质的化学式是 .简述bc段溶液pH一直为7的理由是 .
24.某同学在商店买到一种“果冻蜡烛”。他对“果冻蜡烛”进行如下探究。
(提出问题)“果冻蜡烛”是否含有碳、氢、氧元素?
(查阅资料)“果冻蜡烛”可完全燃烧,燃烧时无烟尘,燃烧过程和熄灭时无异味。
(1)(探究实验)(请完成下列实验报告)
步骤 现象 分析
①点燃“果冻蜡烛”,并在火焰上方罩一个干燥而冷的小烧杯; 烧杯内壁有无色小液滴生成 “果冻蜡烛”燃烧后的产物有________;
②迅速倒转小烧杯,向其中加入适量澄清石灰水,振荡。 ________ “果冻蜡烛”燃烧后的产物有二氧化碳(CO2)
(实验结论)该同学分析:水由氢元素和氧元素组成,二氧化碳由碳元素和氧元素组成,因此“果冻蜡烛”含有碳、氢、氧元素。
(2)(反思与评价)你认为该同学得出的实验结论是否正确?________(填“正确”或“不正确”)。理由:________
五、计算题
25.某兴趣小组的同学进行纯碱样品(杂质仅含NaCl)中质量分数的测定,主要测定流程如下图:
(1)请指出图中过滤操作中的一处错误__________;
(2)若称取样品质量为6.0g,反应后称量烘干沉淀质量为5.5g,请计算纯碱样品中质量分数。(精确到0.01%)__________
26.t℃时,硝酸钾的溶解度为ag,该温度下把bg硝酸钾投入cg水中充分溶解
⑴当时,溶液中溶质质量分数为_____%;
⑵当时,溶液中溶质质量分数为_____%。
参考答案
1.C 2.B 3.C 4.C 5.B 6.D 7.B 8.D 9.C 10.D 11.C 12.B 13.C 14.D 15.A 16.湖水中含有可溶性固体杂质 混合物 氢气 氢元素和氧元素 ①③ 等于 不饱和 28.6% A
17.氯化钾 硝酸钾 饱和 K+、NO3- 温度不低于t1℃
18.蒸馏 节能、易操作 MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2 BC cab > NaCl+H2O+CO2+NH3=NaHCO3↓+NH4Cl
19. BaCO3 CaCO3 BaSO4 三 不变
20. Cu(NO3)2、K2CO3 H2SO4、NaSO4 H2SO4+Ba(NO3)2= Ba2SO4↓+2 HNO3 4 NaSO4、NaNO3
21.Na2CO3 BaCO3 +2HNO3 =Ba(NO3)2+CO2↑+H2O Ba(NO3)2+Na2SO4=BaSO4↓+2NaNO3
22.(1)H2SO4;(2)ZnSO4+Ba(OH)2═BaSO4↓+Zn(OH)2↓.
23.①NaOH ②Ⅰ、HCl、BaCl2 H2SO4+BaCl2=BaSO4↓+ 2HCl
Ⅱ、溶液中出现气泡,过一段时间产生白色沉淀 Ⅲ、NaCl、Na2CO3
bc段说明氯化钡在不断减少的过程.溶液中氯化钡与碳酸钠反应生成的氯化钠溶液呈中性
24.【探究实验】(1)水 (2)澄清石灰水变浑浊
【反思与评价】不正确 果冻蜡烛燃烧时有氧气参加反应,氧气由氧元素组成,所以不能以此判断果冻蜡烛中一定含有氧元素
25.没有用玻璃棒引流 97.17%
26.
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
