3.1物质的转化 同步测试(含答案)
文档属性
| 名称 | 3.1物质的转化 同步测试(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 387.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2020-04-03 00:00:00 | ||
图片预览



文档简介
_3.1__物质的转化(一)__[学生用书A58]
1.下列物质不能使金属生成金属氧化物的是( C )
A.氧气 B.浓硫酸
C.稀硫酸 D.硝酸
2.要除去二氧化碳中混有的少量一氧化碳,可以采用的方法是将混合气体( D )
A.通过澄清石灰水 B.通过灼热的木炭
C.通过水 D.通过灼热的氧化铜
3.在浓硫酸的运输过程中,能将浓硫酸盛放在铁制的容器中。其原因是( B )
A.铁的化学性质稳定,不与硫酸反应
B.铁与浓硫酸反应生成致密的氧化物
C.铁与浓硫酸反应生成FeSO4保护层
D.铁与浓硫酸反应生成Fe2(SO4)3保护层
4.在氢气还原氧化铜的实验中,观察到的现象是( D )
A.有红色的铜生成
B.试管口有水生成
C.有铜和水生成
D.黑色固体变成红色,试管口有水珠生成
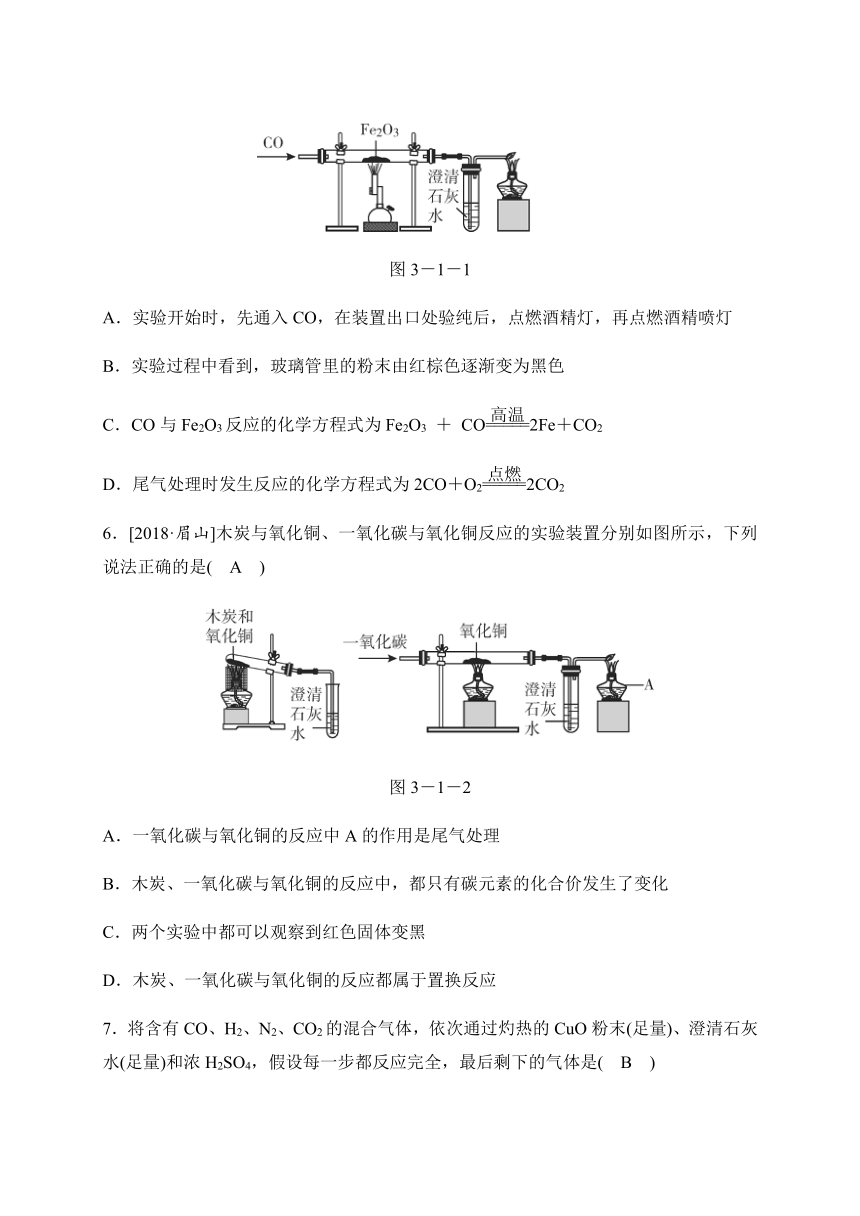
5.[2018·日照]如图是CO与Fe2O3反应的实验装置图,下列说法不正确的( C )
图3-1-1
A.实验开始时,先通入CO,在装置出口处验纯后,点燃酒精灯,再点燃酒精喷灯
B.实验过程中看到,玻璃管里的粉末由红棕色逐渐变为黑色
C.CO与Fe2O3反应的化学方程式为Fe2O3 + CO2Fe+CO2
D.尾气处理时发生反应的化学方程式为2CO+O22CO2
6.[2018·眉山]木炭与氧化铜、一氧化碳与氧化铜反应的实验装置分别如图所示,下列说法正确的是( A )
图3-1-2
A.一氧化碳与氧化铜的反应中A的作用是尾气处理
B.木炭、一氧化碳与氧化铜的反应中,都只有碳元素的化合价发生了变化
C.两个实验中都可以观察到红色固体变黑
D.木炭、一氧化碳与氧化铜的反应都属于置换反应
7.将含有CO、H2、N2、CO2的混合气体,依次通过灼热的CuO粉末(足量)、澄清石灰水(足量)和浓H2SO4,假设每一步都反应完全,最后剩下的气体是( B )
A.N2、CO2 B.N2
C.N2、H2O D.N2、CO
8.如图将插入橡胶塞的一根光亮的红色铜丝绕成螺旋状,在酒精灯的火焰上烧一段时间后趁热迅速伸入盛有澄清石灰水和X气体的集气瓶中,塞紧橡胶塞,看到变黑色的铜丝又变为红色,同时澄清石灰水变浑浊,则集气瓶中的气体X是( C )
图3-1-3
A.H2 B.O2 C.CO D.CO2
9.[2017·杭州]工业上可用如下反应制取金属钡:2Al+4BaO3Ba↑+Ba(AlO2)2。则下列说法正确的是( C )
A.反应物铝能被磁铁吸引
B.生成物Ba(AlO2)2属于氧化物
C.反应前后铝元素的化合价发生改变
D.该反应属于复分解反应
10.用氢气还原氧化铜,实验操作有以下几步:a.加热装有氧化铜的试管;b.通入验纯后的氢气;c.实验结束撤去酒精灯;d.继续通入氢气至试管冷却。正确的操作顺序是( B )
A.a、b、c、d B.b、a、c、d
C.a、b、d、c D.b、a、d、c
11.某同学实验时,用氢气还原16g氧化铜,反应一段时间后,停止加热,冷却后称量剩余固体质量为14.4g,则下列结论正确的是( C )
A.有1.6g水生成
B.有1.4g铜生成
C.实际用去氢气的质量大于0.2g
D.有80%的氧化铜参加反应
12.将CO通入盛有12g Fe2O3的试管内,加热反应一段时间后,停止加热,继续通入CO至试管冷却,此时试管内残留固体的质量为9.6g,则反应生成铁的质量为( B )
A.2.4g B.5.6g C.8.4g D.9.6g
13.某无色气体X可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或两种。为确认其组成,某同学取一定量该气体按如图所示装置进行实验(假设每一步都充分反应或吸收),结果装置①中无明显变化,装置③增重1.8g,装置④增重2.2g。下列关于气体X成分的分析中,错误的是( B )
图3-1-4
小资料:碱石灰的主要成分是氧化钙和氢氧化钠
A.一定没有二氧化碳
B.可能含有甲烷和氢气
C.可能只有甲烷
D.可能含有氢气和一氧化碳
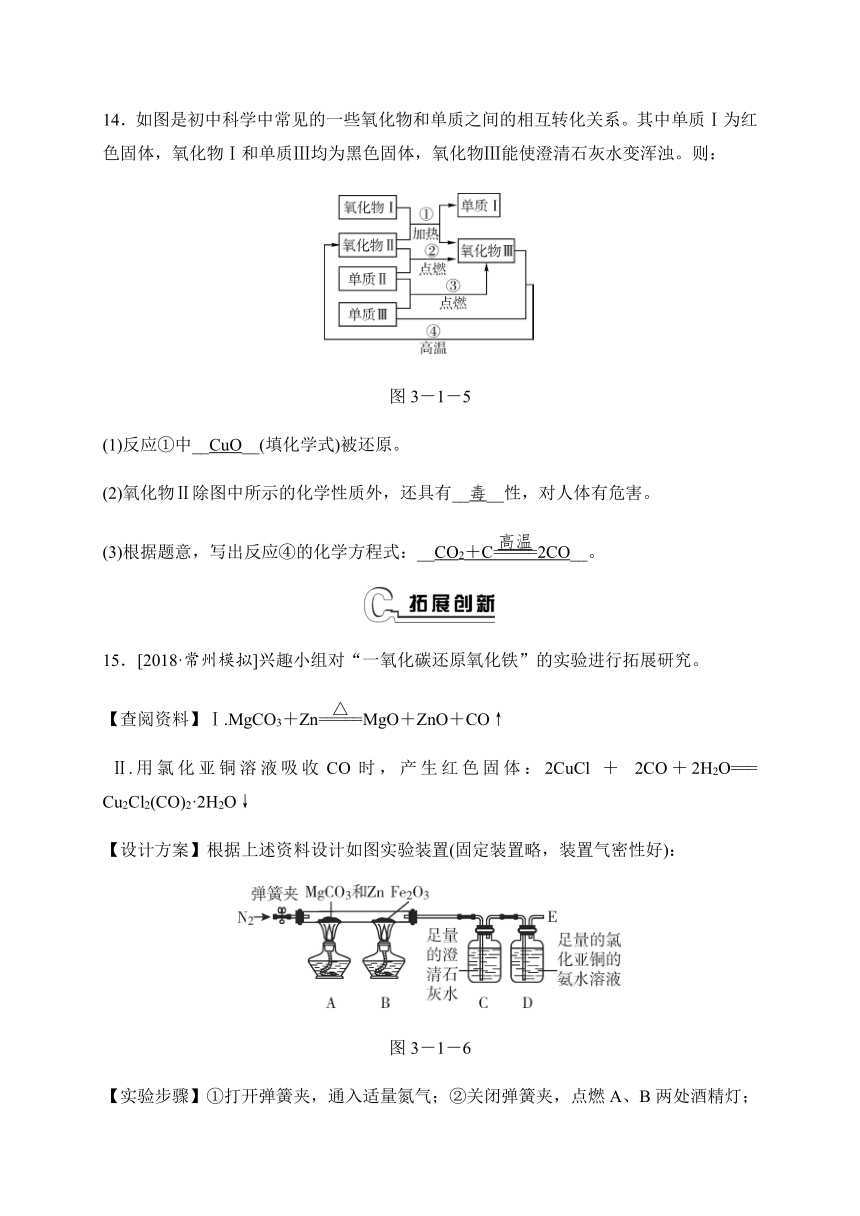
14.如图是初中科学中常见的一些氧化物和单质之间的相互转化关系。其中单质Ⅰ为红色固体,氧化物Ⅰ和单质Ⅲ均为黑色固体,氧化物Ⅲ能使澄清石灰水变浑浊。则:
图3-1-5
(1)反应①中__CuO__(填化学式)被还原。
(2)氧化物Ⅱ除图中所示的化学性质外,还具有__毒__性,对人体有危害。
(3)根据题意,写出反应④的化学方程式:__CO2+C2CO__。
15.[2018·常州模拟]兴趣小组对“一氧化碳还原氧化铁”的实验进行拓展研究。
【查阅资料】Ⅰ.MgCO3+ZnMgO+ZnO+CO↑
Ⅱ.用氯化亚铜溶液吸收CO时,产生红色固体:2CuCl + 2CO+2H2O=== Cu2Cl2(CO)2·2H2O↓
【设计方案】根据上述资料设计如图实验装置(固定装置略,装置气密性好):
图3-1-6
【实验步骤】①打开弹簧夹,通入适量氮气;②关闭弹簧夹,点燃A、B两处酒精灯;③观察实验现象;④熄灭两只酒精灯。
【实验分析】(1)步骤①的目的是__排尽装置中的空气,防止加热混合气体引起爆炸__。
(2)步骤③时,B处玻璃管中红棕色粉末变黑,该反应的化学方程为__Fe2O3+3CO2Fe+3CO2__,C处现象是__澄清石灰水变浑浊__,D处出现红色固体。
(3)下列关于该实验的说法正确的是__AD__。
A.B处固体质量逐渐减小
B.D处现象证明A、B处发生了反应
C.必须在E处加一只点燃的酒精灯
D.步骤④后,应继续通氮气至玻璃管冷却
(4)已知A处参加反应的MgCO3质量为1.68g,C处得到沉淀质量为1g。从环保角度考虑D中CuCl质量最少需__0.995__g。
16.[2017·杭州]小金利用如图装置进行甲、乙对比实验,探究温度对CO和 Fe2O3反应的影响(固定装置略)。
图3-1-7
(1)从实验安全角度考虑,图示装置还应采取的改进措施是__在装置末端尖嘴导管处,放置一盏燃着的酒精灯(合理即可)__。
(2)完全反应后,两组的生成物均为黑色粉末(纯净物),分别用两组生成物进行以下实验:
步骤
操作
甲组现象
乙组现象
1
称量黑色粉末质量/g
m1
m2
2
取黑色粉末,用磁铁吸引
能被吸引
能被吸引
3
取黑色粉末,加入稀盐酸
全部溶解,有大量气泡
无明显现象
4
取黑色粉末,加入足量CuSO4溶液
有红色物质生成
无明显现象
①甲组的黑色粉末与稀盐酸反应的化学方程式是__Fe+2HCl===FeCl2+H2↑__。
②小金查阅资料后发现Fe3O4在常温下不与稀盐酸、CuSO4溶液反应,故猜想乙组的生成物为 Fe3O4。他又发现m2恰好为__4.64__g,这可成为支持上述猜想的新证据。
(3)甲、乙两组实验说明温度对CO和Fe2O3反应有影响,且均体现出CO的__还原性和可燃性(写出还原性即可)__(填写化学性质)。
3.1__物质的转化(二)__[学生用书B58]
1.造成大气污染的二氧化硫主要来自( B )
A.硫酸厂排放的废气
B.大量燃烧含硫的燃料
C.火山爆发产生的气体
D.汽车排放的大量尾气
2.汽车尾气含有的下列气体,在空气中易形成酸雨的是( C )
A.一氧化碳 B.二氧化碳
C.二氧化氮 D.碳氢化合物
3.下列非金属氧化物中不能与水反应生成酸的是( C )
A.二氧化碳 B.二氧化硫
C.二氧化硅 D.三氧化硫
4.下列金属氧化物中能与水反应生成碱的是( D )
A.Fe2O3 B.CuO C.MnO2 D.Na2O
5.下列转化不能通过一步反应实现的是( C )
A.Ba(OH)2→NaOH B.HCl→NaCl
C.Fe2O3→Fe(OH)3 D.MgCO3→MgCl2
【解析】Ba(OH)2可与Na2SO4(或Na2CO3)反应,生成BaSO4(或BaCO3)沉淀和NaOH,反应可以一步实现;HCl可与NaOH、钠盐等发生复分解反应生成NaCl,可一步完成;Fe2O3属金属氧化物,能与还原剂发生氧化还原反应生成金属单质Fe,能与酸发生复分解反应生成铁盐和水,不能与碱反应生成Fe(OH)3,因此由Fe2O3到Fe(OH)3不能一步反应实现;MgCO3与HCl反应生成MgCl2、H2O和CO2,可以一步实现。
6.下列氧化物放入水中,溶液的pH>7的是( A )
A.氧化钙 B.二氧化碳
C.二氧化硫 D.氧化铜
7.[2018·嘉兴舟山]某同学在学习了金属及其化合物之间的转化规律后,绘制了可以通过一步反应制取MgSO4的思维导图,其中所选用的物质错误的是( B )
图3-1-8
A.①—Mg
B.②—MgCl2
C.③—H2SO4
D.④—Mg(OH)2
8.如图是小凡用手势OK表示初中化学反应中生成水的不同方法,要求手指上的物质分别通过某种基本类型的反应能直接生成H2O,则物质X一定不是下列物质中的( D )
图3-1-9
A.H2 B.H2CO3 C.KOH D.CH4
【解析】氢气在氧气中燃烧生成水,该反应属于化合反应;碳酸分解生成水和二氧化碳,该反应属于分解反应;稀盐酸与氢氧化钾反应生成氯化钾和水,该反应属于复分解反应;甲烷在氧气中燃烧生成二氧化碳和水,该反应不属于基本类型。
9.物质X可发生下列所示的两个反应,则X可能是下列物质中的( A )
①X+酸→盐+水 ②X+水→碱
A.CaO B.Fe2O3 C.CO2 D.NaOH
10.[2018·台州]下列选项所示的物质转化均能一步实现的是( D )
A.FeFe2O3Fe(OH)3
B.CuOCuSO4CuCl2
C.SSO2H2SO4
D.CO2Na2CO3NaOH
11.下列转化能一步完成的是( A )
①CH4→CO2 ②HNO3→HCl ③CaO→Ca(OH)2 ④BaCl2→Ba(NO3)2
⑤CuO→Cu
A.①③④⑤ B.②③④⑤
C.①②④⑤ D.①②③④
12.下列各组变化中,每一转化在一定条件下均能一步实现的是( C )
图3-1-10
A.①和② B.②和③
C.①和③ D.①②③
13.甲、乙、丙、丁四种物质有如图所示的转化关系(部分反应物和生成物已略去),则甲、 乙、丙、丁依次是( C )
图3-1-11
A.C、CO、CO2、H2CO3
B.CO、CO2、C、H2CO3
C.CaO、Ca(OH)2、CaCl2、CaCO3
D.CaCO3、Ca(OH)2、CaCl2、CaO
14.[2017·湖州]通过一步化学反应实现如图所示的X、Y、Z三种物质间转化,表格中X、Y、Z对应的物质不能实现这种转化的是( B )
图3-1-12
选项
X
Y
Z
A
CO2
Na2CO3
CaCO3
B
CuO
Cu(NO3)2
Cu(OH)2
C
HCl
BaCl2
NaCl
D
Mg
MgO
MgCl2
15.小科同学在学习了金属、金属氧化物和碱之间的相互关系后,发现如下规律:金属+O2→金属氧化物,金属氧化物+H2O→碱。请你根据这一规律,写一个金属氧化物和水反应生成碱的化学方程式:__CaO+H2O===Ca(OH)2(合理即可)__。
是不是所有的金属氧化物都能和水反应生成对应的碱?__不是__(选填“是”或“不是”)。
16.已知A、E、F是单质,B、C、D是化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成。其中B是式量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如图所示。
图3-1-13
(1)A、E的化学式为A:__O2__;E:__H2__。
(2)请你写出下列变化的化学方程式:
A+F→C__O2+CCO2__。
D→B+C__H2CO3CO2↑+H2O__。
17.某科学兴趣小组的同学在做完木炭还原氧化铜的实验后,发现试管中仍有黑色固体存在,他们对黑色固体是什么进行了探究:
【提出猜想】甲同学:是木炭;
乙同学:是氧化铜;
丙同学:__是木炭和氧化铜的混合物__。
【查阅资料】木炭、铜都不与稀硫酸反应;CuO、Fe2O3、MgO等氧化物能与稀硫酸反应生成盐和水。
【实验设计】向盛有黑色固体的试管中加入足量稀硫酸,充分振荡,静置后观察现象。
【分析讨论】他们对该实验方案进行了讨论,达成了共识:若试管内溶液呈蓝色,黑色固体不存在,证明__乙__同学猜想正确;若试管内液体无色,有黑色固体存在,证明__甲__同学猜想正确;若出现的现象是__试管内溶液呈蓝色且有黑色固体存在__,证明丙同学的猜想正确;发生反应的化学方程式为__CuO+H2SO4===CuSO4+H2O__。
18.海水经过晾晒后得到粗盐和苦卤,重结晶后的食盐中还含有硫酸钠、氯化镁、氯化钙等可溶性杂质,他们在溶液中主要以SO、Ca2+、Mg2+的形式存在,为将这些杂质离子除净,应加入过量的氯化钡、氢氧化钠、碳酸钠等物质将其转化为沉淀,过滤除去;再加入适量的盐酸,得到精盐水,最后经蒸发即得精盐。以下是某化工厂对海水进行综合利用的示意图:
图3-1-14
(1)在苦卤制镁的过程中加入了石灰乳(主要成分是氢氧化钙),石灰乳是用生石灰制得的,请写出制取石灰乳的化学方程式:__CaO+H2O===Ca(OH)2__。
(2)在制备精盐的过程中,氯化钡和碳酸钠溶液的添加顺序是否可以颠倒?__不可以__,理由是__碳酸钠的作用是除去Ca2+和多余的氯化钡__。
(3)在利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是__除去多余的氢氧化钠和碳酸钠__。
19.下列框图中的物质均为初中科学常见的物质,其中A是建筑材料的主要成分,B属于氧化物,如图是它们之间的相互转化关系。请回答:
图3-1-15
(1)写出下列物质的化学式:A:__CaCO3__;C:__CO2__。
(2)得到F溶液的操作Ⅰ的名称为__过滤__。
(3)若G是黄色溶液,I是红褐色沉淀,请写出G + F → I的化学方程式:__FeCl3+3NaOH===Fe(OH)3↓+3NaCl__。
(4)指出反应①的基本类型是__化合__反应。
20.煤燃烧后的产物主要是CO2,也含有一定量的SO2,还可能含有CO。小明同学进行环境调查时发现:某火力发电厂(以煤为燃料)周围的树木已经枯萎,发电厂排放的废气中也可能含CO。他将收集的废气样品用如图所示装置恰当组合后进行检验,已知其中的药品均足量。请回答下列问题:
图3-1-16
(1)上述装置中,仪器A的名称是__酒精灯__。
(2)你认为发电厂周围树木枯萎的原因可能是__火力发电厂由于燃烧煤产生二氧化硫,易形成酸雨__。
(3)为确定发电厂排放的废气中是否含CO,请根据拟定的气体流向,确定并填写组合装置中各导管口(用字母表示)的连接顺序:
废气→( a )→( b )→( e )→( f )→( d )→( c )→尾气处理
(4)实验结果证明该发电厂排放的废气中含有CO。则实验过程中与此相关的实验现象有黑色粉末变成红色,澄清石灰水变浑浊。上述现象对应反应的化学方程式依次为__CuO+COCu+CO2__;__CO2+Ca(OH)2===CaCO3↓+H2O__。
(5)请说明你对该实验尾气的处理方法:__用气球收集(或点燃,使CO充分燃烧)__。
1.下列物质不能使金属生成金属氧化物的是( C )
A.氧气 B.浓硫酸
C.稀硫酸 D.硝酸
2.要除去二氧化碳中混有的少量一氧化碳,可以采用的方法是将混合气体( D )
A.通过澄清石灰水 B.通过灼热的木炭
C.通过水 D.通过灼热的氧化铜
3.在浓硫酸的运输过程中,能将浓硫酸盛放在铁制的容器中。其原因是( B )
A.铁的化学性质稳定,不与硫酸反应
B.铁与浓硫酸反应生成致密的氧化物
C.铁与浓硫酸反应生成FeSO4保护层
D.铁与浓硫酸反应生成Fe2(SO4)3保护层
4.在氢气还原氧化铜的实验中,观察到的现象是( D )
A.有红色的铜生成
B.试管口有水生成
C.有铜和水生成
D.黑色固体变成红色,试管口有水珠生成
5.[2018·日照]如图是CO与Fe2O3反应的实验装置图,下列说法不正确的( C )
图3-1-1
A.实验开始时,先通入CO,在装置出口处验纯后,点燃酒精灯,再点燃酒精喷灯
B.实验过程中看到,玻璃管里的粉末由红棕色逐渐变为黑色
C.CO与Fe2O3反应的化学方程式为Fe2O3 + CO2Fe+CO2
D.尾气处理时发生反应的化学方程式为2CO+O22CO2
6.[2018·眉山]木炭与氧化铜、一氧化碳与氧化铜反应的实验装置分别如图所示,下列说法正确的是( A )
图3-1-2
A.一氧化碳与氧化铜的反应中A的作用是尾气处理
B.木炭、一氧化碳与氧化铜的反应中,都只有碳元素的化合价发生了变化
C.两个实验中都可以观察到红色固体变黑
D.木炭、一氧化碳与氧化铜的反应都属于置换反应
7.将含有CO、H2、N2、CO2的混合气体,依次通过灼热的CuO粉末(足量)、澄清石灰水(足量)和浓H2SO4,假设每一步都反应完全,最后剩下的气体是( B )
A.N2、CO2 B.N2
C.N2、H2O D.N2、CO
8.如图将插入橡胶塞的一根光亮的红色铜丝绕成螺旋状,在酒精灯的火焰上烧一段时间后趁热迅速伸入盛有澄清石灰水和X气体的集气瓶中,塞紧橡胶塞,看到变黑色的铜丝又变为红色,同时澄清石灰水变浑浊,则集气瓶中的气体X是( C )
图3-1-3
A.H2 B.O2 C.CO D.CO2
9.[2017·杭州]工业上可用如下反应制取金属钡:2Al+4BaO3Ba↑+Ba(AlO2)2。则下列说法正确的是( C )
A.反应物铝能被磁铁吸引
B.生成物Ba(AlO2)2属于氧化物
C.反应前后铝元素的化合价发生改变
D.该反应属于复分解反应
10.用氢气还原氧化铜,实验操作有以下几步:a.加热装有氧化铜的试管;b.通入验纯后的氢气;c.实验结束撤去酒精灯;d.继续通入氢气至试管冷却。正确的操作顺序是( B )
A.a、b、c、d B.b、a、c、d
C.a、b、d、c D.b、a、d、c
11.某同学实验时,用氢气还原16g氧化铜,反应一段时间后,停止加热,冷却后称量剩余固体质量为14.4g,则下列结论正确的是( C )
A.有1.6g水生成
B.有1.4g铜生成
C.实际用去氢气的质量大于0.2g
D.有80%的氧化铜参加反应
12.将CO通入盛有12g Fe2O3的试管内,加热反应一段时间后,停止加热,继续通入CO至试管冷却,此时试管内残留固体的质量为9.6g,则反应生成铁的质量为( B )
A.2.4g B.5.6g C.8.4g D.9.6g
13.某无色气体X可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或两种。为确认其组成,某同学取一定量该气体按如图所示装置进行实验(假设每一步都充分反应或吸收),结果装置①中无明显变化,装置③增重1.8g,装置④增重2.2g。下列关于气体X成分的分析中,错误的是( B )
图3-1-4
小资料:碱石灰的主要成分是氧化钙和氢氧化钠
A.一定没有二氧化碳
B.可能含有甲烷和氢气
C.可能只有甲烷
D.可能含有氢气和一氧化碳
14.如图是初中科学中常见的一些氧化物和单质之间的相互转化关系。其中单质Ⅰ为红色固体,氧化物Ⅰ和单质Ⅲ均为黑色固体,氧化物Ⅲ能使澄清石灰水变浑浊。则:
图3-1-5
(1)反应①中__CuO__(填化学式)被还原。
(2)氧化物Ⅱ除图中所示的化学性质外,还具有__毒__性,对人体有危害。
(3)根据题意,写出反应④的化学方程式:__CO2+C2CO__。
15.[2018·常州模拟]兴趣小组对“一氧化碳还原氧化铁”的实验进行拓展研究。
【查阅资料】Ⅰ.MgCO3+ZnMgO+ZnO+CO↑
Ⅱ.用氯化亚铜溶液吸收CO时,产生红色固体:2CuCl + 2CO+2H2O=== Cu2Cl2(CO)2·2H2O↓
【设计方案】根据上述资料设计如图实验装置(固定装置略,装置气密性好):
图3-1-6
【实验步骤】①打开弹簧夹,通入适量氮气;②关闭弹簧夹,点燃A、B两处酒精灯;③观察实验现象;④熄灭两只酒精灯。
【实验分析】(1)步骤①的目的是__排尽装置中的空气,防止加热混合气体引起爆炸__。
(2)步骤③时,B处玻璃管中红棕色粉末变黑,该反应的化学方程为__Fe2O3+3CO2Fe+3CO2__,C处现象是__澄清石灰水变浑浊__,D处出现红色固体。
(3)下列关于该实验的说法正确的是__AD__。
A.B处固体质量逐渐减小
B.D处现象证明A、B处发生了反应
C.必须在E处加一只点燃的酒精灯
D.步骤④后,应继续通氮气至玻璃管冷却
(4)已知A处参加反应的MgCO3质量为1.68g,C处得到沉淀质量为1g。从环保角度考虑D中CuCl质量最少需__0.995__g。
16.[2017·杭州]小金利用如图装置进行甲、乙对比实验,探究温度对CO和 Fe2O3反应的影响(固定装置略)。
图3-1-7
(1)从实验安全角度考虑,图示装置还应采取的改进措施是__在装置末端尖嘴导管处,放置一盏燃着的酒精灯(合理即可)__。
(2)完全反应后,两组的生成物均为黑色粉末(纯净物),分别用两组生成物进行以下实验:
步骤
操作
甲组现象
乙组现象
1
称量黑色粉末质量/g
m1
m2
2
取黑色粉末,用磁铁吸引
能被吸引
能被吸引
3
取黑色粉末,加入稀盐酸
全部溶解,有大量气泡
无明显现象
4
取黑色粉末,加入足量CuSO4溶液
有红色物质生成
无明显现象
①甲组的黑色粉末与稀盐酸反应的化学方程式是__Fe+2HCl===FeCl2+H2↑__。
②小金查阅资料后发现Fe3O4在常温下不与稀盐酸、CuSO4溶液反应,故猜想乙组的生成物为 Fe3O4。他又发现m2恰好为__4.64__g,这可成为支持上述猜想的新证据。
(3)甲、乙两组实验说明温度对CO和Fe2O3反应有影响,且均体现出CO的__还原性和可燃性(写出还原性即可)__(填写化学性质)。
3.1__物质的转化(二)__[学生用书B58]
1.造成大气污染的二氧化硫主要来自( B )
A.硫酸厂排放的废气
B.大量燃烧含硫的燃料
C.火山爆发产生的气体
D.汽车排放的大量尾气
2.汽车尾气含有的下列气体,在空气中易形成酸雨的是( C )
A.一氧化碳 B.二氧化碳
C.二氧化氮 D.碳氢化合物
3.下列非金属氧化物中不能与水反应生成酸的是( C )
A.二氧化碳 B.二氧化硫
C.二氧化硅 D.三氧化硫
4.下列金属氧化物中能与水反应生成碱的是( D )
A.Fe2O3 B.CuO C.MnO2 D.Na2O
5.下列转化不能通过一步反应实现的是( C )
A.Ba(OH)2→NaOH B.HCl→NaCl
C.Fe2O3→Fe(OH)3 D.MgCO3→MgCl2
【解析】Ba(OH)2可与Na2SO4(或Na2CO3)反应,生成BaSO4(或BaCO3)沉淀和NaOH,反应可以一步实现;HCl可与NaOH、钠盐等发生复分解反应生成NaCl,可一步完成;Fe2O3属金属氧化物,能与还原剂发生氧化还原反应生成金属单质Fe,能与酸发生复分解反应生成铁盐和水,不能与碱反应生成Fe(OH)3,因此由Fe2O3到Fe(OH)3不能一步反应实现;MgCO3与HCl反应生成MgCl2、H2O和CO2,可以一步实现。
6.下列氧化物放入水中,溶液的pH>7的是( A )
A.氧化钙 B.二氧化碳
C.二氧化硫 D.氧化铜
7.[2018·嘉兴舟山]某同学在学习了金属及其化合物之间的转化规律后,绘制了可以通过一步反应制取MgSO4的思维导图,其中所选用的物质错误的是( B )
图3-1-8
A.①—Mg
B.②—MgCl2
C.③—H2SO4
D.④—Mg(OH)2
8.如图是小凡用手势OK表示初中化学反应中生成水的不同方法,要求手指上的物质分别通过某种基本类型的反应能直接生成H2O,则物质X一定不是下列物质中的( D )
图3-1-9
A.H2 B.H2CO3 C.KOH D.CH4
【解析】氢气在氧气中燃烧生成水,该反应属于化合反应;碳酸分解生成水和二氧化碳,该反应属于分解反应;稀盐酸与氢氧化钾反应生成氯化钾和水,该反应属于复分解反应;甲烷在氧气中燃烧生成二氧化碳和水,该反应不属于基本类型。
9.物质X可发生下列所示的两个反应,则X可能是下列物质中的( A )
①X+酸→盐+水 ②X+水→碱
A.CaO B.Fe2O3 C.CO2 D.NaOH
10.[2018·台州]下列选项所示的物质转化均能一步实现的是( D )
A.FeFe2O3Fe(OH)3
B.CuOCuSO4CuCl2
C.SSO2H2SO4
D.CO2Na2CO3NaOH
11.下列转化能一步完成的是( A )
①CH4→CO2 ②HNO3→HCl ③CaO→Ca(OH)2 ④BaCl2→Ba(NO3)2
⑤CuO→Cu
A.①③④⑤ B.②③④⑤
C.①②④⑤ D.①②③④
12.下列各组变化中,每一转化在一定条件下均能一步实现的是( C )
图3-1-10
A.①和② B.②和③
C.①和③ D.①②③
13.甲、乙、丙、丁四种物质有如图所示的转化关系(部分反应物和生成物已略去),则甲、 乙、丙、丁依次是( C )
图3-1-11
A.C、CO、CO2、H2CO3
B.CO、CO2、C、H2CO3
C.CaO、Ca(OH)2、CaCl2、CaCO3
D.CaCO3、Ca(OH)2、CaCl2、CaO
14.[2017·湖州]通过一步化学反应实现如图所示的X、Y、Z三种物质间转化,表格中X、Y、Z对应的物质不能实现这种转化的是( B )
图3-1-12
选项
X
Y
Z
A
CO2
Na2CO3
CaCO3
B
CuO
Cu(NO3)2
Cu(OH)2
C
HCl
BaCl2
NaCl
D
Mg
MgO
MgCl2
15.小科同学在学习了金属、金属氧化物和碱之间的相互关系后,发现如下规律:金属+O2→金属氧化物,金属氧化物+H2O→碱。请你根据这一规律,写一个金属氧化物和水反应生成碱的化学方程式:__CaO+H2O===Ca(OH)2(合理即可)__。
是不是所有的金属氧化物都能和水反应生成对应的碱?__不是__(选填“是”或“不是”)。
16.已知A、E、F是单质,B、C、D是化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成。其中B是式量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如图所示。
图3-1-13
(1)A、E的化学式为A:__O2__;E:__H2__。
(2)请你写出下列变化的化学方程式:
A+F→C__O2+CCO2__。
D→B+C__H2CO3CO2↑+H2O__。
17.某科学兴趣小组的同学在做完木炭还原氧化铜的实验后,发现试管中仍有黑色固体存在,他们对黑色固体是什么进行了探究:
【提出猜想】甲同学:是木炭;
乙同学:是氧化铜;
丙同学:__是木炭和氧化铜的混合物__。
【查阅资料】木炭、铜都不与稀硫酸反应;CuO、Fe2O3、MgO等氧化物能与稀硫酸反应生成盐和水。
【实验设计】向盛有黑色固体的试管中加入足量稀硫酸,充分振荡,静置后观察现象。
【分析讨论】他们对该实验方案进行了讨论,达成了共识:若试管内溶液呈蓝色,黑色固体不存在,证明__乙__同学猜想正确;若试管内液体无色,有黑色固体存在,证明__甲__同学猜想正确;若出现的现象是__试管内溶液呈蓝色且有黑色固体存在__,证明丙同学的猜想正确;发生反应的化学方程式为__CuO+H2SO4===CuSO4+H2O__。
18.海水经过晾晒后得到粗盐和苦卤,重结晶后的食盐中还含有硫酸钠、氯化镁、氯化钙等可溶性杂质,他们在溶液中主要以SO、Ca2+、Mg2+的形式存在,为将这些杂质离子除净,应加入过量的氯化钡、氢氧化钠、碳酸钠等物质将其转化为沉淀,过滤除去;再加入适量的盐酸,得到精盐水,最后经蒸发即得精盐。以下是某化工厂对海水进行综合利用的示意图:
图3-1-14
(1)在苦卤制镁的过程中加入了石灰乳(主要成分是氢氧化钙),石灰乳是用生石灰制得的,请写出制取石灰乳的化学方程式:__CaO+H2O===Ca(OH)2__。
(2)在制备精盐的过程中,氯化钡和碳酸钠溶液的添加顺序是否可以颠倒?__不可以__,理由是__碳酸钠的作用是除去Ca2+和多余的氯化钡__。
(3)在利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是__除去多余的氢氧化钠和碳酸钠__。
19.下列框图中的物质均为初中科学常见的物质,其中A是建筑材料的主要成分,B属于氧化物,如图是它们之间的相互转化关系。请回答:
图3-1-15
(1)写出下列物质的化学式:A:__CaCO3__;C:__CO2__。
(2)得到F溶液的操作Ⅰ的名称为__过滤__。
(3)若G是黄色溶液,I是红褐色沉淀,请写出G + F → I的化学方程式:__FeCl3+3NaOH===Fe(OH)3↓+3NaCl__。
(4)指出反应①的基本类型是__化合__反应。
20.煤燃烧后的产物主要是CO2,也含有一定量的SO2,还可能含有CO。小明同学进行环境调查时发现:某火力发电厂(以煤为燃料)周围的树木已经枯萎,发电厂排放的废气中也可能含CO。他将收集的废气样品用如图所示装置恰当组合后进行检验,已知其中的药品均足量。请回答下列问题:
图3-1-16
(1)上述装置中,仪器A的名称是__酒精灯__。
(2)你认为发电厂周围树木枯萎的原因可能是__火力发电厂由于燃烧煤产生二氧化硫,易形成酸雨__。
(3)为确定发电厂排放的废气中是否含CO,请根据拟定的气体流向,确定并填写组合装置中各导管口(用字母表示)的连接顺序:
废气→( a )→( b )→( e )→( f )→( d )→( c )→尾气处理
(4)实验结果证明该发电厂排放的废气中含有CO。则实验过程中与此相关的实验现象有黑色粉末变成红色,澄清石灰水变浑浊。上述现象对应反应的化学方程式依次为__CuO+COCu+CO2__;__CO2+Ca(OH)2===CaCO3↓+H2O__。
(5)请说明你对该实验尾气的处理方法:__用气球收集(或点燃,使CO充分燃烧)__。
同课章节目录
- 第一章 宇宙的起源与演化
- 1 我们的宇宙
- 2 热大爆炸宇宙模型
- 3 恒星的一生
- 4 星际航行和空间技术
- 第二章 地球的演化和生物圈的形成
- 1 地球的演化
- 2 生命起源
- 3 生物进化
- 4 生态平衡
- 第三章 物质的转化和元素的循环
- 1 物质的转化
- 2 自然界中的碳循环和氧循环
- 3 自然界中的氮循环
- 第四章 健康与保健
- 1 健康、亚健康和疾病
- 2 运动与健康
- 3 免疫与健康
- 4 营养与健康
- 5 卫生与健康
- 6 环境与健康
- 第五章 生物的遗传和变异
- 1 生物的遗传
- 2 生物的变异
- 第六章 能源与社会
- 1 能源和能源的分类
- 2 太阳能的利用
- 3 核能的开发与放射性防护
- 4 新能源与可持续发展
- 第七章 科学与社会发展
- 1 科学就是力量
- 2 科学推动技术发展
- 3 科学技术推动经济增长
- 4 科学技术与可持续发展
