华师大版九年级科学下册 第3章质量评估试卷(含答案)
文档属性
| 名称 | 华师大版九年级科学下册 第3章质量评估试卷(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 452.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2020-04-03 00:00:00 | ||
图片预览




文档简介
第3章质量评估试卷[学生用书活页P131]
[时间:60分钟 分值:120分]
一、选择题(每题2分,共30分)
1.[金华]“浙中生态廊道”不仅是深化金华“五水共治”的新战场,也是一条集生态保护、休闲观光、文化体验于一体的“山水林田湖”生命共同体。下列关于“浙中生态廊道”的叙述不合理的是( B )
A.有利于治理水污染
B.可以杜绝酸雨的形成
C.有利于治理雾霾污染
D.有利于保护水域生态系统
2.温室效应主要是由于大气中哪种气体含量增加所致( B )
A.NO2 B.CO2 C.SO2 D.氟利昂
3.下列各组物质中,都属于金属氧化物的是( A )
A.氧化钾、氧化铁、氧化铜
B.氧化钾、氢氧化钠、氧化铁
C.氧化银、氧化钠、氧气
D.氧化钠、二氧化碳、一氧化碳
4.下列说法中正确的是( A )
A.碱的组成中一定含有氢、氧两种元素
B.金属都可以与盐酸反应生成盐和氢气
C.铁与氧气反应一定生成四氧化三铁
D.含有金属元素和氧元素的化合物一定是金属氧化物
5.下列物质间的转化,不能一步实现的是( B )
A.CO2→H2CO3
B.CuO→Cu(OH)2
C.H2CO3→CO2
D.Cu(OH)2→CuO
6.关于下列物质的转化过程:H2→H2O,CO →CO2,C→ CO2说法不正确的是( B )
A.都能通过化合反应实现
B.都能通过置换反应实现
C.都能通过和单质反应实现
D.变化前后都有元素化合价改变
7.铁、稀硫酸、石灰水和氯化铜溶液之间的反应关系如图所示,图中两圆相交部分(A、B、C、D)表示物质间反应的类型或主要实验现象。下列说法错误的是( D )
图1
A.A处发生置换反应 B.B处发生复分解反应
C.C处产生气泡 D.D处生成白色沉淀
8.下列对反应X+3NaOH===3Y+Fe(OH)3↓的分析,错误的是( B )
A.X中含有三价元素
B.X可能是Fe2(SO4)3
C.Y中一定含有Na元素
D.Y可能是NaNO3
9.把足量的铁粉分别投入到各组物质的溶液中,充分反应后过滤,滤液中只有一种溶质的是( B )
A.Na2SO4和CuSO4
B.H2SO4 和 CuSO4
C.HCl 和H2SO4
D.CuCl2 和 Cu(NO3)2
10.下列物质的转化能实现的是( A )
A.H2SO4HCl
B.CONa2CO3
C.Cu(OH)2NaOH
D.NaNO3Ba(NO3)2
11.相同质量的下列物质分别溶于等质量的水中,所得溶液中溶质的质量分数最大的是( A )
A.Na2O
B.NaOH
C.CuSO4·5H2O
D.H2SO4
12.[2018·杭州]如图为氢气还原氧化铜的实验装置图,下列有关分析正确的是( B )
图2
A.装置中试管口需略向下倾斜,主要是为了利于通入氢气
B.在给试管内药品加热前,需先通氢气排尽试管内的空气
C.待药品完全反应后,需同时撤去酒精灯和通氢气的导管
D.该实验装置也可直接用于一氧化碳还原氧化铜的实验
13.把6g碳在24g氧气中充分燃烧,生成二氧化碳的质量是( B )
A.30g
B.22g
C.32g
D.44g
14. 实验室有三瓶化肥未贴标签,只知道它们分别是碳酸氢铵(NH4HCO3)、氯化铵(NH4Cl)和尿素[CO(NH2)2]中的一种。为鉴别三种化肥,某同学分别取少量样品编号为A、B、C,并进行如图实验(此处箭头表示得出实验结论)。根据实验,下列说法中不正确的是( D )
图3
A.三种化肥中,尿素的含氮量最高
B.B物质为碳酸氢铵
C.常温下如要鉴别B、C两种样品,能采取闻气味的方法
D.如果实验Ⅱ中B、C两种样品没有另取,则会使检验结果不准确
【解析】NH4Cl中氮元素的质量分数为×100%≈26.2%;NH4HCO3中氮元素的质量分数为×100%≈17.7%;CO(NH2)2中氮元素的质量分数为×100%≈46.7%;因为碳酸氢铵与盐酸反应产生氯化铵、水、二氧化碳,氯化铵与盐酸不反应,所以B物质为碳酸氢铵且只要含有碳酸氢铵和氯化铵就能通过加入盐酸鉴别开;因为碳酸氢铵、氯化铵都是铵态氮肥,但是碳酸氢铵能分解,而氯化铵常温不分解,所以能采取闻气味的方法鉴别。
15.[2018·河南]甲、乙、丙有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去),下列各组物质按照甲、乙、丙的顺序不符合要求的是( C )
图4
A.C、CO、CO2
B.H2O2、H2O、O2
C.KOH、K2CO3、KNO3
D.Fe2O3、FeCl3、Fe(OH)3
二、填空题(每空1分,共14分)
16.某居民家中每年冬季取暖用煤约400kg,所用煤中含硫的质量分数约为1%。若其中的硫元素全部转化为二氧化硫,那么该居民家中每年冬季取暖向大气中排放约__8__kg的二氧化硫。
17.[2018·金华]A、B、C、D是初中科学常见的四种物质,其中A、B属于相同物质类别的化合物,C、D物质类别不同,它们之间的转化和反应关系如图。图中“→”表示某一种物质经一步反应可转化为另一种物质,“-”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去。请回答:
图5
(1)若C是二氧化碳,B是氢氧化钙,则B→A的化学方程式是__Na2CO3+Ca(OH)2===CaCO3↓+2NaOH(合理即可)__。
(2)若C是锌,A和B都属于酸,写出D可能的化学式:__Na2CO3、CuO、NaOH(或其他碳酸盐、金属氧化物、碱的化学式)三种中的任意两种__(物质类别不同的两种即可)。
18.[2018·河南]A~E均为初中科学常见的物质,它们之间的关系如图所示(部分物质已经略去)已知A是目前世界上年产量最高的金属;B是胃酸的主要成分;C中金属元素的质量分数为40%,其水溶液呈蓝色,常用来配制农药波尔多液;D属于碱;E属于盐。则C的化学式为__CuSO4__;A与B反应的化学方程式为__Fe+2HCl===FeCl2+H2↑__;E转化为D的化学方程式为__Na2CO3+Ca(OH)2=== CaCO3↓+2NaOH(合理即可)__。
图6
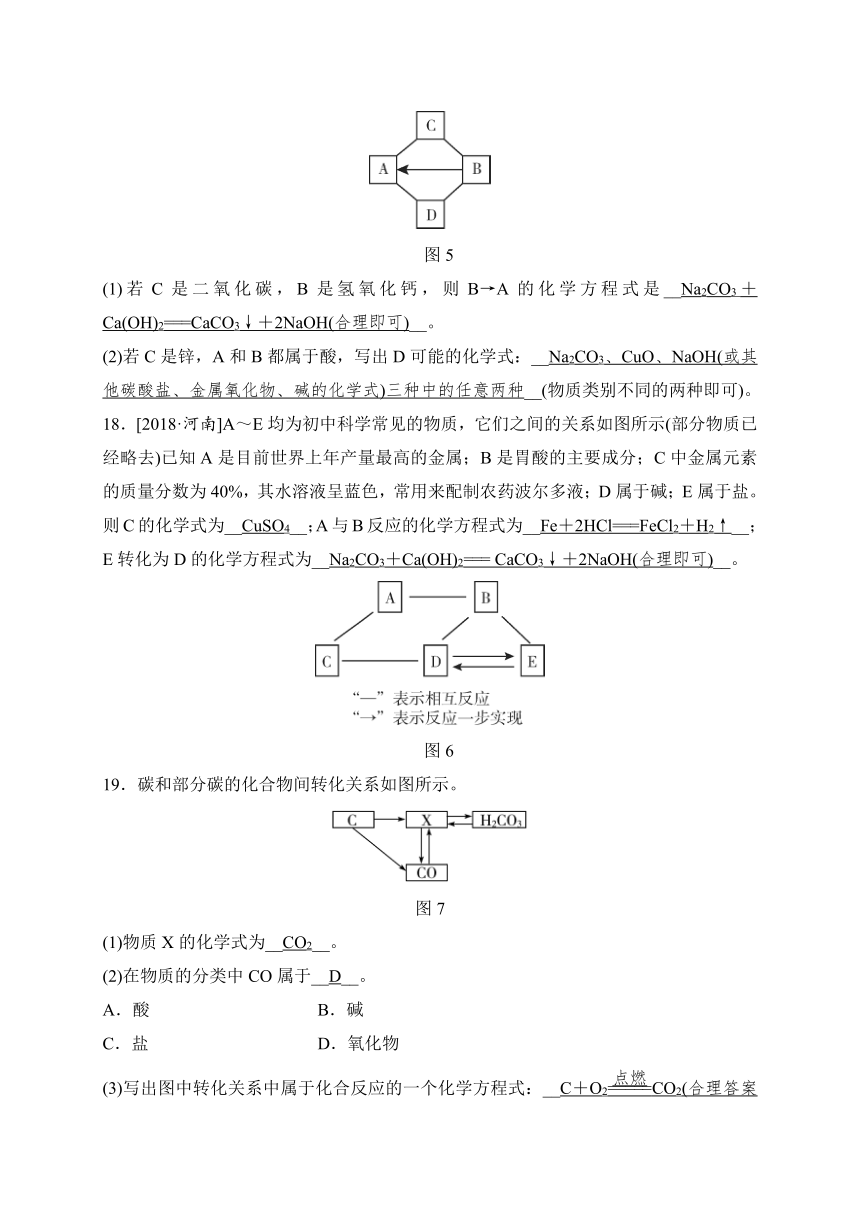
19.碳和部分碳的化合物间转化关系如图所示。
图7
(1)物质X的化学式为__CO2__。
(2)在物质的分类中CO属于__D__。
A.酸 B.碱
C.盐 D.氧化物
(3)写出图中转化关系中属于化合反应的一个化学方程式:__C+O2CO2(合理答案均可)__。
20.下列是初中科学中常见的一些物质:铁、氢气、氧化铜、二氧化碳、硫酸、氢氧化钠、氯化铜。它们进行击鼓传花游戏,条件是相互之间能发生反应就可以进行传递。请把上述物质分别安排在A~G的位置上,使花束能从A传到G。其中A的固体俗称干冰。请回答:
图8
(1)氢氧化钠应放在位置__B__上。
(2)C和D反应的化学方程式为__Fe+CuCl2===FeCl2+Cu__,反应类型为__置换__反应。上述物质除了发生从A到G的化学反应外,常温下还能相互发生化学反应的是__硫酸和氢氧化钠__。
(3)当G换成另一个同类别物质时就能将花传回起点A,它是__碳__(填名称)。
三、实验探究题(每空2分,共50分)
21.如图甲是氢气和氧化铜反应的实验,图乙是木炭和氧化铁反应的实验。
图9
(1)在上述两个实验中,氢气和木炭表现出相同的化学性质是__还原__性。
(2)实验步骤的先后次序非常重要,比如甲实验中,反应前必须先通氢气后点燃酒精灯,否则易发生爆炸;反应结束后必须先__熄灭酒精灯__后__停止通氢气__,否则生成的红色的铜会变成黑色。
(3)某同学正确操作做完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶地发现黑色粉末没有溶解,试管中也未产生预期的气泡,这说明该反应并没有生成__Fe__。
(4)该同学查阅资料,得到铁的氧化物的部分信息见表:
铁的氧化物化学式
Fe2O3
Fe3O4
FeO
颜色
红
黑
黑
化学性质
可溶于酸
常温下不溶于稀酸
可溶于酸
根据以上信息,试写出乙实验试管中反应的化学方程式:__C+6Fe2O34Fe3O4+CO2↑__。
经分析后,该同学试着提高反应温度后,实验出现了预期的现象。
22.[2018·扬州]空气是宝贵的自然资源,如图是以空气等为原料合成尿素[CO(NH2)2]的流程。请按要求回答相关问题:
图10
(1)X是空气中含量最多的气体,其分子式为__N2__。
(2)实验室用大理石和稀盐酸制取二氧化碳的化学方程式为__CaCO3+2HCl ===CaCl2+H2O+CO2↑__。
(3)①天然气的主要成分是CH4,点燃CH4之前应__检验甲烷的纯度__。8g CH4完全燃烧消耗32g O2,生成a g CO2和18g H2O,则a=__22__。
②由CH4在该流程中的作用表明:化学反应中发生物质变化的同时也会伴随有__能量__变化(选填“能量”或“原子个数”)。
(4)尿素属于__氮肥__(选填“氮肥”“磷肥”或“钾肥”);写出NH3合成尿素的化学反应方程式:__CO2+2NH3CO(NH2)2+H2O__。
23.为确定木炭还原氧化铜后的固体成分,请你与兴趣小组的同学完成以下探究。
【对固体猜想】
猜想Ⅰ:全部是金属铜;
猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭;
猜想Ⅳ:除铜外,还含有氧化铜、__木炭__。
【进行实验】实验流程见图:
图11
【问题与讨论】
(1)步骤②包括溶解、过滤两步操作,它们共同用到的玻璃仪器是烧杯、__玻璃棒__。
(2)C的化学式为__CO2__,D的化学式为__CuO__,由此推出固体B中含有__C和Cu__(填化学式),步骤④发生反应的化学方程式为__CuO+H2SO4===CuSO4+H2O__。
(3)结合(2)的结论推断:如果溶液A显蓝色,则溶液A的溶质的化学式为__CuSO4__,说明样品中含有__氧化铜(或CuO)__,则证明猜想__Ⅳ__成立;如果溶液A无色,则证明猜想__Ⅲ__成立。
24.[2017·湖州]科学课上,老师告诉学生“能发生复分解反应的两种盐通常是可溶的”。有“通常”就有“例外”,能否找到某些可溶性盐和难溶性盐发生复分解反应的证据呢?科学兴趣小组进行了探究。
【查阅资料】
①水溶液中的复分解反应一般朝着溶液中离子浓度(单位体积溶液中离子数目的多少)减小的方向进行。
②了解到某些难溶性盐的溶解能力和颜色。
【实验取证】取一支试管,加入少量AgNO3溶液,再加入过量NaCl溶液,有白色沉淀生成。再往该试管中加入少量KI溶液,白色沉淀转化为黄色沉淀。
【分析讨论】
(1)为什么要加入过量的NaCl溶液?请说明理由:__若AgNO3过量,AgI沉淀可能是过量AgNO3与KI反应生成的,无法说明AgI是由AgCl反应得到的__。
(2)写出加入少量KI溶液后发生反应的化学方程式:__KI+AgCl===AgI↓+KCl__。
(3)该反应能发生的原因是AgI在水中的溶解能力__小于__AgCl(选填“大于”“等于”或“小于”)。
【得出结论】某些可溶性盐和难溶性盐之间能发生复分解反应。
四、解答题(25、26题各7分,27题12分,共26分)
25.实验室有一瓶由氯化钾和硝酸钾组成的化肥,但标注的质量分数已模糊不清,小明想通过实验重新标注,以下是他进行的实验步骤:
①取10g样品于烧杯中,加入蒸馏水充分溶解,配制成60g溶液;
②在配制的溶液中,加入一定量的硝酸银溶液,恰好完全反应;
③将上述混合液过滤,沉淀经洗涤、干燥后,称得质量为14.35g。
请根据上述实验回答:(相关反应的化学方程式为KCl+AgNO3===AgCl↓+KNO3)
(1)在过滤操作中使用的玻璃仪器有:烧杯、__漏斗__和玻璃棒。
(2)样品中氯化钾的质量分数为多少?(要求列式计算)
(3)完全反应后,混合液中的硝酸钾质量是多少克?
(4)为了回收硝酸钾,小明对滤液进行蒸发、结晶、称量,发现所得的晶体质量小于计算得出的理论值。造成这种结果的原因可能是__BC__(填字母)。
A.晶体没有干燥
B.蒸发时液体飞溅
C.硝酸钾残留在玻璃棒上
【答案】(2)设样品中氯化钾的质量为x。
KCl+AgNO3===AgCl↓+KNO3
74.5 143.5
x 14.35g
=,x=7.45g,
氯化钾的质量分数=×100%=74.5%。
(3)设恰好完全反应时,生成的硝酸钾质量是y。
KCl+AgNO3===AgCl↓+KNO3
143.5 101
14.35g y
=,y=10.1g,
混合液中的硝酸钾质量=10g-7.45g+10.1g=12.65g。
26.[2018·衢州]科学家尝试通过多种途径减少CO2的排放,或将CO2转化为有用的物质。其中一种途径是利用NaOH溶液来“捕捉”CO2,并将CO2储存或利用,反应流程如图所示。
反应流程图
图12
(1)反应分离室中分离物质的操作是__过滤__。
(2)上述反应流程中,可循环利用的物质是__NaOH和CaO__。
(3)若反应分离室中有溶质质量分数为10.6%的Na2CO3溶液100kg,求完全反应后,理论上可生成CaCO3的质量(要求根据化学方程式计算)。
【答案】(3)设理论上可生成CaCO3质量为x。
Ca(OH)2+Na2CO3===2NaOH+CaCO3↓
106 100
100kg×10.6% x
=,x=10kg。
27.[2017·绍兴]某白色粉末,可能含有硫酸钠、硫酸铜、氯化钠、硝酸钡、碳酸钙中的一种或几种。某科学兴趣小组为探究其成分,设计了如下实验流程(所加试剂均足量)。
图13
(1)操作Ⅰ、Ⅱ的名称是__过滤__。
(2)无色气体的质量是__2.2__g。
(3)固体甲的成分是__碳酸钙与硫酸钡__。
(4)这种白色粉末中一定不含有__硫酸铜__。
(5)求白色粉末中肯定含有的物质总质量。
【解析】(5)设参加反应的碳酸钙质量为x,则
CaCO3CaO+CO2↑
100 44
x 2.2g
=,x=5g;
设滴加Ba(NO3)2溶液后参加反应的硫酸钠质量为y,则
Na2SO4+Ba(NO3)2===BaSO4↓+2NaNO3
142 233
y 4.66g
=,y=2.84g;
设白色粉末加水溶解后参加反应的硫酸钠质量为z,硝酸钡的质量为w,则
Na2SO4+Ba(NO3)2===BaSO4↓+2NaNO3
142 261 233
z w 2.33g
==,z=1.42g,w=2.61g,
白色粉末中肯定含有的物质总质量为2.61g+1.42g+2.84g+5g=11.87g。
[时间:60分钟 分值:120分]
一、选择题(每题2分,共30分)
1.[金华]“浙中生态廊道”不仅是深化金华“五水共治”的新战场,也是一条集生态保护、休闲观光、文化体验于一体的“山水林田湖”生命共同体。下列关于“浙中生态廊道”的叙述不合理的是( B )
A.有利于治理水污染
B.可以杜绝酸雨的形成
C.有利于治理雾霾污染
D.有利于保护水域生态系统
2.温室效应主要是由于大气中哪种气体含量增加所致( B )
A.NO2 B.CO2 C.SO2 D.氟利昂
3.下列各组物质中,都属于金属氧化物的是( A )
A.氧化钾、氧化铁、氧化铜
B.氧化钾、氢氧化钠、氧化铁
C.氧化银、氧化钠、氧气
D.氧化钠、二氧化碳、一氧化碳
4.下列说法中正确的是( A )
A.碱的组成中一定含有氢、氧两种元素
B.金属都可以与盐酸反应生成盐和氢气
C.铁与氧气反应一定生成四氧化三铁
D.含有金属元素和氧元素的化合物一定是金属氧化物
5.下列物质间的转化,不能一步实现的是( B )
A.CO2→H2CO3
B.CuO→Cu(OH)2
C.H2CO3→CO2
D.Cu(OH)2→CuO
6.关于下列物质的转化过程:H2→H2O,CO →CO2,C→ CO2说法不正确的是( B )
A.都能通过化合反应实现
B.都能通过置换反应实现
C.都能通过和单质反应实现
D.变化前后都有元素化合价改变
7.铁、稀硫酸、石灰水和氯化铜溶液之间的反应关系如图所示,图中两圆相交部分(A、B、C、D)表示物质间反应的类型或主要实验现象。下列说法错误的是( D )
图1
A.A处发生置换反应 B.B处发生复分解反应
C.C处产生气泡 D.D处生成白色沉淀
8.下列对反应X+3NaOH===3Y+Fe(OH)3↓的分析,错误的是( B )
A.X中含有三价元素
B.X可能是Fe2(SO4)3
C.Y中一定含有Na元素
D.Y可能是NaNO3
9.把足量的铁粉分别投入到各组物质的溶液中,充分反应后过滤,滤液中只有一种溶质的是( B )
A.Na2SO4和CuSO4
B.H2SO4 和 CuSO4
C.HCl 和H2SO4
D.CuCl2 和 Cu(NO3)2
10.下列物质的转化能实现的是( A )
A.H2SO4HCl
B.CONa2CO3
C.Cu(OH)2NaOH
D.NaNO3Ba(NO3)2
11.相同质量的下列物质分别溶于等质量的水中,所得溶液中溶质的质量分数最大的是( A )
A.Na2O
B.NaOH
C.CuSO4·5H2O
D.H2SO4
12.[2018·杭州]如图为氢气还原氧化铜的实验装置图,下列有关分析正确的是( B )
图2
A.装置中试管口需略向下倾斜,主要是为了利于通入氢气
B.在给试管内药品加热前,需先通氢气排尽试管内的空气
C.待药品完全反应后,需同时撤去酒精灯和通氢气的导管
D.该实验装置也可直接用于一氧化碳还原氧化铜的实验
13.把6g碳在24g氧气中充分燃烧,生成二氧化碳的质量是( B )
A.30g
B.22g
C.32g
D.44g
14. 实验室有三瓶化肥未贴标签,只知道它们分别是碳酸氢铵(NH4HCO3)、氯化铵(NH4Cl)和尿素[CO(NH2)2]中的一种。为鉴别三种化肥,某同学分别取少量样品编号为A、B、C,并进行如图实验(此处箭头表示得出实验结论)。根据实验,下列说法中不正确的是( D )
图3
A.三种化肥中,尿素的含氮量最高
B.B物质为碳酸氢铵
C.常温下如要鉴别B、C两种样品,能采取闻气味的方法
D.如果实验Ⅱ中B、C两种样品没有另取,则会使检验结果不准确
【解析】NH4Cl中氮元素的质量分数为×100%≈26.2%;NH4HCO3中氮元素的质量分数为×100%≈17.7%;CO(NH2)2中氮元素的质量分数为×100%≈46.7%;因为碳酸氢铵与盐酸反应产生氯化铵、水、二氧化碳,氯化铵与盐酸不反应,所以B物质为碳酸氢铵且只要含有碳酸氢铵和氯化铵就能通过加入盐酸鉴别开;因为碳酸氢铵、氯化铵都是铵态氮肥,但是碳酸氢铵能分解,而氯化铵常温不分解,所以能采取闻气味的方法鉴别。
15.[2018·河南]甲、乙、丙有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去),下列各组物质按照甲、乙、丙的顺序不符合要求的是( C )
图4
A.C、CO、CO2
B.H2O2、H2O、O2
C.KOH、K2CO3、KNO3
D.Fe2O3、FeCl3、Fe(OH)3
二、填空题(每空1分,共14分)
16.某居民家中每年冬季取暖用煤约400kg,所用煤中含硫的质量分数约为1%。若其中的硫元素全部转化为二氧化硫,那么该居民家中每年冬季取暖向大气中排放约__8__kg的二氧化硫。
17.[2018·金华]A、B、C、D是初中科学常见的四种物质,其中A、B属于相同物质类别的化合物,C、D物质类别不同,它们之间的转化和反应关系如图。图中“→”表示某一种物质经一步反应可转化为另一种物质,“-”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去。请回答:
图5
(1)若C是二氧化碳,B是氢氧化钙,则B→A的化学方程式是__Na2CO3+Ca(OH)2===CaCO3↓+2NaOH(合理即可)__。
(2)若C是锌,A和B都属于酸,写出D可能的化学式:__Na2CO3、CuO、NaOH(或其他碳酸盐、金属氧化物、碱的化学式)三种中的任意两种__(物质类别不同的两种即可)。
18.[2018·河南]A~E均为初中科学常见的物质,它们之间的关系如图所示(部分物质已经略去)已知A是目前世界上年产量最高的金属;B是胃酸的主要成分;C中金属元素的质量分数为40%,其水溶液呈蓝色,常用来配制农药波尔多液;D属于碱;E属于盐。则C的化学式为__CuSO4__;A与B反应的化学方程式为__Fe+2HCl===FeCl2+H2↑__;E转化为D的化学方程式为__Na2CO3+Ca(OH)2=== CaCO3↓+2NaOH(合理即可)__。
图6
19.碳和部分碳的化合物间转化关系如图所示。
图7
(1)物质X的化学式为__CO2__。
(2)在物质的分类中CO属于__D__。
A.酸 B.碱
C.盐 D.氧化物
(3)写出图中转化关系中属于化合反应的一个化学方程式:__C+O2CO2(合理答案均可)__。
20.下列是初中科学中常见的一些物质:铁、氢气、氧化铜、二氧化碳、硫酸、氢氧化钠、氯化铜。它们进行击鼓传花游戏,条件是相互之间能发生反应就可以进行传递。请把上述物质分别安排在A~G的位置上,使花束能从A传到G。其中A的固体俗称干冰。请回答:
图8
(1)氢氧化钠应放在位置__B__上。
(2)C和D反应的化学方程式为__Fe+CuCl2===FeCl2+Cu__,反应类型为__置换__反应。上述物质除了发生从A到G的化学反应外,常温下还能相互发生化学反应的是__硫酸和氢氧化钠__。
(3)当G换成另一个同类别物质时就能将花传回起点A,它是__碳__(填名称)。
三、实验探究题(每空2分,共50分)
21.如图甲是氢气和氧化铜反应的实验,图乙是木炭和氧化铁反应的实验。
图9
(1)在上述两个实验中,氢气和木炭表现出相同的化学性质是__还原__性。
(2)实验步骤的先后次序非常重要,比如甲实验中,反应前必须先通氢气后点燃酒精灯,否则易发生爆炸;反应结束后必须先__熄灭酒精灯__后__停止通氢气__,否则生成的红色的铜会变成黑色。
(3)某同学正确操作做完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶地发现黑色粉末没有溶解,试管中也未产生预期的气泡,这说明该反应并没有生成__Fe__。
(4)该同学查阅资料,得到铁的氧化物的部分信息见表:
铁的氧化物化学式
Fe2O3
Fe3O4
FeO
颜色
红
黑
黑
化学性质
可溶于酸
常温下不溶于稀酸
可溶于酸
根据以上信息,试写出乙实验试管中反应的化学方程式:__C+6Fe2O34Fe3O4+CO2↑__。
经分析后,该同学试着提高反应温度后,实验出现了预期的现象。
22.[2018·扬州]空气是宝贵的自然资源,如图是以空气等为原料合成尿素[CO(NH2)2]的流程。请按要求回答相关问题:
图10
(1)X是空气中含量最多的气体,其分子式为__N2__。
(2)实验室用大理石和稀盐酸制取二氧化碳的化学方程式为__CaCO3+2HCl ===CaCl2+H2O+CO2↑__。
(3)①天然气的主要成分是CH4,点燃CH4之前应__检验甲烷的纯度__。8g CH4完全燃烧消耗32g O2,生成a g CO2和18g H2O,则a=__22__。
②由CH4在该流程中的作用表明:化学反应中发生物质变化的同时也会伴随有__能量__变化(选填“能量”或“原子个数”)。
(4)尿素属于__氮肥__(选填“氮肥”“磷肥”或“钾肥”);写出NH3合成尿素的化学反应方程式:__CO2+2NH3CO(NH2)2+H2O__。
23.为确定木炭还原氧化铜后的固体成分,请你与兴趣小组的同学完成以下探究。
【对固体猜想】
猜想Ⅰ:全部是金属铜;
猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭;
猜想Ⅳ:除铜外,还含有氧化铜、__木炭__。
【进行实验】实验流程见图:
图11
【问题与讨论】
(1)步骤②包括溶解、过滤两步操作,它们共同用到的玻璃仪器是烧杯、__玻璃棒__。
(2)C的化学式为__CO2__,D的化学式为__CuO__,由此推出固体B中含有__C和Cu__(填化学式),步骤④发生反应的化学方程式为__CuO+H2SO4===CuSO4+H2O__。
(3)结合(2)的结论推断:如果溶液A显蓝色,则溶液A的溶质的化学式为__CuSO4__,说明样品中含有__氧化铜(或CuO)__,则证明猜想__Ⅳ__成立;如果溶液A无色,则证明猜想__Ⅲ__成立。
24.[2017·湖州]科学课上,老师告诉学生“能发生复分解反应的两种盐通常是可溶的”。有“通常”就有“例外”,能否找到某些可溶性盐和难溶性盐发生复分解反应的证据呢?科学兴趣小组进行了探究。
【查阅资料】
①水溶液中的复分解反应一般朝着溶液中离子浓度(单位体积溶液中离子数目的多少)减小的方向进行。
②了解到某些难溶性盐的溶解能力和颜色。
【实验取证】取一支试管,加入少量AgNO3溶液,再加入过量NaCl溶液,有白色沉淀生成。再往该试管中加入少量KI溶液,白色沉淀转化为黄色沉淀。
【分析讨论】
(1)为什么要加入过量的NaCl溶液?请说明理由:__若AgNO3过量,AgI沉淀可能是过量AgNO3与KI反应生成的,无法说明AgI是由AgCl反应得到的__。
(2)写出加入少量KI溶液后发生反应的化学方程式:__KI+AgCl===AgI↓+KCl__。
(3)该反应能发生的原因是AgI在水中的溶解能力__小于__AgCl(选填“大于”“等于”或“小于”)。
【得出结论】某些可溶性盐和难溶性盐之间能发生复分解反应。
四、解答题(25、26题各7分,27题12分,共26分)
25.实验室有一瓶由氯化钾和硝酸钾组成的化肥,但标注的质量分数已模糊不清,小明想通过实验重新标注,以下是他进行的实验步骤:
①取10g样品于烧杯中,加入蒸馏水充分溶解,配制成60g溶液;
②在配制的溶液中,加入一定量的硝酸银溶液,恰好完全反应;
③将上述混合液过滤,沉淀经洗涤、干燥后,称得质量为14.35g。
请根据上述实验回答:(相关反应的化学方程式为KCl+AgNO3===AgCl↓+KNO3)
(1)在过滤操作中使用的玻璃仪器有:烧杯、__漏斗__和玻璃棒。
(2)样品中氯化钾的质量分数为多少?(要求列式计算)
(3)完全反应后,混合液中的硝酸钾质量是多少克?
(4)为了回收硝酸钾,小明对滤液进行蒸发、结晶、称量,发现所得的晶体质量小于计算得出的理论值。造成这种结果的原因可能是__BC__(填字母)。
A.晶体没有干燥
B.蒸发时液体飞溅
C.硝酸钾残留在玻璃棒上
【答案】(2)设样品中氯化钾的质量为x。
KCl+AgNO3===AgCl↓+KNO3
74.5 143.5
x 14.35g
=,x=7.45g,
氯化钾的质量分数=×100%=74.5%。
(3)设恰好完全反应时,生成的硝酸钾质量是y。
KCl+AgNO3===AgCl↓+KNO3
143.5 101
14.35g y
=,y=10.1g,
混合液中的硝酸钾质量=10g-7.45g+10.1g=12.65g。
26.[2018·衢州]科学家尝试通过多种途径减少CO2的排放,或将CO2转化为有用的物质。其中一种途径是利用NaOH溶液来“捕捉”CO2,并将CO2储存或利用,反应流程如图所示。
反应流程图
图12
(1)反应分离室中分离物质的操作是__过滤__。
(2)上述反应流程中,可循环利用的物质是__NaOH和CaO__。
(3)若反应分离室中有溶质质量分数为10.6%的Na2CO3溶液100kg,求完全反应后,理论上可生成CaCO3的质量(要求根据化学方程式计算)。
【答案】(3)设理论上可生成CaCO3质量为x。
Ca(OH)2+Na2CO3===2NaOH+CaCO3↓
106 100
100kg×10.6% x
=,x=10kg。
27.[2017·绍兴]某白色粉末,可能含有硫酸钠、硫酸铜、氯化钠、硝酸钡、碳酸钙中的一种或几种。某科学兴趣小组为探究其成分,设计了如下实验流程(所加试剂均足量)。
图13
(1)操作Ⅰ、Ⅱ的名称是__过滤__。
(2)无色气体的质量是__2.2__g。
(3)固体甲的成分是__碳酸钙与硫酸钡__。
(4)这种白色粉末中一定不含有__硫酸铜__。
(5)求白色粉末中肯定含有的物质总质量。
【解析】(5)设参加反应的碳酸钙质量为x,则
CaCO3CaO+CO2↑
100 44
x 2.2g
=,x=5g;
设滴加Ba(NO3)2溶液后参加反应的硫酸钠质量为y,则
Na2SO4+Ba(NO3)2===BaSO4↓+2NaNO3
142 233
y 4.66g
=,y=2.84g;
设白色粉末加水溶解后参加反应的硫酸钠质量为z,硝酸钡的质量为w,则
Na2SO4+Ba(NO3)2===BaSO4↓+2NaNO3
142 261 233
z w 2.33g
==,z=1.42g,w=2.61g,
白色粉末中肯定含有的物质总质量为2.61g+1.42g+2.84g+5g=11.87g。
同课章节目录
- 第一章 宇宙的起源与演化
- 1 我们的宇宙
- 2 热大爆炸宇宙模型
- 3 恒星的一生
- 4 星际航行和空间技术
- 第二章 地球的演化和生物圈的形成
- 1 地球的演化
- 2 生命起源
- 3 生物进化
- 4 生态平衡
- 第三章 物质的转化和元素的循环
- 1 物质的转化
- 2 自然界中的碳循环和氧循环
- 3 自然界中的氮循环
- 第四章 健康与保健
- 1 健康、亚健康和疾病
- 2 运动与健康
- 3 免疫与健康
- 4 营养与健康
- 5 卫生与健康
- 6 环境与健康
- 第五章 生物的遗传和变异
- 1 生物的遗传
- 2 生物的变异
- 第六章 能源与社会
- 1 能源和能源的分类
- 2 太阳能的利用
- 3 核能的开发与放射性防护
- 4 新能源与可持续发展
- 第七章 科学与社会发展
- 1 科学就是力量
- 2 科学推动技术发展
- 3 科学技术推动经济增长
- 4 科学技术与可持续发展
