化合反应和分解反应习题(课件 22张ppt)
文档属性
| 名称 | 化合反应和分解反应习题(课件 22张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2020-04-04 00:00:00 | ||
图片预览








文档简介
课件22张PPT。第2节 化合反应和分解反应第一章 化学反应 华师版 九年级答案显示习题链接ACCA、C、E;B、D(1)大(2)遵守(3)2HgO=====2Hg+O2↑;分解反应AC(1)1:2(2)3;可能(3)化合反应△答案显示习题链接A(1)3.4 g (2)分解反应 (3)22:9放热;确保铁粉完全参加反应;Fe+S=====FeS(1)水雾(2)石灰水变浑浊;Ca(OH)2+CO2===CaCO3↓+H2O (3)Na2CO3;质量守恒定律都是分解反应;生成物中都有二氧化碳;生成物均为氧化物(合理即可)△1.工业上将赤铁矿冶炼成铁是一个复杂的过程,炼铁高炉中主要发生了下列反应:
①C+O2=====CO2 ②CO2+C=====2CO
③CaCO3=====CaO+CO2↑
④Fe2O3+3CO=====2Fe+3CO2
其中属于化合反应的是( )
A.①和② B.②和③ C.③和④ D.①和④A高温高温高温高温2.(中考?扬州)自然界中的物质大多数是化合物,下列物质属于氧化物的是( )
A.KCl B.CuSO4
C.MnO2 D.HNO3C【 解析】根据氧化物的概念:氧化物是只含有两种元素且其中一种元素是氧元素的化合物。3.(中考?淮安)下列化学反应中属于分解反应的是( )
A.NH3+H2O+CO2===NH4HCO3
B.2Al+3H2SO4===Al2(SO4)3+3H2↑
C.2KMnO4=====K2MnO4+MnO2+O2↑
D.CuSO4+Ca(OH)2===CaSO4+Cu(OH)2↓C△4.以下各反应中,属于化合反应的是___________,属于分解反应的是__________。
A.铁+氧气――→四氧化三铁
B.氯酸钾―――→氯化钾+氧气
C.磷+氧气――→五氧化二磷
D.高锰酸钾――→锰酸钾+二氧化锰+氧气
E.二氧化碳+碳――→一氧化碳A、C、EB、D点燃点燃二氧化锰加热加热高温5.某同学在敞口容器中做了两个实验:一是氧化汞(HgO)受热分解生成汞和氧气;二是铝粉在氧气中燃烧生成固体氧化铝。他准确称量了反应前后容器及所盛物质的质量,发现反应前后质量都发生了变化。请填空:
(1)铝粉燃烧生成氧化铝的质量比参加反应的铝粉的质量________(填“大”“小”或“不变”)。
(2)你认为这两个反应是否遵守质量守恒定律?________________(填“遵守”或“不遵守”)。
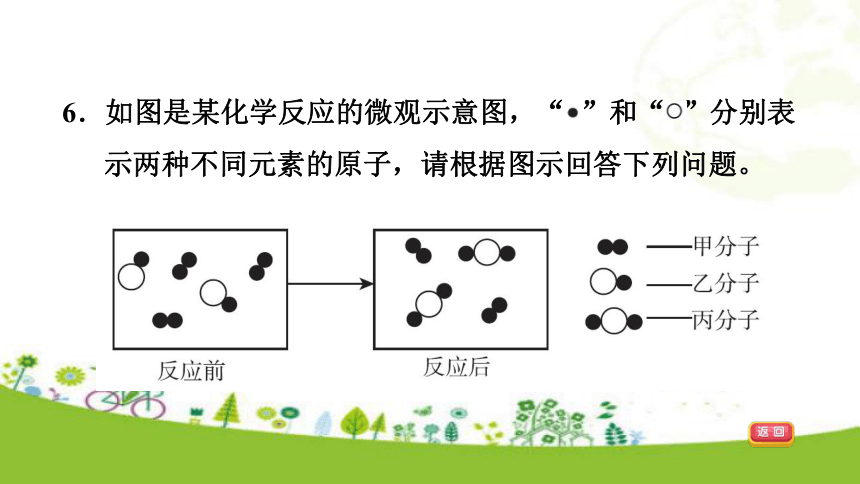
(3)请写出氧化汞受热分解的化学方程式:______________________,该反应的基本反应类型是__________。大遵守2HgO=====2Hg+O2↑分解反应△6.如图是某化学反应的微观示意图,“ ”和“ ”分别表示两种不同元素的原子,请根据图示回答下列问题。6.如图是某化学反应的微观示意图,“ ”和“ ”分别表示两种不同元素的原子,请根据图示回答下列问题。
(1)参加反应的甲和乙的分子个数比是________。
(2)1个丙分子由________个原子构成; 由大量丙分子聚集成的丙物质__________(填“可能”或“不可能”)是氧化物。
(3)该反应的基本反应类型是________________。1:23 化合反应可能7.(中考?邵阳)下列各图中,“ ”和“ ”分别表示两种不同元素的原子,其中可表示氧化物的是( ) A【 解析】氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素,A可能表示氧化物。8.(中考?雅安)如图为某化学反应的微观示意图,图中“ ”表示硫原子,“ ”表示氧原子。下列说法中错误的是( )
A.甲是SO2 B.该反应属于化合反应
C.反应前后,分子种类、原子种类均不变
D.反应中,甲、乙、丙三种物质的分子个数比为2:1:2 C9.(中考?泰安)下列图示是化学概念之间关系的形象表示,其中不正确的是( )【 解析】混合物是由两种或两种以上的物质组成的;纯净物是由一种物质组成的。纯净物又分为单质和化合物,故A错误。【答案】A10.一定条件下,下列物质在密闭容器内充分反应,反应前后各物质的质量如下:
则:
(1)反应后A的待测质量为___________。
(2)该反应所属的基本反应类型是___________。
(3)反应中B和D两种物质变化的质量比为___________。【 解析】(1)根据质量守恒定律可知,反应后A的待测质量为(1.7 g+2.2 g+7.9 g+0.9 g)-(6.6 g+2.7 g)=3.4 g;由表中的数据可知:反应后A的质量增加,是生成物;反应后B的质量增加,是生成物,增加了6.6 g-2.2 g=4.4 g;反应后C的质量减少,是反应物,减少了7.9 g;反应后D的质量增加,是生成物,增加了2.7 g-0.9 g=1.8 g;该反应的反应物是一种,生成物是三种,因此该反应所属的基本反应类型是分解反应;反应中B和D两种物质变化的质量比为4.4 g:1.8 g=22:9。【答案】(1)3.4 g (2)分解反应 (3)22:911.(中考?嘉兴)如图所示是某同学对“铁粉和硫反应”所做的改进实验,用烧红的玻璃棒接触纸筒后混合物剧烈反应,玻璃棒移开后反应继续进行直至底部,由此可知该反应是一个__________(填“吸热”或“放热”)反应,为确保冷却后的生成物不能被磁铁吸引,实验中的硫粉要稍过量,目的是______________________。写出该反应的化学方程式____________________________。11.(中考?嘉兴)如图所示是某同学对“铁粉和硫反应”所做的改进实验,用烧红的玻璃棒接触纸筒后混合物剧烈反应,玻璃棒移开后反应继续进行直至底部,由此可知该反应是一个__________(填“吸热”或“放热”)反应,为确保冷却后的生成物不能被磁铁吸引,实验中的硫粉要稍过量,目的是______________________。写出该反应的化学方程式____________________________。放热确保铁粉完全参加反应Fe+S=====FeS△12.碳酸氢钠常用于食品和医药工业,某兴趣小组对碳酸氢钠进行探究。
【查阅资料】碳酸氢钠受热易分解,生成水、二氧化碳和一种常见的固体。
【进行实验】为了验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的碳酸氢钠放到铜片上加热(碳酸氢钠不与铜反应),如图所示。(1)加热一段时间后,观察到烧杯内壁有________。
(2)充分加热后,将烧杯迅速倒转过来,倒入澄清石灰水,振荡,观察到________________,写出该反应的化学方程式____________________________________。
(3)碳酸氢钠受热分解后生成的白色固体可能是_________,作此猜想的依据是__________________。水雾石灰水变浑浊 Na2CO3Ca(OH)2+CO2===CaCO3↓+H2O质量守恒定律13.对知识的比较与归纳是学习化学的重要方法,现有以下三个化学方程式:
(1)H2CO3===H2O+CO2↑
(2)CaCO3=====CaO+CO2↑
(3)Cu2(OH)2CO3=====2CuO+H2O+CO2↑
通过比较发现它们有许多相似之处,请你写出其中的三条:________________________________________________________________________都是分解反应;生成物中都有二氧化碳;生成物均为氧化物(合理即可)高温△谢谢!
①C+O2=====CO2 ②CO2+C=====2CO
③CaCO3=====CaO+CO2↑
④Fe2O3+3CO=====2Fe+3CO2
其中属于化合反应的是( )
A.①和② B.②和③ C.③和④ D.①和④A高温高温高温高温2.(中考?扬州)自然界中的物质大多数是化合物,下列物质属于氧化物的是( )
A.KCl B.CuSO4
C.MnO2 D.HNO3C【 解析】根据氧化物的概念:氧化物是只含有两种元素且其中一种元素是氧元素的化合物。3.(中考?淮安)下列化学反应中属于分解反应的是( )
A.NH3+H2O+CO2===NH4HCO3
B.2Al+3H2SO4===Al2(SO4)3+3H2↑
C.2KMnO4=====K2MnO4+MnO2+O2↑
D.CuSO4+Ca(OH)2===CaSO4+Cu(OH)2↓C△4.以下各反应中,属于化合反应的是___________,属于分解反应的是__________。
A.铁+氧气――→四氧化三铁
B.氯酸钾―――→氯化钾+氧气
C.磷+氧气――→五氧化二磷
D.高锰酸钾――→锰酸钾+二氧化锰+氧气
E.二氧化碳+碳――→一氧化碳A、C、EB、D点燃点燃二氧化锰加热加热高温5.某同学在敞口容器中做了两个实验:一是氧化汞(HgO)受热分解生成汞和氧气;二是铝粉在氧气中燃烧生成固体氧化铝。他准确称量了反应前后容器及所盛物质的质量,发现反应前后质量都发生了变化。请填空:
(1)铝粉燃烧生成氧化铝的质量比参加反应的铝粉的质量________(填“大”“小”或“不变”)。
(2)你认为这两个反应是否遵守质量守恒定律?________________(填“遵守”或“不遵守”)。
(3)请写出氧化汞受热分解的化学方程式:______________________,该反应的基本反应类型是__________。大遵守2HgO=====2Hg+O2↑分解反应△6.如图是某化学反应的微观示意图,“ ”和“ ”分别表示两种不同元素的原子,请根据图示回答下列问题。6.如图是某化学反应的微观示意图,“ ”和“ ”分别表示两种不同元素的原子,请根据图示回答下列问题。
(1)参加反应的甲和乙的分子个数比是________。
(2)1个丙分子由________个原子构成; 由大量丙分子聚集成的丙物质__________(填“可能”或“不可能”)是氧化物。
(3)该反应的基本反应类型是________________。1:23 化合反应可能7.(中考?邵阳)下列各图中,“ ”和“ ”分别表示两种不同元素的原子,其中可表示氧化物的是( ) A【 解析】氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素,A可能表示氧化物。8.(中考?雅安)如图为某化学反应的微观示意图,图中“ ”表示硫原子,“ ”表示氧原子。下列说法中错误的是( )
A.甲是SO2 B.该反应属于化合反应
C.反应前后,分子种类、原子种类均不变
D.反应中,甲、乙、丙三种物质的分子个数比为2:1:2 C9.(中考?泰安)下列图示是化学概念之间关系的形象表示,其中不正确的是( )【 解析】混合物是由两种或两种以上的物质组成的;纯净物是由一种物质组成的。纯净物又分为单质和化合物,故A错误。【答案】A10.一定条件下,下列物质在密闭容器内充分反应,反应前后各物质的质量如下:
则:
(1)反应后A的待测质量为___________。
(2)该反应所属的基本反应类型是___________。
(3)反应中B和D两种物质变化的质量比为___________。【 解析】(1)根据质量守恒定律可知,反应后A的待测质量为(1.7 g+2.2 g+7.9 g+0.9 g)-(6.6 g+2.7 g)=3.4 g;由表中的数据可知:反应后A的质量增加,是生成物;反应后B的质量增加,是生成物,增加了6.6 g-2.2 g=4.4 g;反应后C的质量减少,是反应物,减少了7.9 g;反应后D的质量增加,是生成物,增加了2.7 g-0.9 g=1.8 g;该反应的反应物是一种,生成物是三种,因此该反应所属的基本反应类型是分解反应;反应中B和D两种物质变化的质量比为4.4 g:1.8 g=22:9。【答案】(1)3.4 g (2)分解反应 (3)22:911.(中考?嘉兴)如图所示是某同学对“铁粉和硫反应”所做的改进实验,用烧红的玻璃棒接触纸筒后混合物剧烈反应,玻璃棒移开后反应继续进行直至底部,由此可知该反应是一个__________(填“吸热”或“放热”)反应,为确保冷却后的生成物不能被磁铁吸引,实验中的硫粉要稍过量,目的是______________________。写出该反应的化学方程式____________________________。11.(中考?嘉兴)如图所示是某同学对“铁粉和硫反应”所做的改进实验,用烧红的玻璃棒接触纸筒后混合物剧烈反应,玻璃棒移开后反应继续进行直至底部,由此可知该反应是一个__________(填“吸热”或“放热”)反应,为确保冷却后的生成物不能被磁铁吸引,实验中的硫粉要稍过量,目的是______________________。写出该反应的化学方程式____________________________。放热确保铁粉完全参加反应Fe+S=====FeS△12.碳酸氢钠常用于食品和医药工业,某兴趣小组对碳酸氢钠进行探究。
【查阅资料】碳酸氢钠受热易分解,生成水、二氧化碳和一种常见的固体。
【进行实验】为了验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的碳酸氢钠放到铜片上加热(碳酸氢钠不与铜反应),如图所示。(1)加热一段时间后,观察到烧杯内壁有________。
(2)充分加热后,将烧杯迅速倒转过来,倒入澄清石灰水,振荡,观察到________________,写出该反应的化学方程式____________________________________。
(3)碳酸氢钠受热分解后生成的白色固体可能是_________,作此猜想的依据是__________________。水雾石灰水变浑浊 Na2CO3Ca(OH)2+CO2===CaCO3↓+H2O质量守恒定律13.对知识的比较与归纳是学习化学的重要方法,现有以下三个化学方程式:
(1)H2CO3===H2O+CO2↑
(2)CaCO3=====CaO+CO2↑
(3)Cu2(OH)2CO3=====2CuO+H2O+CO2↑
通过比较发现它们有许多相似之处,请你写出其中的三条:________________________________________________________________________都是分解反应;生成物中都有二氧化碳;生成物均为氧化物(合理即可)高温△谢谢!
