用分解反应制取氧气习题(课件 30张ppt)
文档属性
| 名称 | 用分解反应制取氧气习题(课件 30张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2020-04-04 00:00:00 | ||
图片预览







文档简介
课件30张PPT。第3节 用分解反应制取氧气第一章 化学反应 华师版 九年级答案显示习题链接B(1)物理变化 (2)混合物 (3)氮气BDDBC(1)锥形瓶 (2)催化作用,加快过氧化氢的分解 (3)检查装置气密性(4)2H2O2=====2H2O+O2↑;正MnO2答案显示习题链接DC(1)试管 (2)A (3)2H2O2=====2H2O+O2↑ (4)D (5)c(1)调节分液漏斗活塞,使H2O2溶液的滴加速率减慢(2)C (3)B、C (3)“用带火星的木条检验,发现木条没有复燃”,说明集气瓶内氧气的浓度较小。CMnO21.下列有关氧气的说法错误的是( )
A.空气中的氧气主要来自于植物的光合作用
B.工业上用分离液态空气的方法制取氧气是分解反应
C.用含有氧元素的物质反应才有可能产生氧气
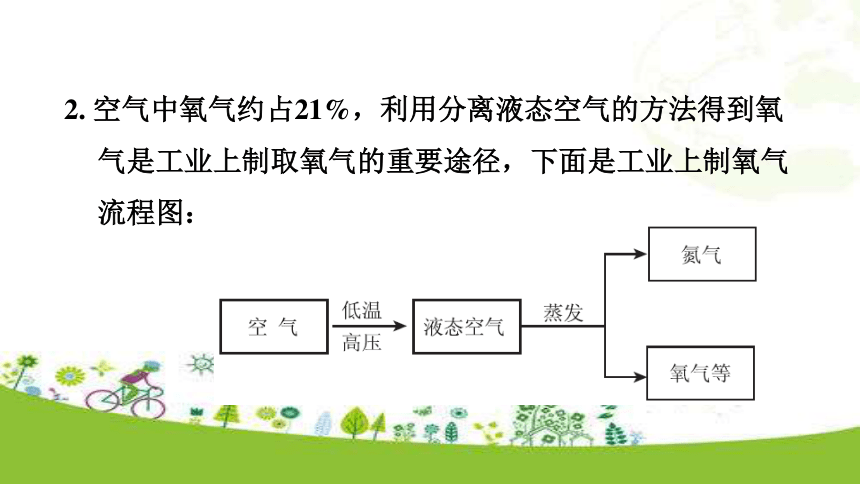
D.实验室常用加热高锰酸钾的方法制取氧气B【 解析】工业上分离液态空气制取氧气是物理变化。2. 空气中氧气约占21%,利用分离液态空气的方法得到氧气是工业上制取氧气的重要途径,下面是工业上制氧气流程图:(1)工业上分离液态空气制氧气的变化属于____________(填“物理变化”或“化学变化”)。
(2)这样制得的氧气是__________(填“纯净物”或“混合物”)。
(3)在一个标准大气压下,液氮的沸点为-196 ℃,液氧的沸点为-183 ℃,在蒸发的过程中________(填“氮气”或“氧气”)先被蒸发出来。物理变化混合物氮气3.用双氧水制取氧气时,若忘记加二氧化锰,其结果是( )
A.不放出氧气 B.放出氧气速率慢
C.放出氧气总量会减少 D.放出的氧气不纯B4.下列关于氧气的说法,错误的是( )
A.实验室制取氧气时,不一定要加催化剂
B.水中的生物能依靠溶于水中的少量氧气生存
C.通常状况下,氧气的密度略大于空气
D.氧气可以支持燃烧,说明氧气具有可燃性【 解析】氧气能支持燃烧,具有助燃性,但氧气不具有可燃性。D5.同学们在做氧气性质的实验时,将点燃的木炭伸入集气瓶内,有的现象明显,有的却不明显。导致现象不明显的原因可能是( )
A.排水法收集结束时集气瓶内有水残留
B.导管口连续放出气泡时才开始收集氧气
C.排水法收集满氧气后盖上毛玻璃片拿出水面
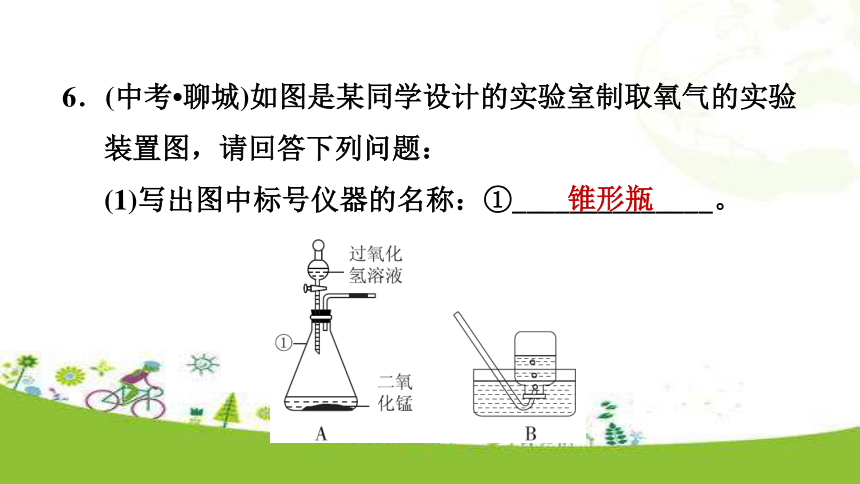
D.排水法收集氧气前未将集气瓶灌满水D6.(中考?聊城)如图是某同学设计的实验室制取氧气的实验装置图,请回答下列问题:
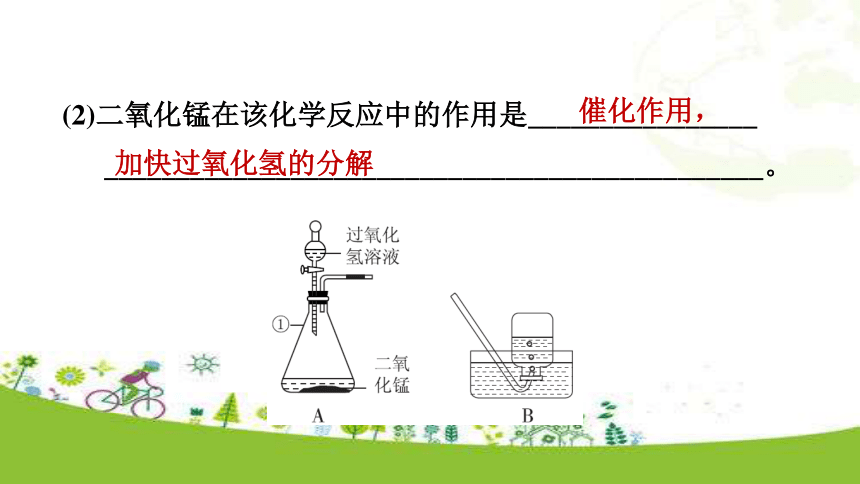
(1)写出图中标号仪器的名称:①______________。锥形瓶(2)二氧化锰在该化学反应中的作用是________________
______________________________________________。加快过氧化氢的分解催化作用,(3)组装好A装置后,该同学先向分液漏斗中加入水,然后将导管另一端浸入水中,并打开分液漏斗的活塞,观察导管口是否有连续的气泡冒出,该操作的目的是__________________。检查装置气密性(4)A装置中发生反应的化学方程式为____________________________,应将收集满氧气的集气瓶______(填“正”或“倒”)放在桌面上。正7.(中考?桂林)关于反应2KClO3=====2KCl+3O2↑的说法,错误的是( )
A.MnO2是该反应的催化剂
B.MnO2的质量在反应后减少
C.MnO2加快KClO3的分解速率
D.MnO2的化学性质在反应前后没有改变MnO2△B8.(中考?南宁)向一定溶质质量分数的过氧化氢溶液中加入少量二氧化锰,立即有大量的氧气产生,下列说法正确的是( )
A.过氧化氢中含有水和氧气
B.过氧化氢能使二氧化锰分解放出氧气
C.二氧化锰能加快过氧化氢分解生成水和氧气
D.该反应中有过氧化氢和二氧化锰两种反应物,不属于分解反应C9.(中考?福建)下列对催化剂描述正确的是( )
A.任何化学反应都需要催化剂
B.催化剂在反应前后本身的质量发生了变化
C.只有分解反应才需要催化剂
D.某些化学反应可以有多种催化剂D10.用向上排空气法收集氧气,检验氧气是否集满的最简便的方法是( )
A.看集气瓶口是否有较大气泡冒出
B.将带火星的木条伸入集气瓶中,看木条是否复燃
C.将带火星的木条伸到集气瓶口,看木条是否复燃
D.倒入澄清的石灰水,看是否变浑浊C【 解析】此题的易错点在于“1.忽略了是向上排空气法收集,而不是排水法收集;2.要验满,所以不能伸入瓶内”。11.(中考?昆明)根据下列装置图回答问题:
(1)仪器a的名称是________。试管(2)实验室用高锰酸钾制取氧气,选择的发生装置是________(填标号)。A(3)实验室还可用过氧化氢溶液和二氧化锰制取氧气,反应的化学方程式为_________________________________。2H2O2=====2H2O+O2↑(4)某气体能与氧气反应,不溶于水且不与水反应,选择的收集装置是________(填标号)。D(5)用装置C收集NH3,该气体应从________(填标号)端通入集气瓶。【 解析】根据反应物的状态、反应发生需要的条件选择发生装置,根据反应物、生成物和反应条件书写化学方程式:高锰酸钾制取氧气需要加热,可选用装置A作发生装置;过氧化氢在二氧化锰的催化作用下生成水和氧气。根据气体的性质选择收集装置:某气体能与氧气反应,不溶于水且不与水反应,可用排水法收集,选择的收集装置是D;氨气的密度比空气小,可用向下排空气法收集,用装置C收集,气体应从c端通入集气瓶。【答案】c12.(中考?宁波)利用如图实验装置制取氧气。
(1)实验中,若产生氧气的速率太大,不利于收集。为了
减小反应速率,可以进行的合理操作是_______________
_________________________________________。调节分液漏斗活塞,使H2O2溶液的滴加速率减慢(2)若需要一瓶干燥的氧气,应将装置A产生的氧气通过干燥装置后再与________(填“B”“C”或“D”)相连。C(3)若用排水法收集了一瓶气体,并用带火星的木条检验,发现木条没有复燃,可能的原因有________。
A.实验所用的过氧化氢溶液的溶质质量分数偏小
B.开始收集时,倒置于水槽中的集气瓶未装满水
C.导管口一出现气泡就立即收集【 解析】(1)为了减小反应速率,可以调节分液漏斗活塞。(2)氧气既可用排水法收集,又可用向上排空气法收集;但排水法会使收集的氧气中含有水蒸气,故收集干燥的氧气只能用向上排空气法。 (3)“用带火星的木条检验,发现木条没有复燃”,说明集气瓶内氧气的浓度较小。【答案】B、C13.(中考?宜昌)加热一定量氯酸钾和二氧化锰的混合物,下列图像能正确表示对应变化关系的是( )【 解析】氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,随着反应的进行,生成氧气质量逐渐增大,完全反应后氧气质量不再变化,A不正确;随着反应的进行,固体质量逐渐减小,剩余固体中锰元素质量分数逐渐增大,B不正确;随着反应的进行,不断生成氧气,剩余固体中氧元素质量逐渐减小,完全反应后氧元素质量不再变化,C正确;反应前氯化钾质量是0,D不正确。【答案】C谢谢!
A.空气中的氧气主要来自于植物的光合作用
B.工业上用分离液态空气的方法制取氧气是分解反应
C.用含有氧元素的物质反应才有可能产生氧气
D.实验室常用加热高锰酸钾的方法制取氧气B【 解析】工业上分离液态空气制取氧气是物理变化。2. 空气中氧气约占21%,利用分离液态空气的方法得到氧气是工业上制取氧气的重要途径,下面是工业上制氧气流程图:(1)工业上分离液态空气制氧气的变化属于____________(填“物理变化”或“化学变化”)。
(2)这样制得的氧气是__________(填“纯净物”或“混合物”)。
(3)在一个标准大气压下,液氮的沸点为-196 ℃,液氧的沸点为-183 ℃,在蒸发的过程中________(填“氮气”或“氧气”)先被蒸发出来。物理变化混合物氮气3.用双氧水制取氧气时,若忘记加二氧化锰,其结果是( )
A.不放出氧气 B.放出氧气速率慢
C.放出氧气总量会减少 D.放出的氧气不纯B4.下列关于氧气的说法,错误的是( )
A.实验室制取氧气时,不一定要加催化剂
B.水中的生物能依靠溶于水中的少量氧气生存
C.通常状况下,氧气的密度略大于空气
D.氧气可以支持燃烧,说明氧气具有可燃性【 解析】氧气能支持燃烧,具有助燃性,但氧气不具有可燃性。D5.同学们在做氧气性质的实验时,将点燃的木炭伸入集气瓶内,有的现象明显,有的却不明显。导致现象不明显的原因可能是( )
A.排水法收集结束时集气瓶内有水残留
B.导管口连续放出气泡时才开始收集氧气
C.排水法收集满氧气后盖上毛玻璃片拿出水面
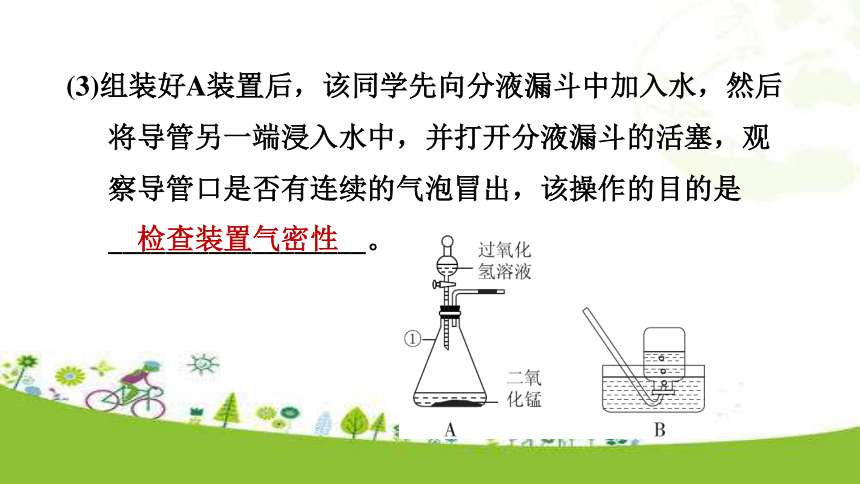
D.排水法收集氧气前未将集气瓶灌满水D6.(中考?聊城)如图是某同学设计的实验室制取氧气的实验装置图,请回答下列问题:
(1)写出图中标号仪器的名称:①______________。锥形瓶(2)二氧化锰在该化学反应中的作用是________________
______________________________________________。加快过氧化氢的分解催化作用,(3)组装好A装置后,该同学先向分液漏斗中加入水,然后将导管另一端浸入水中,并打开分液漏斗的活塞,观察导管口是否有连续的气泡冒出,该操作的目的是__________________。检查装置气密性(4)A装置中发生反应的化学方程式为____________________________,应将收集满氧气的集气瓶______(填“正”或“倒”)放在桌面上。正7.(中考?桂林)关于反应2KClO3=====2KCl+3O2↑的说法,错误的是( )
A.MnO2是该反应的催化剂
B.MnO2的质量在反应后减少
C.MnO2加快KClO3的分解速率
D.MnO2的化学性质在反应前后没有改变MnO2△B8.(中考?南宁)向一定溶质质量分数的过氧化氢溶液中加入少量二氧化锰,立即有大量的氧气产生,下列说法正确的是( )
A.过氧化氢中含有水和氧气
B.过氧化氢能使二氧化锰分解放出氧气
C.二氧化锰能加快过氧化氢分解生成水和氧气
D.该反应中有过氧化氢和二氧化锰两种反应物,不属于分解反应C9.(中考?福建)下列对催化剂描述正确的是( )
A.任何化学反应都需要催化剂
B.催化剂在反应前后本身的质量发生了变化
C.只有分解反应才需要催化剂
D.某些化学反应可以有多种催化剂D10.用向上排空气法收集氧气,检验氧气是否集满的最简便的方法是( )
A.看集气瓶口是否有较大气泡冒出
B.将带火星的木条伸入集气瓶中,看木条是否复燃
C.将带火星的木条伸到集气瓶口,看木条是否复燃
D.倒入澄清的石灰水,看是否变浑浊C【 解析】此题的易错点在于“1.忽略了是向上排空气法收集,而不是排水法收集;2.要验满,所以不能伸入瓶内”。11.(中考?昆明)根据下列装置图回答问题:
(1)仪器a的名称是________。试管(2)实验室用高锰酸钾制取氧气,选择的发生装置是________(填标号)。A(3)实验室还可用过氧化氢溶液和二氧化锰制取氧气,反应的化学方程式为_________________________________。2H2O2=====2H2O+O2↑(4)某气体能与氧气反应,不溶于水且不与水反应,选择的收集装置是________(填标号)。D(5)用装置C收集NH3,该气体应从________(填标号)端通入集气瓶。【 解析】根据反应物的状态、反应发生需要的条件选择发生装置,根据反应物、生成物和反应条件书写化学方程式:高锰酸钾制取氧气需要加热,可选用装置A作发生装置;过氧化氢在二氧化锰的催化作用下生成水和氧气。根据气体的性质选择收集装置:某气体能与氧气反应,不溶于水且不与水反应,可用排水法收集,选择的收集装置是D;氨气的密度比空气小,可用向下排空气法收集,用装置C收集,气体应从c端通入集气瓶。【答案】c12.(中考?宁波)利用如图实验装置制取氧气。
(1)实验中,若产生氧气的速率太大,不利于收集。为了
减小反应速率,可以进行的合理操作是_______________
_________________________________________。调节分液漏斗活塞,使H2O2溶液的滴加速率减慢(2)若需要一瓶干燥的氧气,应将装置A产生的氧气通过干燥装置后再与________(填“B”“C”或“D”)相连。C(3)若用排水法收集了一瓶气体,并用带火星的木条检验,发现木条没有复燃,可能的原因有________。
A.实验所用的过氧化氢溶液的溶质质量分数偏小
B.开始收集时,倒置于水槽中的集气瓶未装满水
C.导管口一出现气泡就立即收集【 解析】(1)为了减小反应速率,可以调节分液漏斗活塞。(2)氧气既可用排水法收集,又可用向上排空气法收集;但排水法会使收集的氧气中含有水蒸气,故收集干燥的氧气只能用向上排空气法。 (3)“用带火星的木条检验,发现木条没有复燃”,说明集气瓶内氧气的浓度较小。【答案】B、C13.(中考?宜昌)加热一定量氯酸钾和二氧化锰的混合物,下列图像能正确表示对应变化关系的是( )【 解析】氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,随着反应的进行,生成氧气质量逐渐增大,完全反应后氧气质量不再变化,A不正确;随着反应的进行,固体质量逐渐减小,剩余固体中锰元素质量分数逐渐增大,B不正确;随着反应的进行,不断生成氧气,剩余固体中氧元素质量逐渐减小,完全反应后氧元素质量不再变化,C正确;反应前氯化钾质量是0,D不正确。【答案】C谢谢!
