人教版高中化学必修一课件 第四章 第三节 第一课时 硫 二氧化硫 三氧化硫 (2)(共25张PPT)
文档属性
| 名称 | 人教版高中化学必修一课件 第四章 第三节 第一课时 硫 二氧化硫 三氧化硫 (2)(共25张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-04-07 00:00:00 | ||
图片预览








文档简介
(共25张PPT)
第一课时 硫 二氧化硫 三氧化硫
第四章《非金属及其化合物》
第三节 硫和氮的氧化物
【学习目标】
1、了解SO2的物理性质,掌握SO2的主要化学性质;
2、了解可逆反应的概念,知道SO2的漂白原理。
4-3-1 硫 二氧化硫 三氧化硫
【学习目标】
1、了解SO2的物理性质,掌握SO2的主要化学性质;
2、了解可逆反应的概念,知道SO2的漂白原理。
4-3-1 硫 二氧化硫 三氧化硫
4、硫,俗称_____,是一种___色晶体,____于水,
____于酒精,易溶于____。
(一) 硫单质
4-3-1 硫 二氧化硫 三氧化硫
硫磺
黄
难溶
难溶
CS2
4、硫,俗称_____,是一种___色晶体,____于水,
____于酒精,易溶于____。
(一) 硫单质
4-3-1 硫 二氧化硫 三氧化硫
硫磺
黄
难溶
难溶
CS2
(一) 硫单质
4-3-1 硫 二氧化硫 三氧化硫
5、空气污染物的来源:
工厂石油、天然气、煤等含硫化石燃料的燃烧。
①S + O2 SO2
② 2H2S + 3O2 2SO2 + 2H2O↑
4-3-1 硫 二氧化硫 三氧化硫
21.(1) 将SO2通入品红,现象_________________,
加热溶液煮沸后,现象为_______________;
将Cl2通入品红,现象__________________,
加热溶液煮沸后,现象为________________。
(2) 将Cl2通入石蕊,现象__________________;
将SO2通入石蕊,现象_________________。
(3) SO2使溴水褪色,是否是SO2的漂白性?
否,Br2有氧化性,SO2有还原性,
是发生氧化还原反应使溴水褪色。
SO2使红色酚酞溶液褪色,是SO2的漂白性?
否,是发生酸碱中和使酚酞变色。
(二)二氧化硫(SO2)
4-3-1 硫 二氧化硫 三氧化硫
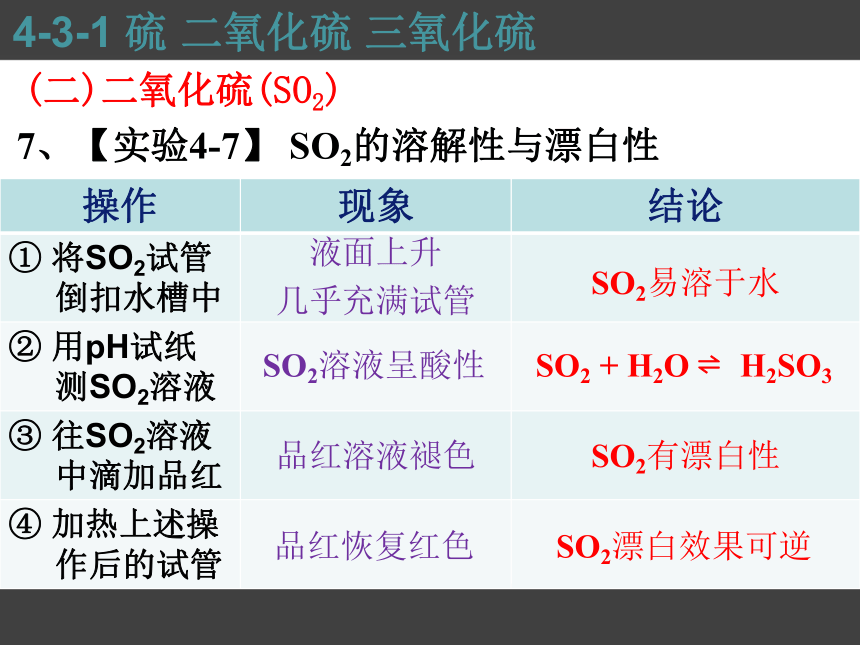
液面上升
几乎充满试管
SO2溶液呈酸性
品红溶液褪色
品红恢复红色
SO2易溶于水
SO2 + H2O ? H2SO3
SO2有漂白性
SO2漂白效果可逆
7、【实验4-7】 SO2的溶解性与漂白性
操作 现象 结论
① 将SO2试管
倒扣水槽中
② 用pH试纸
测SO2溶液
③ 往SO2溶液
中滴加品红
④ 加热上述操
作后的试管
(二)二氧化硫(SO2)
4-3-1 硫 二氧化硫 三氧化硫
液面上升
几乎充满试管
SO2溶液呈酸性
品红溶液褪色
品红恢复红色
SO2易溶于水
SO2 + H2O ? H2SO3
SO2有漂白性
SO2漂白效果可逆
7、【实验4-7】 SO2的溶解性与漂白性
操作 现象 结论
① 将SO2试管
倒扣水槽中
② 用pH试纸
测SO2溶液
③ 往SO2溶液
中滴加品红
④ 加热上述操
作后的试管
4-3-1 硫 二氧化硫 三氧化硫
21.(1) 将SO2通入品红,现象_________________,
加热溶液煮沸后,现象为_______________;
将Cl2通入品红,现象__________________,
加热溶液煮沸后,现象为________________。
(2) 将Cl2通入石蕊,现象__________________;
将SO2通入石蕊,现象_________________。
(3) SO2使溴水褪色,是否是SO2的漂白性?
否,Br2有氧化性,SO2有还原性,
是发生氧化还原反应使溴水褪色。
SO2使红色酚酞溶液褪色,是SO2的漂白性?
否,是发生酸碱中和使酚酞变色。
(二)二氧化硫(SO2)
4-3-1 硫 二氧化硫 三氧化硫
7、【实验4-7】 SO2的溶解性与漂白性
(1) SO2与氯水的漂白性有什么异同?
① 氯水的漂白是不可逆的过程,且具有普遍性;
② SO2的漂白是可逆过程:SO2 + H2O ? H2SO3 ,
且只能漂白有限的几种物质(品红和草织物)。
(二)二氧化硫(SO2)
4-3-1 硫 二氧化硫 三氧化硫
7、【实验4-7】 SO2的溶解性与漂白性
(2) 可逆反应:为什么加热后品红溶液又出现了红色?
SO2的漂白是和品红生成不稳定的无色物质,
加热逆向反应生成SO2, SO2挥发后品红恢复红色:
SO2 + H2O ? H2SO3
(二)二氧化硫(SO2)
4-3-1 硫 二氧化硫 三氧化硫
9、如何鉴别SO2和CO2 ?
① 澄清石灰水 ② 品红溶液
(1) 澄清石灰水不能鉴别:
CO2 + Ca(OH)2 = CaCO3↓ + H2O
SO2 + Ca(OH)2 = CaSO3↓ + H2O
(2) 品红溶液可以:
CO2不能漂白品红溶液;
SO2能够漂白品红溶液。
(二)二氧化硫(SO2)
4-3-1 硫 二氧化硫 三氧化硫
9、如何鉴别SO2和CO2 ?
① 澄清石灰水 ② 品红溶液
(1) 澄清石灰水不能鉴别:
CO2 + Ca(OH)2 = CaCO3↓ + H2O
SO2 + Ca(OH)2 = CaSO3↓ + H2O
(2) 品红溶液可以:
CO2不能漂白品红溶液;
SO2能够漂白品红溶液。
(二)二氧化硫(SO2)
4-3-1 硫 二氧化硫 三氧化硫
10、SO2的氧化性和还原性
S ← SO2 → SO3
① SO2 + O2 SO3
② SO2 + 2H2S = 3S↓ + 2H2O
(三)三氧化硫(SO3)
4-3-1 硫 二氧化硫 三氧化硫
11、硫粉在过量的中O2燃烧,
能否直接生成SO3?
不能,只能生成SO2,
SO2要生成SO3,还需要催化剂等条件:
SO2 + O2 SO3
(二)二氧化硫(SO2)
4-3-1 硫 二氧化硫 三氧化硫
7、【实验4-7】 SO2的溶解性与漂白性
(2) 可逆反应:为什么加热后品红溶液又出现了红色?
SO2的漂白是和品红生成不稳定的无色物质,
加热逆向反应生成SO2, SO2挥发后品红恢复红色:
SO2 + H2O ? H2SO3
(三)三氧化硫(SO3)
4-3-1 硫 二氧化硫 三氧化硫
12、SO2与SO3都具有酸性氧化物的通性,
完成下列表格:
(三)三氧化硫(SO3)
4-3-1 硫 二氧化硫 三氧化硫
12、SO2与SO3都具有酸性氧化物的通性,
完成下列表格:
17、
4-3-1 硫 二氧化硫 三氧化硫
(1) ⑥中反应方程式为:______________________。
(2) ①中现象_____________,证明SO2溶液有__性。
(3) ②中的品红溶液_________,证明SO2有____性。
(4) ③中现象______________,证明SO2有____性。
(5) ④中现象______________, 证明SO2有____性。
6) ⑤的作用是_______,____________________。
Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O
石蕊试液变红
酸
褪为无色
漂白
产生淡黄色沉淀
氧化
紫红色褪为无色
还原
吸收尾气
SO2 + 2NaOH = Na2SO3 + H2O
16.下列有关SO3的说法正确的是
A.S在过量O2中充分燃烧生成SO3
B.标准状况下,1 mol SO3的体积为22.4 L
C.将SO3加入BaCl2溶液有白色沉淀
D.SO2、SO3均具有漂白性,能使石蕊褪色
4-3-1 硫 二氧化硫 三氧化硫
C
16.下列有关SO3的说法正确的是
A.S在过量O2中充分燃烧生成SO3
B.标准状况下,1 mol SO3的体积为22.4 L
C.将SO3加入BaCl2溶液有白色沉淀
D.SO2、SO3均具有漂白性,能使石蕊褪色
4-3-1 硫 二氧化硫 三氧化硫
C
4-3-1 硫 二氧化硫 三氧化硫
21.(1) 将SO2通入品红,现象_________________,
加热溶液煮沸后,现象为_______________;
将Cl2通入品红,现象__________________,
加热溶液煮沸后,现象为________________。
(2) 将Cl2通入石蕊,现象__________________;
将SO2通入石蕊,现象_________________。
(3) SO2使溴水褪色,是否是SO2的漂白性?
否,Br2有氧化性,SO2有还原性,
是发生氧化还原反应使溴水褪色。
SO2使红色酚酞溶液褪色,是SO2的漂白性?
否,是发生酸碱中和使酚酞变色。
4-3-1 硫 二氧化硫 三氧化硫
21.(1) 将SO2通入品红,现象_________________,
加热溶液煮沸后,现象为_______________;
将Cl2通入品红,现象__________________,
加热溶液煮沸后,现象为________________。
(2) 将Cl2通入石蕊,现象__________________;
将SO2通入石蕊,现象_________________。
(3) SO2使溴水褪色,是否是SO2的漂白性?
否,Br2有氧化性,SO2有还原性,
是发生氧化还原反应使溴水褪色。
SO2使红色酚酞溶液褪色,是SO2的漂白性?
否,是发生酸碱中和使酚酞变色。
谢谢诸位!
让我们一起努力将化学变得更美好!
第一课时 硫 二氧化硫 三氧化硫
第四章《非金属及其化合物》
第三节 硫和氮的氧化物
【学习目标】
1、了解SO2的物理性质,掌握SO2的主要化学性质;
2、了解可逆反应的概念,知道SO2的漂白原理。
4-3-1 硫 二氧化硫 三氧化硫
【学习目标】
1、了解SO2的物理性质,掌握SO2的主要化学性质;
2、了解可逆反应的概念,知道SO2的漂白原理。
4-3-1 硫 二氧化硫 三氧化硫
4、硫,俗称_____,是一种___色晶体,____于水,
____于酒精,易溶于____。
(一) 硫单质
4-3-1 硫 二氧化硫 三氧化硫
硫磺
黄
难溶
难溶
CS2
4、硫,俗称_____,是一种___色晶体,____于水,
____于酒精,易溶于____。
(一) 硫单质
4-3-1 硫 二氧化硫 三氧化硫
硫磺
黄
难溶
难溶
CS2
(一) 硫单质
4-3-1 硫 二氧化硫 三氧化硫
5、空气污染物的来源:
工厂石油、天然气、煤等含硫化石燃料的燃烧。
①S + O2 SO2
② 2H2S + 3O2 2SO2 + 2H2O↑
4-3-1 硫 二氧化硫 三氧化硫
21.(1) 将SO2通入品红,现象_________________,
加热溶液煮沸后,现象为_______________;
将Cl2通入品红,现象__________________,
加热溶液煮沸后,现象为________________。
(2) 将Cl2通入石蕊,现象__________________;
将SO2通入石蕊,现象_________________。
(3) SO2使溴水褪色,是否是SO2的漂白性?
否,Br2有氧化性,SO2有还原性,
是发生氧化还原反应使溴水褪色。
SO2使红色酚酞溶液褪色,是SO2的漂白性?
否,是发生酸碱中和使酚酞变色。
(二)二氧化硫(SO2)
4-3-1 硫 二氧化硫 三氧化硫
液面上升
几乎充满试管
SO2溶液呈酸性
品红溶液褪色
品红恢复红色
SO2易溶于水
SO2 + H2O ? H2SO3
SO2有漂白性
SO2漂白效果可逆
7、【实验4-7】 SO2的溶解性与漂白性
操作 现象 结论
① 将SO2试管
倒扣水槽中
② 用pH试纸
测SO2溶液
③ 往SO2溶液
中滴加品红
④ 加热上述操
作后的试管
(二)二氧化硫(SO2)
4-3-1 硫 二氧化硫 三氧化硫
液面上升
几乎充满试管
SO2溶液呈酸性
品红溶液褪色
品红恢复红色
SO2易溶于水
SO2 + H2O ? H2SO3
SO2有漂白性
SO2漂白效果可逆
7、【实验4-7】 SO2的溶解性与漂白性
操作 现象 结论
① 将SO2试管
倒扣水槽中
② 用pH试纸
测SO2溶液
③ 往SO2溶液
中滴加品红
④ 加热上述操
作后的试管
4-3-1 硫 二氧化硫 三氧化硫
21.(1) 将SO2通入品红,现象_________________,
加热溶液煮沸后,现象为_______________;
将Cl2通入品红,现象__________________,
加热溶液煮沸后,现象为________________。
(2) 将Cl2通入石蕊,现象__________________;
将SO2通入石蕊,现象_________________。
(3) SO2使溴水褪色,是否是SO2的漂白性?
否,Br2有氧化性,SO2有还原性,
是发生氧化还原反应使溴水褪色。
SO2使红色酚酞溶液褪色,是SO2的漂白性?
否,是发生酸碱中和使酚酞变色。
(二)二氧化硫(SO2)
4-3-1 硫 二氧化硫 三氧化硫
7、【实验4-7】 SO2的溶解性与漂白性
(1) SO2与氯水的漂白性有什么异同?
① 氯水的漂白是不可逆的过程,且具有普遍性;
② SO2的漂白是可逆过程:SO2 + H2O ? H2SO3 ,
且只能漂白有限的几种物质(品红和草织物)。
(二)二氧化硫(SO2)
4-3-1 硫 二氧化硫 三氧化硫
7、【实验4-7】 SO2的溶解性与漂白性
(2) 可逆反应:为什么加热后品红溶液又出现了红色?
SO2的漂白是和品红生成不稳定的无色物质,
加热逆向反应生成SO2, SO2挥发后品红恢复红色:
SO2 + H2O ? H2SO3
(二)二氧化硫(SO2)
4-3-1 硫 二氧化硫 三氧化硫
9、如何鉴别SO2和CO2 ?
① 澄清石灰水 ② 品红溶液
(1) 澄清石灰水不能鉴别:
CO2 + Ca(OH)2 = CaCO3↓ + H2O
SO2 + Ca(OH)2 = CaSO3↓ + H2O
(2) 品红溶液可以:
CO2不能漂白品红溶液;
SO2能够漂白品红溶液。
(二)二氧化硫(SO2)
4-3-1 硫 二氧化硫 三氧化硫
9、如何鉴别SO2和CO2 ?
① 澄清石灰水 ② 品红溶液
(1) 澄清石灰水不能鉴别:
CO2 + Ca(OH)2 = CaCO3↓ + H2O
SO2 + Ca(OH)2 = CaSO3↓ + H2O
(2) 品红溶液可以:
CO2不能漂白品红溶液;
SO2能够漂白品红溶液。
(二)二氧化硫(SO2)
4-3-1 硫 二氧化硫 三氧化硫
10、SO2的氧化性和还原性
S ← SO2 → SO3
① SO2 + O2 SO3
② SO2 + 2H2S = 3S↓ + 2H2O
(三)三氧化硫(SO3)
4-3-1 硫 二氧化硫 三氧化硫
11、硫粉在过量的中O2燃烧,
能否直接生成SO3?
不能,只能生成SO2,
SO2要生成SO3,还需要催化剂等条件:
SO2 + O2 SO3
(二)二氧化硫(SO2)
4-3-1 硫 二氧化硫 三氧化硫
7、【实验4-7】 SO2的溶解性与漂白性
(2) 可逆反应:为什么加热后品红溶液又出现了红色?
SO2的漂白是和品红生成不稳定的无色物质,
加热逆向反应生成SO2, SO2挥发后品红恢复红色:
SO2 + H2O ? H2SO3
(三)三氧化硫(SO3)
4-3-1 硫 二氧化硫 三氧化硫
12、SO2与SO3都具有酸性氧化物的通性,
完成下列表格:
(三)三氧化硫(SO3)
4-3-1 硫 二氧化硫 三氧化硫
12、SO2与SO3都具有酸性氧化物的通性,
完成下列表格:
17、
4-3-1 硫 二氧化硫 三氧化硫
(1) ⑥中反应方程式为:______________________。
(2) ①中现象_____________,证明SO2溶液有__性。
(3) ②中的品红溶液_________,证明SO2有____性。
(4) ③中现象______________,证明SO2有____性。
(5) ④中现象______________, 证明SO2有____性。
6) ⑤的作用是_______,____________________。
Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O
石蕊试液变红
酸
褪为无色
漂白
产生淡黄色沉淀
氧化
紫红色褪为无色
还原
吸收尾气
SO2 + 2NaOH = Na2SO3 + H2O
16.下列有关SO3的说法正确的是
A.S在过量O2中充分燃烧生成SO3
B.标准状况下,1 mol SO3的体积为22.4 L
C.将SO3加入BaCl2溶液有白色沉淀
D.SO2、SO3均具有漂白性,能使石蕊褪色
4-3-1 硫 二氧化硫 三氧化硫
C
16.下列有关SO3的说法正确的是
A.S在过量O2中充分燃烧生成SO3
B.标准状况下,1 mol SO3的体积为22.4 L
C.将SO3加入BaCl2溶液有白色沉淀
D.SO2、SO3均具有漂白性,能使石蕊褪色
4-3-1 硫 二氧化硫 三氧化硫
C
4-3-1 硫 二氧化硫 三氧化硫
21.(1) 将SO2通入品红,现象_________________,
加热溶液煮沸后,现象为_______________;
将Cl2通入品红,现象__________________,
加热溶液煮沸后,现象为________________。
(2) 将Cl2通入石蕊,现象__________________;
将SO2通入石蕊,现象_________________。
(3) SO2使溴水褪色,是否是SO2的漂白性?
否,Br2有氧化性,SO2有还原性,
是发生氧化还原反应使溴水褪色。
SO2使红色酚酞溶液褪色,是SO2的漂白性?
否,是发生酸碱中和使酚酞变色。
4-3-1 硫 二氧化硫 三氧化硫
21.(1) 将SO2通入品红,现象_________________,
加热溶液煮沸后,现象为_______________;
将Cl2通入品红,现象__________________,
加热溶液煮沸后,现象为________________。
(2) 将Cl2通入石蕊,现象__________________;
将SO2通入石蕊,现象_________________。
(3) SO2使溴水褪色,是否是SO2的漂白性?
否,Br2有氧化性,SO2有还原性,
是发生氧化还原反应使溴水褪色。
SO2使红色酚酞溶液褪色,是SO2的漂白性?
否,是发生酸碱中和使酚酞变色。
谢谢诸位!
让我们一起努力将化学变得更美好!
