2020高二物理选修3-5第十八章原子结构第3节氢原子光谱(31页ppt)
文档属性
| 名称 | 2020高二物理选修3-5第十八章原子结构第3节氢原子光谱(31页ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 4.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 物理 | ||
| 更新时间 | 2020-04-09 00:00:00 | ||
图片预览






文档简介
(共31张PPT)
课前准备
1.预习第十八章 原子结构 第3-4节内容
2.准备笔记本和草稿纸
物理选修3-5
第十八章 原子结构
第三节 氢原子光谱
本节重点
1.了解连续谱、线状谱和吸收谱的概念。
2.知道氢原子光谱的实验规律。
3.知道经典电磁理论应用到核式结构时遇到的困难 。
烟花中的绚烂的色彩从哪里来?
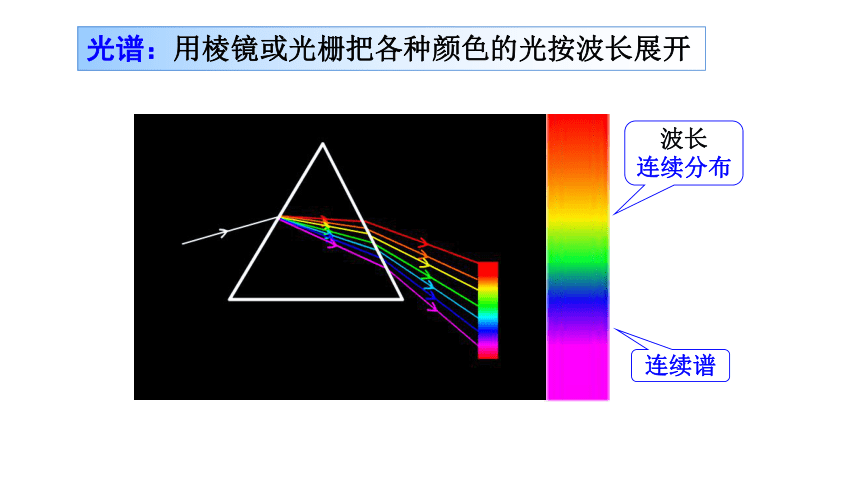
光谱:用棱镜或光栅把各种颜色的光按波长展开
波长
连续分布
连续谱
炽热的固体
炽热的液体
高(气)压的气体
一、连续谱:波长连续分布的谱线
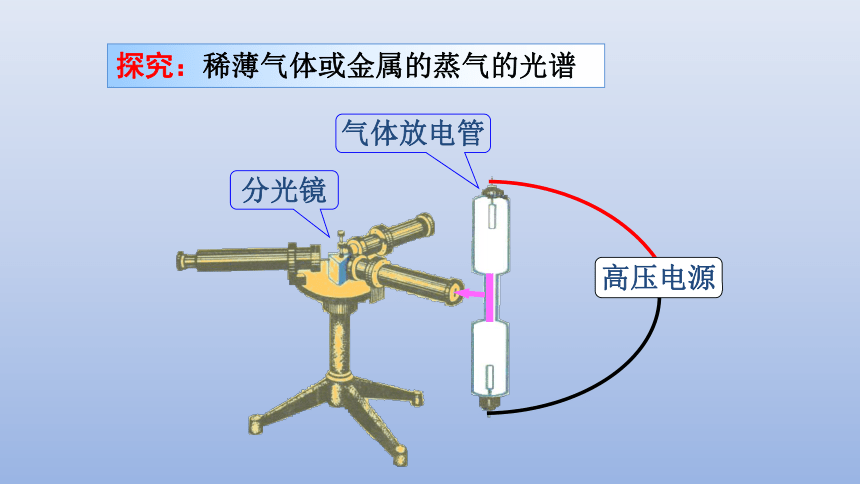
探究:稀薄气体或金属的蒸气的光谱
气体放电管
高压电源
分光镜
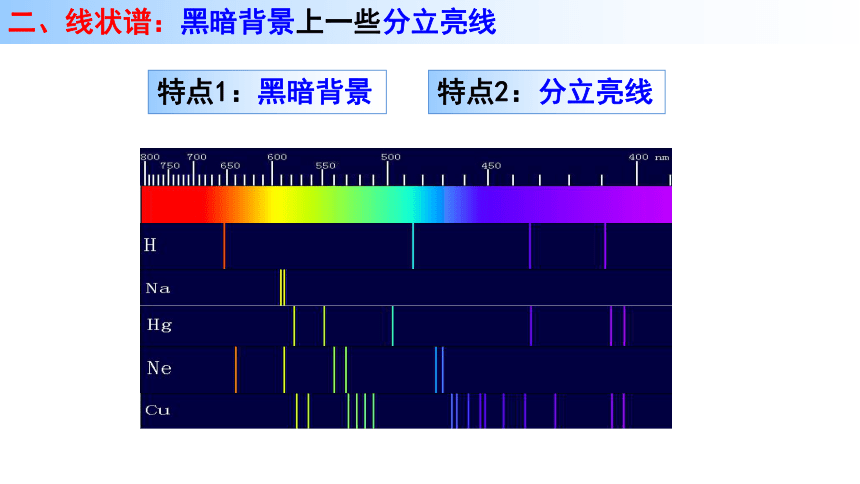
二、线状谱:黑暗背景上一些分立亮线
特点1:黑暗背景
特点2:分立亮线
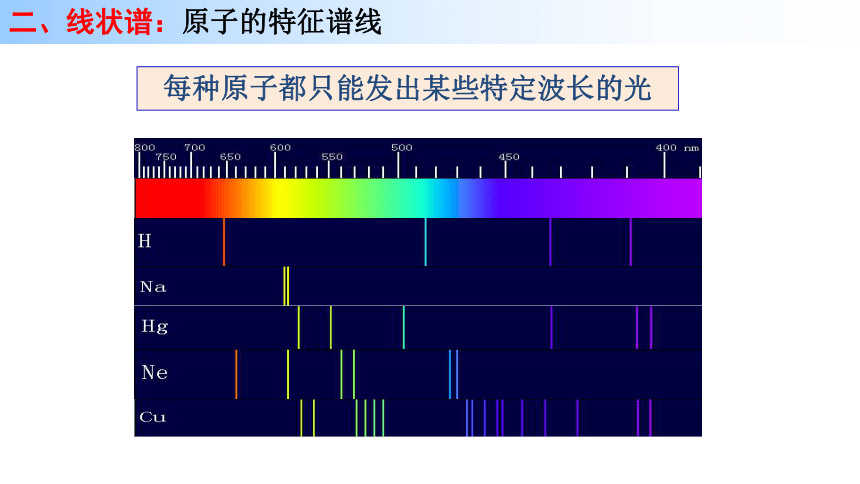
每种原子都只能发出某些特定波长的光
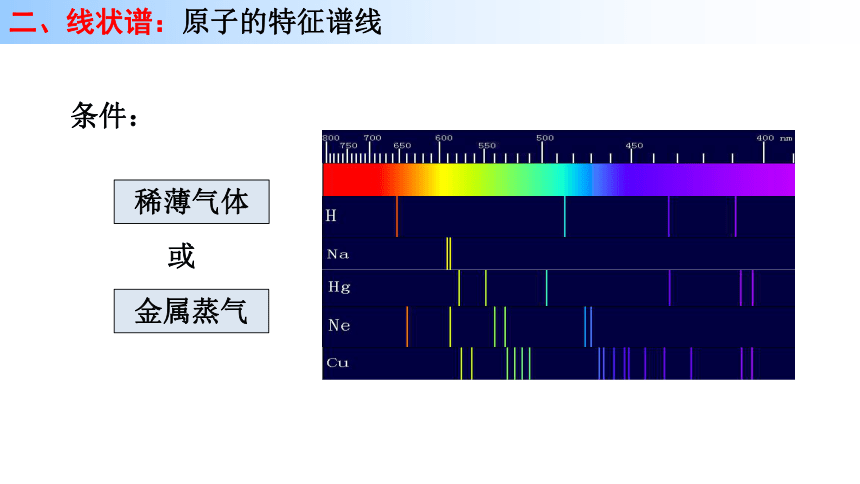
二、线状谱:原子的特征谱线
二、线状谱:原子的特征谱线
条件:
或
稀薄气体
金属蒸气
铜——蓝色火焰
钠——橙黄色火焰
锶——红色火焰
钡——黄绿色火焰
烟花中的绚烂的色彩从哪里来?
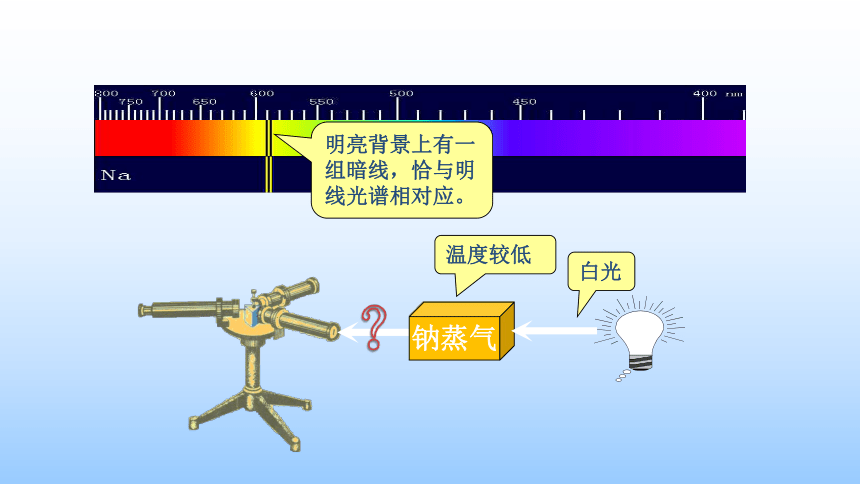
钠蒸气
明亮背景上有一组暗线,恰与明线光谱相对应。
白光
温度较低
?
氢蒸气
白光
温度较低
连续谱
Na的吸收光谱
Na的明线状谱
三、吸收光谱:连续明亮背景上一些分立暗线
特点1:黑暗背景
特点2:分立亮线
明线光谱:
特点1:连续明亮背景
特点2:分立暗线
吸收光谱:
吸收光谱也是原子的特征光谱
1666年,牛顿用三棱镜得到太阳光的光谱:
如果用三棱镜进一步展开?
1814年,德国物理学家夫琅和费发现:
夫琅和费太阳光谱手稿
太阳光谱中的暗线如何形成?
太阳光谱中的暗线如何形成?
德国物理学家基尔霍夫通过分析太阳大气层的吸收光谱,与已知元素的光谱相比较,知道太阳的大气中存在钠、镁、铜、锌、镍等金属元素,创立了光谱分析学。
1.速度快:可在1分钟甚至数秒钟内,同时给出二十多种元素的分析结果。
光谱分析学的诞生及优点
2.操作简便:无需任何分离操作而直接进行光谱分析,可同时测定多种元素或化合物。
3.灵敏度高:相对灵敏度可达到千万分之一至十亿分之一,绝对灵敏度达10-8g~10-9g。
X射线照射激发荧光,通过分析荧光判断越王勾践宝剑的成分.
1.鉴别物质的化学组成
四、光谱分析的应用
通过分光镜鉴定农药残留、微量元素、霉菌毒素等
1.鉴别物质的化学组成
四、光谱分析的应用
监测空气中二氧化硫等有害气体含量
2.发现新元素
3.探索原子结构
1.鉴别物质的化学组成
四、光谱分析的应用
铯、铷、铊、铟、镓等元素的发现
气体放电管: 管中稀薄气体导电时发光。
五、氢原子光谱——探究氢原子光谱实验
气体放电管
分光镜
高压感应圈
= 364.56×9/5 nm
= 364.56×4/3 nm
= 364.56×25/21nm
= 364.56×9/8 nm
五、氢原子光谱——探究氢原子光谱规律
可见光区
红
绿
紫
蓝
Hα= 656.3nm
Hβ= 486.1nm
Hγ= 434.1nm
Hδ= 410.2nm
巴耳末公式:
R 为里德伯常量
莱曼系
紫外线区
五、氢原子光谱——探究氢原子光谱规律
红外
线
区
帕邢系
布喇开系
普丰德系
五、氢原子光谱——探究氢原子光谱规律
1890 年瑞典物理学家里德伯给出氢原子光谱公式
里德伯常数
打开破解原子“密码” 大门的钥匙!
五、氢原子光谱——探究氢原子光谱规律
辐射频率连续变化
1.矛盾一:
无法解释原子的稳定性
2.矛盾二:
无法解释原子光谱的分立性
核外电子绕核运动
辐射电磁波
原子不稳定
原子是
稳定的
辐射频率只是
某些特定值
六、经典理论的困难
电子轨道半径连续变小
经典理论认为
事实
A
氢原子光谱——敲黑板,划重点啦!
一、各种光谱的特点、条件应用:
二、氢原子光谱的实验规律:
三、经典理论的困难:
类型 形式 条件 用途
连续光谱 波长连续分布 炽热的固体、液体和高压气体发 光
线状光谱 黑暗背景上一些分离的亮线 稀薄气体或金属蒸汽发光 光谱分析
吸收光谱 连续明亮背景上的一些暗线 白光通过温度较低的气体 光谱分析
无法解释原子的稳定性和原子光谱的分立性
1.(多选)下列关于光谱和光谱分析的说法中,正确的是( )
A.霓虹灯的光谱是线状光谱
B.太阳光谱是吸收光谱
C.根据太阳光谱中的暗线,可以分析太阳周围大气的物质成分
D. 通过分析月光的光谱能鉴别月球的物质成分
小试牛刀
A B C
2.已知氢原子光谱的巴耳末公式 , 则巴耳末系最小波长与最大波长之比为 ( )
【解析】选 A .当n=∞时,最小波长 ,当n=3 时,最大波长 ,故 。
小试牛刀
我学会了吗?
1. 连续谱、线状谱和吸收谱的特点?条件?
2. 氢原子光谱的实验规律?
3. 经典电磁理论应用到核式结构时遇到了什么困难 ?
课前准备
1.预习第十八章 原子结构 第3-4节内容
2.准备笔记本和草稿纸
物理选修3-5
第十八章 原子结构
第三节 氢原子光谱
本节重点
1.了解连续谱、线状谱和吸收谱的概念。
2.知道氢原子光谱的实验规律。
3.知道经典电磁理论应用到核式结构时遇到的困难 。
烟花中的绚烂的色彩从哪里来?
光谱:用棱镜或光栅把各种颜色的光按波长展开
波长
连续分布
连续谱
炽热的固体
炽热的液体
高(气)压的气体
一、连续谱:波长连续分布的谱线
探究:稀薄气体或金属的蒸气的光谱
气体放电管
高压电源
分光镜
二、线状谱:黑暗背景上一些分立亮线
特点1:黑暗背景
特点2:分立亮线
每种原子都只能发出某些特定波长的光
二、线状谱:原子的特征谱线
二、线状谱:原子的特征谱线
条件:
或
稀薄气体
金属蒸气
铜——蓝色火焰
钠——橙黄色火焰
锶——红色火焰
钡——黄绿色火焰
烟花中的绚烂的色彩从哪里来?
钠蒸气
明亮背景上有一组暗线,恰与明线光谱相对应。
白光
温度较低
?
氢蒸气
白光
温度较低
连续谱
Na的吸收光谱
Na的明线状谱
三、吸收光谱:连续明亮背景上一些分立暗线
特点1:黑暗背景
特点2:分立亮线
明线光谱:
特点1:连续明亮背景
特点2:分立暗线
吸收光谱:
吸收光谱也是原子的特征光谱
1666年,牛顿用三棱镜得到太阳光的光谱:
如果用三棱镜进一步展开?
1814年,德国物理学家夫琅和费发现:
夫琅和费太阳光谱手稿
太阳光谱中的暗线如何形成?
太阳光谱中的暗线如何形成?
德国物理学家基尔霍夫通过分析太阳大气层的吸收光谱,与已知元素的光谱相比较,知道太阳的大气中存在钠、镁、铜、锌、镍等金属元素,创立了光谱分析学。
1.速度快:可在1分钟甚至数秒钟内,同时给出二十多种元素的分析结果。
光谱分析学的诞生及优点
2.操作简便:无需任何分离操作而直接进行光谱分析,可同时测定多种元素或化合物。
3.灵敏度高:相对灵敏度可达到千万分之一至十亿分之一,绝对灵敏度达10-8g~10-9g。
X射线照射激发荧光,通过分析荧光判断越王勾践宝剑的成分.
1.鉴别物质的化学组成
四、光谱分析的应用
通过分光镜鉴定农药残留、微量元素、霉菌毒素等
1.鉴别物质的化学组成
四、光谱分析的应用
监测空气中二氧化硫等有害气体含量
2.发现新元素
3.探索原子结构
1.鉴别物质的化学组成
四、光谱分析的应用
铯、铷、铊、铟、镓等元素的发现
气体放电管: 管中稀薄气体导电时发光。
五、氢原子光谱——探究氢原子光谱实验
气体放电管
分光镜
高压感应圈
= 364.56×9/5 nm
= 364.56×4/3 nm
= 364.56×25/21nm
= 364.56×9/8 nm
五、氢原子光谱——探究氢原子光谱规律
可见光区
红
绿
紫
蓝
Hα= 656.3nm
Hβ= 486.1nm
Hγ= 434.1nm
Hδ= 410.2nm
巴耳末公式:
R 为里德伯常量
莱曼系
紫外线区
五、氢原子光谱——探究氢原子光谱规律
红外
线
区
帕邢系
布喇开系
普丰德系
五、氢原子光谱——探究氢原子光谱规律
1890 年瑞典物理学家里德伯给出氢原子光谱公式
里德伯常数
打开破解原子“密码” 大门的钥匙!
五、氢原子光谱——探究氢原子光谱规律
辐射频率连续变化
1.矛盾一:
无法解释原子的稳定性
2.矛盾二:
无法解释原子光谱的分立性
核外电子绕核运动
辐射电磁波
原子不稳定
原子是
稳定的
辐射频率只是
某些特定值
六、经典理论的困难
电子轨道半径连续变小
经典理论认为
事实
A
氢原子光谱——敲黑板,划重点啦!
一、各种光谱的特点、条件应用:
二、氢原子光谱的实验规律:
三、经典理论的困难:
类型 形式 条件 用途
连续光谱 波长连续分布 炽热的固体、液体和高压气体发 光
线状光谱 黑暗背景上一些分离的亮线 稀薄气体或金属蒸汽发光 光谱分析
吸收光谱 连续明亮背景上的一些暗线 白光通过温度较低的气体 光谱分析
无法解释原子的稳定性和原子光谱的分立性
1.(多选)下列关于光谱和光谱分析的说法中,正确的是( )
A.霓虹灯的光谱是线状光谱
B.太阳光谱是吸收光谱
C.根据太阳光谱中的暗线,可以分析太阳周围大气的物质成分
D. 通过分析月光的光谱能鉴别月球的物质成分
小试牛刀
A B C
2.已知氢原子光谱的巴耳末公式 , 则巴耳末系最小波长与最大波长之比为 ( )
【解析】选 A .当n=∞时,最小波长 ,当n=3 时,最大波长 ,故 。
小试牛刀
我学会了吗?
1. 连续谱、线状谱和吸收谱的特点?条件?
2. 氢原子光谱的实验规律?
3. 经典电磁理论应用到核式结构时遇到了什么困难 ?
