人教版九年级化学第十一单元课题1-生活中常见的盐-碳酸盐(共26张PPT)
文档属性
| 名称 | 人教版九年级化学第十一单元课题1-生活中常见的盐-碳酸盐(共26张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 33.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-04-12 00:00:00 | ||
图片预览






文档简介
(共26张PPT)
课题1 生活中常见的盐
之碳酸盐
请同学们扫描二维码完成课前预习测
滨河实验中学
施 勇
2020-3-18
1.新课导入
发酵前
发酵后
成果展
额外加入醋
自己动手,丰衣足食
鸡壳
食用碱
小苏打
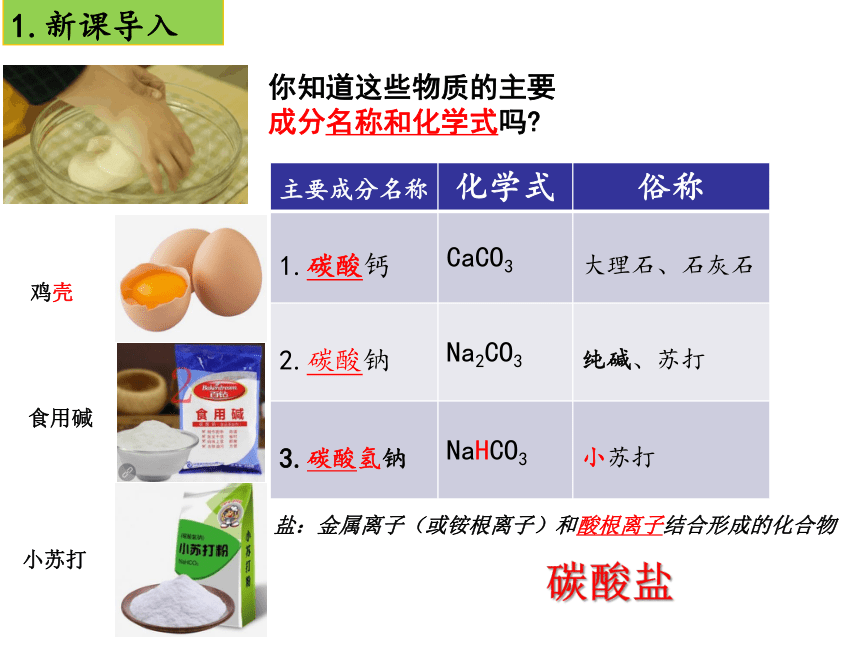
主要成分名称 化学式 俗称
1.碳酸钙 CaCO3 大理石、石灰石
2.碳酸钠 Na2CO3 纯碱、苏打
3.碳酸氢钠 NaHCO3 小苏打
你知道这些物质的主要成分名称和化学式吗?
1.新课导入
碳酸盐
盐:金属离子(或铵根离子)和酸根离子结合形成的化合物
碳酸钙
CaCO3
来源以及生活中的用途?
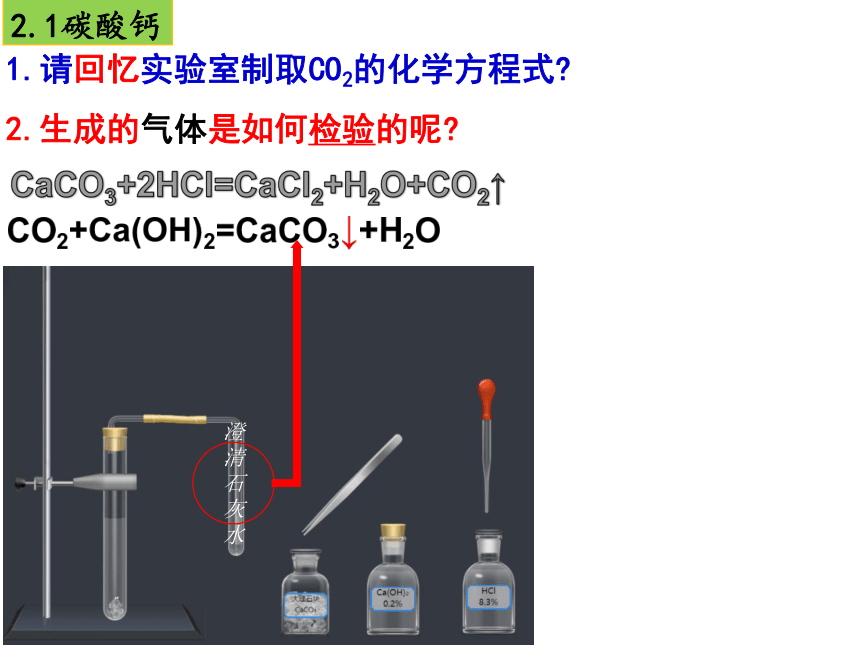
2.1碳酸钙
1.请回忆实验室制取CO2的化学方程式?
2.生成的气体是如何检验的呢?
CO2+Ca(OH)2=CaCO3↓+H2O
澄清石灰水
2.1碳酸钙
2.2碳酸钠和碳酸氢钠
碳酸钠的用途
玻璃
洗涤剂
面点加工
造纸
纺织
碳酸氢钠的用途
治疗胃酸过多
面点发酵剂
饮料原料
灭火剂原料
思考
碳酸钠(Na2CO3)
和
碳酸氢钠(NaHCO3)
酸碱性
?
结论:
1.Na2CO3和NaHCO3溶液
均显碱性
2.pH(Na2CO3)>pH(NaHCO3)
实验演示
2.2 碳酸钠和碳酸氢钠
纯碱不是碱,而是盐!
反应 实验现象 实验分析
(用化学方程式表示)
Na2CO3与稀HCl
NaHCO3与稀HCl
探究实验,完成后请填好表格
产生气体
产生气体
反应 实验现象 实验分析
(用化学方程式表示)
Na2CO3与稀HCl
NaHCO3与稀HCl
探究实验,完成后请填好表格
有气体产生,生成的气体使澄清石灰水变浑浊
有气体产生,生成的气体使澄清石灰水变浑浊
Na2CO3+2HCl=2NaCl+H2O+CO2↑
NaHCO3+HCl=NaCl+H2O+CO2↑
结论:凡是物质组成里含有碳酸根(或碳酸氢根)离子的盐都能与盐酸反应生成CO2和H2O。
CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
Na2CO3 + 2HCl==2NaCl + H2O + CO2↑
NaHCO3 + HCl == NaCl + H2O + CO2↑
某物质
+HCl
产生气体
变浑浊
+Ca(OH)2
CO2
CaCO3
碳酸盐
提问:找规律
练一练:利用如图装置证明某样品中含有碳酸盐(夹持仪器略去)。 (1)所需要的试剂分别是:A 、B ; (2)实验中观察到的现象有 。
稀HCl
澄清石灰水
A中产生大量气泡,
B中澄清石灰水变浑浊。
<归纳>:CO32-或HCO3-的检验方法
(1)取少许样品放入试管;
(2)加入稀盐酸;
(3)再将产生的气体通入澄清石灰水,观察现象。
---这种方法适用于检验溶液或固体中是否含有CO32-或HCO3-
样品、
稀盐酸
澄清石灰水
规律:碳酸盐与酸反应均能生成H2O和CO2
物质(碳酸盐) 稀HCl 稀H2SO4
Na2CO3 Na2CO3+2HCl=
2NaCl+H2O+CO2↑ 1?
NaHCO3 NaHCO3+HCl=
NaCl+H2O+CO2↑ 2?
K2CO3 3? 5?
MgCO3 4? 6?
Na2CO3+H2SO4=
Na2SO4+H2O+CO2↑
2NaHCO3+H2SO4=
Na2SO4+2H2O+2CO2↑
K2CO3+2HCl=
2KCl+H2O+CO2↑
MgCO3+2HCl=
MgCl2+H2O+CO2↑
试一试:写出下列方程式
K2CO3+H2SO4=
K2SO4+H2O+CO2↑
MgCO3+H2SO4=
MgSO4+H2O+CO2↑
练一练:蒸馒头时,在发酵的面团里加入些纯碱(Na2CO3),其作用是( ) A.使馒头变白 B.既除去生成的酸,又使馒头软而体积大 C.加快面团的发酵速度 D.产生二氧化碳使馒头质量变大
B
前
后
额外加入醋
趣味实验:“软”蛋制作
1.生鸡蛋1个;
2.白醋适量;
3.观察现象;
鸡蛋表面……
一天后再观察……
原理:CaCO3(碳酸盐)与醋酸(CH3COOH)反应生成--->H2O+CO2↑
练一练:制作松花蛋常用到熟石灰和纯碱等原料,因此,食用它时常有涩味,为了减轻涩味,可在食用前添加调味品。这种调味品最好是( ) A.酱油 B.食盐 C.香油 D.食醋
D
练一练:已知不同温度下,碳酸钠和碳酸氢钠的溶解度如表所示:
温度/℃ 0 20 40 60
碳酸钠/g 7.0 21.8 48.8 46.4
碳酸氢钠/g 6.9 9.6 12.7 16.4
(1)碳酸钠、碳酸氢钠溶液都能使紫色石蕊试液变成 。 (2)服用碳酸氢钠治疗胃酸过多时,胃液的pH (填“增大”、“减小”或“不变”),发生反应的化学方程式是 。 (3)为区分碳酸钠和碳酸氢钠两种白色固体。在20℃时,各盛有100mL水的甲、乙两烧杯中,分别加入等质量的碳酸钠和碳酸氢钠固体,充分溶解后,现象如图所示。乙烧杯中加入的物质是 (填化学式),加入的质量m的范围为: 。
蓝色
增大
NaHCO3+HCl=NaCl+H2O+CO2↑
Na2CO3
9.6g<m≤21.8g
演示实验:向盛有少量Na2CO3溶液的试管里滴入澄清的石灰水,观察现象。
现象
原理
溶液变浑浊
Na2CO3 + Ca(OH)2 == CaCO3↓+ 2NaOH
NaOH的工业制取:纯碱Na2CO3和熟石灰Ca(OH)2制取烧碱
Na2CO3 + Ca(OH)2 = CaCO3↓+ 2NaOH
由纯碱制烧碱
纯碱
烧碱
操作:过滤
3.氢氧化钠的工业制取
碳酸盐 物理性质 化学性质 用途
碳酸钙CaCO3 白色固体,难溶于水 与酸反应 建筑材料,补钙剂,珍珠首饰等
碳酸钠Na2CO3
(纯碱不是碱,而是盐) 白色固体,易溶于水 与酸反应,与碱反应 玻璃、造纸、纺织,洗涤剂等
碳酸氢钠NaHCO3
白色固体,易溶于水 与酸反应 焙制糕点,治疗胃酸过多,灭火器原料等
4.总结
练一练:1.有关酸、碱、盐的应用不正确的是( ) A.稀盐酸能与金属氧化物反应,可用于金属除锈 B.固体氢氧化钠易潮解,可干燥氧气、二氧化碳等气体 C.熟石灰可以用来改良酸性土壤 D.碳酸钠溶液可以鉴别烧碱溶液和澄清石灰水
B
练一练:2.酸、碱、盐与生产生活密切相关,下列关于物质的用途叙述不正确的是( ) A.碳酸钙可用作补钙剂 B.烧碱用于改良酸性土壤 C.纯碱用于实验室制取少量氢氧化钠 D.盐酸可用于清除铁锈
B
课堂练习
课堂小结
本节我们学习的主要内容是什么?
1.碳酸钙、碳酸钠和碳酸氢钠等碳酸盐在生活和生产中都有广泛的应用;
2.介绍三种碳酸盐的有关物理与化学性质;
3.CO32-离子和HCO3-离子的检验;
4.工业制烧碱;
课后阅读资料
1.我国制碱工业的先驱---
侯德榜 (侯氏制碱法).
2.石笋和钟乳石的形成---
千姿百态的溶洞
CaCO3+CO2+H2O=Ca(HCO3)2
Ca(HCO3 )2 CaCO3 + CO2 + H2O
课后作业:
1.《知能》B本:77-79页(QQ群作业)
2.12xue平台
致谢:
感谢各位老师们的聆听,感谢郭老师的专业指导和课组周老师、温老师和赵老师的宝贵意见。
不足之处希望大家多提意见,谢谢!谢谢!
微信号(手机号):13428963881
课题1 生活中常见的盐
之碳酸盐
请同学们扫描二维码完成课前预习测
滨河实验中学
施 勇
2020-3-18
1.新课导入
发酵前
发酵后
成果展
额外加入醋
自己动手,丰衣足食
鸡壳
食用碱
小苏打
主要成分名称 化学式 俗称
1.碳酸钙 CaCO3 大理石、石灰石
2.碳酸钠 Na2CO3 纯碱、苏打
3.碳酸氢钠 NaHCO3 小苏打
你知道这些物质的主要成分名称和化学式吗?
1.新课导入
碳酸盐
盐:金属离子(或铵根离子)和酸根离子结合形成的化合物
碳酸钙
CaCO3
来源以及生活中的用途?
2.1碳酸钙
1.请回忆实验室制取CO2的化学方程式?
2.生成的气体是如何检验的呢?
CO2+Ca(OH)2=CaCO3↓+H2O
澄清石灰水
2.1碳酸钙
2.2碳酸钠和碳酸氢钠
碳酸钠的用途
玻璃
洗涤剂
面点加工
造纸
纺织
碳酸氢钠的用途
治疗胃酸过多
面点发酵剂
饮料原料
灭火剂原料
思考
碳酸钠(Na2CO3)
和
碳酸氢钠(NaHCO3)
酸碱性
?
结论:
1.Na2CO3和NaHCO3溶液
均显碱性
2.pH(Na2CO3)>pH(NaHCO3)
实验演示
2.2 碳酸钠和碳酸氢钠
纯碱不是碱,而是盐!
反应 实验现象 实验分析
(用化学方程式表示)
Na2CO3与稀HCl
NaHCO3与稀HCl
探究实验,完成后请填好表格
产生气体
产生气体
反应 实验现象 实验分析
(用化学方程式表示)
Na2CO3与稀HCl
NaHCO3与稀HCl
探究实验,完成后请填好表格
有气体产生,生成的气体使澄清石灰水变浑浊
有气体产生,生成的气体使澄清石灰水变浑浊
Na2CO3+2HCl=2NaCl+H2O+CO2↑
NaHCO3+HCl=NaCl+H2O+CO2↑
结论:凡是物质组成里含有碳酸根(或碳酸氢根)离子的盐都能与盐酸反应生成CO2和H2O。
CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
Na2CO3 + 2HCl==2NaCl + H2O + CO2↑
NaHCO3 + HCl == NaCl + H2O + CO2↑
某物质
+HCl
产生气体
变浑浊
+Ca(OH)2
CO2
CaCO3
碳酸盐
提问:找规律
练一练:利用如图装置证明某样品中含有碳酸盐(夹持仪器略去)。 (1)所需要的试剂分别是:A 、B ; (2)实验中观察到的现象有 。
稀HCl
澄清石灰水
A中产生大量气泡,
B中澄清石灰水变浑浊。
<归纳>:CO32-或HCO3-的检验方法
(1)取少许样品放入试管;
(2)加入稀盐酸;
(3)再将产生的气体通入澄清石灰水,观察现象。
---这种方法适用于检验溶液或固体中是否含有CO32-或HCO3-
样品、
稀盐酸
澄清石灰水
规律:碳酸盐与酸反应均能生成H2O和CO2
物质(碳酸盐) 稀HCl 稀H2SO4
Na2CO3 Na2CO3+2HCl=
2NaCl+H2O+CO2↑ 1?
NaHCO3 NaHCO3+HCl=
NaCl+H2O+CO2↑ 2?
K2CO3 3? 5?
MgCO3 4? 6?
Na2CO3+H2SO4=
Na2SO4+H2O+CO2↑
2NaHCO3+H2SO4=
Na2SO4+2H2O+2CO2↑
K2CO3+2HCl=
2KCl+H2O+CO2↑
MgCO3+2HCl=
MgCl2+H2O+CO2↑
试一试:写出下列方程式
K2CO3+H2SO4=
K2SO4+H2O+CO2↑
MgCO3+H2SO4=
MgSO4+H2O+CO2↑
练一练:蒸馒头时,在发酵的面团里加入些纯碱(Na2CO3),其作用是( ) A.使馒头变白 B.既除去生成的酸,又使馒头软而体积大 C.加快面团的发酵速度 D.产生二氧化碳使馒头质量变大
B
前
后
额外加入醋
趣味实验:“软”蛋制作
1.生鸡蛋1个;
2.白醋适量;
3.观察现象;
鸡蛋表面……
一天后再观察……
原理:CaCO3(碳酸盐)与醋酸(CH3COOH)反应生成--->H2O+CO2↑
练一练:制作松花蛋常用到熟石灰和纯碱等原料,因此,食用它时常有涩味,为了减轻涩味,可在食用前添加调味品。这种调味品最好是( ) A.酱油 B.食盐 C.香油 D.食醋
D
练一练:已知不同温度下,碳酸钠和碳酸氢钠的溶解度如表所示:
温度/℃ 0 20 40 60
碳酸钠/g 7.0 21.8 48.8 46.4
碳酸氢钠/g 6.9 9.6 12.7 16.4
(1)碳酸钠、碳酸氢钠溶液都能使紫色石蕊试液变成 。 (2)服用碳酸氢钠治疗胃酸过多时,胃液的pH (填“增大”、“减小”或“不变”),发生反应的化学方程式是 。 (3)为区分碳酸钠和碳酸氢钠两种白色固体。在20℃时,各盛有100mL水的甲、乙两烧杯中,分别加入等质量的碳酸钠和碳酸氢钠固体,充分溶解后,现象如图所示。乙烧杯中加入的物质是 (填化学式),加入的质量m的范围为: 。
蓝色
增大
NaHCO3+HCl=NaCl+H2O+CO2↑
Na2CO3
9.6g<m≤21.8g
演示实验:向盛有少量Na2CO3溶液的试管里滴入澄清的石灰水,观察现象。
现象
原理
溶液变浑浊
Na2CO3 + Ca(OH)2 == CaCO3↓+ 2NaOH
NaOH的工业制取:纯碱Na2CO3和熟石灰Ca(OH)2制取烧碱
Na2CO3 + Ca(OH)2 = CaCO3↓+ 2NaOH
由纯碱制烧碱
纯碱
烧碱
操作:过滤
3.氢氧化钠的工业制取
碳酸盐 物理性质 化学性质 用途
碳酸钙CaCO3 白色固体,难溶于水 与酸反应 建筑材料,补钙剂,珍珠首饰等
碳酸钠Na2CO3
(纯碱不是碱,而是盐) 白色固体,易溶于水 与酸反应,与碱反应 玻璃、造纸、纺织,洗涤剂等
碳酸氢钠NaHCO3
白色固体,易溶于水 与酸反应 焙制糕点,治疗胃酸过多,灭火器原料等
4.总结
练一练:1.有关酸、碱、盐的应用不正确的是( ) A.稀盐酸能与金属氧化物反应,可用于金属除锈 B.固体氢氧化钠易潮解,可干燥氧气、二氧化碳等气体 C.熟石灰可以用来改良酸性土壤 D.碳酸钠溶液可以鉴别烧碱溶液和澄清石灰水
B
练一练:2.酸、碱、盐与生产生活密切相关,下列关于物质的用途叙述不正确的是( ) A.碳酸钙可用作补钙剂 B.烧碱用于改良酸性土壤 C.纯碱用于实验室制取少量氢氧化钠 D.盐酸可用于清除铁锈
B
课堂练习
课堂小结
本节我们学习的主要内容是什么?
1.碳酸钙、碳酸钠和碳酸氢钠等碳酸盐在生活和生产中都有广泛的应用;
2.介绍三种碳酸盐的有关物理与化学性质;
3.CO32-离子和HCO3-离子的检验;
4.工业制烧碱;
课后阅读资料
1.我国制碱工业的先驱---
侯德榜 (侯氏制碱法).
2.石笋和钟乳石的形成---
千姿百态的溶洞
CaCO3+CO2+H2O=Ca(HCO3)2
Ca(HCO3 )2 CaCO3 + CO2 + H2O
课后作业:
1.《知能》B本:77-79页(QQ群作业)
2.12xue平台
致谢:
感谢各位老师们的聆听,感谢郭老师的专业指导和课组周老师、温老师和赵老师的宝贵意见。
不足之处希望大家多提意见,谢谢!谢谢!
微信号(手机号):13428963881
同课章节目录
