人教版高中化学选修5 第二章 2.1脂肪烃 上课课件(共41张ppt)
文档属性
| 名称 | 人教版高中化学选修5 第二章 2.1脂肪烃 上课课件(共41张ppt) |
|
|
| 格式 | zip | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-04-13 00:00:00 | ||
图片预览







文档简介
(共41张PPT)
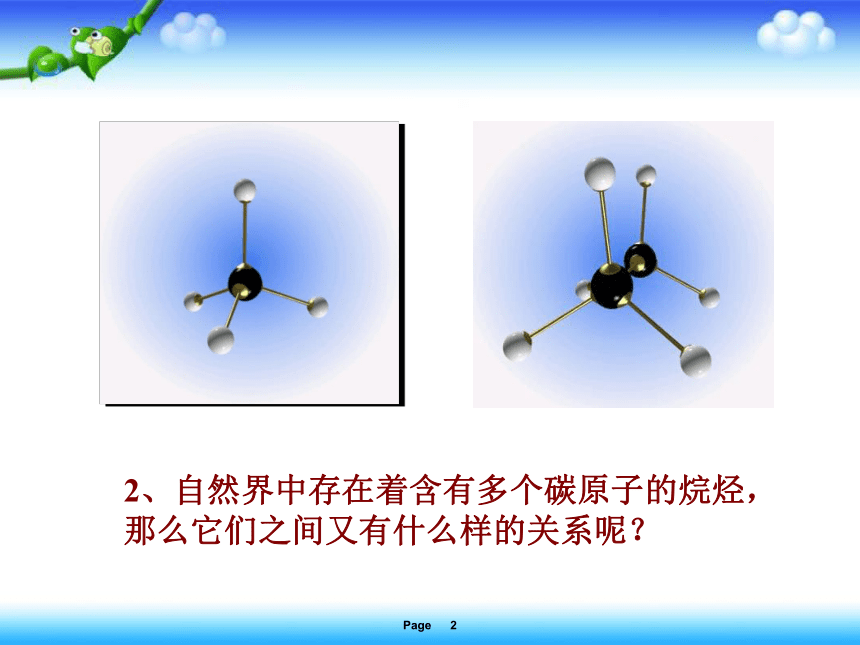
1、下图为实验室制备哪种物质的装置?
可以为实验室制备甲烷的装置
导入新课
2、自然界中存在着含有多个碳原子的烷烃,那么它们之间又有什么样的关系呢?
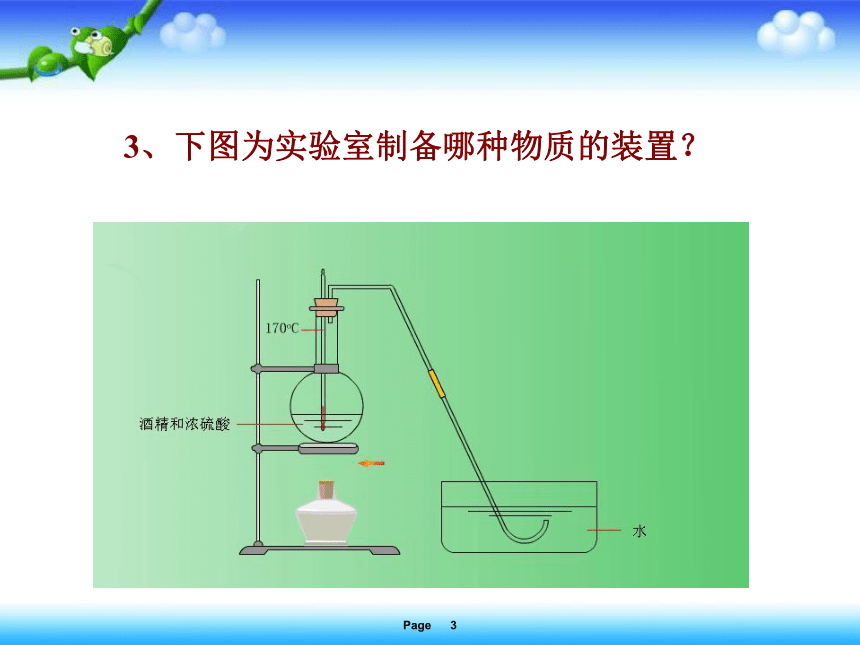
3、下图为实验室制备哪种物质的装置?
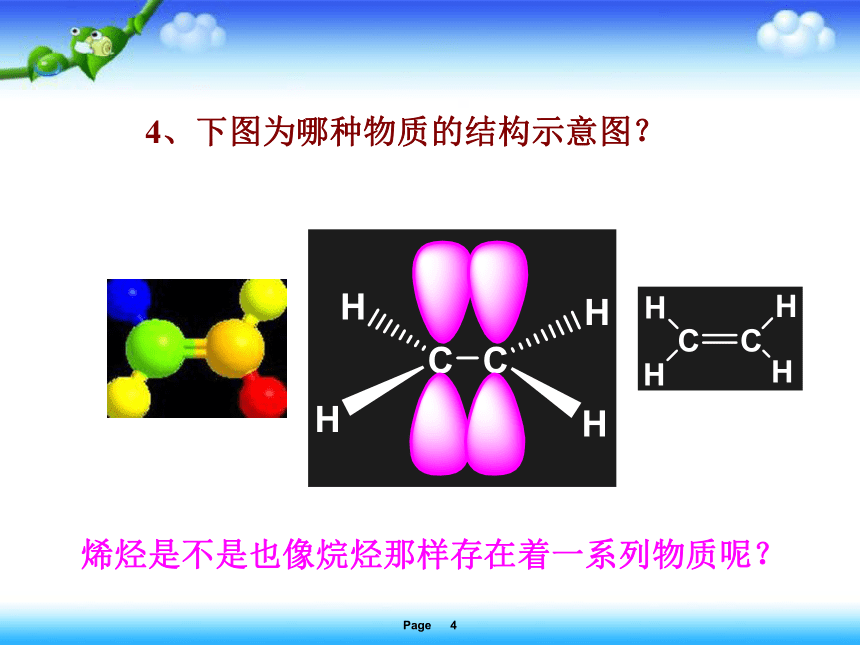
4、下图为哪种物质的结构示意图?
烯烃是不是也像烷烃那样存在着一系列物质呢?
第一节 脂肪烃
一、烷烃和烯烃
二、烯烃的顺反异构
三、炔烃
四、脂肪烃的来源及应用
教学目标
知识与能力
了解烯烃炔烃的结构特点。
掌握烯烃炔烃的化学性质,会写相关方程式。
了解烯烃的顺反异构和乙炔的实验室制法。
认识结构与性质的关系。
过程与方法
情感态度与价值观
从结构的角度进一步认识化学反应的实质。
利用教学中的实验探究脂肪烃的性质。
充分发挥学生学习的主动性。
培养学生勤于观察、勤于总结思考的科学态度。
教学重难点
重点
难点
烯烃、炔烃的结构特点和化学性质。
乙炔的实验室制法。
烯烃的顺反异构。
复习:
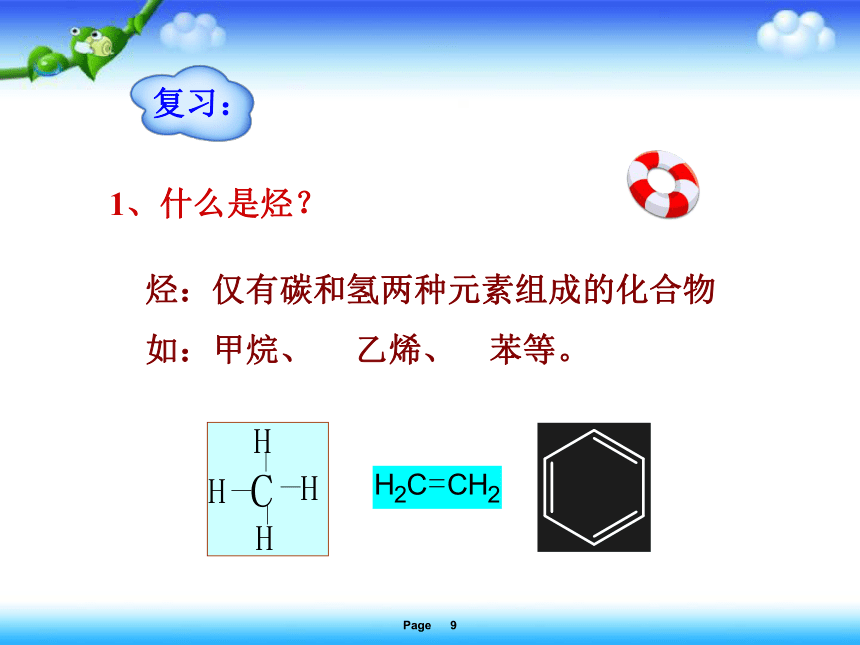
1、什么是烃?
烃:仅有碳和氢两种元素组成的化合物
如:甲烷、 乙烯、 苯等。
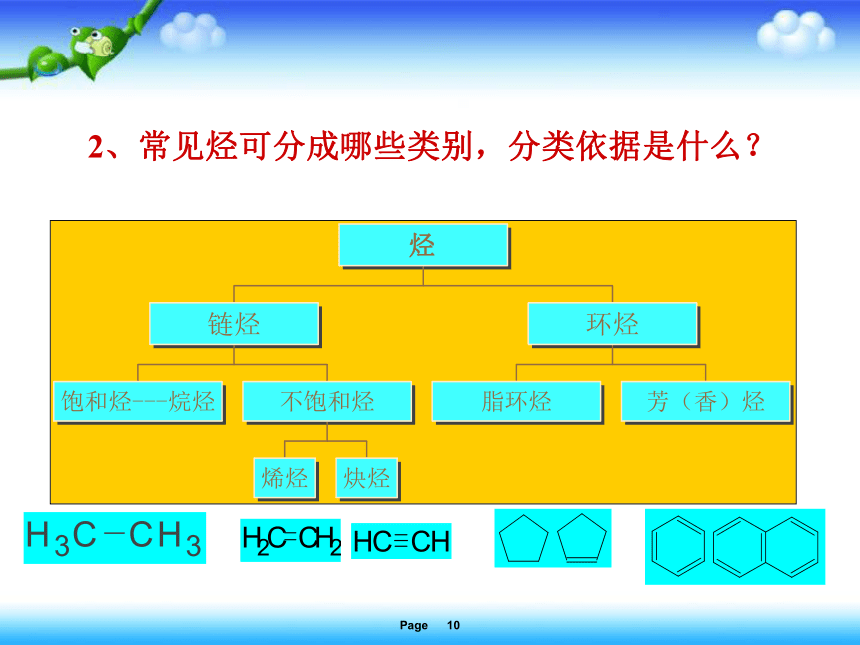
2、常见烃可分成哪些类别,分类依据是什么?
链烃即为脂肪烃,所以脂肪烃包括:
结论:
烷烃
炔烃
烯烃
一、烷烃和烯烃
思考与交流:
1、观察表格2-1,试以分子中碳原子数为横坐标,以沸点或相对密度为纵坐标,画出烷烃碳原子个数与沸点及相对密度的曲线?
(一)物理性质
表2-1部分烷烃的沸点和相对密度
2、观察表格,试以分子中碳原子数为横坐标,以沸点或相对密度为纵坐标,画出烯烃碳原子个数与沸点及相对密度的曲线?
表2-2部分烯烃的沸点和相对密度
结论:
烷烃、烯烃的物理性质随着分子中碳原子数的递增呈现规律性的变化,沸点逐渐升高,相对密度逐渐增大,常温下的存在状态由气态逐渐过渡到液态、固态。
正烷烃的沸点曲线
(二)化学性质
2.1 取代反应
H
+ Cl2
光照
Cl
思考:
乙烷反应生成一氯乙烷,结构上发生怎样的变化?
碳链结构不变,只是乙烷中的一个氢原子被氯原子取代。
结论:
有机物中的某些原子或原子团被其他原子或原子团所代替的反应是取代反应。
2.2 加成反应
H
Br
+ Br—Br
Br
H
H
H
思考:
乙烯反应生成1,2—二氯乙烷,结构上发生怎样的变化?
碳原子之间的键和方式改变,乙烯双键变单键,原双键碳原子分别加上溴原子。
结论:
有机物双键中的Π键断裂加上其他原子或原子团形成两个σ-键的反应是取代反应。
分析比较:
烃的类别 分子结构特点 代表物质 主要化学性质
烷烃
烯烃
结构不同,性质不同。
二、烯烃的顺反异构
同侧
异
侧
顺-2-丁烯
反-2-丁烯
=
产生顺反异构的条件?
1、产生顺反异构的条件
① 分子中必须存在限制旋转的因素, 如:双键或脂环。
② 每个不能旋转的碳原子上必须连有2个不同的原子或原子团。
2、顺反构型命名法
顺式:相同基团在双键同侧
反式:相同基团在双键异侧
顺-2, 2, 5 - 三甲基 -3 -己烯
反- 4 -甲基 - 2 - 戊烯
顺 , 顺 -2, 5 – 庚二烯
乙炔分子的结构示意图
三、炔烃
思考:
观察乙炔分子的结构示意图,试推断炔烃分子结构特点。
(一)炔烃结构
如:乙炔
炔烃:
分子里含有碳碳三键的一类脂肪烃。
1-丁炔
(二)炔烃的制备
实 验 装 置
制备方程式:
(三)炔烃的性质
3.1 可燃性
2C2H2+5O2 4CO2+2H2O
点燃
现象:明亮火焰
3.2 与溴加成
反应方程式:
现象:使溴水褪色。
3.3 与其他物质的加成反应
与氢气加成:
不完全加成生成同碳原子数烯烃;
完全加成生成同碳原子数烷烃
与卤化氢加成:
产物生成遵循马氏规则。
四、脂肪烃的来源及其应用
元素:主要含有C、H元素(95%以上)
物质:主要由各种烷烃、环烷烃和芳香烃所组成的混合物。
(一)、石油
状态:大部分是液态烃,同时溶有少量的气态烃、固态烃,没有固定的熔沸点。
常压加热炉
减压加热炉
常压分馏塔
减压分馏塔
原油
重油
轻柴油
重柴油
煤油
汽油
石油气
轻润滑油
中润滑油
重润滑油
渣油
附:石油分馏示意图
知识小结
1、烷烃、烯烃同系物的性质变化
2、烷烃的取代反应
3、烯烃、炔烃的加成反应
4、脂肪烃的鉴别方法。
课堂练习
1. 下列分子式属于饱和链烃的是
A. C3H4 B. C5H12
C. C4H8 D. C7H8
B
2. 下列化合物不能使溴水退色的是
A. 2—丁烯 B. 1,3—丁二烯
C. 2—丁炔 D. 丁烷
D
3.丙炔和2分子HBr加成的主要产物是
A. 1,1—二溴丙烷 B. 1,2—二溴丙烷
C. 2,2—二溴丙烷 D. 2,3—二溴丙烷
C
4. 写出下列物质的结构式:
甲烷 甲苯
CH4
1、下图为实验室制备哪种物质的装置?
可以为实验室制备甲烷的装置
导入新课
2、自然界中存在着含有多个碳原子的烷烃,那么它们之间又有什么样的关系呢?
3、下图为实验室制备哪种物质的装置?
4、下图为哪种物质的结构示意图?
烯烃是不是也像烷烃那样存在着一系列物质呢?
第一节 脂肪烃
一、烷烃和烯烃
二、烯烃的顺反异构
三、炔烃
四、脂肪烃的来源及应用
教学目标
知识与能力
了解烯烃炔烃的结构特点。
掌握烯烃炔烃的化学性质,会写相关方程式。
了解烯烃的顺反异构和乙炔的实验室制法。
认识结构与性质的关系。
过程与方法
情感态度与价值观
从结构的角度进一步认识化学反应的实质。
利用教学中的实验探究脂肪烃的性质。
充分发挥学生学习的主动性。
培养学生勤于观察、勤于总结思考的科学态度。
教学重难点
重点
难点
烯烃、炔烃的结构特点和化学性质。
乙炔的实验室制法。
烯烃的顺反异构。
复习:
1、什么是烃?
烃:仅有碳和氢两种元素组成的化合物
如:甲烷、 乙烯、 苯等。
2、常见烃可分成哪些类别,分类依据是什么?
链烃即为脂肪烃,所以脂肪烃包括:
结论:
烷烃
炔烃
烯烃
一、烷烃和烯烃
思考与交流:
1、观察表格2-1,试以分子中碳原子数为横坐标,以沸点或相对密度为纵坐标,画出烷烃碳原子个数与沸点及相对密度的曲线?
(一)物理性质
表2-1部分烷烃的沸点和相对密度
2、观察表格,试以分子中碳原子数为横坐标,以沸点或相对密度为纵坐标,画出烯烃碳原子个数与沸点及相对密度的曲线?
表2-2部分烯烃的沸点和相对密度
结论:
烷烃、烯烃的物理性质随着分子中碳原子数的递增呈现规律性的变化,沸点逐渐升高,相对密度逐渐增大,常温下的存在状态由气态逐渐过渡到液态、固态。
正烷烃的沸点曲线
(二)化学性质
2.1 取代反应
H
+ Cl2
光照
Cl
思考:
乙烷反应生成一氯乙烷,结构上发生怎样的变化?
碳链结构不变,只是乙烷中的一个氢原子被氯原子取代。
结论:
有机物中的某些原子或原子团被其他原子或原子团所代替的反应是取代反应。
2.2 加成反应
H
Br
+ Br—Br
Br
H
H
H
思考:
乙烯反应生成1,2—二氯乙烷,结构上发生怎样的变化?
碳原子之间的键和方式改变,乙烯双键变单键,原双键碳原子分别加上溴原子。
结论:
有机物双键中的Π键断裂加上其他原子或原子团形成两个σ-键的反应是取代反应。
分析比较:
烃的类别 分子结构特点 代表物质 主要化学性质
烷烃
烯烃
结构不同,性质不同。
二、烯烃的顺反异构
同侧
异
侧
顺-2-丁烯
反-2-丁烯
=
产生顺反异构的条件?
1、产生顺反异构的条件
① 分子中必须存在限制旋转的因素, 如:双键或脂环。
② 每个不能旋转的碳原子上必须连有2个不同的原子或原子团。
2、顺反构型命名法
顺式:相同基团在双键同侧
反式:相同基团在双键异侧
顺-2, 2, 5 - 三甲基 -3 -己烯
反- 4 -甲基 - 2 - 戊烯
顺 , 顺 -2, 5 – 庚二烯
乙炔分子的结构示意图
三、炔烃
思考:
观察乙炔分子的结构示意图,试推断炔烃分子结构特点。
(一)炔烃结构
如:乙炔
炔烃:
分子里含有碳碳三键的一类脂肪烃。
1-丁炔
(二)炔烃的制备
实 验 装 置
制备方程式:
(三)炔烃的性质
3.1 可燃性
2C2H2+5O2 4CO2+2H2O
点燃
现象:明亮火焰
3.2 与溴加成
反应方程式:
现象:使溴水褪色。
3.3 与其他物质的加成反应
与氢气加成:
不完全加成生成同碳原子数烯烃;
完全加成生成同碳原子数烷烃
与卤化氢加成:
产物生成遵循马氏规则。
四、脂肪烃的来源及其应用
元素:主要含有C、H元素(95%以上)
物质:主要由各种烷烃、环烷烃和芳香烃所组成的混合物。
(一)、石油
状态:大部分是液态烃,同时溶有少量的气态烃、固态烃,没有固定的熔沸点。
常压加热炉
减压加热炉
常压分馏塔
减压分馏塔
原油
重油
轻柴油
重柴油
煤油
汽油
石油气
轻润滑油
中润滑油
重润滑油
渣油
附:石油分馏示意图
知识小结
1、烷烃、烯烃同系物的性质变化
2、烷烃的取代反应
3、烯烃、炔烃的加成反应
4、脂肪烃的鉴别方法。
课堂练习
1. 下列分子式属于饱和链烃的是
A. C3H4 B. C5H12
C. C4H8 D. C7H8
B
2. 下列化合物不能使溴水退色的是
A. 2—丁烯 B. 1,3—丁二烯
C. 2—丁炔 D. 丁烷
D
3.丙炔和2分子HBr加成的主要产物是
A. 1,1—二溴丙烷 B. 1,2—二溴丙烷
C. 2,2—二溴丙烷 D. 2,3—二溴丙烷
C
4. 写出下列物质的结构式:
甲烷 甲苯
CH4
