人教版高中化学选修5 第三章 3.2 醛 上课课件(共33张ppt)
文档属性
| 名称 | 人教版高中化学选修5 第三章 3.2 醛 上课课件(共33张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 851.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-04-15 00:00:00 | ||
图片预览









文档简介
(共33张PPT)
导入新课
甲醛
含甲醛粘合剂成分的层压板
醛
含乙醛成分的橡胶促进剂
桂皮含肉桂醛
杏仁含苯甲醛
思考
1. 那么醛是一类什么样的物质,结构如何?性质如何?
2. 你还知道哪些属于醇类的物质?
醇的结构尤其是官能团羟基决定了醇的性质,那么醛的结构和性质又如何呢?
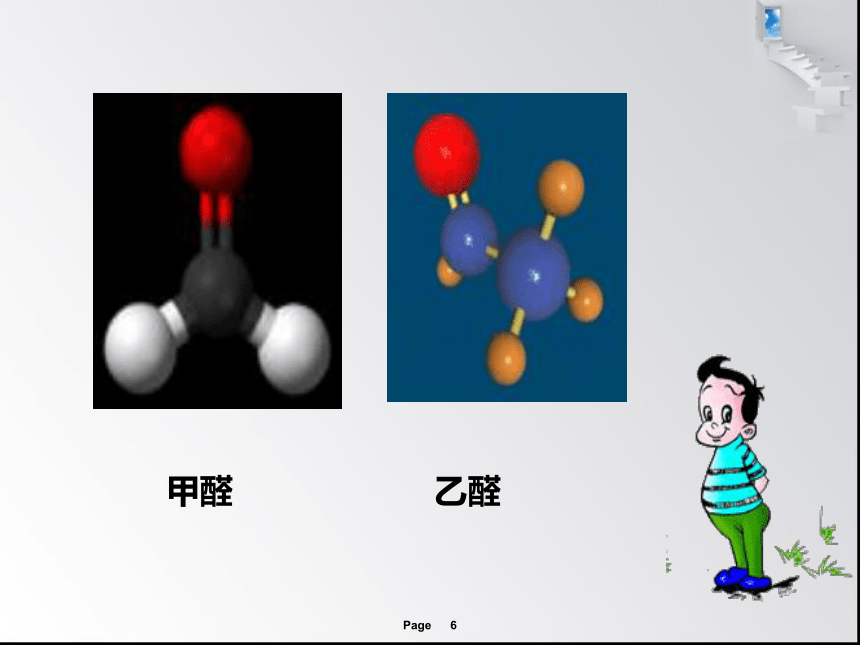
甲醛 乙醛
第二节 醛
一、醛的结构
二、醛的性质
教学目标
知识与能力
理解醛的结构。
能写出醛的官能团。
掌握醛的主要化学性质。
认识结构与性质的关系。
过程与方法
情感态度与价值观
从结构的角度学习醛的化学性质。
利用教学中的试验探究醛的性质。
充分发挥学生学习的主动性。
培养学生勤于观察、勤于总结思考的科学态度。
教学重难点
重 点
难 点
乙醛的结构特点和主要化学性质。
乙醛与银氨溶液、新制氢氧化铜溶液反应的方程式的写法。
思考
回忆乙醇的结构,写出乙醇的性质?
观察乙醛与乙醇结构的异同,推测乙醛的化学性质?
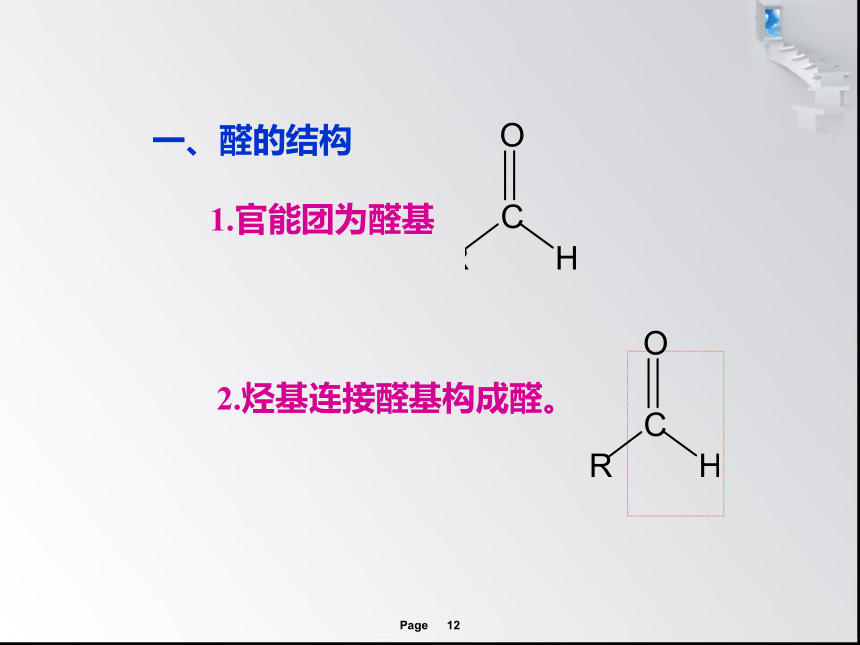
一、醛的结构
1.官能团为醛基
2.烃基连接醛基构成醛。
举例:
乙醛
苯甲醛
3.分类
1、按醛和酮中的烃基种类分
脂肪醛
芳香醛
脂环醛
2、按烃基饱和与否分
饱和醛
不饱和醛
3、按羰基数目分
一元醛酮
多元醛酮
4,4 - 二甲基己醛
4-甲基-2-戊酮
二、醛和酮的命名
脂肪醛酮系统命名法:选择含有羰基的最长碳链为主链,编号从靠近醛基(酮基)一端开始。
芳香醛酮的命名:以脂肪醛酮作为母体,
芳烃的烃 基作为取代基。
苯甲醛
苯乙酮
2—苯丁醛
三、醛 的性质
思考:
观察下面实验,描述实验现象,写出反应方程式,联系日常生活,推测其用途。
(一).氧化反应:
1.与银氨溶液的反应
结论:
1.1 方程式:
CH3CHO +2Ag(NH3)2OH
CH3COONH4+2Ag +3NH3+ H2O
1.2 实质:
有机反应中,加氧或去氢都是氧化。
1.3 结论:
醛有还原性,可以被弱氧化剂氧化。
1.4 应用:
思考:
观察下面实验,描述实验现象,写出反应方程式。
2。与新制氢氧化铜溶液的反应
结论:
2.1 方程式:
2.2 实质:
醛基中碳氢键断裂,形成碳氧键和氧氢键。
2.3 结论:
+
2Cu(OH)2
+
Cu2O
醛有还原性,可以被弱氧化剂氧化。
3.加成反应:
思考:
观察实验,回忆乙醇生成乙醛的反应实质,试推测乙醛如何转化为乙醇。
结论:
3.1 方程式:
3.2 实质:
碳氧双键中π键断裂,形成两个新的σ键。
3.3 结论:
醛还原生成醇。
+
Ni
4. 氧化反应:
思考:
观察实验,描述实验现象,写出反应方程式。
探究:
醛类和酮类官能团相似,那么性质有何异同呢?
酮基
醛基
醛 酮
+
Ni
+
Ni
都可与氢气加成:醛与氢气加成生成伯醇
酮与氢气加成生成仲醇
醛有还原性,可被弱氧化剂 氧化,发生银镜反应等,还可与希夫试剂显色。
酮还原性较差,不能被弱氧化剂氧化,不能发生银镜反应等。
性质差异可鉴别醛类与酮类。
课堂小结
1.醛的化学性质取决于官能团: —CHO
CH3CHO +2Ag(NH3)2OH
CH3COONH4+2Ag +3NH3+ H2O
+
2Cu(OH)2
+
Cu2O
+
Ni
2.醛的鉴别方法:
加入银氨溶液加热有银镜生成。
加入新制氢氧化铜溶液加热有砖红色沉淀生成。
课堂练习
1.下列物质能与斐林试剂反应的是:(??? )
A.乙醛??? B.乙烷???? C.乙烯???? D.乙醇
2. “福尔马林”指的是:(??? )
A.40%的乙醇溶液??????? B.40%的的苯甲醇溶液
C.40%的甲醛溶液??????? D. 40%的丙酮溶液
A
C
3.下列物质中,能与银氨溶液反应生成银镜的是:(??? )
A.苯酚????? B.丙酮???? C.乙烯????? D.苯甲醛
4. 乙醛加氢还原生成____,苯甲醛加氢还原生成______________ 。
5.实验室中,鉴别醛、酮可用的试剂是____________或____________。
D
苯甲醇
乙醇
银氨溶液
新制氢氧化铜
6.完成下列反应方程式:
CH3CH2CHO +2Ag(NH3)2OH
CH3COONH4+2Ag +3NH3+ H2O
+H2
导入新课
甲醛
含甲醛粘合剂成分的层压板
醛
含乙醛成分的橡胶促进剂
桂皮含肉桂醛
杏仁含苯甲醛
思考
1. 那么醛是一类什么样的物质,结构如何?性质如何?
2. 你还知道哪些属于醇类的物质?
醇的结构尤其是官能团羟基决定了醇的性质,那么醛的结构和性质又如何呢?
甲醛 乙醛
第二节 醛
一、醛的结构
二、醛的性质
教学目标
知识与能力
理解醛的结构。
能写出醛的官能团。
掌握醛的主要化学性质。
认识结构与性质的关系。
过程与方法
情感态度与价值观
从结构的角度学习醛的化学性质。
利用教学中的试验探究醛的性质。
充分发挥学生学习的主动性。
培养学生勤于观察、勤于总结思考的科学态度。
教学重难点
重 点
难 点
乙醛的结构特点和主要化学性质。
乙醛与银氨溶液、新制氢氧化铜溶液反应的方程式的写法。
思考
回忆乙醇的结构,写出乙醇的性质?
观察乙醛与乙醇结构的异同,推测乙醛的化学性质?
一、醛的结构
1.官能团为醛基
2.烃基连接醛基构成醛。
举例:
乙醛
苯甲醛
3.分类
1、按醛和酮中的烃基种类分
脂肪醛
芳香醛
脂环醛
2、按烃基饱和与否分
饱和醛
不饱和醛
3、按羰基数目分
一元醛酮
多元醛酮
4,4 - 二甲基己醛
4-甲基-2-戊酮
二、醛和酮的命名
脂肪醛酮系统命名法:选择含有羰基的最长碳链为主链,编号从靠近醛基(酮基)一端开始。
芳香醛酮的命名:以脂肪醛酮作为母体,
芳烃的烃 基作为取代基。
苯甲醛
苯乙酮
2—苯丁醛
三、醛 的性质
思考:
观察下面实验,描述实验现象,写出反应方程式,联系日常生活,推测其用途。
(一).氧化反应:
1.与银氨溶液的反应
结论:
1.1 方程式:
CH3CHO +2Ag(NH3)2OH
CH3COONH4+2Ag +3NH3+ H2O
1.2 实质:
有机反应中,加氧或去氢都是氧化。
1.3 结论:
醛有还原性,可以被弱氧化剂氧化。
1.4 应用:
思考:
观察下面实验,描述实验现象,写出反应方程式。
2。与新制氢氧化铜溶液的反应
结论:
2.1 方程式:
2.2 实质:
醛基中碳氢键断裂,形成碳氧键和氧氢键。
2.3 结论:
+
2Cu(OH)2
+
Cu2O
醛有还原性,可以被弱氧化剂氧化。
3.加成反应:
思考:
观察实验,回忆乙醇生成乙醛的反应实质,试推测乙醛如何转化为乙醇。
结论:
3.1 方程式:
3.2 实质:
碳氧双键中π键断裂,形成两个新的σ键。
3.3 结论:
醛还原生成醇。
+
Ni
4. 氧化反应:
思考:
观察实验,描述实验现象,写出反应方程式。
探究:
醛类和酮类官能团相似,那么性质有何异同呢?
酮基
醛基
醛 酮
+
Ni
+
Ni
都可与氢气加成:醛与氢气加成生成伯醇
酮与氢气加成生成仲醇
醛有还原性,可被弱氧化剂 氧化,发生银镜反应等,还可与希夫试剂显色。
酮还原性较差,不能被弱氧化剂氧化,不能发生银镜反应等。
性质差异可鉴别醛类与酮类。
课堂小结
1.醛的化学性质取决于官能团: —CHO
CH3CHO +2Ag(NH3)2OH
CH3COONH4+2Ag +3NH3+ H2O
+
2Cu(OH)2
+
Cu2O
+
Ni
2.醛的鉴别方法:
加入银氨溶液加热有银镜生成。
加入新制氢氧化铜溶液加热有砖红色沉淀生成。
课堂练习
1.下列物质能与斐林试剂反应的是:(??? )
A.乙醛??? B.乙烷???? C.乙烯???? D.乙醇
2. “福尔马林”指的是:(??? )
A.40%的乙醇溶液??????? B.40%的的苯甲醇溶液
C.40%的甲醛溶液??????? D. 40%的丙酮溶液
A
C
3.下列物质中,能与银氨溶液反应生成银镜的是:(??? )
A.苯酚????? B.丙酮???? C.乙烯????? D.苯甲醛
4. 乙醛加氢还原生成____,苯甲醛加氢还原生成______________ 。
5.实验室中,鉴别醛、酮可用的试剂是____________或____________。
D
苯甲醇
乙醇
银氨溶液
新制氢氧化铜
6.完成下列反应方程式:
CH3CH2CHO +2Ag(NH3)2OH
CH3COONH4+2Ag +3NH3+ H2O
+H2
