人教版化学九年级下册第9单元《溶液》测试题(含答案)
文档属性
| 名称 | 人教版化学九年级下册第9单元《溶液》测试题(含答案) |  | |
| 格式 | zip | ||
| 文件大小 | 279.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-04-14 10:52:25 | ||
图片预览




文档简介
第9单元《溶液》测试题
一、单选题(每小题只有一个正确答案)
1.化学知识涉及衣、食、住、行各个领域,下列有 关说法全部正确的一组是
A衣 衣服上的油污用汽油清洗是利用其乳化作用
B食 生火煮饭离不开氧气,是因为氧气具有可燃性
C住 能闻到新装修房屋里的异味,是因为分子之间有间隔
D行 活性炭包可用于吸附车内的异味
A.A B.B C.C D.D
2.对下列事实解释正确的是
事实 解释
A 酒精灯不用时.需用灯帽盖好 酒精分子会不断运动到空气中
B 常温下铜为固态而水银是液态 粒子热胀冷缩
C 将糖加入水中一段时间后.每一口水都有甜味 水分子间有一定间隔
D 金刚石比石墨硬度大 碳原子的结构不同
A.A B.B C.C D.D
3.下列有关水的叙述正确的是
A.所有溶液中的溶剂均为水 B.受热时水分子的体积逐渐变大
C.衣服晒干过程中水分子分解为气体 D.与肥皂水混合能产生大量泡沫的是软水
4.实验室有一块质量为12.5g的石灰石样品(杂质不溶于水,也不参加反应),高温煅烧一段时间后,称得固体质量为10.3g,向固体中加入100g稀盐酸,恰好完全反应,过滤,所得滤液质量为105.6g。则与稀盐酸反应的碳酸钙占样品的质量分数为
A.20% B.40% C.50% D.80%
5.将硝酸钾的不饱和溶液变为饱和溶液的方法不可行的是 ( )
A.升温 B.降温 C.蒸发水 D.加溶质
6.调味品是重要的食品添加剂,将下面调味品加入水中,不能形成溶液的是
A.白醋 B.白糖 C.味精 D.芝麻油
7.下列是对初中化学中“三”的总结,不完全正确的一组是( )
A.构成物质的三种微粒:原子、分子、离子
B.灭火的三种方法:隔绝氧气、降低着火点、清除或隔离可燃物
C.常见的三种防锈措施:保持洁净和干燥、表面覆盖保护层、改变金属内部结构
D.清除污垢常涉及三种原理:乳化(如洗涤剂)、溶解(如干洗剂)、化学反应(如酸液除锈)
8.氯化钾(KCl)和氯酸钾(KClO3)的溶解度随温度变化曲线如图所示,下列说法正确的是
A.30℃时,KCl饱和溶液的溶质质量分数为35%
B.60℃时,a点对应KCl溶液恒温加水可变饱和
C.KCl的溶解度随温度变化的趋势比KClO3大
D.90℃150gKClO3饱和溶液降温到10℃可析出45g晶体
9.下列实验目的对应实验方案不正确的是
选项 实验目的 实验方案
A 除去MnO2中少量KCl 加水溶解、过滤、洗涤、干燥
B 除去N2中少量O2 通过灼热的足量的铜网
C 除去CO2中少量CO 通入O2点燃
D 鉴别纯铝和硬铝 将两者相互刻画,比较硬度
A.A B.B C.C D.D
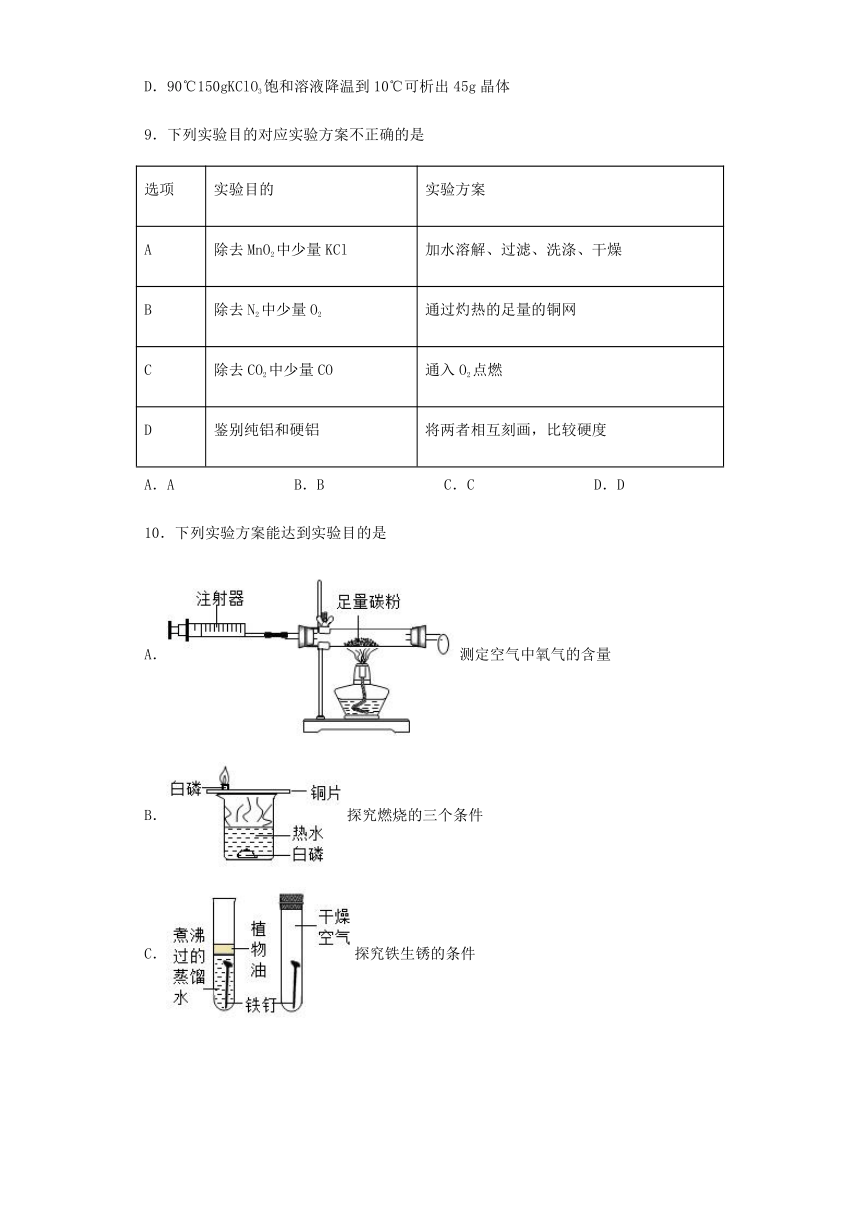
10.下列实验方案能达到实验目的是
A.测定空气中氧气的含量
B.探究燃烧的三个条件
C.探究铁生锈的条件
D.探究同种溶质在不同溶剂中的溶解性
11.对比实验是化学中常用的实验手段。下列探究不需要进行对比实验的是
A.物质溶解性的大小
B.可燃物燃烧的条件
C.烧碱样品中氢氧化钠的含量
D.影响金属与酸反应速率的因素
12.如图为甲乙两物质的溶解度曲线,下列说法正确的是
A.甲的溶解度大于乙的溶解度
B.要使接近饱和的乙溶液转化为饱和溶液,可以采用蒸发溶剂 的方法
C.t1℃时,甲、乙两物质饱和溶液中溶质的质量分数均为15%
D.t2℃时,将50 g甲物质放入100 g水中,得到溶液的质量为150 g
13.今年4月份同学们都参加全市的中考实验技能考试,让同学们切身体会到了规范操作的重要性。下列实验操作符合规范要求的是( )
A.“高锰酸钾制取氧气”实验中,收集好气体后应先将导管移出水槽再停止加热
B.“粗盐中难溶性杂质的去除”实验中,过滤时将悬浊液直接倒入漏斗里
C.“配制一定溶质质量分数的氯化钠溶液”实验中,多余的氯化钠应放回原瓶
D.“溶液酸碱性的检验”实验中,测定溶液pH时应先将试纸湿润
二、填空题
14.用化学知识回答下列问题:
(1)打开汽水瓶盖,汽水会自动喷出的原因是 ;
(2)用洗涤剂去除油污是因为洗涤剂具有 功能;
(3)食品袋内充入氮气的目的是 ;
(4)防治“白色污染”的措施有 。(答一点即可)
15.右图是A、B、C三种固体物质的溶解度曲线。
(1)t1℃时,A、B、C三种物质溶解度由大到小的顺序是 ;
(2)若A中含有少量B时,提纯A可采用的方法是 ;
(3)t2℃时,将A、B、C三种物质的饱和溶液同时降温到t1℃,所得溶液中溶质质量分数最小的是 。
16.写出下表所示溶液中溶质的化学式:
溶液 溶质的化学式 溶液 溶质的化学式
硫酸铜溶液 ____ 医用生理盐水 ___
高锰酸钾消毒液 _____ 澄清石灰水 _____
17.如下图是 A、B、C 三种固体物质的溶解度曲线,请回答:
(1)20℃时,溶解度大小相等的物质是________;
(2)三种物质中,________的溶解度受温度影响最大。
(3)将A的不饱和溶液变为饱和溶液,可以采取的方法是____(任填一种)。
18.根据下列数型图像回答:
(1)图一是盐酸和氢氧化钠溶液进行中和反应时,反应过程中溶液的pH变化曲线,向盐酸中加入的氢氧化钠溶液质量为ng时,所得溶液中含有的离子为______(填离子符号) 。
(2)图二是20℃时,取10mL10%的NaOH溶液与烧杯中,逐滴加入10%的盐酸,随着盐酸的加入,烧杯中溶液温度与加入盐酸体积的变化关系。
①由图可知中和反应是_____反应(填“吸热”、“放热” );
②甲同学用氢氧化钠固体与稀盐酸反应也得到相同的结论,乙同学认为不严密,因为_______________。
(3)图三是a、b、c三种物质的溶解度曲线。a与c的溶解度曲线相交于P点,据图回答:
①t1℃时,接近饱和的c物质溶液,在不改变溶液质量的条件下,可用________的方法达到饱和状态。
②当t2℃时,150g a物质饱和溶液降温到t1℃时,可析出______a物质。
(4)下图托盘天平两边是等质量的铁和镁 分别跟等质量等浓度的稀硫酸反应, 反应的时间t与生成氢气质量m的 变化关系如图四。试回答:从开始反应到不在产生气体为止,天平指针偏转情况是____________
三、推断题
19.我国化工专家侯德榜创立了“侯氏制碱法”,促进了世界制碱技术的发展。其流程简图和部分物质的溶解度曲线如下:
已知:①母液中有一种铵态氮肥
②
请回答下列问题:
(1)操作a的名称是_____。
(2)结合图2分析,图1反应1中NaHCO3作为晶体析出的原因是_____,从图2中还能获得的一条信息是_____。
(3)图1中得到的母液中一定含有的阳离子是_____ (填离子符号), 流程中可以循环使用的物质是_____。
(4)从图2可以看出温度高于60°C,NaHCO3 的溶解度曲线“消失”了,其原因可能是_____。
20.A、B、C、D、E、F之间存在如图的转化关系(部分物质及反应条件已略去)、已知A是一种气体肥料;D含有人体中含量最高的金属元素,其相对分子质量为100.则C的用途为_____;E→F的化学方程式为____;图示转化关系中未涉及的基本反应类型为_____。
四、实验题
21.课外小组的同学自制一块多槽铁板,设计了下图所示装置,用以探究燃烧的条件。(说明:金属板上白磷足量)。回答下列问题:
(1)推出可燃物燃烧需要一定温度的依据是__________。
(2)将过氧化氢溶液滴入盛有MnO2 的金属槽中,发生反应的化学方程式为__________。
(3)有同学提出“将NaOH换成水,然后将水换成浓硫酸,也可以完成探究活动”。你认为是否可行,为什么?_____________。
22.如图所示是某化学小组部分实验过程的装置图:
(1)写出标号仪器的名称:b_____。
(2)A图中所称食盐的质量为_____g,若食盐与砝码的位置颠倒了,游码显示仍为A图,则食盐的实际质量为_____g。
(3)如图B所示操作,可能造成的后果是_____。
(4)欲量取40mL水,应选用的仪器是50mL的量筒和_____,某同学如C图读数,则实际量取的液体_____40mL(填“大于”“小于”或“等于”)。
(5)指出D操作可能造成的后果_____。
(6)如图所示,实验室要加热约150mL的水,要完成该实验需要准备的仪器有_____(填序号)。
五、计算题
23.现有时的碳酸钠溶液,则
从该溶液中取出,其质量分数为________,其中含溶质________
将剩余溶液蒸发水后,其溶液的溶质质量分数是________.
24.水是生命之源,人类的生产、生活都离不开水。
(1)自然界中的水含有许多可溶性和不溶性杂质。长期饮用硬水可能会引起体内结石,生活中常用来_________区分软水与硬水,常用___________的方法来降低水的硬度。在水的净化过程中,除去水中不溶性的固体杂质,其实验操作方法称为_________。
(2)水是常用的溶剂,配制下列溶液时,以水做溶剂的是______________(填序号)。
A.食盐 B.医用碘酒 C.高锰酸钾 D.植物油
(3)右图曲线A、B、C分别代表三种固体物质的溶解度曲线,根据图示回答:
①对A物质来说,a点的意义是_____________。
②将t1℃ 140gA的饱和溶液升温至t2℃时,可用图上的______________点表示。
③若将t2℃时A、 B、C三种物质的饱和溶液降温到t1℃所得溶液质量分数由大到小的顺序是________。
④t1℃时,将30g A物质放入50g水中,充分搅拌后所得溶液的溶质质量分数为_____________。(计算结果保留一位小数)
⑤如果要获得C的晶体,采用的方法是_______(填“升温”或“降温”)。
(4)世博园区内用“活性炭+超滤膜+紫外线”组合工艺获得直饮水。其中活性炭的作用是_______;化合物X是一种新型的自来水消毒剂,工业上制取X 的化学方程式为:Cl2 + 2 NaClO2 == 2 NaCl + 2 X,则X的化学式为__________________;能够充分说明水的组成的化学反应方程式为______________________。
参考答案
1.D 2.A 3.D 4.B 5.A 6.D 7.B 8.D 9.C 10.D 11.C 12.B 13.A
14.(1) 压强减小,二氧化碳(气体)溶解度降低; (2) 乳化 ;(3) 防腐(或防挤压变形等合理即可);(4) 回收各种废弃塑料 (合理即可)
15.(1)B>A=C (2)冷却热饱和溶液(或降温结晶) (3)C
16.CuSO4 NaCl KMnO4 Ca(OH)2
17.A和B A 降温,加溶质A等
18.(1)Na+ Cl-
(2)①放热 ②氢氧化钠固体溶于水也放出热量
(3)①升温 ②30
(4)先向右偏,后平衡
19.过滤 此温度下碳酸氢钠的溶解度较小 氯化铵的溶解度受温度的影响较大 Na+、NH4+ CO2 温度高于60℃时,碳酸氢钠开始分解
20.作干燥剂 置换反应
21.滴水之前白磷不燃烧,滴水之后白磷燃烧 不行,铁能与硫酸反应生成氢气,有爆炸的危险
22.漏斗 12.4 7.6 试管炸裂 胶头滴管 小于 液体溅出 ①④⑤⑥
23.,;
24.肥皂水 加热煮沸 过滤 AC t1℃ 时A的溶解度是40g B C B>C>A 28.6% 升温 吸附 ClO2 2H2O2H2↑ + O2↑或2H2 + O22H2O
同课章节目录
