第8章 常见的酸碱盐 限时训练题(含答案)
文档属性
| 名称 | 第8章 常见的酸碱盐 限时训练题(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-04-16 00:00:00 | ||
图片预览

文档简介
中小学教育资源及组卷应用平台
第8章 常见的酸碱盐 限时训练题
(时间:45分钟 满分:70分)
可能用到的相对原子质量:H-1 O-16 C-12 N-14 Cu-64 Na-23
一.选择题(每小题3分,共30分)
1、下列物质的溶液长期放置在空气中,溶液质量因发生化学变化而减少的是 ( )
A.烧碱 B.石灰水 C.浓盐酸 D.氯化钾
2、分别向甲、乙、丙三种无色溶液中滴加紫色石蕊试液、观察到甲溶液变红色,乙溶液变蓝色,丙溶液变紫色。则它们的pH由小到大的排列是( )
A.甲、乙、丙 B.甲、丙、乙 C.乙、甲、丙 D.丙、甲、乙
3、“雪碧”等碳酸饮料的pH小于7,晃动后打开瓶盖,其pH将( )
A.变大 B.变小 C.不变 D.无法判断
4、下列物质中能与澄清石灰水反应,但反应若不加指示剂则无明显现象的是( )
A.氯化铁溶液 B.碳酸钠溶液 C.稀盐酸 D.碳酸钾溶液
5、尿素[CO(NH2)2]是一种重要的化学肥料。下列说法正确的是( )
A.尿素属于复合肥料 B.60g尿素中含有氮元素的质量为28g
C.尿素中含有氢分子 D.尿素中碳、氧两种元素的质量比为1:1
6、食盐、食醋、纯碱均是家庭厨房中常用的物质,利用这些物质,我能够完成的实验是( )
①检验自来水中是否含有氯离子? ②除去热水瓶中的水垢?
③区分食盐和纯碱? ④检验鸡蛋壳中是否含有碳酸钙
A.①②? B.①③ ?? C.①④? D.②③④
7、.下列各组离子在pH=1的溶液中能大量共存,并形成无色透明溶液的是( )
A.Fe3+、NO3-、OH- B.K+、NO3-、CO32-
C.Ba2+、MnO4-、SO42- D.NH4+、Cl-、SO42-
8、下列各组物质的溶液,不用其他试剂,不能将它们鉴别出来的是( )
A.CuSO4、HCl、MgSO4、NaOH B.H2SO4、FeCl3、NaOH、NaCl
C.NaCl、Ba(OH)2、Na2CO3、Na2SO4 D.K2SO4、Na2CO3、BaCl2、HCl
9、下列各组物质中,能发生复分解反应且反应前后溶液总质量不变的是( )
A.铁和硫酸铜溶液 B.氢氧化钠溶液和盐酸
C.硫酸和氯化钡溶液 D.氯化钾溶液和硫酸钠溶液
10、下列各组实验中不能达到实验目的的是( )
选项 实验目的 实验方法
A 鉴别氢氧化钠、氯化钠、硝酸铵三种固体 分别取样,加水溶解
B 除去氮气中少量的氧气 通过灼热的铜网
C 鉴别CuSO4、MgSO4、NaCl、KOH四种溶液 不加其它试剂,利用物质的颜色和相互反应进行鉴别
D 除去硝酸钠中少量的氯化钠 加过量的AgNO3溶液,过滤
二、非选择题(共6题,40分)
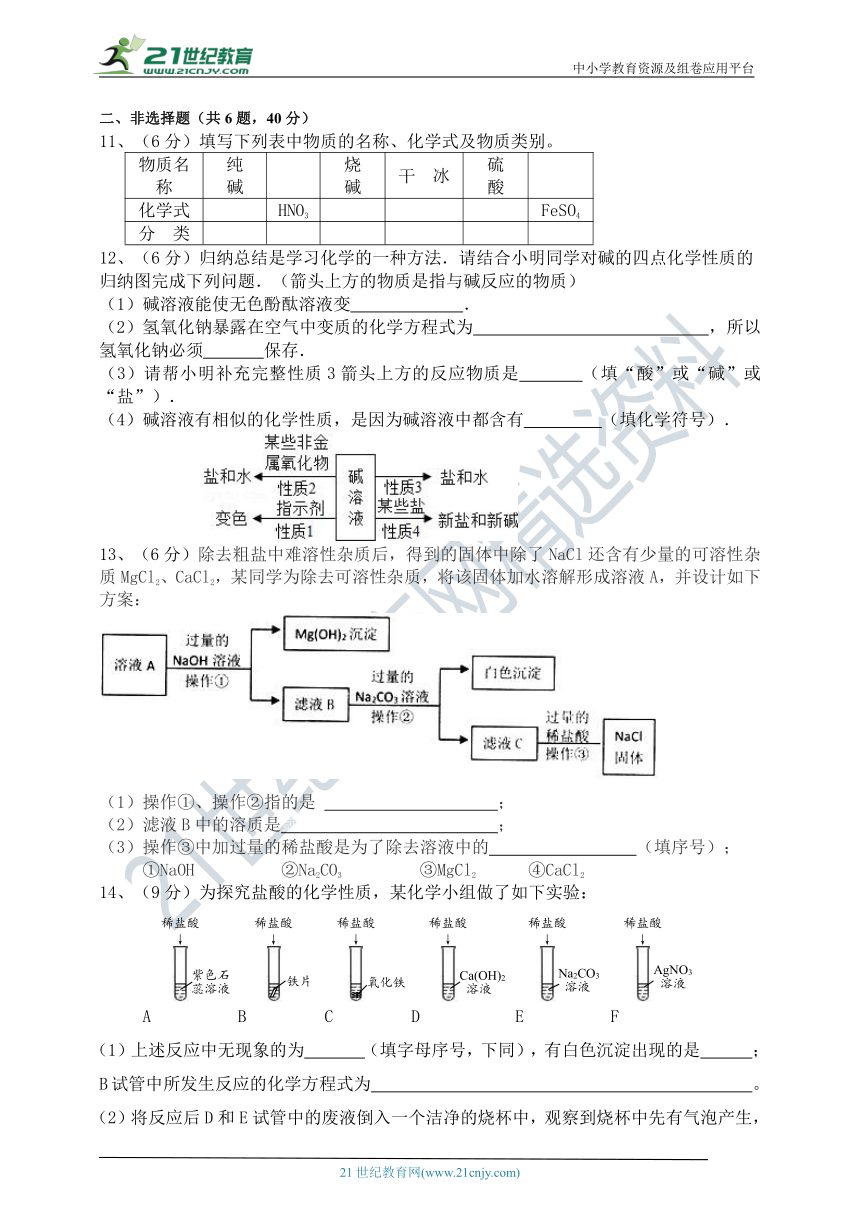
11、(6分)填写下列表中物质的名称、化学式及物质类别。
物质名称 纯 碱 烧 碱 干 冰 硫 酸
化学式 HNO3 FeSO4
分 类
12、(6分)归纳总结是学习化学的一种方法.请结合小明同学对碱的四点化学性质的归纳图完成下列问题.(箭头上方的物质是指与碱反应的物质)
(1)碱溶液能使无色酚酞溶液变 .
(2)氢氧化钠暴露在空气中变质的化学方程式为 ,所以氢氧化钠必须 保存.
(3)请帮小明补充完整性质3箭头上方的反应物质是 (填“酸”或“碱”或“盐”).
(4)碱溶液有相似的化学性质,是因为碱溶液中都含有 (填化学符号).
13、(6分)除去粗盐中难溶性杂质后,得到的固体中除了NaCl还含有少量的可溶性杂质MgCl2、CaCl2,某同学为除去可溶性杂质,将该固体加水溶解形成溶液A,并设计如下方案:
(1)操作①、操作②指的是 _________________ ;
(2)滤液B中的溶质是氯化钠、氢氧化钠、氯 化钙;
(3)操作③中加过量的稀盐酸是为了除去溶液中的① ②(填序号);
①NaOH? ?②Na2CO3? ?③MgCl2? ?④CaCl2
14、(9分)为探究盐酸的化学性质,某化学小组做了如下实验:
A B C D E F
(1)上述反应中无现象的为 (填字母序号,下同),有白色沉淀出现的是 ;B试管中所发生反应的化学方程式为 。
(2)将反应后D和E试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行探究。
【提出问题】滤液中溶质的成分是什么?
【假设与猜想】猜想一:NaCl 猜想二:NaCl和CaCl2
猜想三:NaCl、Ca(OH)2和HCl 猜想四: 。
【讨论与交流】经讨论,同学们一致认为猜想 是错误的。
【实验与结论】
实验步骤 实验现象 实验结论
取少量滤液于试管中,滴加适量碳酸钠溶液 无现象 猜想四成立
取少量滤液于试管中,滴加适量
【拓展与迁移】稀盐酸和稀硫酸有相似的化学性质是因为它们的溶液中都存在 。
15.(8分)A、B、C、D、E、F六种物质都是初中化学内容中涉及的化合物,转化关系如下图所示,其中D是最常见的溶剂。
⑴根据上图推断,C是?? ? ,D是?? ? ,E是? ? (填写化学式)。
⑵写出反应①的化学方程式????????????????????? ,
写出反应②的化学方程式??????????? ??????????。
反应④属于?????????? 反应(填写基本反应类型)。
16.(5分)向盛有193.8g硫酸铜溶液的烧杯中,逐滴加入质量分数为8%的氧氧化钠溶液,反应过程中生成沉淀的质量与所用氧氧化钠溶液的质量关系如图所示。
请计算:
(1)恰好完全反应时生成沉淀的质量。
(2)恰好完全反应时溶液中溶质的质量分数。
参考答案
一.选择题(每小题3分,共30分)
1.B 2.B 3.A 4.C 5.B 6.D 7.D 8.C 9.B 10.D
二、非选择题(共6题,40分)
11.Na2CO3 盐; 硝酸 酸; NaOH 碱; CO2 氧化物; H2SO4 酸;硫酸亚铁 盐
12. (1)红色; (2)2NaOH+CO2=Na2CO3+H2O,密封; (3)酸; (4)OH﹣
13. (1)过滤; (2)氯化钠、氢氧化钠、氯化钙; (3)①②。
14. (1)D F Fe+2HCl===FeCl2+H2↑
(2)【假设与猜想】NaCl和Na2CO3 【讨论与交流】三
【实验与结论】稀盐酸(或氯化钙溶液或氯化钡溶液) 有气泡产生(或有白色沉淀产生)(合理即可)
【拓展与迁移】H+(或氢离子)
15. ⑴CO2, H2O, Ca(OH)2。
⑵CaCO3高温CaO+ CO2↑,CO2+ NaOH= Na2CO3+ H2O。复分解。
16.解:设生成氧氧化铜的质量为x,生成硫酸钠的质量为y。
CuSO4+ 2NaOH=Cu(OH)2↓+Na2SO4
80 98 142
100g×8% x y
=,解得x=9.8g
=,解得y=14.2g
溶液中溶质质量分数=×100%=5%
答:(1)恰好完全反应时生成沉淀的质量为9.8g;(2)所得溶液中溶质的质量分数为5%。
紫色石
蕊溶液
稀盐酸
↓
铁片
稀盐酸
↓
氧化铁
稀盐酸
↓
Ca(OH)2
溶液
稀盐酸
↓
稀盐酸
↓
Na2CO3
溶液
AgNO3
溶液
稀盐酸
↓
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
