2.2化学能转化为电能(第3课时 )同步课件13页
文档属性
| 名称 | 2.2化学能转化为电能(第3课时 )同步课件13页 |

|
|
| 格式 | zip | ||
| 文件大小 | 4.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-04-16 00:00:00 | ||
图片预览






文档简介
(共13张PPT)
第三单元 化学能与电能的转化
化学能转化为电能
第3课时
Zn
Cu
ZnSO4
CuSO4
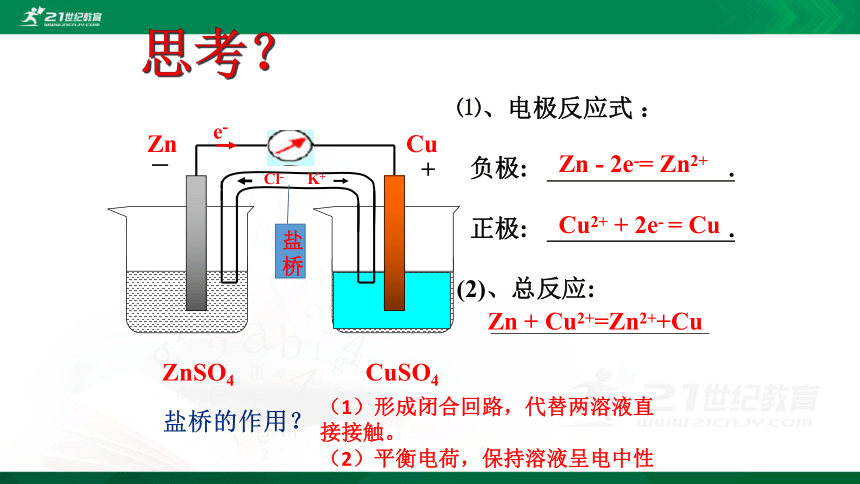
⑴、电极反应式 :
负极: .
正极: .
(2)、总反应:
Zn - 2e-= Zn2+
Cu2+ + 2e- = Cu
Zn + Cu2+=Zn2++Cu
e-
—
+
?
Cl- K+
思考?
盐桥
盐桥的作用?
(1)形成闭合回路,代替两溶液直接接触。
(2)平衡电荷,保持溶液呈电中性
练习1、某化学兴趣小组为了探究铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
编号 电极材料 电解质溶液 电流计指针偏转方向(既为正极)
1 Mg、Al 稀盐酸 偏向Al
2 Al、Cu 稀盐酸 偏向Cu
3 Al、C(石墨) 稀盐酸 偏向石墨
4 Mg、Al 氢氧化钠溶液 偏向Mg
5 Al、Zn 浓硝酸 偏向Al
试根据表中的实验现象回答下列问题: (1)实验1、2中Al所作的电极(正极或负极)是否相同________(填“相同”或“不相同”)。
不相同
(2)根据实验3完成下列填空: ①铝为________极,电极反应式:_____________________。 ②石墨为________极,电极反应式:__________________。 ③电池总反应式:___________________________________。
负
2Al-6e-===2Al3+
正
6H++6e-===3H2↑
2Al+6HCl===2AlCl3+3H2↑
(3)实验4中铝作负极还是正极?________,理由是__________________________________。
(4)解释实验5中电流计指针偏向铝的原因:___________________________________________ ________________________________________________
(5)根据实验结果总结出影响铝在原电池中作正极或负极的因素:______________________________。
负极
铝可与氢氧化钠溶液发生氧化还原反应,而镁不与氢氧化钠溶液发生反应
在浓硝酸中被钝化,锌在浓硝酸中被氧化,即在浓硝酸中Zn作原电池的负极,Al作原电池的正极,所以电流计指针偏向铝
①另一个电极材料的活泼性;②铝电极与电解质溶液能否发生自发的氧化还原反应
练习2、将镁条、铝条平行插入盛有一定浓度NaOH溶液的烧杯中,用导线和电流表连接成原电池,装置如图所示。此电池工作时,下列叙述正确的是( )
①镁为正极 ②电子由铝片通过导线流向镁片 ③该电池的内电路中,阳离子向负极迁移 ④镁片上发生的反应为:Mg-2e-===Mg2+ ⑤该装置能够将电能转化为化学能 ⑥负极反应为Al-3e-+4OH-===AlO2-+2H2O ⑦正极发生还原反应,负极发生氧化反应 ⑧Al是电池负极,开始工作时溶液中会立即有白色沉淀析出
A.①②⑦⑧ B.③④⑤⑥ C.①②⑥⑦ D.②③⑤⑧
C
厚德 博学 励志 笃行
厚德 博学 励志 笃行
探究金属腐蚀的原因
铁锈主要成分 :Fe2O3 ·xH2O
金属阳离子
失e-
(氧化反应)
金属原子
金属腐蚀的本质:
M – ne- → Mn+
是指金属或合金跟接触的气体或液体发生氧化还原反应而腐蚀损耗的过程。
金属腐蚀
厚德 博学 励志 笃行
化学腐蚀
金属跟干燥气体或非电解质液体直接接触反应
不纯金属或合金跟电解质溶液接触形成原电池
电化学腐蚀
金属腐蚀
更普遍
厚德 博学 励志 笃行
碳粉、铁粉、
食盐水
实验改进
探究电化学腐蚀的原因
厚德 博学 励志 笃行
6个小时后
碳粉、铁粉、
食盐水
厚德 博学 励志 笃行
负极: 2Fe – 4e- = 2Fe2+
正极: O2+4e- +2H2O = 4OH-
总式:2Fe + O2 +2H2O =2 Fe(OH)2
4 Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
2Fe(OH)3=Fe2O3·xH2O+(3-x) H2O
电化学腐蚀——吸氧腐蚀
酸性很弱或中性水膜
厚德 博学 励志 笃行
负极: Fe – 2e- = Fe2+
正极: 2H+ +2e- = H2↑
总式:Fe + 2H+ = Fe2+ + H2↑
思考与交流:酸雨降下之后腐蚀的原理和刚才探究的原理有什么区别?
碳粉、铁粉、
稀醋酸
电化学腐蚀——析氢腐蚀
酸性较强水膜
练习1.利用反应2Cu+O2+2H2SO4===2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池。
(1)负极材料是________(写名称),电极反应式为_________________________。
(2)正极电极反应式为_____________________________。
(3)溶液中向________极移动。
铜
Cu?2e?Cu2+
O2+4e?+4H+===2H2O
负
第三单元 化学能与电能的转化
化学能转化为电能
第3课时
Zn
Cu
ZnSO4
CuSO4
⑴、电极反应式 :
负极: .
正极: .
(2)、总反应:
Zn - 2e-= Zn2+
Cu2+ + 2e- = Cu
Zn + Cu2+=Zn2++Cu
e-
—
+
?
Cl- K+
思考?
盐桥
盐桥的作用?
(1)形成闭合回路,代替两溶液直接接触。
(2)平衡电荷,保持溶液呈电中性
练习1、某化学兴趣小组为了探究铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
编号 电极材料 电解质溶液 电流计指针偏转方向(既为正极)
1 Mg、Al 稀盐酸 偏向Al
2 Al、Cu 稀盐酸 偏向Cu
3 Al、C(石墨) 稀盐酸 偏向石墨
4 Mg、Al 氢氧化钠溶液 偏向Mg
5 Al、Zn 浓硝酸 偏向Al
试根据表中的实验现象回答下列问题: (1)实验1、2中Al所作的电极(正极或负极)是否相同________(填“相同”或“不相同”)。
不相同
(2)根据实验3完成下列填空: ①铝为________极,电极反应式:_____________________。 ②石墨为________极,电极反应式:__________________。 ③电池总反应式:___________________________________。
负
2Al-6e-===2Al3+
正
6H++6e-===3H2↑
2Al+6HCl===2AlCl3+3H2↑
(3)实验4中铝作负极还是正极?________,理由是__________________________________。
(4)解释实验5中电流计指针偏向铝的原因:___________________________________________ ________________________________________________
(5)根据实验结果总结出影响铝在原电池中作正极或负极的因素:______________________________。
负极
铝可与氢氧化钠溶液发生氧化还原反应,而镁不与氢氧化钠溶液发生反应
在浓硝酸中被钝化,锌在浓硝酸中被氧化,即在浓硝酸中Zn作原电池的负极,Al作原电池的正极,所以电流计指针偏向铝
①另一个电极材料的活泼性;②铝电极与电解质溶液能否发生自发的氧化还原反应
练习2、将镁条、铝条平行插入盛有一定浓度NaOH溶液的烧杯中,用导线和电流表连接成原电池,装置如图所示。此电池工作时,下列叙述正确的是( )
①镁为正极 ②电子由铝片通过导线流向镁片 ③该电池的内电路中,阳离子向负极迁移 ④镁片上发生的反应为:Mg-2e-===Mg2+ ⑤该装置能够将电能转化为化学能 ⑥负极反应为Al-3e-+4OH-===AlO2-+2H2O ⑦正极发生还原反应,负极发生氧化反应 ⑧Al是电池负极,开始工作时溶液中会立即有白色沉淀析出
A.①②⑦⑧ B.③④⑤⑥ C.①②⑥⑦ D.②③⑤⑧
C
厚德 博学 励志 笃行
厚德 博学 励志 笃行
探究金属腐蚀的原因
铁锈主要成分 :Fe2O3 ·xH2O
金属阳离子
失e-
(氧化反应)
金属原子
金属腐蚀的本质:
M – ne- → Mn+
是指金属或合金跟接触的气体或液体发生氧化还原反应而腐蚀损耗的过程。
金属腐蚀
厚德 博学 励志 笃行
化学腐蚀
金属跟干燥气体或非电解质液体直接接触反应
不纯金属或合金跟电解质溶液接触形成原电池
电化学腐蚀
金属腐蚀
更普遍
厚德 博学 励志 笃行
碳粉、铁粉、
食盐水
实验改进
探究电化学腐蚀的原因
厚德 博学 励志 笃行
6个小时后
碳粉、铁粉、
食盐水
厚德 博学 励志 笃行
负极: 2Fe – 4e- = 2Fe2+
正极: O2+4e- +2H2O = 4OH-
总式:2Fe + O2 +2H2O =2 Fe(OH)2
4 Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
2Fe(OH)3=Fe2O3·xH2O+(3-x) H2O
电化学腐蚀——吸氧腐蚀
酸性很弱或中性水膜
厚德 博学 励志 笃行
负极: Fe – 2e- = Fe2+
正极: 2H+ +2e- = H2↑
总式:Fe + 2H+ = Fe2+ + H2↑
思考与交流:酸雨降下之后腐蚀的原理和刚才探究的原理有什么区别?
碳粉、铁粉、
稀醋酸
电化学腐蚀——析氢腐蚀
酸性较强水膜
练习1.利用反应2Cu+O2+2H2SO4===2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池。
(1)负极材料是________(写名称),电极反应式为_________________________。
(2)正极电极反应式为_____________________________。
(3)溶液中向________极移动。
铜
Cu?2e?Cu2+
O2+4e?+4H+===2H2O
负
